Bakgrundsdokument Kardiovaskulär primärprevention vid inflammatorisk reumatisk sjukdom
Arbetsgruppen för kardiovaskulär primärprevention Svensk Reumatologisk Förening 2026
För en sammanfattande rekommendation från arbetsgruppen hänvisas till Lathund för kardiovaskulär primärprevention vid inflammatorisk reumatisk sjukdom.
Bakgrund
Studier av mortalitet vid inflammatorisk reumatisk sjukdom (IRS)
Ett flertal studier har påvisat en ökad mortalitet jämfört med befolkningen i allmänhet vid reumatoid artrit (RA), med standardiserad mortalitetskvot (SMR) mellan 1.2 och 2.3 i olika studier (1-3). Dödligheten var förhöjd även vid långtidsuppföljning av patienter som behandlats enligt moderna behandlingsprinciper (så kallad treat-to-target) (4). Även vid systemisk lupus erythematosus (SLE) är totalmortalitet ökad jämfört med befolkningen i allmänhet (SMR 1.8, med högst dödlighet bland unga och minskande överdödlighet vid högre ålder vid SLE-diagnos) (5, 6). Ökad dödlighet i kardiovaskulär sjukdom (KVS) har rapporterats i ett flertal epidemiologiska arbeten vid RA (1-3, 7-10). Även den specifika risken för kardiovaskulär död har visats vara ökad vid SLE (5).
Vid RA har flera studier visat på ökad dödlighet specifikt i ischemisk hjärtsjukdom (7, 8, 11, 12). Mortaliteten i koronarsjukdom har visats vara signifikant ökad vid seropositiv RA, men inte hos seronegativa RA-patienter (13). Angående dödlighet i cerebrovaskulär sjukdom har resultaten varit mer motsägelsefulla (8, 14, 15).
Även vid radiografisk axial spondylartrit respektive ankyloserande spondylit (AxSpA) har flertalet undersökningar visat att patienter med AxSpA har förhöjd dödlighet, som bland annat hänger samman med sjukdomens svårighetsgrad och med sjukdomsdurationen. Uppskattningen av SMR har varierat mellan 1.5 och 1.9 i olika kliniska studier (16-19), med likartade resultat i nationell, registerbaserad studie från Sverige (20). Det har föreslagits att den ökade dödligheten delvis förklaras av retledningsrubbningar, aortainsufficiens och påverkan på myokardiet (18). En ökad dödlighet i ischemisk hjärtsjukdom och cerebrovaskulär sjukdom jämfört med bakgrundsbefolkningen har också påvisats (21).
Resultaten av studier av totalmortalitet hos patienter med psoriasisartrit (PsA) jämfört med befolkningen i allmänhet har gett motstridiga resultat (22-25). I en metaanalys fann man inte någon ökad signifikant ökad totalmortalitet, men en måttligt ökad dödlighet från kardiovaskulära sjukdomar (19). Selektionsbias kan spela en betydande roll vid denna heterogena sjukdom (26). En nationell svensk registerstudie påvisade nyligen en måttligt ökad dödlighet (hazard ratio 1.11), som förklarades av en ökad förekomst av KVS och andra komorbiditeter (27).
En förhöjd totalmortalitet har påvisats även vid flera reumatologiska systemsjukdomar, såsom systemisk skleros (28, 29), idiopatisk inflammatorisk myopati (29, 30) och ANCA-associerad vaskulit (AAV) (31). Det är ofta svårt att skilja direkta kärlkomplikationer av systemsjukdomar från aterosklerotisk kärlsjukdom, men mycket talar för att överdödligheten åtminstone delvis betingas av kardiovaskulär komorbiditet (30-33). Risken för kardiovaskulär död vid AAV var i en stor amerikansk kohortstudie signifikant högre hos dem med antikroppar mot myeloperoxidas jämfört med dem med anti-proteinas-3 antikroppar (31).
Studier av kardiovaskulär morbiditet vid IRS
Flera epidemiologiska studier har påvisat en högre incidens av kardiovaskulära händelser hos patienter med RA jämfört med normalbefolkningen (11, 12, 34-39). Traditionella etablerade riskfaktorer för KVS kan inte förklara den ökade risken (35, 38). Redan något år efter diagnos har patienter med RA ökad risk för akut koronart syndrom (AKS) jämfört med normalbefolkningen (40). Ett par studier har gett hållpunkter för ökad förekomst av atypiskt infarktinsjuknande och ökad förekomst av tyst ischemisk hjärtsjukdom samt plötslig död vid RA (38, 41-43). Även dödlighet efter hjärtinfarkt är ökad, både på kort (inom ett år) och lång sikt (> ett år) (44-46) och RA-sjukdomen i sig självt har föreslagits vara en oberoende kardiovaskulär riskfaktor jämförbar med diabetes mellitus (47). Risken för ischemisk hjärtsjukdom vid RA har visats vara sjunkande över tid (40, 48), men samma bild ses för normalbefolkningen varför den relativa riskökningen för patienter med RA kvarstår (49). Flertalet studier visar även på ökad risk för stroke vid RA (35, 36, 50, 51). Svenska data visar också en ökad risk, och den risken är fördubblad avseende ischemisk stroke efter 10 år med RA jämfört normalbefolkningen (52).
I en stor amerikansk tvärsnittsundersökning fann man att såväl förekomsten av hjärt- kärlsjukdom som av konventionella riskfaktorer för hjärt- kärlsjukdom var förhöjda hos patienter med AxSpA jämfört med hos matchade kontroller (53), och en meta-analys av longitudinella studier talar sammantaget också för en ökad risk för hjärtinfarkt och stroke vid AxSpA (54). Även i svenska data ses ökade risker för AKS för AxSpA, PsA och odifferentierad SpA; ca 50, 80, 30% ökning för respektive grupp jämfört normalbefolkningen (55).
När det gäller den sammantagna bilden avseende PsA är bilden något mindre klar (56). En studie av en stor kohort av patienter med PsA från en universitetsklinik i Toronto visade en förhöjd prevalens av KVS jämfört med bakgrundsbefolkningen (57). Riskökningen var framför allt kopplad till traditionella kardiovaskulära riskfaktorer och till svårighetsgraden av psoriasis (57). Longitudinella studier talar för en ökad risk för hjärtinfarkt vid PsA, medan resultaten avseende stroke är motstridiga (56). En hög förekomst av traditionella riskfaktorer, framförallt dyslipidemi (18), har rapporterats och har sannolikt stor betydelse för kardiovaskulär risk hos patienter med psoriasis och PsA. I svenska data ses ökad risk för stroke även för AxSpA, PsA och odifferentierad SpA; ca 30, 30, 20% ökning för respektive grupp jämfört normalbefolkningen (55).
Vad gäller SLE visar prospektiva studier en hög incidens av hjärtinfarkt och stroke. Den relativa risken jämfört med normalpopulationen ligger i de flesta studier mellan 2 och 3 (58-63). De högsta relativa riskerna har rapporterats hos premenopausala kvinnor (64), tidigt i sjukdomsförloppet (<1 år efter diagnos – 4-10 gånger ökad) (59, 60, 65), samt hos patienter med nefrit (4-18 gånger ökad) (65, 66) eller annan organskada (67). I ett svenskt material ses en ökad risk för hjärtinfarkt hos patienter jämfört med kontroller, där det även är tydligt att patienter med SLE drabbas av klassisk hjärtinfarkt vid yngre åldrar än matchade kontroller (68). Ytterligare studier har koncentrerat sig på att undersöka incidensen av kardiovaskulär sjuklighet hos SLE-patienter i jämförelse med förväntat baserat på förekomst av traditionella riskfaktorer. Även här är incidensen högre än förväntat (69, 70). En svensk uppföljande registerstudie av koronarangiografiundersökningar visar att förekomsten av ateroskleros är lika vanligt vid SLE som hos normalbefolkningen (ca 90%), men patienterna drabbas av hjärtinfarkt oftare och vid en lägre ålder (61). Mortaliteten efter hjärtinfarkt tycks vara förhöjd jämfört med normalbefolkningen, åtminstone korttidsrisken (67, 71), där det även finns indikationer på att patienter med SLE fick mindre aktiv behandling vid det akuta eventet jämfört med normalbefolkningen (72). Även långtids-mortaliteten efter stroke är förhöjd (73).
Risken att drabbas av kardiovaskulära händelser är förhöjd även vid flera andra systemsjukdomar (74). Vid systemisk skleros finns en ökad förekomst av ischemisk hjärtsjukdom jämfört med normalbefolkningen, även om riskökningen inte är lika tydlig avseende stroke (75, 76). I en nylig metaanalys inkluderande sju studier ses tydligast riskökning hos patienter med systemisk skleros avseende hjärtinfarkt och denna riskökning är mest uttalad hos dem med centromerantikroppar (75).
Vid vaskuliter är det ofta svårt att säkert urskilja aterosklerotisk KVS från en inflammatorisk påverkan på blodkärl men en riskökning för ischemisk hjärtsjukdom (HR 1,9) och stroke (HR 1,5) har visats vid granulomatös polyangit (GPA), (77, 78). Vid GPA ses, liksom vid SLE, den största relativa riskökningen för kardiovaskulära händelser under det första året efter diagnos (77) eller redan före diagnos (79). Även för jättecellsarterit (GCA) har en riskökning påvisats i en registerstudie från södra Sverige (IRR 1.3) och även här ses störst riskökning kort efter diagnos (80). Denna riskökning stöds även av två meta-analyser, med en HR på 1.7-1.8 för hjärtinfarkt och HR 1.4-1.5 för stroke hos patienter med GCA jämfört med normalbefolkningen (81, 82).
Patienter med Sjögrens sjukdom har även de en påvisad ökad risk för ischemisk hjärtsjukdom och stroke (83-87) vilket också är visat vid myosit (88) inklusive inklusionskroppsmyosit (89).
Ateroskleros vid IRS
Ökad förekomst av aterosklerotiska plack i halspulsådrorna vid RA jämfört med kontroller har rapporterats av flera studier, i en metaanalys noterades även ett positivt samband mellan plack och högre grad av inflammation samt manligt kön (90). Även i kranskärlen, studerade med coronary calcium score, fann 9 av 11 studier att RA patienter hade en ökad aterosklerosförekomst jämfört med kontroller (91). Ökad förekomst av subklinisk ateroskleros har också rapporterats vid PsA (92). Vid AxSpA var inte plackförekomsten ökad jämfört med kontroller enligt en metaanalys. Ett positivt samband sågs dock med mer aktiv sjukdom och med systemisk inflammation (93).
SLE patienter har ökad förekomst av plack i karotiderna och ökade förkalkningar i kranskärlen. SLE patienter med nefrit, hypertoni och hög kumulativ steroiddos har särskilt hög risk för aterosklerosförekomst (94, 95). Välkontrollerade kardiovaskulära riskfaktorer och långvarig remission minskade risken att utveckla nya carotisplack (96). Vid systemisk skleros föreligger också en snabb aterosklerosutveckling – det gäller fr.a. den mer kärlsjuka gruppen med centromerantikroppar (97).
Inflammationens betydelse för KVS vid IRS
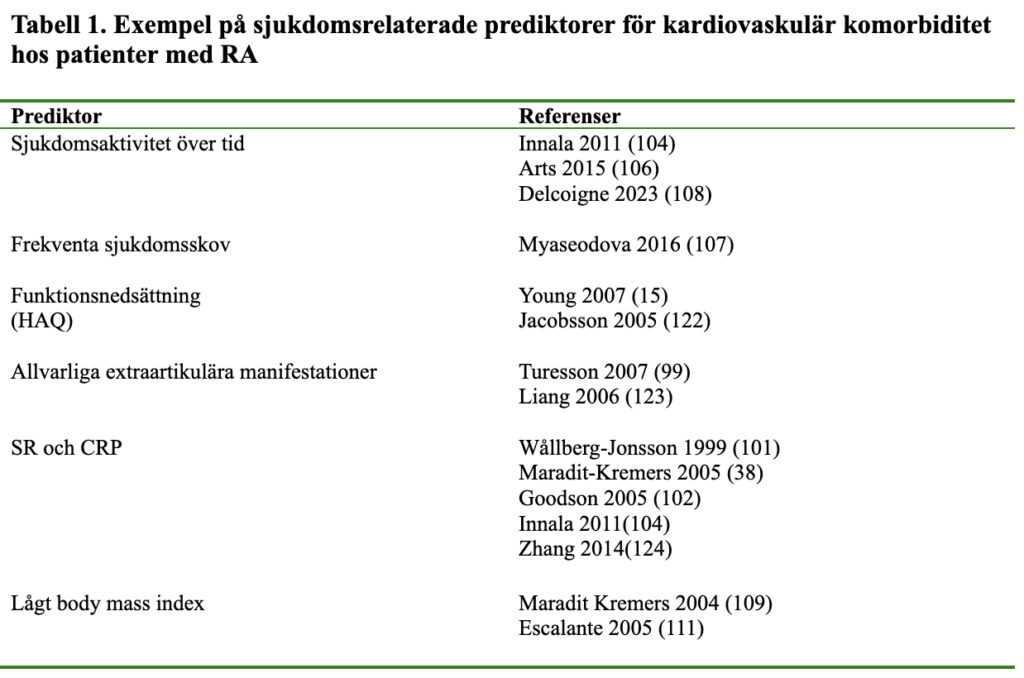
En lång rad studier har visat att sjukdomens svårighetsgrad har betydelse för risken för kardiovaskulär komorbiditet och mortalitet hos patienter med RA (Tabell 1). Allvarliga extraartikulära manifestationer (vaskulit, neuropati, Feltys syndrom, perikardit och pleurit) associerades med en ökad dödlighet i en samhällsbaserad studie av patienter med RA diagnostiserad fram till 1995 (98). I en senare studie kvarstod sambandet mellan extraartikulär RA och kardiovaskulära händelser även efter justering för ålder, kön, rökning, reumatoid faktor och förekomst av erosioner (99). Subkutana reumatiska noduli förefaller också vara associerade med en måttligt ökad totalmortalitet (98) och risk för kardiovaskulära händelser (100).
Sambandet mellan stegrade inflammationsparametrar hos RA patienter och ökad risk för kardiovaskulär död (38, 101-103), såväl som för kardiovaskulära händelser överlag (103-105), ligger i linje med att systemisk inflammation har betydelse för kärlsjukdom. Hög sjukdomsaktivitet över tid och frekventa sjukdomsskov predikterar också kardiovaskulär co-morbiditet vid RA (104, 106, 107). I en nyligen genomförd studie undersöktes korttidsrisk för AKS hos svenska och norska RA patienter i relation till sjukdomsaktiviteten (108). Sjukdomsaktivitet mättes vid ett läkarbesök och förekomst av AKS händelser undersöktes under 6 månaders uppföljningstid. Patienter som inte var i remission vid respektive besök, hade högre risk för AKS händelser än de som var i remission.
Att hög sjukdomsaktivitet över tid har betydelse för prognos vid RA illustreras även av ett påvisat samband mellan ökad dödlighet och funktionsnedsättning, mätt med HAQ, som får betraktas som en markör för sambandet mellan mortalitet och svår RA (15, 103). Hos RA patienter är lågt body mass index (BMI), snarare än högt BMI, en riskfaktor för KVS (109-111). Detta har också tolkats som en markör för svår sjukdom då ett lågt BMI ses vid reumatoid kakexi, i sig en markör för kronisk inflammation (87).
Det finns indikationer på att dödligheten efter KVS hos RA patienter har minskat (112). Liknande fynd har beskrivits i ett flertal andra aktuella studier, där tidigt insatt behandling vid RA och bättre kontroll av sjukdomsaktivitet föreslagits vara tänkbara bidragande orsaker till detta (113-115).
IL- 6 har betydelse för sjukdomsmekanismen både vid RA och ateroskleros (116). Huruvida IL-6 spelar roll för den ökade KVS risken vid RA är inte fastställt (117). Data talar för att anti-IL-6 behandling skulle kunna reducera risken för kardiovaskulära händelser hos patienter med stabil ateroskleros i bakgrundsbefolkningen (118), vilket inte har visats vid RA.
Det finns begränsat med uppgifter om betydelsen av inflammationsmarkörer för risken för KVS vid AxSpA och PsA. I en studie undersöktes om risken för kardiovaskulära händelser hos spondylartrit patienter, där AxSpA utgjorde den största gruppen, påverkades av behandling med TNF hämmare. Man fann en reducerad risk för kardiovaskulära händelser hos SpA patienter behandlade med TNF hämmare jmf med de som ej hade sådan behandling (119). I en annan studie fann man att behandling med TNF hämmare, eller annan biologisk behandling, var associerat med en minskad risk för kardiovaskulära händelser hos patienter med RA och AxSpA. De patienter som avslutat biologisk DMARD behandling, hade inte denna reducerade risk för kardiovaskulära händelser (120). Baserat på extrapolering från observationer vid RA har man antagit att mekanismer relaterade till kronisk inflammation bidrar till aterosklerosutveckling och kardiovaskulära händelser även vid AxSpA och PsA (121).
Läkemedelsbehandlingens påverkan på risk för KVS vid IRS beskrivs mer utförligt i dokumentet för läkemedelsbehandling.
Njurfunktion vid IRS och KVS
Nedsatt njurfunktion är en välkänd riskfaktor för KVS generellt. En stor prospektiv studie visar att RA patienter med högre sjukdomsaktivitet har en snabbare minskning av estimaterad Glomerulär Filtrations Ratio (eGFR) och utvecklar kronisk njursvikt oftare än RA patienter i remission/med låg sjukdomsaktivitet (125). Vid inflammatoriska systemsjukdomar, särskilt SLE och de ANCA associerade vaskuliterna, men även vid systemisk skleros är njurinflammation/nefrit en bidragande orsak till ökad risk för KVS. Patienter med SLE som har nefrit och/eller nedsatt njurfunktion har ökad risk att drabbas av ischemisk hjärtsjukdom och ökad mortalitet (65, 126, 127). I en stor spansk studie av patienter med ANCA associerad vaskulit var njurengagemang en av de faktorer som predikterade mortalitet (128). Enligt EULARs rekommendationer är det viktigt att behandla blodtryck, blodfetter och att använda minsta möjliga steroiddos. Om proteinläckaget är > 500 mg/dygn bör dessutom alla patienter med SLE nefrit behandlas med ACE/ARB blockad (129). Det har nyligen visat att Sodium-Glucose Transport 2 (SGLT2) inhibitorer kan förbättra njurfunktionen hos patienter med SLE nefrit (130) och EULARs rekommendationer för behandling av SLE med njurengagemang rekommenderar SGLT2 inhibition till patienter med stabilt nedsatt njurfunktion <60 ml/min/m2 (131).
Antifosfolipid antikroppar
Antifosfolipid syndromet (APS) diagnostiseras baserat på förekomst av antifosfolipid-antikroppar (aPL, ett samlingsnamn för anti-kardiolipinantikroppar (aCL), antikroppar mot ß2GPI (aß2GPI) och positivt utslag i det funktionella lupus antikoagulans testet (LA)) samt trombos (arteriell, venös eller småkärlstrombos) eller graviditetskomplikationer (132). APS är överrepresenterat hos patienter med SLE, men de flesta APS patienter, ca 60-70%, har primär APS, dvs. ingen samtidig reumatisk sjukdom. Nya klassifikationskriterier som använder ett poängsystem och viktar olika typer av tromboser och även tar hänsyn till förekomst av kardiovaskulära riskfaktorer har publicerats 2023 gemensamt av ACR/EULAR, men dessa är ännu främst är avsedda för forskning (133).Flera studier har visat att risken för trombos och ökar om man har positivt LA och/eller antikroppar i höga titrar och mot fler specificiteter som t.ex. ”trippel eller dubbelpositivitet”, vilket innebär positiva test för LA, aß2GPI och aCL (134, 135). Ischemisk stroke är den vanligaste arteriella manifestationen av APS, men hjärtinfarkt och småkärlstromboser förekommer också.
Utförliga riktlinjer för behandling av APS finns i SRFs dokument om riktlinjer för SLE-behandling, samt i EULARs riktlinjer för behandling av APS (132) och kardiovaskulär prevention (129). Trombotisk APS behandlas med antikoagulantia, där warfarin är förstahandsval. Nya orala antikoagulantia (NOAK/DOAC) bör som regel inte ges till dessa patienter då flera studier visat recidiv av arteriella manifestationer, främst stroke. En randomiserad studie fick avbrytas pga. strokerecidiv i NOAC/DOAC armen (136). och en metaanalys stärker dessa resultat (137). Primärprofylax med låg dos ASA (75-100 mg) rekommenderas till patienter med ”högrisk aPL profil” (trippel eller dubbelpositivitet) eller tidigare obstetrisk APS, låg dos ASA kan även övervägas till patienter med lägre riskprofil i vissa fall.
Primärprevention
Kardiovaskulära riskfaktorer och screening
Påverkbara traditionella riskfaktorer och skyddsfaktorer har i normalpopulation visats kunna förklara uppemot 90 % av insjuknandet i KVS (138). Till påverkbara traditionella riskfaktorer räknas rökning, diabetes, hypertoni, bukfetma, lipidrubbning och psykosocial stress. Livsstilsfaktorer som alkoholkonsumtion, fysisk aktivitetsnivå och matvanor betonas alltmer (fig.1).
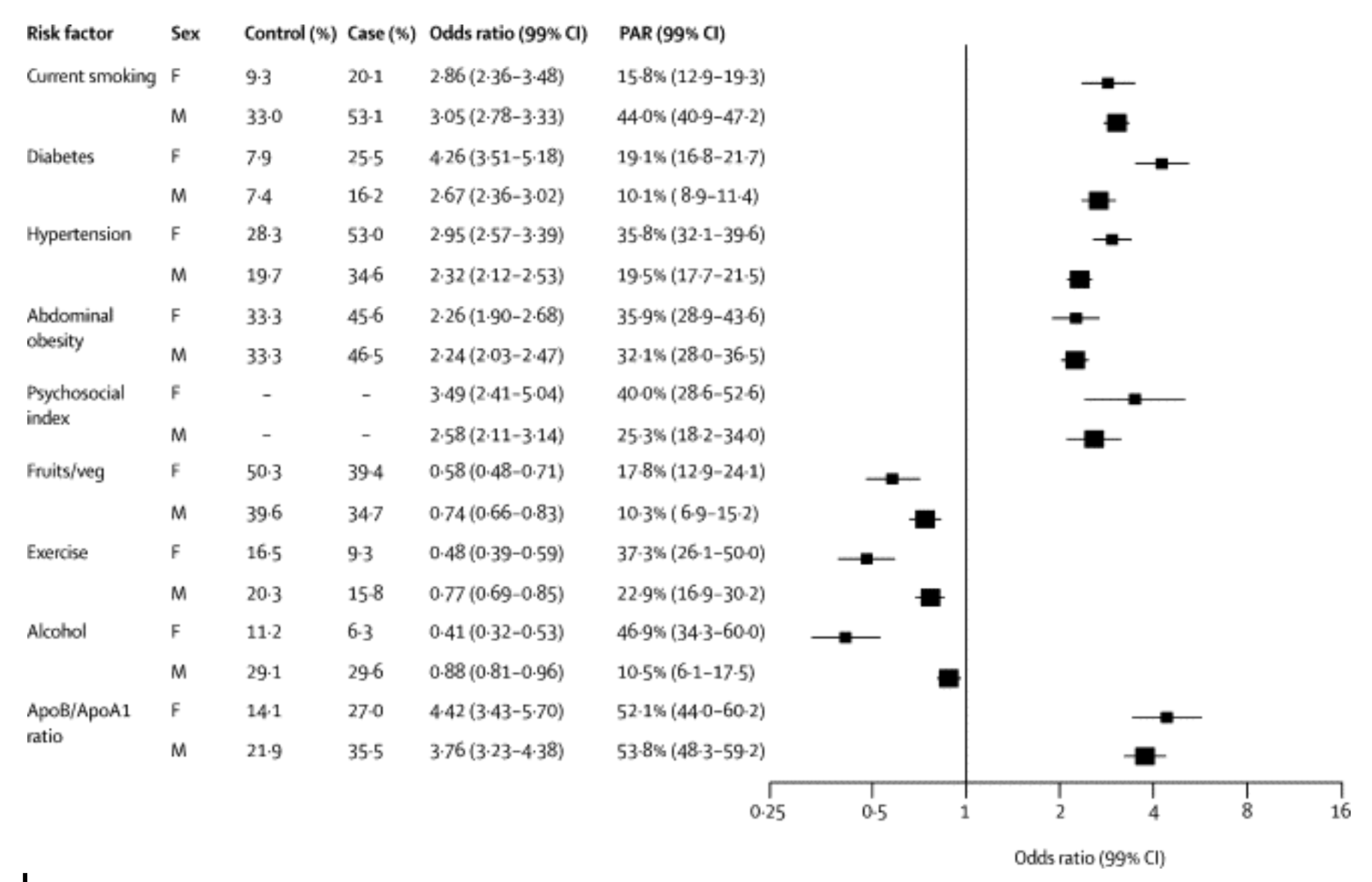
Figur 1: Association av riskfaktorer med akut hjärtinfarkt för män och kvinnor efter justering för ålder, kön och geografisk region. Exponentiell skala. Prevalens kan ej beräknas för psykosociala faktorer av metodskäl (139)
Det har föreslagits att karotis-ultraljud med mätning av intima–media-tjocklek (cIMT) kan användas för att modifiera kardiovaskulär riskskattningen hos patienter med reumatiska sjukdomar (140). Flera cytokiner har i studier föreslagits som potentiella riskmarkörer, men deras kliniska användning är ännu inte etablerad (141-145).
Screening och primärprevention
Primärpreventiva insatser mot KVS på sker på olika nivåer, på befolkningsnivå t.ex. genom skattepolitik och genom hälsosamtal där rökstopp, kostvanor och fysisk aktivitetsnivå lyfts i publika samtal.
För primärprevention på individnivå rekommenderas att i första hand individer med hög risk för KVS ska identifieras, t.ex. genom riktad screening, och dessa bör också erbjudas intervention avseende påverkbara riskfaktorer (146). Internationellt är denna screening och intervention organiserad utifrån lokala förutsättningar (147, 148) och det finns i dagsläget ingen evidens för att rekommendera hur denna screening och intervention ska organiseras. I patientgruppen med IRS finns ett ökat antal individer med hög risk för KVS, och riktad screening samt intervention i denna patientgrupp är motiverad i enlighet med de rekommendationer som tagits fram av EULAR (121, 129) samt specifikt för RA i Sverige inom Vårdförlopp tidig RA och Vårdförlopp etablerad RA. Enligt de senaste rekommendationerna av EULAR bör reumatologer ta ansvar för kardiovaskulär riskbedömning och handläggning av patienter med IRS, i samarbete med primärvården, internmedicinare, kardiologer (121, 129). Interaktionen mellan den inflammatoriska aktiviteten och de traditionella riskfaktorerna för aterosklerosutveckling vid RA har också åskådliggjorts (fig. 2) (104, 110). Studier visar dock på att screeningsgraden för personer med IRS inte är högre än för populationen i övrigt (149, 150).
Användande av en riskalgoritm som ger en helhetssyn utgående från flera riskfaktorer leder till en säkrare skattning av risken att insjukna eller dö i förtid i hjärtkärlsjukdom än en riskbedömning som endast bygger på enstaka riskfaktorer (Tabell 2). Skattningsinstrument räknar fram en ungefärlig risk som ska ses som ett hjälpmedel i den kliniska helhetsbedömningen, där också andra riskfaktorer som inte ingår i riskalgoritmen (exempelvis bukfetma, hereditet, njursjukdom med flera) bör ingå. Riskskattningen kan också användas som stöd i kommunikationen med patienten.
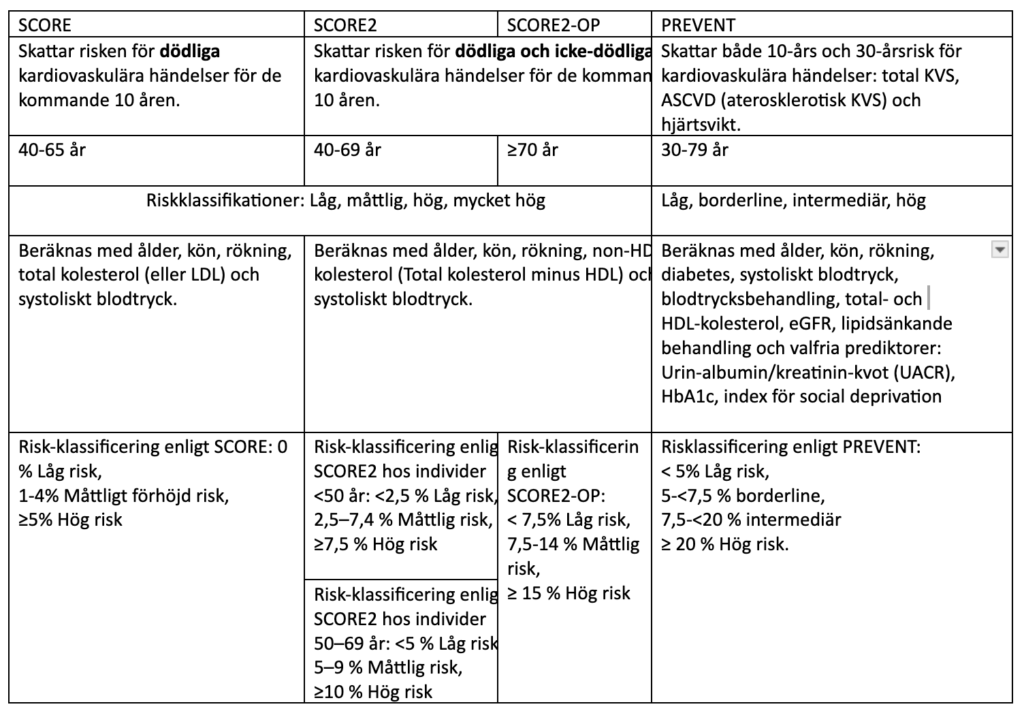
Förutom SCORE har flera riskverktyg använts, bland annat Framingham, QRISK och ASCVD Risk Estimator. SCORE beräknar endast risken för fatala kardiovaskulära händelser och baseras på kohorter fram till 1986 (Tabell 2). De nya algoritmerna publicerades juni 2021 av European Society of Cardiology och baserades på kohorter från 1990-2009.
År 2021 lanserades SCORE2 och SCORE2-OP, beräknar risken för fatala och icke-fatala kardiovaskulära händelser (Tabell 2). De nya algoritmerna tar hänsyn till olika riskregioner och en annan väsentlig skillnad är att SCORE2 använder icke-HDL-kolesterol (= totalkolesterol minus HDL). SCORE2-OP algoritmen är ett motsvarande verktyg för skattning av kardiovaskulär risk hos individer 70–89 år (151-153). År 2023 introducerades PREVENT som uppskattar 10- och 30-årsrisk för total KVS, ASCVD och hjärtsvikt (154) (Tabell 2).
Några svenska nationella behandlingsrekommendationer som bygger på riskskattning med SCORE2 eller SCORE2-OP föreligger ännu inte. De europeiska rekommendationerna bygger dock nu på användning av SCORE2 och SCORE2-OP (155). I dessa europeiska rekommendationer lyfts att patienter med samsjuklighet som inflammatorisk sjukdom har en ökad risk för KVS. För patienter med diabetes mellitus, och därmed även patienter med IRS och diabetes, rekommenderas inte användning av SCORE2 utan endast Nationella Diabetesregistrets (NDR:s) riskskattningsmotor som finns på www.ndr.nu/risk
Ett RA-specifikt riskskattningsverktyg, Expanded Risk Score for cardiovascular disease in RA (ERS-RA), har utvecklats genom användning av den nordamerikanska patientkohorten CORRONA(156). Här beräknas tio-årsrisken för insjuknande i KVS utifrån ålder samt dikotoma variabler avseende kön, rökning, sjukdomsduration, kortisonbehandling, sjukdomsaktivitet, funktionsförmåga, hypertoni, hyperlipidemi och diabetes mellitus. I de valideringsstudier av ERS‑RA som genomförts i kohorter med patienter med reumatoid artrit har riskestimatorn inte visat bättre prediktiv förmåga än etablerade riskskattningsinstrument utvecklade för allmänbefolkningen (157, 158), även om ERS-RA fungerade bra när de validerades externt hos svenska patienter med RA (159).
Den europeiska organisationen EULAR har tagit fram rekommendationer för kardiovaskulär riskbedömning och prevention hos patienter med IRS (121, 129). Dessa innefattar en riskskattning med hjälp av SCORE eller andra riskskattningsinstrument, och en multiplikation av den skattade risken med 1.5 för patienter med RA. För patienter med IRS har SRF:s arbetsgrupp för kardiovaskulär prevention utvecklat en modul för riskskattning vid inflammatorisk reumatisk sjukdom i Svensk Reumatologis Kvalitetsregister (SRQ). Riskskattning och registrering av data i modulen kräver inloggning i SRQ. Modulen ger en beräkning av SCORE, SCORE2 eller SCORE2-OP för alla diagnoser och vid RA en beräkning av SCORE2/SCORE2-OPx1,5 samt ERS-RA. För varje framräknat index anges också bedömning av risknivå och riskfaktorer markeras och uppmärksammas i modulen, som också är anpassad till Vårdförlopp tidig RA.
Tabell 2: Jämförelse av riskskattningsverktygen SCORE, SCORE2, SCORE2-OP och PREVENT. Den kardiovaskulära modulen i SRQ beräknar automatiskt den kardiovaskulära risken med SCORE2 eller SCORE2-OP enligt ålder. SCORE beräknas också fortfarande i KV-modulen i SRQ men framför allt i forskningssyfte.
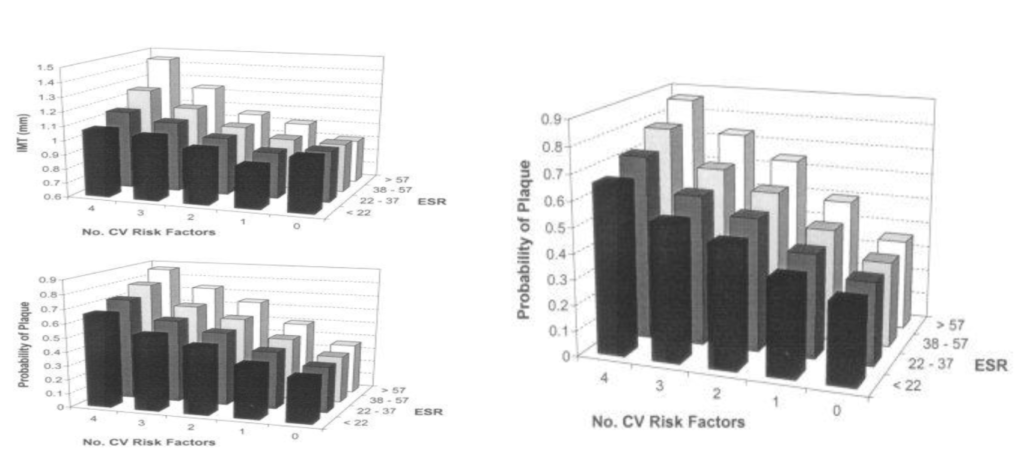
Figur 2. Ålders- och könsjusterat medelvärde av intima-media tjocklek i karotiskärl (IMT) och sannolikhet för plack i karotis, som funktioner av antalet kardiovaskulär riskfaktorer (CV Risk Factors) och kvartiler av SR (ESR, mm/h). Antalet riskfaktorer och SR var vardera signifikant associerade med båda beroende variablerna (P för trend ≤0.001 för vardera). Det fanns en signifikant interaktion mellan SR och antalet riskfaktorer (P för produkttermen SR × antalet kardiovaskulära riskfaktorer ≤0.001). Interaktionen låter förstå att effekten av SR på IMT varierade beroende på antalet riskfaktorer. Vid karotisplack var effekten av SR signifikant utan evidens för interaktion (110).
Evidens för betydelse av intervention mot kardiovaskulära riskfaktorer hos patienter med IRS
Rekommendationer om intervention mot riskfaktorer för KVS hos patienter med reumatiska sjukdomar har baserats på extrapolering från erfarenheter av sådana interventioner i den allmänna befolkningen. En öppen, randomiserad studie jämförde dock nyligen ett strukturerat program för reduktion av hypertoni, hyperlipidemi och hyperglykemi med standarduppföljning hos patienter med RA utan KVS eller diabetes. Man fann signifikant mindre progress av intima media tjocklek (IMT) i arteria carotis och signifikant färre kardiovaskulära händelser i gruppen med aktiv primärprevention (160). Majoriteten av patienterna hade låg sjukdomsaktivitet när studien började. Sammantaget stöder detta nyttan av kardiovaskulär primärprevention hos patienter med RA.
Sammanfattning
Sammanfattning avseende traditionella riskfaktorer vid inflammatorisk reumatisk sjukdom
Rökning
Rökning är en i högsta grad påverkbar riskfaktor för KVS, med stark evidens för att rökstopp bidrar till primärprevention i normalpopulation (161, 162). Ökad risk för KVS för rökare är visat vid SLE (127, 163, 164) och framför allt för patienter med STAT4 riskgenvarianten (165). Vid RA visade en prospektiv studie samband mellan rökning och kardiovaskulär morbiditet (166) och liknande resultat har påvisats i en metaanalys samt i en nyligen genomförd systematisk review av metaanalyser och befintliga systematiska översiktsartiklar (164, 167). Risken att drabbas av kardiovaskulära händelser är lägre hos RA patienter som slutat röka jämfört med RA patienter som alltjämt röker (HR 0,7) (168). Sammantaget rekommenderas, som i normalbefolkningen, rökstopp till patienter med reumatologiska diagnoser.
Hypertoni
Värdet av att behandla hypertoni, såväl systolisk som diastolisk, i avsikt att minska utveckling av KVS är väl dokumenterat i normalbefolkningen (169, 170). Hos patienter med RA (101, 171) och SLE (172) är hypertoni och andra traditionella riskfaktorer vanligen inte lika framträdande, åtminstone relativt sett. Samlad dokumentation talar dock för en tydlig association mellan förekomst av hypertoni och utveckling av KVS vid RA (166, 167), och ett sådant samband har observerats även vid PsA (173). Vidare finns stöd för att hypertoni är både underdiagnostiserad och underbehandlad hos patienter med reumatiska sjukdomar (174). Enligt de senaste EULAR rekommendationerna för KVS-riskprevention ska man överväga ett blodtrycksmål <130/80 för SLE patienter, då lägre blodtryck är associerat med lägre KVS risk. SLE patienter med glomerulonefrit och arteriell hypertension eller en urin protein-kreatinin kvot>500 mg/dag bör behandlas med ACE hämmare eller angiotensin 2 receptor blockerare. Hos patienter med samtidig gikt ska diuretika undvikas och patienter med systemisk skleros ska inte behandlas med betablockerare (129).
Patienter med reumatisk sjukdom och samtidig hypertoni skall således kontrolleras i enlighet med nationella riktlinjer för hypertonibehandling. Beslut om intervention bör, hos den enskilde patienten, baseras på patientens sammanlagda risk för framtida KVS och om patienten pga RA med hög bestående sjukdomsaktivitet eller SLE är särskilt riskbenägen. Den modifierade algoritmen i Lathunden kan ge stöd i behandlingen.
Blodfetter
Höga kolesterolnivåer hos RA patienter, särskilt om de förekommer tillsammans med pågående systemisk inflammation, är kopplade till accelererad subklinisk ateroskleros (110). Aktiv systemisk inflammation, som t.ex. vid aktiv RA(175, 176) eller spondylartrit (177) orsakar dock en sänkning av det farliga total-/LDL-kolesterolet. Hög sjukdomsaktivitet/inflammation sänker också det ”goda kolesterolet” HDL vid många reumatiska sjukdomar (178-180). För att beskriva detta fenomen brukar man tala om en U-formad lipidparadox vid RA. Låga lipidnivåer orsakas av uttalad systemisk inflammation och är kopplade till ökad risk för KVS, men detta gäller också för RA patienter med höga lipidnivåer, på samma sätt som i normalbefolkningen (175, 181). I överensstämmelse med dessa iakttagelser leder ofta framgångsrik behandling till ökade nivåer av total, LDL och HDL kolesterol (182, 183).
Det finns ännu få studier som studerat lipidsänkande behandling vid IRS (184, 185). Både LDL och CRP sänktes av 40 mg atorvastatin hos patienter med RA, därutöver noterades en trend till lägre incidens av kardiovaskulära händelser vilket var i nivå med vad som rapporterats i normalbefolkningen vid motsvarande LDL sänkning (185). En annan studie visade att intensiv behandling med rosuvastatin sänkte LDL kolesterolet och ledde till en minskning av plackstorleken hos patienter med RA (186).
En randomiserad studie på SLE patienter med uppföljning under två år visade att atorvastatin sänkte nivåerna av totalkolesterolet men man såg inte någon effekt på aterosklerosförekomsten (187). I en registerstudie från Taiwan visades dock minskad mortalitet och morbiditet hos SLE patienter som behandlades med statiner (188). Malariamediciner, som ofta används vid SLE, sänker även lipidnivåerna enligt en meta-analys (189).
Vilka målnivåer man ska välja för lipidsänkande behandling måste bedömas individuellt och hänsyn tas till övriga riskfaktorer samt den totala risken för KVS. Enligt EULARs rekommendationer för systemsjukdomar bör lipider behandlas på samma sätt som i normalbefolkningen vid SLE och APS (129).
Diabetes och nedsatt glukostolerans
Diabetes är en stark riskfaktor för KVS och detta bör beaktas också vid reumatisk sjukdom.
Vid nedsatt glukostolerans eller prediabetes är det av vikt att även ha kontroll på övriga konventionella riskfaktorer för att reducera risken för KVS även om möjligheterna att bromsa utvecklingen av diabetes inte är säkerställd (190, 191). Individer med denna typ av rubbning bör därför identifieras och erbjudas intervention mot övriga påverkbara riskfaktorer i enlighet med riktlinjerna för detta.
Publicerade data avseende diabetesförekomst vid RA och SLE har tidigare inte varit entydiga (36, 53, 171, 192-196) men på senare år visar de flesta studier en ökad förekomst av diabetes vid såväl RA (197-199), AxSpA (200) som SLE (201, 202). Vid systemisk skleros respektive APS ter sig inte överrisken för diabetes mellitus vara lika uppenbar (203) (204). Vid PsA finns en mer tydlig koppling till både diabetes mellitus och insulinresistens (205-211). Insulinresistens och nedsatt glukostolerans är visat vid aktiv RA (212) och SLE (213) och kopplingen mellan inflammation och insulinresistens är tydlig (214, 215). Associationen kan ytterligare stärka indikationen för att sträva efter en god inflammationskontroll vid inflammatorisk reumatisk sjukdom (216) (217) (218) (219) samt sträva efter en god metabol kontroll hos patienter med diabetes mellitus (220).
Individer med reumatisk sjukdom och samtidigt förekommande diabetes ska kontrolleras i enlighet med nationella riktlinjer för diabetesvård, då diabetes är en lika stark riskfaktor för KVS hos patienter med reumatiska sjukdomar som i övriga befolkningen (195, 221). Det finns indikationer på att patienter med diabetes och RA eller PsA har en större riskökning för KVS jämfört med dem med endast diabetes (222, 223).
Diabetes, eller nedsatt glukostolerans, tillsammans med bukfetma, hypertoni och hyperlipidemi har setts samverka i riskökningen för bland annat KVS och benämns då metabolt syndrom (224). Det finns en tydlig påvisad riskökning för metabolt syndrom hos patienter med PsA (225, 226) där en gemensam underliggande patofysiologi har föreslagits (227). Även vid RA, SLE och SpA finns en hög förekomst av metabolt syndrom (228-230).
Övervikt och bukfetma
Midje-stusskvot är en bättre prediktor för kardiovaskulär sjukdom än body mass index (BMI) i den allmänna befolkningen (231). Vid RA har lågt BMI i äldre studier visats vara en riskfaktor för kardiovaskulär död (38). Vid långtidsuppföljning av en internationell observationsstudie observerades en ökad kardiovaskulär morbiditet vid lågt BMI enbart hos ACPA-negativa RA-patienter med biologisk behandling (232).
Viktförlust, och förlust av muskelmassa, är associerat med aktiv sjukdom (233). Denna förändring kan dock åtföljas av en ökad bukfetma (234, 235), som associerats med ökad ateroskleros (236), men vars betydelse för endotelfunktion (237) och risk för kardiovaskulära händelser inte är säkerställd.
Vid SLE ses istället hos många patienter en viktuppgång vid hög sjukdomsaktivitet (238). Fetma (BMI >30 kg/m2) har associerats med en måttlig riskökning för hjärtinfarkt vid RA (167), medan SLE-patienter med övervikt (BMI >25 kg/m2) visats ha ökad ateroskleros i karotiderna (239). Det finns bristfälligt underlag angående betydelsen av bukfetma hos patienter med RA och SLE och angående interventionsstudier för att minska bukfetma i dessa grupper.
Fetma har visats vara vanligare hos patienter med PsA jämfört med patienter med RA (240), och en oberoende riskfaktor för mortalitet vid PsA (241).
Övervikt/fetma och bukfetma ingår inte i SCORE-systemen (SCORE, SCORE2 och SCORE2-OP) för skattning av risken för kardiovaskulär död eller kardiovaskulära händelser.
Utifrån det aktuella kunskapsläget är det lämpligt att ta hänsyn till förekomst av bukfetma och övervikt/fetma vid den samlade riskbedömningen hos patienter med reumatisk sjukdom, och vid översyn av påverkbara livsstilsfaktorer.
Alkoholkonsumtion
Den kunskap vi idag har om alkoholens effekter på kardiovaskulär sjukdom bygger på observationsstudier, och det saknas randomiserade interventionsstudier som visar att alkohol kan påverka risken för morbiditet eller mortalitet i någon kardiovaskulär sjukdom. Eftersom det ej finns särskilda observationsstudier eller randomiserade studier för patienter med reumatisk sjukdom som visar på risken att insjukna eller dö i KVS till följd av alkoholkonsumtion, är det tillrådligt att följa de rekommendationer som råder för den allmänna populationen (242, 243). Detta även då det finns tecken på association mellan alkoholintag och radiografisk progression vid RA (164). Hög alkoholkonsumtion ökar risken för insjuknande och död i KVS (244-250). I den hittills största undersökningen av alkohols effekter på ett stort antal hälsoutfall konkluderas att nollkonsumtion av alkohol minimerar risken för försämrad hälsa (249).
Otillräcklig fysisk aktivitet
Personer med reumatisk sjukdom som har låg till måttlig sjukdomsaktivitet kan utöva fysisk aktivitet utan risk för ökad aktivitet i grundsjukdomen. För bästa effekt kan individanpassad träning utformad tillsammans med en fysioterapeut rekommenderas även vid lägre sjukdomsaktivitet. Överväg kardiovaskulär riskbedömning av läkare, särskilt inför träning vid hög eller mycket hög intensitet. Vid hög sjukdomsaktivitet, höga doser av kortison och/eller omfattande organskador, engagemang av hjärta, lungor eller stora leder eller proteser i stora leder skall också träningen planeras i samråd med läkare och fysioterapeut (251).
För att förebygga hjärt-kärlsjukdom gäller samma övergripande rekommendationer för fysisk aktivitet (155, 252-254) (251) som i normalbefolkningen:
- Begränsa stillasittandet. Tid i stillasittande bör bytas ut mot fysisk aktivitet.
- För betydande hälsovinster rekommenderas pulshöjande fysisk aktivitet 150-300 minuter i veckan vid träning på måttlig intensitet. Vid träning på hög intensitet rekommenderas minst 75 – 150 minuter i veckan. Aktiviteten bör spridas över veckan
- För ytterligare hälsovinster rekommenderas muskelstärkande fysisk aktivitet som involverar stora muskelgrupper.
Positiva effekter på kardiovaskulär funktion och hälsa har påvisats vid reumatisk sjukdom (255). Det finns flera studier som undersökt den kardiovaskulära effekten av träning vid RA. Ett flertal studier har varit på en låg-medelhög intensitet med en viss effekt på maximal syreupptagningsförmåga, VO2 max (256, 257). Hård cykelträning (spinning) under 10 veckor gav positiva effekter på bl.a. blodtryck utan att lederna försämrades (258). Kombinerad styrke- och konditionsträning har visat positiv effekt på flera kardiovaskulära riskfaktorer (256). Författarna föreslog därför kombinerad träning som en del av det multidisciplinära omhändertagandet, med individuell optimering av muskulär förmåga för att underlätta åtföljande konditionsträning (256). I en senare större studie av 150 RA patienter (259) var högre nivåer av VO2max associerade med en bättre kardiovaskulär profil, även efter korrektion för sjukdomsaktivitet. I en metaanalys avseende fysisk aktivitet vid PsA baserat på 13 studier sågs tydliga gynnsamma effekter av träning på sjukdomsaktivitet, hälsa och tecken på gynnsamma effekter på vissa kardiovaskulära riskfaktorer (260). I en norsk-svensk multicenterstudie av 100 patienter med axial spondartrit av 3 månaders högintensiv träning sågs förbättrad kardiovaskulär riskprofil och minskad sjukdomsaktivitet (261). I en svensk multicenterstudie av totalt 87 patienter med RA tolererades 3 månaders högintensiv konditions- och styrketräning väl, och man påvisade förbättrad fysisk kondition och minskat midjemått (262).
En systematisk översikt (263) av polymyosit/dermatomyosit (baserad på fyra randomiserade kontrollerade studier) och SLE (baserad på åtta randomiserade kontrollerade studier samt två tidigare meta-analyser) indikerade att träning på måttlig till hög intensitet kan förbättra syreupptagningsförmåga och muskelfunktion samt livskvalitet hos patienter med polymyosit och dermatomyosit i remission. Vid mild eller inaktiv SLE sågs förbättrad syreupptagningsförmåga och minskning av fatigue och depressiva symtom vid träning på måttlig till hög intensitet.
Likaså sågs förbättrad syreupptagningsförmåga och symptom vid träning på måttlig till hög intensitet hos patienter med mild eller inaktiv SLE (263). Det finns förslag att rekommendera både konditionsträning och muskelstärkande träning med gradvis ökande frekvens och intensitet vid SLE (264).
Likaså rekommenderas individanpassad träning vid systemisk skleros inklusive konditionsträning och strukturerad muskelstärkande fysisk aktivitet (265, 266) vid en detaljerad översikt från The Global Fellowship on Rehabilitation and Exercise in Systemic Sclerosis (267).
Generellt är det en utmaning att upprätthålla fysisk aktivitet över tid för patienterna och sjukdomsaktivitet, övervikt och livsstilsrelaterade faktorer påverkar detta (268).
Psykosocial stress
Psykosocial stress är en riskfaktor för hjärt-kärlsjukdom där det finns belägg för att den är jämförbar med övriga riskfaktorer (269, 270), men där underlaget är behäftat med svårigheter att undvika sammanblandning med andra livsstilsfaktorer (271-275). I två metaanalyser är stress associerad med övervikt (276, 277), och i den ena även med undervikt (276). KVS vid arbetsrelaterad stress tycks delvis medieras via försämrad metabol funktion, metabola syndromet (278, 279). Akut känslomässig stress är korrelerat med ökad mortalitet och morbiditet i KVS (271-275, 280, 281). Sömnkvalitet och sömnduration både påverkas av och bidrar till ökad psykosocial stress (282, 283) och är associerad med ökad kardiovaskulär risk (284). Om psykologisk stress påverkar direkt fysiologiskt, via påverkan på reumatologisk sjukdomsaktivitet eller via negativa livsstilsförändringar är svårt att överblicka. Det finns begränsat med information om psykosocial stress vid reumatisk sjukdom (285, 286). I en mindre tvärsnittsstudie vid tidig RA (n=78) var kort sömnduration associerad med en ogynnsam kardiovaskulär riskprofil (287). Ovan nämnd studie av högintensiv träning i 3 månader vid AxSpA innebar förbättrad sömn, minskad smärta och trötthet samt förbättrat känslomässigt stämningsläge (288). Tillräckliga interventionsstudier på området saknas. Europeiska riktlinjer för kardiovaskulär prevention rekommenderar emellertid klinisk genomgång av psykosociala faktorer, såsom stress på arbetet och i familjen, social isolering, depression och ångest (253), och individanpassad klinisk handläggning för att undanröja hinder för en hälsosam livsstil.
Referenser
Referenser
- Wolfe F, Mitchell DM, Sibley JT, Fries JF, Bloch DA, Williams CA, et al. The mortality of rheumatoid arthritis. Arthritis Rheum. 1994;37(4):481-94.
- Sparks JA, Chang SC, Liao KP, Lu B, Fine AR, Solomon DH, et al. Rheumatoid Arthritis and Mortality Among Women During 36 Years of Prospective Follow-Up: Results From the Nurses’ Health Study. Arthritis Care Res (Hoboken). 2016;68(6):753-62.
- Houge IS, Hoff M, Thomas R, Videm V. Mortality is increased in patients with rheumatoid arthritis or diabetes compared to the general population – the Nord-Trøndelag Health Study. Sci Rep. 2020;10(1):3593.
- Heckert SL, Maassen JM, le Cessie S, Goekoop-Ruiterman YPM, Guler-Yuksel M, Lems W, et al. Long-term mortality in treated-to-target RA and UA: results of the BeSt and IMPROVED cohort. Ann Rheum Dis. 2023.
- Bultink IEM, de Vries F, van Vollenhoven RF, Lalmohamed A. Mortality, causes of death and influence of medication use in patients with systemic lupus erythematosus vs matched controls. Rheumatology (Oxford). 2021;60(1):207-16.
- Moe SR, Haukeland H, Brunborg C, Botea A, Damjanic N, Wivestad GA, et al. Persisting mortality gap in systemic lupus erythematosus; a population-based study on juvenile- and adult-onset SLE in Norway 1999-2022. Rheumatology (Oxford). 2023.
- Myllykangas-Luosujarvi R, Aho K, Kautiainen H, Isomaki H. Cardiovascular mortality in women with rheumatoid arthritis. J Rheumatol. 1995;22(6):1065-7.
- Wållberg-Jonsson S, Öhman ML, Rantapää-Dahlqvist S. Cardiovascular morbidity and mortality in patients with seropositive rheumatoid arthritis in Northern Sweden. J Rheumatol. 1997;24(3):445-51.
- Avina-Zubieta JA, Choi HK, Sadatsafavi M, Etminan M, Esdaile JM, Lacaille D. Risk of cardiovascular mortality in patients with rheumatoid arthritis: a meta-analysis of observational studies. Arthritis Rheum. 2008;59(12):1690-7.
- Meune C, Touze E, Trinquart L, Allanore Y. High risk of clinical cardiovascular events in rheumatoid arthritis: Levels of associations of myocardial infarction and stroke through a systematic review and meta-analysis. Arch Cardiovasc Dis. 2010;103(4):253-61.
- Watson DJ, Rhodes T, Guess HA. All-cause mortality and vascular events among patients with rheumatoid arthritis, osteoarthritis, or no arthritis in the UK General Practice Research Database. J Rheumatol. 2003;30(6):1196-202.
- Logstrup BB, Ellingsen T, Pedersen AB, Darvalics B, Olesen KKW, Botker HE, et al. Cardiovascular risk and mortality in rheumatoid arthritis compared with diabetes mellitus and the general population. Rheumatology (Oxford). 2021;60(3):1400-9.
- Joerns EK, Lopez-Ruiz A, Lennon RJ, Crowson CS, George RJ, Kronzer VL, et al. Differences in Cause-Specific Mortality in Patients With Rheumatoid Arthritis by Sex and Seropositivity. J Rheumatol. 2025.
- Björnådal L, Baecklund E, Yin L, Granath F, Klareskog L, Ekbom A. Decreasing mortality in patients with rheumatoid arthritis: results from a large population based cohort in Sweden, 1964-95. J Rheumatol. 2002;29(5):906-12.
- Young A, Koduri G, Batley M, Kulinskaya E, Gough A, Norton S, et al. Mortality in rheumatoid arthritis. Increased in the early course of disease, in ischaemic heart disease and in pulmonary fibrosis. Rheumatology (Oxford). 2007;46(2):350-7.
- Radford EP, Doll R, Smith PG. Mortality among patients with ankylosing spondylitis not given X-ray therapy. N Engl J Med. 1977;297(11):572-6.
- Lehtinen K. Mortality and causes of death in 398 patients admitted to hospital with ankylosing spondylitis. Ann Rheum Dis. 1993;52(3):174-6.
- Peters MJ, van der Horst-Bruinsma IE, Dijkmans BA, Nurmohamed MT. Cardiovascular risk profile of patients with spondylarthropathies, particularly ankylosing spondylitis and psoriatic arthritis. Semin Arthritis Rheum. 2004;34(3):585-92.
- Chaudhary H, Bohra N, Syed K, Donato A, Murad MH, Karmacharya P. All-Cause and Cause-Specific Mortality in Psoriatic Arthritis and Ankylosing Spondylitis: A Systematic Review and Meta-Analysis. Arthritis Care Res (Hoboken). 2023;75(5):1052-65.
- Exarchou S, Lie E, Lindstrom U, Askling J, Forsblad-d’Elia H, Turesson C, et al. Mortality in ankylosing spondylitis: results from a nationwide population-based study. Ann Rheum Dis. 2016;75(8):1466-72.
- Haroon NN, Paterson JM, Li P, Inman RD, Haroon N. Patients With Ankylosing Spondylitis Have Increased Cardiovascular and Cerebrovascular Mortality: A Population-Based Study. Ann Intern Med. 2015;163(6):409-16.
- Wong K, Gladman DD, Husted J, Long JA, Farewell VT. Mortality studies in psoriatic arthritis: results from a single outpatient clinic. I. Causes and risk of death. Arthritis Rheum. 1997;40(10):1868-72.
- Buckley C, Cavill C, Taylor G, Kay H, Waldron N, Korendowych E, et al. Mortality in psoriatic arthritis – a single-center study from the UK. J Rheumatol. 2010;37(10):2141-4.
- Elalouf O, Muntyanu A, Polachek A, Pereira D, Ye JY, Lee KA, et al. Mortality in psoriatic arthritis: Risk, causes of death, predictors for death. Semin Arthritis Rheum. 2020;50(4):571-5.
- Colaco K, Widdifield J, Luo J, Rosen CF, Alhusayen R, Paterson JM, et al. Trends in mortality and cause-specific mortality among patients with psoriasis and psoriatic arthritis in Ontario, Canada. J Am Acad Dermatol. 2021;84(5):1302-9.
- Bond S, Farewell VT, Schentag CT, Lawless JF, Gladman DD. Reporting of mortality in a psoriatic arthritis clinic is primarily a function of the number of clinic contacts and not disease severity. J Rheumatol. 2005;32(12):2364-7.
- Exarchou S, Di Giuseppe D, Klingberg E, Sigurdardottir V, Wedren S, Lindstrom U, et al. Mortality in patients with psoriatic arthritis in Sweden: a nationwide, population-based cohort study. Ann Rheum Dis. 2024;83(4):446-56.
- Ooi C, Solanki K, Lao C, Frampton C, White D. Mortality in the Waikato Hospital Systemic Sclerosis Cohort. Int J Rheum Dis. 2018;21(1):253-60.
- Patel S, Russell MD, Bechman K, Adas MA, Yang Z, Alveyn E, et al. The incidence and mortality of connective tissue diseases: a population-level cohort study in England from 2012 to 2023. Rheumatology (Oxford). 2025.
- Limaye V, Hakendorf P, Woodman RJ, Blumbergs P, Roberts-Thomson P. Mortality and its predominant causes in a large cohort of patients with biopsy-determined inflammatory myositis. Intern Med J. 2012;42(2):191-8.
- Wallace ZS, Fu X, Harkness T, Stone JH, Zhang Y, Choi H. All-cause and cause-specific mortality in ANCA-associated vasculitis: overall and according to ANCA type. Rheumatology (Oxford). 2020;59(9):2308-15.
- Pagkopoulou E, Arvanitaki A, Daoussis D, Garyfallos A, Kitas G, Dimitroulas T. Comorbidity burden in systemic sclerosis: beyond disease-specific complications. Rheumatol Int. 2019;39(9):1507-17.
- Soulaidopoulos S, Madenidou AV, Daoussis D, Melissaropoulos K, Mavrogeni S, Kitas G, et al. Cardiovascular Disease in the Systemic Vasculitides. Curr Vasc Pharmacol. 2020;18(5):463-72.
- John H, Kitas G, Toms T, Goodson N. Cardiovascular co-morbidity in early rheumatoid arthritis. Best Pract Res Clin Rheumatol. 2009;23(1):71-82.
- del Rincon ID, Williams K, Stern MP, Freeman GL, Escalante A. High incidence of cardiovascular events in a rheumatoid arthritis cohort not explained by traditional cardiac risk factors. Arthritis Rheum. 2001;44(12):2737-45.
- Solomon DH, Karlson EW, Rimm EB, Cannuscio CC, Mandl LA, Manson JE, et al. Cardiovascular morbidity and mortality in women diagnosed with rheumatoid arthritis. Circulation. 2003;107(9):1303-7.
- Turesson C, Jarenros A, Jacobsson L. Increased incidence of cardiovascular disease in patients with rheumatoid arthritis: results from a community based study. Ann Rheum Dis. 2004;63(8):952-5.
- Maradit-Kremers H, Nicola PJ, Crowson CS, Ballman KV, Gabriel SE. Cardiovascular death in rheumatoid arthritis: a population-based study. Arthritis Rheum. 2005;52(3):722-32.
- Avina-Zubieta JA, Thomas J, Sadatsafavi M, Lehman AJ, Lacaille D. Risk of incident cardiovascular events in patients with rheumatoid arthritis: a meta-analysis of observational studies. Ann Rheum Dis. 2012;71(9):1524-9.
- Holmqvist M, Ljung L, Askling J. Acute coronary syndrome in new-onset rheumatoid arthritis: a population-based nationwide cohort study of time trends in risks and excess risks. Ann Rheum Dis. 2017;76(10):1642-7.
- Wislowska M, Sypula S, Kowalik I. Echocardiographic findings, 24-hour electrocardiographic Holter monitoring in patients with rheumatoid arthritis according to Steinbrocker’s criteria, functional index, value of Waaler-Rose titre and duration of disease. Clin Rheumatol. 1998;17(5):369-77.
- McEntegart A, Capell HA, Creran D, Rumley A, Woodward M, Lowe GD. Cardiovascular risk factors, including thrombotic variables, in a population with rheumatoid arthritis. Rheumatology (Oxford). 2001;40(6):640-4.
- Douglas KM, Pace AV, Treharne GJ, Saratzis A, Nightingale P, Erb N, et al. Excess recurrent cardiac events in rheumatoid arthritis patients with acute coronary syndrome. Ann Rheum Dis. 2006;65(3):348-53.
- Singh G, Miller JD, Huse DM, Pettitt D, D’Agostino RB, Russell MW. Consequences of increased systolic blood pressure in patients with osteoarthritis and rheumatoid arthritis. J Rheumatol. 2003;30(4):714-9.
- Van Doornum S, Brand C, King B, Sundararajan V. Increased case fatality rates following a first acute cardiovascular event in patients with rheumatoid arthritis. Arthritis Rheum. 2006;54(7):2061-8.
- Södergren A, Stegmayr B, Lundberg V, Öhman ML, Wållberg-Jonsson S. Increased incidence of and impaired prognosis after acute myocardial infarction among patients with seropositive rheumatoid arthritis. Ann Rheum Dis. 2007;66(2):263-6.
- Kitas G, Banks MJ, Bacon PA. Cardiac involvement in rheumatoid disease. Clin Med. 2001;1(1):18-21.
- Yazdani K, Xie H, Avina-Zubieta JA, Zheng Y, Abrahamowicz M, Lacaille D. Has the excess risk of acute myocardial infarction in rheumatoid arthritis relative to the general population declined? A population study of trends over time. Semin Arthritis Rheum. 2021;51(2):442-9.
- Sodergren A, Solbritt R-D, Ljung L. Time Trends of Cardiovascular Disease in the General Population and Inflammatory Arthritis. Rheum Dis Clin North Am. 2023;49(1):1-17.
- Södergren A, Stegmayr B, Öhman ML, Wållberg-Jonsson S. Increased incidence of stroke and impaired prognosis after stroke among patients with seropositive rheumatoid arthritis. Clin Exp Rheumatol. 2009;27(4):641-4.
- Solomon DH, Goodson NJ, Katz JN, Weinblatt ME, Avorn J, Setoguchi S, et al. Patterns of cardiovascular risk in rheumatoid arthritis. Ann Rheum Dis. 2006;65(12):1608-12.
- Holmqvist M, Gränsmark E, Mantel A, Alfredsson L, Jacobsson LT, Wallberg-Jonsson S, et al. Occurrence and relative risk of stroke in incident and prevalent contemporary rheumatoid arthritis. Ann Rheum Dis. 2013;72(4):541-6.
- Han C, Robinson DW, Jr., Hackett MV, Paramore LC, Fraeman KH, Bala MV. Cardiovascular disease and risk factors in patients with rheumatoid arthritis, psoriatic arthritis, and ankylosing spondylitis. J Rheumatol. 2006;33(11):2167-72.
- Mathieu S, Pereira B, Soubrier M. Cardiovascular events in ankylosing spondylitis: an updated meta-analysis. Semin Arthritis Rheum. 2015;44(5):551-5.
- Bengtsson K, Forsblad-d’Elia H, Lie E, Klingberg E, Dehlin M, Exarchou S, et al. Are ankylosing spondylitis, psoriatic arthritis and undifferentiated spondyloarthritis associated with an increased risk of cardiovascular events? A prospective nationwide population-based cohort study. Arthritis Res Ther. 2017;19(1):102.
- Horreau C, Pouplard C, Brenaut E, Barnetche T, Misery L, Cribier B, et al. Cardiovascular morbidity and mortality in psoriasis and psoriatic arthritis: a systematic literature review. J Eur Acad Dermatol Venereol. 2013;27 Suppl 3:12-29.
- Gladman DD, Ang M, Su L, Tom BD, Schentag CT, Farewell VT. Cardiovascular morbidity in psoriatic arthritis. Ann Rheum Dis. 2009;68(7):1131-5.
- Hak AE, Karlson EW, Feskanich D, Stampfer MJ, Costenbader KH. Systemic lupus erythematosus and the risk of cardiovascular disease: results from the nurses’ health study. Arthritis Rheum. 2009;61(10):1396-402.
- Avina-Zubieta JA, To F, Vostretsova K, De Vera M, Sayre EC, Esdaile JM. Risk of Myocardial Infarction and Stroke in Newly Diagnosed Systemic Lupus Erythematosus: A General Population-Based Study. Arthritis Care Res (Hoboken). 2017.
- Arkema EV, Svenungsson E, Von Euler M, Sjowall C, Simard JF. Stroke in systemic lupus erythematosus: a Swedish population-based cohort study. Ann Rheum Dis. 2017;76(9):1544-9.
- Tornvall P, Göransson A, Ekman J, Järnbert-Pettersson H. Myocardial Infarction in Systemic Lupus Erythematosus: Incidence and Coronary Angiography Findings. Angiology. 2021;72(5):459-64.
- Joyce DP, Berger JS, Guttmann A, Hasan G, Buyon JP, Belmont HM, et al. Prevalence of cardiovascular events in a population-based registry of patients with systemic lupus erythematosus. Arthritis Res Ther. 2024;26(1):160.
- Han JY, Cho SK, Kim H, Jeon Y, Kang G, Jung SY, et al. Increased cardiovascular risk in Korean patients with systemic lupus erythematosus: a population-based cohort study. Sci Rep. 2024;14(1):1082.
- Bengtsson C, Ohman ML, Nived O, Rantapaa Dahlqvist S. Cardiovascular event in systemic lupus erythematosus in northern Sweden: incidence and predictors in a 7-year follow-up study. Lupus. 2012;21(4):452-9.
- Hermansen ML, Lindhardsen J, Torp-Pedersen C, Faurschou M, Jacobsen S. The risk of cardiovascular morbidity and cardiovascular mortality in systemic lupus erythematosus and lupus nephritis: a Danish nationwide population-based cohort study. Rheumatology (Oxford). 2017.
- Wong CY, Ma BMY, Zhang D, Cheung W, Chan TM, Yap DYH. Cardiovascular risk factors and complications in patients with systemic lupus erythematosus with and without nephritis: a systematic review and meta-analysis. Lupus Sci Med. 2024;11(1).
- Sagheer S, Deka P, Pathak D, Khan U, Zaidi SH, Akhlaq A, et al. Clinical Outcomes of Acute Myocardial Infarction Hospitalizations With Systemic Lupus Erythematosus: An Analysis of Nationwide Readmissions Database. Curr Probl Cardiol. 2022;47(11):101086.
- Nived O, Ingvarsson RF, Joud A, Linge P, Tyden H, Jonsen A, et al. Disease duration, age at diagnosis and organ damage are important factors for cardiovascular disease in SLE. Lupus Sci Med. 2020;7(1).
- Esdaile JM, Abrahamowicz M, Grodzicky T, Li Y, Panaritis C, du Berger R, et al. Traditional Framingham risk factors fail to fully account for accelerated atherosclerosis in systemic lupus erythematosus. Arthritis Rheum. 2001;44(10):2331-7.
- Fischer LM, Schlienger RG, Matter C, Jick H, Meier CR. Effect of rheumatoid arthritis or systemic lupus erythematosus on the risk of first-time acute myocardial infarction. Am J Cardiol. 2004;93(2):198-200.
- Ke SR, Liu CW, Wu YW, Lai KR, Wu CY, Lin JW, et al. Systemic lupus erythematosus is associated with poor outcome after acute myocardial infarction. Nutr Metab Cardiovasc Dis. 2019;29(12):1400-7.
- Mohamed MO, Roddy E, Ya’qoub L, Myint PK, Al Alasnag M, Alraies C, et al. Acute Myocardial Infarction in Autoimmune Rheumatologic Disease: A Nationwide Analysis of Clinical Outcomes and Predictors of Management Strategy. Mayo Clin Proc. 2021;96(2):388-99.
- Rossides M, Simard JF, Svenungsson E, von Euler M, Arkema EV. Mortality and Functionality after Stroke in Patients with Systemic Lupus Erythematosus. J Rheumatol. 2017;44(11):1590-6.
- Conrad N, Verbeke G, Molenberghs G, Goetschalckx L, Callender T, Cambridge G, et al. Autoimmune diseases and cardiovascular risk: a population-based study on 19 autoimmune diseases and 12 cardiovascular diseases in 22 million individuals in the UK. Lancet. 2022;400(10354):733-43.
- Cen X, Feng S, Wei S, Yan L, Sun L. Systemic sclerosis and risk of cardiovascular disease: A PRISMA-compliant systemic review and meta-analysis of cohort studies. Medicine (Baltimore). 2020;99(47):e23009.
- Yen TH, Chen YW, Hsieh TY, Chen YM, Huang WN, Chen YH, et al. The risk of major adverse cardiovascular events in patients with systemic sclerosis: a nationwide, population-based cohort study. Rheumatology (Oxford). 2023.
- Aviña-Zubieta JA, Mai A, Amiri N, Dehghan N, Ann Tan J, Sayre EC, et al. Risk of Myocardial Infarction and Stroke in Patients With Granulomatosis With Polyangiitis (Wegener’s): A Population-Based Study. Arthritis Rheumatol. 2016;68(11):2752-9.
- Houben E, Mendel A, Carette S, Voskuyl AE, Penne EL, Pagnoux C. Predictors of fatal and non-fatal cardiovascular events in ANCA-associated vasculitis: Data from the Toronto CanVasc cohort. Joint Bone Spine. 2020;87(3):221-4.
- Nygaard L, Polcwiartek C, Nelveg-Kristensen KE, Carlson N, Kristensen S, Torp-Pedersen C, et al. Increased risk of cardiovascular disease preceding diagnosis of incident ANCA-associated vasculitis: a Danish nationwide study. Rheumatology (Oxford). 2023.
- Stamatis P, Mohammad MA, Gisslander K, Merkel PA, Englund M, Turesson C, et al. Myocardial infarction in a population-based cohort of patients with biopsy-confirmed giant cell arteritis in southern Sweden. RMD Open. 2024;10(2).
- Rathore SS, Srikaram P, Gudena S, Manoj S, Allam SR, Hatamleh MA, et al. Risk of cardiovascular events in giant cell arteritis: systematic review and meta-analysis. Hellenic J Cardiol. 2025;83:78-87.
- Jain H, Shahzad M, Patel N, Passey S, Singh J, Khan R, et al. Is Giant Cell Arteritis Associated with Increased Risk of Cardiovascular Disease? A Meta-Analysis. Cardiol Rev. 2025.
- Mofors J, Holmqvist M, Westermark L, Björk A, Kvarnström M, Forsblad-d’Elia H, et al. Concomitant Ro/SSA and La/SSB antibodies are biomarkers for the risk of venous thromboembolism and cerebral infarction in primary Sjögren’s syndrome. J Intern Med. 2019;286(4):458-68.
- Beltai A, Barnetche T, Daien C, Lukas C, Gaujoux-Viala C, Combe B, et al. Cardiovascular Morbidity and Mortality in Primary Sjögren’s Syndrome: A Systematic Review and Meta-Analysis. Arthritis Care Res (Hoboken). 2020;72(1):131-9.
- Ungprasert P, Suksaranjit P, Spanuchart I, Leeaphorn N, Permpalung N. Risk of coronary artery disease in patients with idiopathic inflammatory myopathies: a systematic review and meta-analysis of observational studies. Semin Arthritis Rheum. 2014;44(1):63-7.
- Zhen C, Wang Y, Wang H, Wang X. The risk of ischemic stroke in patients with idiopathic inflammatory myopathies: a systematic review and meta-analysis. Clin Rheumatol. 2021;40(10):4101-8.
- Loiseau P, Mailhac A, Duhaut P, Thomsen RW. Arterial cardiovascular outcomes and venous thromboembolism in patients with primary Sjogren’s syndrome: a Danish cohort study. Rheumatology (Oxford). 2025;64(8):4678-86.
- Shah JT, Shah KT, Mazori DR, Caplan AS, Hejazi E, Garshick MS, et al. Cardiovascular comorbidities are associated with dermatomyositis: A cross-sectional study in the All of Us Research Program. J Am Acad Dermatol. 2024;90(5):1013-6.
- Beecher G, Muhammad S, Shammas I, Chamberlain AM, Larson K, Mandrekar J, et al. Increased Risk of Myocardial Infarction in Inclusion Body Myositis: A Non-Concurrent Cohort Study. Eur J Neurol. 2025;32(5):e70177.
- Ambrosino P, Lupoli R, Di Minno A, Tasso M, Peluso R, Di Minno MN. Subclinical atherosclerosis in patients with rheumatoid arthritis. A meta-analysis of literature studies. Thromb Haemost. 2015;113(5):916-30.
- Farshad S, Halalau A, Townsend W, Schiopu E. Utility of Coronary Calcium Scoring (CCS) in Connective Tissue Disorders (CTDs) for the Evaluation of Subclinical Coronary Atherosclerosis – A Systematic Review. ACR Open Rheumatol. 2020;2(2):84-91.
- Gonzalez-Juanatey C, Llorca J, Amigo-Diaz E, Dierssen T, Martin J, Gonzalez-Gay MA. High prevalence of subclinical atherosclerosis in psoriatic arthritis patients without clinically evident cardiovascular disease or classic atherosclerosis risk factors. Arthritis Rheum. 2007;57(6):1074-80.
- Arida A, Protogerou AD, Konstantonis G, Konsta M, Delicha EM, Kitas GD, et al. Subclinical Atherosclerosis Is Not Accelerated in Patients with Ankylosing Spondylitis with Low Disease Activity: New Data and Metaanalysis of Published Studies. J Rheumatol. 2015;42(11):2098-105.
- Tektonidou MG, Kravvariti E, Konstantonis G, Tentolouris N, Sfikakis PP, Protogerou A. Subclinical atherosclerosis in Systemic Lupus Erythematosus: Comparable risk with Diabetes Mellitus and Rheumatoid Arthritis. Autoimmun Rev. 2017;16(3):308-12.
- Gustafsson JT, Herlitz Lindberg M, Gunnarsson I, Pettersson S, Elvin K, Öhrvik J, et al. Excess atherosclerosis in systemic lupus erythematosus,-A matter of renal involvement: Case control study of 281 SLE patients and 281 individually matched population controls. PLoS One. 2017;12(4):e0174572.
- Papazoglou N, Sfikakis PP, Tektonidou MG. Atherosclerotic Plaque Progression and Incident Cardiovascular Events in a 10-Year Prospective Study of Patients With Systemic Lupus Erythematosus: The Impact of Persistent Cardiovascular Risk Factor Target Attainment and Sustained DORIS Remission. Arthritis Rheumatol. 2025;77(6):716-26.
- Nordin A, Jensen-Urstad K, Bjornadal L, Pettersson S, Larsson A, Svenungsson E. Ischemic arterial events and atherosclerosis in patients with systemic sclerosis: a population-based case-control study. Arthritis Res Ther. 2013;15(4):R87.
- Turesson C, O’Fallon WM, Crowson CS, Gabriel SE, Matteson EL. Occurrence of extraarticular disease manifestations is associated with excess mortality in a community based cohort of patients with rheumatoid arthritis. J Rheumatol. 2002;29(1):62-7.
- Turesson C, McClelland RL, Christianson TJ, Matteson EL. Severe extra-articular disease manifestations are associated with an increased risk of first ever cardiovascular events in patients with rheumatoid arthritis. Ann Rheum Dis. 2007;66(1):70-5.
- Kaushik P, Solomon DH, Greenberg JD, Anderson JT, Reed G, Pala O, et al. Subcutaneous nodules are associated with cardiovascular events in patients with rheumatoid arthritis: results from a large US registry. Clin Rheumatol. 2015;34(10):1697-704.
- Wållberg-Jonsson S, Johansson H, Öhman ML, Rantapää-Dahlqvist S. Extent of inflammation predicts cardiovascular disease and overall mortality in seropositive rheumatoid arthritis. A retrospective cohort study from disease onset. J Rheumatol. 1999;26(12):2562-71.
- Goodson NJ, Symmons DP, Scott DG, Bunn D, Lunt M, Silman AJ. Baseline levels of C-reactive protein and prediction of death from cardiovascular disease in patients with inflammatory polyarthritis: a ten-year followup study of a primary care-based inception cohort. Arthritis Rheum. 2005;52(8):2293-9.
- Ajeganova S, Andersson ML, Frostegard J, Hafstrom I. Disease factors in early rheumatoid arthritis are associated with differential risks for cardiovascular events and mortality depending on age at onset: a 10-year observational cohort study. J Rheumatol. 2013;40(12):1958-66.
- Innala L, Möller B, Ljung L, Magnusson S, Smedby T, Södergren A, et al. Cardiovascular events in early RA are a result of inflammatory burden and traditional risk factors: a five year prospective study. Arthritis Res Ther. 2011;13(4):R131.
- Zhang J, Chen L, Delzell E, Muntner P, Hillegass WB, Safford MM, et al. Republished: The association between inflammatory markers, serum lipids and the risk of cardiovascular events in patients with rheumatoid arthritis. Postgrad Med J. 2014;90(1070):722-9.
- Arts EE, Fransen J, den Broeder AA, Popa CD, van Riel PL. The effect of disease duration and disease activity on the risk of cardiovascular disease in rheumatoid arthritis patients. Ann Rheum Dis. 2015;74(6):998-1003.
- Myasoedova E, Chandran A, Ilhan B, Major BT, Michet CJ, Matteson EL, et al. The role of rheumatoid arthritis (RA) flare and cumulative burden of RA severity in the risk of cardiovascular disease. 2016;75(3):560-5.
- Delcoigne B, Provan SA, Kristianslund EK, Askling J, Ljung L. How does current disease activity in rheumatoid arthritis affect the short-term risk of acute coronary syndrome? A clinical register based study from Sweden and Norway. Eur J Intern Med. 2023;115:55-61.
- Maradit-Kremers H, Nicola PJ, Crowson CS, Ballman KV, Gabriel SE. Prognostic importance of low body mass index in relation to cardiovascular mortality in rheumatoid arthritis. Arthritis Rheum. 2004;50(11):3450-7.
- del Rincon I, Freeman GL, Haas RW, O’Leary DH, Escalante A. Relative contribution of cardiovascular risk factors and rheumatoid arthritis clinical manifestations to atherosclerosis. Arthritis Rheum. 2005;52(11):3413-23.
- Escalante A, Haas RW, del Rincon I. Paradoxical effect of body mass index on survival in rheumatoid arthritis: role of comorbidity and systemic inflammation. Arch Intern Med. 2005;165(14):1624-9.
- Myasoedova E, Davis JM, Roger VL, Achenbach SJ, Crowson CS. Improved Incidence of Cardiovascular Disease in Patients With Incident Rheumatoid Arthritis in the 2000s: A Population-based Cohort Study. Journal of Rheumatology. 2021;48(9):1379-87.
- Myasoedova E, Gabriel SE, Matteson EL, Davis JM, Therneau TM, Crowson CS. Decreased Cardiovascular Mortality in Patients with Incident Rheumatoid Arthritis (RA) in Recent Years: Dawn of a New Era in Cardiovascular Disease in RA? Journal of Rheumatology. 2017;44(6):732-9.
- Lacaille D, Avina-Zubieta JA, Sayre EC, Abrahamowicz M. Improvement in 5-year mortality in incident rheumatoid arthritis compared with the general population-closing the mortality gap. Ann Rheum Dis. 2017;76(6):1057-63.
- Provan SA, Lillegraven S, Sexton J, Angel K, Austad C, Haavardsholm EA, et al. Trends in all-cause and cardiovascular mortality in patients with incident rheumatoid arthritis: a 20-year follow-up matched case-cohort study. Rheumatology (Oxford). 2020;59(3):505-12.
- Weber BN, Giles JT, Liao KP. Shared inflammatory pathways of rheumatoid arthritis and atherosclerotic cardiovascular disease. Nat Rev Rheumatol. 2023;19(7):417-28.
- Davies R, Williams J, Sime K, Jin HS, Thompson C, Jordan L, et al. The role of interleukin-6 trans-signalling on cardiovascular dysfunction in inflammatory arthritis. Rheumatology (Oxford). 2021;60(6):2852-61.
- Ridker PM, Rane M. Interleukin-6 Signaling and Anti-Interleukin-6 Therapeutics in Cardiovascular Disease. Circ Res. 2021;128(11):1728-46.
- Chan SCW, Teo CK, Li PH, Lau KK, Lau CS, Chung HY. Cardiovascular risk in patients with spondyloarthritis and association with anti-TNF drugs. Ther Adv Musculoskelet Dis. 2021;13:1759720X211032444.
- Lee JL, Sinnathurai P, Buchbinder R, Hill C, Lassere M, March L. Biologics and cardiovascular events in inflammatory arthritis: a prospective national cohort study. Arthritis Res Ther. 2018;20(1):171.
- Agca R, Heslinga SC. EULAR recommendations for cardiovascular disease risk management in patients with rheumatoid arthritis and other forms of inflammatory joint disorders: 2015/2016 update. 2017;76(1):17-28.
- Jacobsson LT, Turesson C, Gulfe A, Kapetanovic MC, Petersson IF, Saxne T, et al. Treatment with tumor necrosis factor blockers is associated with a lower incidence of first cardiovascular events in patients with rheumatoid arthritis. J Rheumatol. 2005;32(7):1213-8.
- Liang KP, Liang KV, Matteson EL, McClelland RL, Christianson TJ, Turesson C. Incidence of noncardiac vascular disease in rheumatoid arthritis and relationship to extraarticular disease manifestations. Arthritis Rheum. 2006;54(2):642-8.
- Zhang J, Chen L, Delzell E, Muntner P, Hillegass WB, Safford MM, et al. The association between inflammatory markers, serum lipids and the risk of cardiovascular events in patients with rheumatoid arthritis. Ann Rheum Dis. 2014;73(7):1301-8.
- Fukui S, Winkelmayer WC, Tedeschi SK, Marrugo J, Guan H, Harrold L, et al. Disease activity of rheumatoid arthritis and kidney function decline: a large prospective registry study. Ann Rheum Dis. 2025;84(2):201-9.
- Wells DK, Ward MM. Nephritis and the risk of acute myocardial infarction in patients with systemic lupus erythematosus. Clin Exp Rheumatol. 2010;28(2):223-9.
- Gustafsson J, Gunnarsson I, Borjesson O, Pettersson S, Moller S, Fei GZ, et al. Predictors of the first cardiovascular event in patients with systemic lupus erythematosus – a prospective cohort study. Arthritis Res Ther. 2009;11(6):R186.
- Solans-Laque R, Fraile G, Rodriguez-Carballeira M, Caminal L, Castillo MJ, Martinez-Valle F, et al. Clinical characteristics and outcome of Spanish patients with ANCA-associated vasculitides: Impact of the vasculitis type, ANCA specificity, and treatment on mortality and morbidity. Medicine (Baltimore). 2017;96(8):e6083.
- Drosos GC, Vedder D, Houben E, Boekel L, Atzeni F, Badreh S, et al. EULAR recommendations for cardiovascular risk management in rheumatic and musculoskeletal diseases, including systemic lupus erythematosus and antiphospholipid syndrome. Ann Rheum Dis. 2022;81(6):768-79.
- Ramirez-Mulhern I, Navarro-Sanchez V, Rivero-Otamendi E, Sanchez-Mejia DE, Zavala-Miranda MF, Mejia-Vilet JM. Effects of sodium-glucose transporter 2 inhibitors in patients with lupus nephritis: a before-and-after retrospective cohort study. Rheumatology (Oxford). 2025.
- Fanouriakis A, Kostopoulou M, Anders HJ, Andersen J, Aringer M, Beresford MW, et al. EULAR recommendations for the management of systemic lupus erythematosus with kidney involvement: 2025 update. Ann Rheum Dis. 2025.
- Tektonidou MG, Andreoli L, Limper M, Amoura Z, Cervera R, Costedoat-Chalumeau N, et al. EULAR recommendations for the management of antiphospholipid syndrome in adults. Ann Rheum Dis. 2019;78(10):1296-304.
- Barbhaiya M, Zuily S, Naden R, Hendry A, Manneville F, Amigo MC, et al. The 2023 ACR/EULAR Antiphospholipid Syndrome Classification Criteria. Arthritis Rheumatol. 2023;75(10):1687-702.
- Vikerfors A, Johansson AB, Gustafsson JT, Jönsen A, Leonard D, Zickert A, et al. Clinical manifestations and anti-phospholipid antibodies in 712 patients with systemic lupus erythematosus: evaluation of two diagnostic assays. Rheumatology (Oxford). 2013;52(3):501-9.
- Pengo V, Ruffatti A, Legnani C, Gresele P, Barcellona D, Erba N, et al. Clinical course of high-risk patients diagnosed with antiphospholipid syndrome. J Thromb Haemost. 2010;8(2):237-42.
- Pengo V, Denas G, Zoppellaro G, Jose SP, Hoxha A, Ruffatti A, et al. Rivaroxaban vs warfarin in high-risk patients with antiphospholipid syndrome. Blood. 2018;132(13):1365-71.
- Adelhelm JBH, Christensen R, Balbi GGM, Voss A. Therapy with direct oral anticoagulants for secondary prevention of thromboembolic events in the antiphospholipid syndrome: a systematic review and meta-analysis of randomised trials. Lupus Sci Med. 2023;10(2).
- Yusuf S, Hawken S, Ounpuu S, Dans T, Avezum A, Lanas F, et al. Effect of potentially modifiable risk factors associated with myocardial infarction in 52 countries (the INTERHEART study): case-control study. Lancet. 2004;364(9438):937-52.
- Yusuf S, Hawken S, Ounpuu S, Dans T, Avezum A, Lanas F, et al. Effect of potentially modifiable risk factors associated with myocardial infarction in 52 countries (the INTERHEART study): case-control study. Lancet. 2004;364(9438):937-52.
- Campos Fernandez C, Fragio Gil JJ, Gonzalez Mazario R, Martinez Calabuig P, Roman Ivorra JA. SCORE2 is superior to SCORE in predicting the presence of carotid plaques and intima-media thickness in rheumatoid arthritis patients: a cross-sectional study using carotid ultrasound. Ther Adv Musculoskelet Dis. 2024;16:1759720X241302667.
- He XW, Wang E, Bao YY, Wang F, Zhu M, Hu XF, et al. High serum levels of sclerostin and Dickkopf-1 are associated with acute ischaemic stroke. Atherosclerosis. 2016;253:22-8.
- Nussdorf A, Park E, Amigues I, Geraldino-Pardilla L, Bokhari S, Giles JT, et al. Associations of galectin-3 levels with measures of vascular disease in patients with rheumatoid arthritis. Semin Arthritis Rheum. 2024;65:152357.
- Pamies A, Llop D, Ibarretxe D, Rosales R, Girona J, Masana L, et al. Enhanced Association of Novel Cardiovascular Biomarkers Fetuin-A and Catestatin with Serological and Inflammatory Markers in Rheumatoid Arthritis Patients. Int J Mol Sci. 2024;25(18).
- Yang Z, Shi L, Xue Y, Zeng T, Shi Y, Lin Y, et al. Interleukin-32 increases in coronary arteries and plasma from patients with coronary artery disease. Clin Chim Acta. 2019;497:104-9.
- Rydell E, Jacobsson LTH, Turesson C. Circulating Interleukin 17A and Other Inflammatory Proteins May Predict Cardiovascular Disease in Early Rheumatoid Arthritis. J Rheumatol. 2024;51(8):752-8.
- Läkemedelsverket 2014;Pageshttps://lakemedelsverket.se/aterosklerotisk_hjart-karlsjukdom.
- Weijers JM, Semb AG, Rollefstad S, Kitas GD, van Riel P. Strategies for implementation of guideline recommended cardiovascular risk management for patients with rheumatoid arthritis: results from a questionnaire survey of expert rheumatology centers. Rheumatol Int. 2020;40(4):523-7.
- Semb AG, Ikdahl E, Wibetoe G, Crowson C, Rollefstad S. Atherosclerotic cardiovascular disease prevention in rheumatoid arthritis. Nat Rev Rheumatol. 2020;16(7):361-79.
- Schmidt TJ, Avina-Zubieta JA, Sayre EC, Abrahamowicz M, Esdaile JM, Lacaille D. Quality of care for cardiovascular disease prevention in rheumatoid arthritis: compliance with hyperlipidemia screening guidelines. Rheumatology (Oxford). 2018;57(10):1789-94.
- Schmidt TJ, Avina-Zubieta JA, Sayre EC, Abrahamowicz M, Esdaile JM, Lacaille D. Cardiovascular Disease Prevention in Rheumatoid Arthritis: Compliance with Diabetes Screening Guidelines. J Rheumatol. 2018;45(10):1367-74.
- SCORE2-OP risk prediction algorithms: estimating incident cardiovascular event risk in older persons in four geographical risk regions. Eur Heart J. 2021;42(25):2455-67.
- SCORE2 risk prediction algorithms: new models to estimate 10-year risk of cardiovascular disease in Europe. Eur Heart J. 2021;42(25):2439-54.
- Brunström M, Andersson J, Eliasson M, Fu M, Hansson PO, Söderberg S. [SCORE2 – an updated model for cardiovascular risk prediction]. Lakartidningen. 2021;118.
- Khan SS, Matsushita K, Sang Y, Ballew SH, Grams ME, Surapaneni A, et al. Development and Validation of the American Heart Association’s PREVENT Equations. Circulation. 2024;149(6):430-49.
- Visseren FLJ, Mach F, Smulders YM, Carballo D, Koskinas KC, Back M, et al. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J. 2021;42(34):3227-337.
- Solomon DH, Greenberg J, Curtis JR, Liu M, Farkouh ME, Tsao P, et al. Derivation and internal validation of an expanded cardiovascular risk prediction score for rheumatoid arthritis: a Consortium of Rheumatology Researchers of North America Registry Study. Arthritis Rheumatol. 2015;67(8):1995-2003.
- Crowson CS, Gabriel SE, Semb AG, van Riel P, Karpouzas G, Dessein PH, et al. Rheumatoid arthritis-specific cardiovascular risk scores are not superior to general risk scores: a validation analysis of patients from seven countries. Rheumatology (Oxford). 2017;56(7):1102-10.
- Wahlin B, Innala L, Magnusson S, Möller B, Smedby T, Rantapää-Dahlqvist S, et al. Performance of the Expanded Cardiovascular Risk Prediction Score for Rheumatoid Arthritis Is Not Superior to the ACC/AHA Risk Calculator. The Journal of Rheumatology. 2019;46(2):130-7.
- Ljung L, Ueda P, Liao KP, Greenberg JD, Etzel CJ, Solomon DH, et al. Performance of the Expanded Cardiovascular Risk Prediction Score for Rheumatoid Arthritis in a geographically distant National Register-based cohort: an external validation. RMD Open. 2018;4(2):e000771.
- Burggraaf B, van Breukelen-van der Stoep DF, de Vries MA, Klop B, Liem AH, van de Geijn GM, et al. Effect of a treat-to-target intervention of cardiovascular risk factors on subclinical and clinical atherosclerosis in rheumatoid arthritis: a randomised clinical trial. Ann Rheum Dis. 2019;78(3):335-41.
- Stampfer MJ, Hu FB, Manson JE, Rimm EB, Willett WC. Primary prevention of coronary heart disease in women through diet and lifestyle. N Engl J Med. 2000;343(1):16-22.
- van Dam RM, Li T, Spiegelman D, Franco OH, Hu FB. Combined impact of lifestyle factors on mortality: prospective cohort study in US women. BMJ. 2008;337:a1440.
- Toloza SM, Uribe AG, McGwin G, Jr., Alarcon GS, Fessler BJ, Bastian HM, et al. Systemic lupus erythematosus in a multiethnic US cohort (LUMINA). XXIII. Baseline predictors of vascular events. Arthritis Rheum. 2004;50(12):3947-57.
- Wieczorek M, Gwinnutt JM, Ransay-Colle M, Balanescu A, Bischoff-Ferrari H, Boonen A, et al. Smoking, alcohol consumption and disease-specific outcomes in rheumatic and musculoskeletal diseases (RMDs): systematic reviews informing the 2021 EULAR recommendations for lifestyle improvements in people with RMDs. RMD Open. 2022;8(1).
- Reid S, Hagberg N, Sandling JK, Alexsson A, Pucholt P, Sjöwall C, et al. Interaction between the STAT4 rs11889341(T) risk allele and smoking confers increased risk of myocardial infarction and nephritis in patients with systemic lupus erythematosus. Ann Rheum Dis. 2021;80(9):1183-9.
- Crowson CS, Rollefstad S, Ikdahl E, Kitas GD, van Riel P, Gabriel SE, et al. Impact of risk factors associated with cardiovascular outcomes in patients with rheumatoid arthritis. Ann Rheum Dis. 2018;77(1):48-54.
- Baghdadi LR, Woodman RJ, Shanahan EM, Mangoni AA. The impact of traditional cardiovascular risk factors on cardiovascular outcomes in patients with rheumatoid arthritis: a systematic review and meta-analysis. PLoS One. 2015;10(2):e0117952.
- Roelsgaard IK, Ikdahl E, Rollefstad S, Wibetoe G, Esbensen BA, Kitas GD, et al. Smoking cessation is associated with lower disease activity and predicts cardiovascular risk reduction in rheumatoid arthritis patients. Rheumatology (Oxford). 2020;59(8):1997-2004.
- Lewington S, Clarke R, Qizilbash N, Peto R, Collins R. Age-specific relevance of usual blood pressure to vascular mortality: a meta-analysis of individual data for one million adults in 61 prospective studies. Lancet. 2002;360(9349):1903-13.
- Collins R, Peto R, MacMahon S, Hebert P, Fiebach NH, Eberlein KA, et al. Blood pressure, stroke, and coronary heart disease. Part 2, Short-term reductions in blood pressure: overview of randomised drug trials in their epidemiological context. Lancet. 1990;335(8693):827-38.
- Gonzalez A, Maradit Kremers H, Crowson CS, Ballman KV, Roger VL, Jacobsen SJ, et al. Do cardiovascular risk factors confer the same risk for cardiovascular outcomes in rheumatoid arthritis patients as in non-rheumatoid arthritis patients? Ann Rheum Dis. 2008;67(1):64-9.
- Rahman P, Urowitz MB, Gladman DD, Bruce IN, Genest J, Jr. Contribution of traditional risk factors to coronary artery disease in patients with systemic lupus erythematosus. J Rheumatol. 1999;26(11):2363-8.
- Eder L, Wu Y, Chandran V, Cook R, Gladman DD. Incidence and predictors for cardiovascular events in patients with psoriatic arthritis. Ann Rheum Dis. 2016;75(9):1680-6.
- Protogerou AD, Panagiotakos DB, Zampeli E, Argyris AA, Arida K, Konstantonis GD, et al. Arterial hypertension assessed ”out-of-office” in a contemporary cohort of rheumatoid arthritis patients free of cardiovascular disease is characterized by high prevalence, low awareness, poor control and increased vascular damage-associated ”white coat” phenomenon. Arthritis Res Ther. 2013;15(5):R142.
- Myasoedova E, Crowson CS, Kremers HM, Roger VL, Fitz-Gibbon PD, Therneau TM, et al. Lipid paradox in rheumatoid arthritis: the impact of serum lipid measures and systemic inflammation on the risk of cardiovascular disease. Ann Rheum Dis. 2011;70(3):482-7.
- Behl T, Kaur I, Sehgal A, Zengin G, Brisc C, Brisc MC, et al. The Lipid Paradox as a Metabolic Checkpoint and Its Therapeutic Significance in Ameliorating the Associated Cardiovascular Risks in Rheumatoid Arthritis Patients. Int J Mol Sci. 2020;21(24).
- Jacobsson L, Forsblad d’Elia H, Husmark T, Lopis Soler J, Nilsson N, Lindstrom U, et al. The lipid paradox is also present in early axial spondyloarthritis: results from the Swedish part of the SPondyloArthritis Caught Early (SPACE) cohort. Scand J Rheumatol. 2025;54(2):106-11.
- Rantapää-Dahlqvist S, Wållberg-Jonsson S, Dahlen G. Lipoprotein (a), lipids, and lipoproteins in patients with rheumatoid arthritis. Ann Rheum Dis. 1991;50(6):366-8.
- Svenungsson E, Gunnarsson I, Fei GZ, Lundberg IE, Klareskog L, Frostegård J. Elevated triglycerides and low levels of high-density lipoprotein as markers of disease activity in association with up-regulation of the tumor necrosis factor alpha/tumor necrosis factor receptor system in systemic lupus erythematosus. Arthritis Rheum. 2003;48(9):2533-40.
- Mathieu S, Gossec L, Dougados M, Soubrier M. Cardiovascular profile in ankylosing spondylitis: a systematic review and meta-analysis. Arthritis Care Res (Hoboken). 2011;63(4):557-63.
- Liao KP, Liu J, Lu B, Solomon DH, Kim SC. Association between lipid levels and major adverse cardiovascular events in rheumatoid arthritis compared to non-rheumatoid arthritis patients. Arthritis Rheumatol. 2015;67(8):2004-10.
- Charles-Schoeman C, Wang X, Lee YY, Shahbazian A, Navarro-Millán I, Yang S, et al. Association of Triple Therapy With Improvement in Cholesterol Profiles Over Two-Year Followup in the Treatment of Early Aggressive Rheumatoid Arthritis Trial. Arthritis Rheumatol. 2016;68(3):577-86.
- Navarro-Millán I, Charles-Schoeman C, Yang S, Bathon JM, Bridges SL, Jr., Chen L, et al. Changes in lipoproteins associated with methotrexate or combination therapy in early rheumatoid arthritis: results from the treatment of early rheumatoid arthritis trial. Arthritis Rheum. 2013;65(6):1430-8.
- McCarey DW, McInnes IB, Madhok R, Hampson R, Scherbakov O, Ford I, et al. Trial of Atorvastatin in Rheumatoid Arthritis (TARA): double-blind, randomised placebo-controlled trial. Lancet. 2004;363(9426):2015-21.
- Kitas GD, Nightingale P, Armitage J, Sattar N, Belch JJF, Symmons DPM. A Multicenter, Randomized, Placebo-Controlled Trial of Atorvastatin for the Primary Prevention of Cardiovascular Events in Patients With Rheumatoid Arthritis. Arthritis Rheumatol. 2019;71(9):1437-49.
- Rollefstad S, Ikdahl E, Hisdal J, Olsen IC, Holme I, Hammer HB, et al. Rosuvastatin-Induced Carotid Plaque Regression in Patients With Inflammatory Joint Diseases: The Rosuvastatin in Rheumatoid Arthritis, Ankylosing Spondylitis and Other Inflammatory Joint Diseases Study. Arthritis Rheumatol. 2015;67(7):1718-28.
- Petri MA, Kiani AN, Post W, Christopher-Stine L, Magder LS. Lupus Atherosclerosis Prevention Study (LAPS). Ann Rheum Dis. 2011;70(5):760-5.
- Yu HH, Chen PC, Yang YH, Wang LC, Lee JH, Lin YT, et al. Statin reduces mortality and morbidity in systemic lupus erythematosus patients with hyperlipidemia: A nationwide population-based cohort study. Atherosclerosis. 2015;243(1):11-8.
- Tao CY, Shang J, Chen T, Yu D, Jiang YM, Liu D, et al. Impact of antimalarial (AM) on serum lipids in systemic lupus erythematosus (SLE) patients: A systematic review and meta-analysis. Medicine (Baltimore). 2019;98(14):e15030.
- Aguiar EJ, Morgan PJ, Collins CE, Plotnikoff RC, Callister R. Efficacy of interventions that include diet, aerobic and resistance training components for type 2 diabetes prevention: a systematic review with meta-analysis. Int J Behav Nutr Phys Act. 2014;11:2.
- Hemmingsen B, Sonne DP, Metzendorf MI, Richter B. Insulin secretagogues for prevention or delay of type 2 diabetes mellitus and its associated complications in persons at increased risk for the development of type 2 diabetes mellitus. Cochrane Database Syst Rev. 2016;10:CD012151.
- Bruce IN, Urowitz MB, Gladman DD, Ibanez D, Steiner G. Risk factors for coronary heart disease in women with systemic lupus erythematosus: the Toronto Risk Factor Study. Arthritis Rheum. 2003;48(11):3159-67.
- Simard JF, Mittleman MA. Prevalent rheumatoid arthritis and diabetes among NHANES III participants aged 60 and older. J Rheumatol. 2007;34(3):469-73.
- Svenungsson E, Jensen-Urstad K, Heimburger M, Silveira A, Hamsten A, de Faire U, et al. Risk factors for cardiovascular disease in systemic lupus erythematosus. Circulation. 2001;104(16):1887-93.
- van den Oever IA, van Sijl AM, Nurmohamed MT. Management of cardiovascular risk in patients with rheumatoid arthritis: evidence and expert opinion. Ther Adv Musculoskelet Dis. 2013;5(4):166-81.
- Liao KP, Solomon DH. Traditional cardiovascular risk factors, inflammation and cardiovascular risk in rheumatoid arthritis. Rheumatology (Oxford). 2013;52(1):45-52.
- Albrecht K, Luque Ramos A, Hoffmann F, Redeker I, Zink A. High prevalence of diabetes in patients with rheumatoid arthritis: results from a questionnaire survey linked to claims data. Rheumatology (Oxford). 2018;57(2):329-36.
- Nikiphorou E, de Lusignan S, Mallen C, Roberts J, Khavandi K, Bedarida G, et al. Prognostic value of comorbidity indices and lung diseases in early rheumatoid arthritis: a UK population-based study. Rheumatology (Oxford). 2019.
- McFarlane IM, Zhaz Leon SY, Bhamra MS, Burza A, Waite SA, Rodriguez Alvarez M, et al. Assessment of Cardiovascular Disease Risk and Therapeutic Patterns among Urban Black Rheumatoid Arthritis Patients. Med Sci (Basel). 2019;7(2).
- Liao KF, Kuo YH, Lai SW. Diabetes mellitus in ankylosing spondylitis. Ann Rheum Dis. 2019.
- Castro LL, Lanna CCD, Ribeiro ALP, Telles RW. Recognition and control of hypertension, diabetes, and dyslipidemia in patients with systemic lupus erythematosus. Clin Rheumatol. 2018;37(10):2693-8.
- Muñoz C, Isenberg DA. Review of major endocrine abnormalities in patients with systemic lupus erythematosus. Clin Exp Rheumatol. 2019;37(5):791-6.
- Panopoulos S, Tektonidou M, Drosos AA, Liossis SN, Dimitroulas T, Garyfallos A, et al. Prevalence of comorbidities in systemic sclerosis versus rheumatoid arthritis: a comparative, multicenter, matched-cohort study. Arthritis Res Ther. 2018;20(1):267.
- Panopoulos S, Thomas K, Georgiopoulos G, Boumpas D, Katsiari C, Bertsias G, et al. Comparable or higher prevalence of comorbidities in antiphospholipid syndrome vs rheumatoid arthritis: a multicenter, case-control study. Rheumatology (Oxford). 2021;60(1):170-8.
- Cohen AD, Dreiher J, Shapiro Y, Vidavsky L, Vardy DA, Davidovici B, et al. Psoriasis and diabetes: a population-based cross-sectional study. J Eur Acad Dermatol Venereol. 2008;22(5):585-9.
- Gisondi P, Tessari G, Conti A, Piaserico S, Schianchi S, Peserico A, et al. Prevalence of metabolic syndrome in patients with psoriasis: a hospital-based case-control study. Br J Dermatol. 2007;157(1):68-73.
- Sommer DM, Jenisch S, Suchan M, Christophers E, Weichenthal M. Increased prevalence of the metabolic syndrome in patients with moderate to severe psoriasis. Arch Dermatol Res. 2006;298(7):321-8.
- Coto-Segura P, Eiris-Salvado N, Gonzalez-Lara L, Queiro-Silva R, Martinez-Camblor P, Maldonado-Seral C, et al. Psoriasis, psoriatic arthritis and type 2 diabetes mellitus: a systematic review and meta-analysis. Br J Dermatol. 2013;169(4):783-93.
- Ogdie A, Schwartzman S, Husni ME. Recognizing and managing comorbidities in psoriatic arthritis. Curr Opin Rheumatol. 2015;27(2):118-26.
- Charlton R, Green A, Shaddick G, Snowball J, Nightingale A, Tillett W, et al. Risk of type 2 diabetes and cardiovascular disease in an incident cohort of people with psoriatic arthritis: a population-based cohort study. Rheumatology (Oxford). 2019;58(1):144-8.
- Landgren AJ, Bilberg A, Eliasson B, Larsson I, Dehlin M, Jacobsson L, et al. Cardiovascular risk factors are highly overrepresented in Swedish patients with psoriatic arthritis compared with the general population. Scand J Rheumatol. 2020;49(3):195-9.
- Svenson KL, Pollare T, Lithell H, Hallgren R. Impaired glucose handling in active rheumatoid arthritis: relationship to peripheral insulin resistance. Metabolism. 1988;37(2):125-30.
- El Magadmi M, Ahmad Y, Turkie W, Yates AP, Sheikh N, Bernstein RM, et al. Hyperinsulinemia, insulin resistance, and circulating oxidized low density lipoprotein in women with systemic lupus erythematosus. J Rheumatol. 2006;33(1):50-6.
- Festa A, D’Agostino R, Jr., Howard G, Mykkanen L, Tracy RP, Haffner SM. Chronic subclinical inflammation as part of the insulin resistance syndrome: the Insulin Resistance Atherosclerosis Study (IRAS). Circulation. 2000;102(1):42-7.
- Greenfield JR, Campbell LV. Relationship between inflammation, insulin resistance and type 2 diabetes: ’cause or effect’? Curr Diabetes Rev. 2006;2(2):195-211.
- Paul SK, Montvida O, Best JH, Gale S, Pethö-Schramm A, Sarsour K. Association of biological antirheumatic therapy with risk for type 2 diabetes: a retrospective cohort study in incident rheumatoid arthritis. BMJ Open. 2021;11(6):e042246.
- Baker JF, England BR, George M, Cannon G, Sauer B, Ogdie A, et al. Disease activity, cytokines, chemokines and the risk of incident diabetes in rheumatoid arthritis. Ann Rheum Dis. 2021;80(5):566-72.
- Genovese MC, Burmester GR, Hagino O, Thangavelu K, Iglesias-Rodriguez M, John GS, et al. Interleukin-6 receptor blockade or TNFα inhibition for reducing glycaemia in patients with RA and diabetes: post hoc analyses of three randomised, controlled trials. Arthritis Res Ther. 2020;22(1):206.
- Salmasi S, Sayre EC, Antonio Aviña-Zubieta J, Esdaile JM, De Vera MA. Adherence to Antimalarial Therapy and Risk of Type 2 Diabetes Mellitus Among Patients With Systemic Lupus Erythematosus: A Population-Based Study. Arthritis Care Res (Hoboken). 2021;73(5):702-6.
- Sandoval-Rosario M, Nayeri BM, Rascon A, Boring M, Aseret-Manygoats T, Helmick CG, et al. Prevalence of Arthritis Among Adults with Prediabetes and Arthritis-Specific Barriers to Important Interventions for Prediabetes – United States, 2009-2016. MMWR Morb Mortal Wkly Rep. 2018;67(44):1238-41.
- Semb AG, Rollefstad S, Ikdahl E, Wibetoe G, Sexton J, Crowson C, et al. Diabetes mellitus and cardiovascular risk management in patients with rheumatoid arthritis: an international audit. RMD Open. 2021;7(2).
- Kwon OC, Han K, Chun J, Kim R, Hong SW, Kim JH, et al. Effects of immune-mediated inflammatory diseases on cardiovascular diseases in patients with type 2 diabetes: a nationwide population-based study. Sci Rep. 2022;12(1):11548.
- Alsing CL, Igland J, Nystad TW, Midtbo H, Ikdahl E, Naess H, et al. Data-driven identification of subgroups in early rheumatoid arthritis: mortality and cardiovascular disease in a cohort from western Norway. RMD Open. 2025;11(3).
- Huang PL. A comprehensive definition for metabolic syndrome. Dis Model Mech. 2009;2(5-6):231-7.
- Haroon M, Rafiq Chaudhry AB, Fitzgerald O. Higher Prevalence of Metabolic Syndrome in Patients with Psoriatic Arthritis: A Comparison with a Control Group of Noninflammatory Rheumatologic Conditions. J Rheumatol. 2016;43(2):463-4.
- Andreasson S, Sodergren A. Prevalence of metabolic syndrome and its components in psoriatic arthritis compared with general population, cutaneous psoriasis, and other inflammatory arthropathies: a meta-analysis. Clin Rheumatol. 2025;44(10):3787-99.
- Raychaudhuri SP. Comorbidities of psoriatic arthritis — metabolic syndrome and prevention: a report from the GRAPPA 2010 annual meeting. J Rheumatol. 2012;39(2):437-40.
- Jafari M, Patel K, Mahapatro A, Amirian B, Saeedi C, Sahu S, et al. Global prevalence of metabolic syndrome in patients with Rheumatoid arthritis: a systematic review and meta-analysis. BMC Rheumatol. 2025;9(1):116.
- Hintenberger R, Affenzeller B, Vladychuk V, Pieringer H. Cardiovascular risk in axial spondyloarthritis-a systematic review. Clin Rheumatol. 2023;42(10):2621-33.
- Mok CC. Metabolic syndrome and systemic lupus erythematosus: the connection. Expert Rev Clin Immunol. 2019;15(7):765-75.
- Yusuf S, Hawken S, Ounpuu S, Bautista L, Franzosi MG, Commerford P, et al. Obesity and the risk of myocardial infarction in 27,000 participants from 52 countries: a case-control study. Lancet. 2005;366(9497):1640-9.
- Karpouzas GA, Gonzalez-Gay MA, Corrales A, Myasoedova E, Rantapaa-Dahlqvist S, Sfikakis PP, et al. Influence of body mass index on cardiovascular risk in rheumatoid arthritis varies across anti-citrullinated protein antibody status and biologic use. RMD Open. 2025;11(2).
- Walsmith J, Abad L, Kehayias J, Roubenoff R. Tumor necrosis factor-alpha production is associated with less body cell mass in women with rheumatoid arthritis. J Rheumatol. 2004;31(1):23-9.
- Westhovens R, Nijs J, Taelman V, Dequeker J. Body composition in rheumatoid arthritis. Br J Rheumatol. 1997;36(4):444-8.
- Elkan AC, Engvall IL, Cederholm T, Hafstrom I. Rheumatoid cachexia, central obesity and malnutrition in patients with low-active rheumatoid arthritis: feasibility of anthropometry, Mini Nutritional Assessment and body composition techniques. Eur J Nutr. 2009;48(5):315-22.
- Yoshida T, Hashimoto M, Kawahara R, Yamamoto H, Tanaka M, Ito H, et al. Non-obese visceral adiposity is associated with the risk of atherosclerosis in Japanese patients with rheumatoid arthritis: a cross-sectional study. Rheumatol Int. 2018;38(9):1679-89.
- Delgado-Frías E, González-Gay MA, Muñiz-Montes JR, Gómez Rodríguez-Bethencourt MA, González-Díaz A, Díaz-González F, et al. Relationship of abdominal adiposity and body composition with endothelial dysfunction in patients with rheumatoid arthritis. Clin Exp Rheumatol. 2015;33(4):516-23.
- Kipen Y, Briganti EM, Strauss BJ, Littlejohn GO, Morand EF. Three year follow-up of body composition changes in pre-menopausal women with systemic lupus erythematosus. Rheumatology (Oxford). 1999;38(1):59-65.
- Sacre K, Escoubet B, Zennaro MC, Chauveheid MP, Gayat E, Papo T. Overweight Is a Major Contributor to Atherosclerosis in Systemic Lupus Erythematosus Patients at Apparent Low Risk for Cardiovascular Disease: A Cross-Sectional Controlled Study. Medicine (Baltimore). 2015;94(48):e2177.
- Radner H, Lesperance T, Accortt NA, Solomon DH. Incidence and Prevalence of Cardiovascular Risk Factors Among Patients With Rheumatoid Arthritis, Psoriasis, or Psoriatic Arthritis. Arthritis Care Res (Hoboken). 2017;69(10):1510-8.
- Haddad A, Saliba W, Lavi I, Batheesh A, Kasem S, Gazitt T, et al. The Association of Psoriatic Arthritis With All-cause Mortality and Leading Causes of Death in Psoriatic Arthritis. J Rheumatol. 2022;49(2):165-70.
- Allebeck P, Andreasson S, Wåhlin S, Ramstedt M, Gripenberg J, Damström-Thakker K, et al. Alkoholkonsumtion och risknivåer. Kunskapsunderlag och förslag till rekommendationer. . Stockholm: Centrum för epidemiologi och samhällsmedicin, Stockholms läns landsting; 2018.
- Socialstyrelsen. Nationella riktlinjer 2024:
Vård vid ohälsosamma
levnadsvanor. 2024.
- Corrao G, Bagnardi V, Zambon A, La Vecchia C. A meta-analysis of alcohol consumption and the risk of 15 diseases. Prev Med. 2004;38(5):613-9.
- Corrao G, Rubbiati L, Bagnardi V, Zambon A, Poikolainen K. Alcohol and coronary heart disease: a meta-analysis. Addiction. 2000;95(10):1505-23.
- Zhang C, Qin YY, Chen Q, Jiang H, Chen XZ, Xu CL, et al. Alcohol intake and risk of stroke: a dose-response meta-analysis of prospective studies. Int J Cardiol. 2014;174(3):669-77.
- Taylor B, Irving HM, Baliunas D, Roerecke M, Patra J, Mohapatra S, et al. Alcohol and hypertension: gender differences in dose-response relationships determined through systematic review and meta-analysis. Addiction. 2009;104(12):1981-90.
- Wood AM, Kaptoge S, Butterworth AS, Willeit P, Warnakula S, Bolton T, et al. Risk thresholds for alcohol consumption: combined analysis of individual-participant data for 599 912 current drinkers in 83 prospective studies. Lancet. 2018;391(10129):1513-23.
- Alcohol use and burden for 195 countries and territories, 1990-2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet. 2018;392(10152):1015-35.
- Ding C, O’Neill D, Bell S, Stamatakis E, Britton A. Association of alcohol consumption with morbidity and mortality in patients with cardiovascular disease: original data and meta-analysis of 48,423 men and women. BMC Med. 2021;19(1):167.
- Yrkesföreningar för fysisk aktivitet (YFA). Dorn IM JE, Börjesson M, Hagströmer M, red. . Fysisk aktivitet i sjukdomsprevention och sjukdomsbehandling, FYSS 2021: The Swedish National Institute of Public Health, Yrkesföreningar för fysisk aktivitet.; 2021.
- Garber CE, Blissmer B, Deschenes MR, Franklin BA, Lamonte MJ, Lee IM, et al. American College of Sports Medicine position stand. Quantity and quality of exercise for developing and maintaining cardiorespiratory, musculoskeletal, and neuromotor fitness in apparently healthy adults: guidance for prescribing exercise. Med Sci Sports Exerc. 2011;43(7):1334-59.
- Piepoli MF, Hoes AW, Agewall S, Albus C, Brotons C, Catapano AL, et al. 2016 European Guidelines on cardiovascular disease prevention in clinical practice: The Sixth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (constituted by representatives of 10 societies and by invited experts) Developed with the special contribution of the European Association for Cardiovascular Prevention & Rehabilitation (EACPR). Atherosclerosis. 2016;252:207-74.
- Arnett DK, Khera A, Blumenthal RS. 2019 ACC/AHA Guideline on the Primary Prevention of Cardiovascular Disease: Part 1, Lifestyle and Behavioral Factors. JAMA Cardiol. 2019.
- Gwinnutt JM, Wieczorek M, Cavalli G, Balanescu A, Bischoff-Ferrari HA, Boonen A, et al. Effects of physical exercise and body weight on disease-specific outcomes of people with rheumatic and musculoskeletal diseases (RMDs): systematic reviews and meta-analyses informing the 2021 EULAR recommendations for lifestyle improvements in people with RMDs. RMD Open. 2022;8(1).
- Stavropoulos-Kalinoglou A, Metsios GS, Veldhuijzen van Zanten JJ, Nightingale P, Kitas GD, Koutedakis Y. Individualised aerobic and resistance exercise training improves cardiorespiratory fitness and reduces cardiovascular risk in patients with rheumatoid arthritis. Ann Rheum Dis. 2013;72(11):1819-25.
- van den Ende CH, Hazes JM, le Cessie S, Mulder WJ, Belfor DG, Breedveld FC, et al. Comparison of high and low intensity training in well controlled rheumatoid arthritis. Results of a randomised clinical trial. Ann Rheum Dis. 1996;55(11):798-805.
- Hörnberg K, Ångström L, Wållberg-Jonsson S. Benefits of spinning exercise on cardiovascular risk factors in Rheumatoid Arthritis: A pilot study. Cardiopulm Phys Ther J. 2014;25(3):68-74.
- Metsios GS, Koutedakis Y, Veldhuijzen van Zanten JJ, Stavropoulos-Kalinoglou A, Vitalis P, Duda JL, et al. Cardiorespiratory fitness levels and their association with cardiovascular profile in patients with rheumatoid arthritis: a cross-sectional study. Rheumatology (Oxford). 2015.
- Kessler J, Chouk M, Ruban T, Prati C, Wendling D, Verhoeven F. Psoriatic arthritis and physical activity: a systematic review. Clin Rheumatol. 2021;40(11):4379-89.
- Sveaas SH, Bilberg A, Berg IJ, Provan SA, Rollefstad S, Semb AG, et al. High intensity exercise for 3 months reduces disease activity in axial spondyloarthritis (axSpA): a multicentre randomised trial of 100 patients. Br J Sports Med. 2020;54(5):292-7.
- Bilberg A, Mannerkorpi K, Borjesson M, Svedlund S, Sivertsson J, Klingberg E, et al. High-intensity interval training improves cardiovascular and physical health in patients with rheumatoid arthritis: a multicentre randomised controlled trial. Br J Sports Med. 2024;58(23):1409-18.
- Alexanderson H, Bostrom C. Exercise therapy in patients with idiopathic inflammatory myopathies and systemic lupus erythematosus – A systematic literature review. Best Pract Res Clin Rheumatol. 2020;34(2):101547.
- Blaess J, Geneton S, Goepfert T, Appenzeller S, Bordier G, Davergne T, et al. Recommendations for physical activity and exercise in persons living with Systemic Lupus Erythematosus (SLE): consensus by an international task force. RMD Open. 2024;10(2).
- de Oliveira NC, Portes LA, Pettersson H, Alexanderson H, Bostrom C. Aerobic and resistance exercise in systemic sclerosis: State of the art. Musculoskeletal Care. 2017;15(4):316-23.
- Mallmann ALS, de Moraes DN, Doria LD, Dos Santos LP, Pilotti S, de Souza Antunes MA, et al. Effects of interventions with resistance exercises on muscle strength, physical disability, and quality of life in systemic sclerosis patients: a systematic review with meta-analysis. Adv Rheumatol. 2025;65(1):34.
- Pettersson H, Alexanderson H, Poole JL, Varga J, Regardt M, Russell AM, et al. Exercise as a multi-modal disease-modifying medicine in systemic sclerosis: An introduction by The Global Fellowship on Rehabilitation and Exercise in Systemic Sclerosis (G-FoRSS). Best Pract Res Clin Rheumatol. 2021;35(3):101695.
- Bremander A, Malm K, Andersson ML. Physical activity in established rheumatoid arthritis and variables associated with maintenance of physical activity over a seven-year period – a longitudinal observational study. BMC Rheumatol. 2020;4:53.
- Kivimaki M, Steptoe A. Effects of stress on the development and progression of cardiovascular disease. Nat Rev Cardiol. 2018;15(4):215-29.
- Backe EM, Seidler A, Latza U, Rossnagel K, Schumann B. The role of psychosocial stress at work for the development of cardiovascular diseases: a systematic review. Int Arch Occup Environ Health. 2012;85(1):67-79.
- Orth-Gomer K, Wamala SP, Horsten M, Schenck-Gustafsson K, Schneiderman N, Mittleman MA. Marital stress worsens prognosis in women with coronary heart disease: The Stockholm Female Coronary Risk Study. JAMA. 2000;284(23):3008-14.
- Rosengren A, Hawken S, Ounpuu S, Sliwa K, Zubaid M, Almahmeed WA, et al. Association of psychosocial risk factors with risk of acute myocardial infarction in 11119 cases and 13648 controls from 52 countries (the INTERHEART study): case-control study. Lancet. 2004;364(9438):953-62.
- Wang HX, Leineweber C, Kirkeeide R, Svane B, Schenck-Gustafsson K, Theorell T, et al. Psychosocial stress and atherosclerosis: family and work stress accelerate progression of coronary disease in women. The Stockholm Female Coronary Angiography Study. J Intern Med. 2007;261(3):245-54.
- Smyth A, O’Donnell M, Lamelas P, Teo K, Rangarajan S, Yusuf S. Physical Activity and Anger or Emotional Upset as Triggers of Acute Myocardial Infarction: The INTERHEART Study. Circulation. 2016;134(15):1059-67.
- Fang F, Fall K, Mittleman MA, Sparen P, Ye W, Adami HO, et al. Suicide and cardiovascular death after a cancer diagnosis. N Engl J Med. 2012;366(14):1310-8.
- Nyberg ST, Heikkila K, Fransson EI, Alfredsson L, De Bacquer D, Bjorner JB, et al. Job strain in relation to body mass index: pooled analysis of 160 000 adults from 13 cohort studies. J Intern Med. 2012;272(1):65-73.
- Wardle J, Chida Y, Gibson EL, Whitaker KL, Steptoe A. Stress and adiposity: a meta-analysis of longitudinal studies. Obesity (Silver Spring). 2011;19(4):771-8.
- Chandola T, Brunner E, Marmot M. Chronic stress at work and the metabolic syndrome: prospective study. Bmj. 2006;332(7540):521-5.
- Chandola T, Britton A, Brunner E, Hemingway H, Malik M, Kumari M, et al. Work stress and coronary heart disease: what are the mechanisms? Eur Heart J. 2008;29(5):640-8.
- Nawrot TS, Perez L, Kunzli N, Munters E, Nemery B. Public health importance of triggers of myocardial infarction: a comparative risk assessment. Lancet. 2011;377(9767):732-40.
- Mostofsky E, Maclure M, Sherwood JB, Tofler GH, Muller JE, Mittleman MA. Risk of acute myocardial infarction after the death of a significant person in one’s life: the Determinants of Myocardial Infarction Onset Study. Circulation. 2012;125(3):491-6.
- Akerstedt T. Psychosocial stress and impaired sleep. Scand J Work Environ Health. 2006;32(6):493-501.
- Minkel JD, Banks S, Htaik O, Moreta MC, Jones CW, McGlinchey EL, et al. Sleep deprivation and stressors: evidence for elevated negative affect in response to mild stressors when sleep deprived. Emotion. 2012;12(5):1015-20.
- Yin J, Jin X, Shan Z, Li S, Huang H, Li P, et al. Relationship of Sleep Duration With All-Cause Mortality and Cardiovascular Events: A Systematic Review and Dose-Response Meta-Analysis of Prospective Cohort Studies. J Am Heart Assoc. 2017;6(9).
- Maynard JW, Fang H, Petri M. Low socioeconomic status is associated with cardiovascular risk factors and outcomes in systemic lupus erythematosus. J Rheumatol. 2012;39(4):777-83.
- Liu YL, Szklo M, Davidson KW, Bathon JM, Giles JT. Differential Association of Psychosocial Comorbidities With Subclinical Atherosclerosis in Rheumatoid Arthritis. Arthritis Care Res (Hoboken). 2015;67(10):1335-44.
- Hörnberg K, Pomeroy J, Sandberg C, Ångström L, Södergren A, Sundström B. Isotemporal Substitution of Time Between Sleep and Physical Activity: Associations With Cardiovascular Risk Factors in Early Rheumatoid Arthritis. ACR Open Rheumatol. 2021;3(3):138-46.
- Sveaas SH, Dagfinrud H, Berg IJ, Provan SA, Johansen MW, Pedersen E, et al. High-Intensity Exercise Improves Fatigue, Sleep, and Mood in Patients With Axial Spondyloarthritis: Secondary Analysis of a Randomized Controlled Trial. Phys Ther. 2020;100(8):1323-32.

