Hantering av antireumatiska läkemedel vid elektiv ortopedisk kirurgi
Introduktion
En översikt från Svensk Reumatologisk Förening för 2026.
Arbetsgrupp: Karin Bengtsson*, Francesca Faustini, Meliha C.Kapetanovic, Theodoros Lappas, Linda Mark, Johanna Sundbaum.
*huvudansvarig för detta dokument
Det är vanligt att uppehåll görs med antireumatisk behandling i samband med elektiv ortopedisk kirurgi. Underlaget för detta har granskats. Detta dokument är baserat på befintlig litteratur till och med oktober 2025 och omfattar användandet av syntetiska och biologiska immunmodulerande läkemedel (csDMARDs, tsDMARDs, bDMARDs) och kortikosteroider i samband med elektiv ortopedisk kirurgi. De studier som finns av komplikationer kopplade till antireumatisk medicinering vid kirurgi är i huvudsak retrospektiva observationsstudier av patienter med reumatoid artrit som genomgått elektiva ortopedkirurgiska ingrepp av varierande typ. I dagsläget saknas randomiserade kontrollerade studier. Flertalet studier fokuserar på TNF-hämmare (adalimumab, etanercept och infliximab) samt metotrexat. Även om det finns stöd för att bDMARD behandling kan vara associerad med ökad risk för postoperativ infektion är evidensen för att behandlingsuppehåll med bDMARDs minskar risken för postoperativ infektion fortsatt låg. Rekommendationen för 2026 är oförändrad jämfört med föregående år.
Sammanfattning
Sammanfattande rekommendation
Inför kirurgi görs alltid en individuell bedömning med sammanvägning av patientens riskfaktorer för infektion, typ av ingrepp och risk för sjukdomsskov vid uppehåll av antireumatisk terapi. För utvalda patienter kan man göra avsteg från nedanstående generella rekommendationer och både avstå uppehåll liksom göra uppehåll med terapi.
csDMARDs: Inget uppehåll (alternativt överväga uppehåll operationsdygnet och till risken för omedelbara postoperativa komplikationer bedöms vara över). Undantag är cyklofosfamid och klorambucil där rekommendationen är sista dos 1 vecka före, och återinsättning 1-2 veckor efter ingreppet vid okomplicerat förlopp/ sårläkning, baserat på preparatens biverkningsprofil med risk för benmärgshämning mm. För leflunomid finns försämrad sårläkning rapporterat vilket kan motivera ett uppehåll postoperativt.
tsDMARDs: För JAK-hämmare (för närvarande baracitinib, filgotinib, tofacitinib och upadacitinib) föreslås uppehåll 4 dagar före kirurgi. Återinsättning 1-2 veckor efter ingrepp/vid sårläkning.
bDMARDs: Ingrepp planeras i möjligaste mån till tidpunkt för nästa planerade dos. Undantaget är rituximab där ingen exakt tidsgräns kan fastslås, men principen är ingrepp så långt som är rimligt efter senaste dos. I normalfallet återinsättning 1-2 veckor efter ingrepp/vid sårläkning för samtliga bDMARDs.
Kortikosteroider: Sträva efter lägsta fungerande dos perorala steroider i god tid före kirurgi, om möjligt ≤10 mg prednisolon. Avstå intraartikulära steroider i led som ska opereras minst 3 månaderna före kirurgi. Samråd med operatör efter behov. Beakta risk för binjurebarkssvikt, följ lokala rutiner.
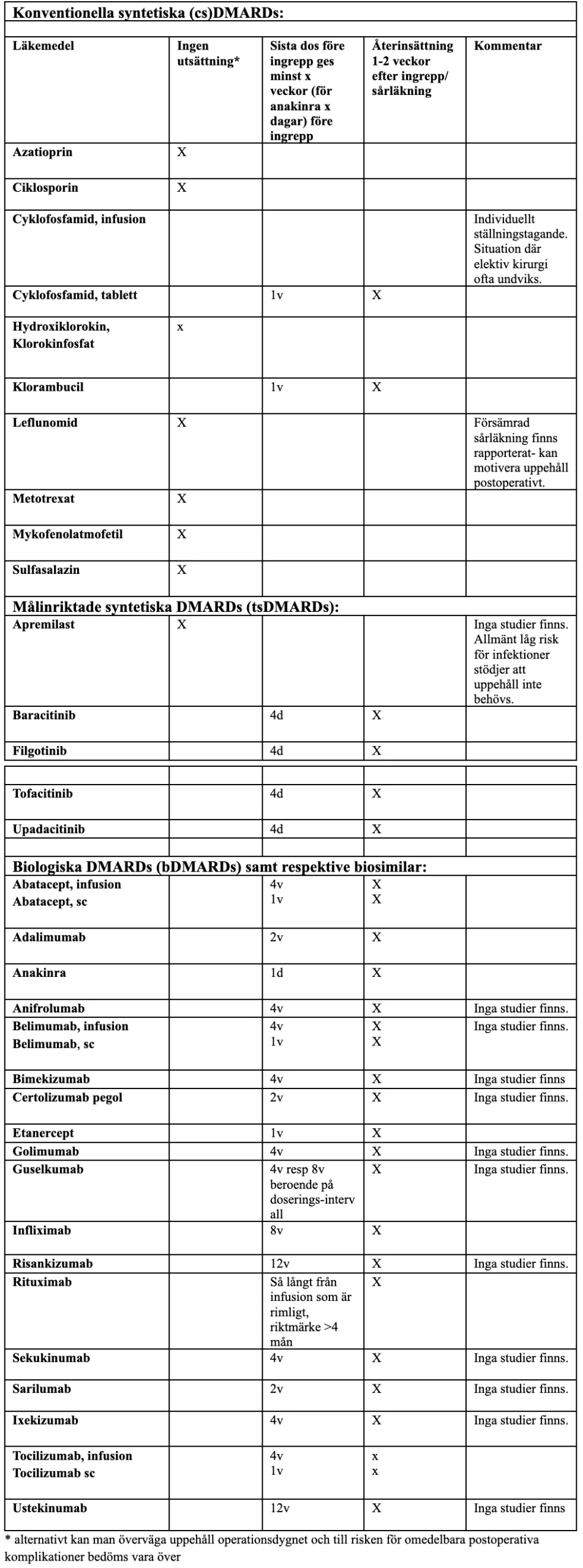
Tabell över läkemedel som ingår i denna översikt, uppdelat i syntetiska och biologiska DMARDs i alfabetisk ordning efter generiskt namn. Förslag för tidpunkt för sista dos före kirurgi och återinsättning om man efter en sammanvägd bedömning beslutat om doseringsanpassning.
Innehåll
Bakgrund – skäl till läkemedelsuppehåll
De huvudsakliga skälen till uppehåll med antireumatisk terapi i samband med kirurgi är risker för:
- postoperativ infektion
- försämrad läkningsprocess
- annan problematik perioperativt t.ex påverkad njur-, lever- eller blodbild eller risk för läkemedelsinteraktioner.
Mot dessa risker som kan vara kopplade till den immunmodulerande behandlingen måste man väga risken för ökad sjukdomsaktivitet i samband med terapiuppehåll som i sig också kan medföra ökad infektionsrisk, försämrad sårläkning och försvårad mobilisering. Höga kortisondoser som terapialternativ vid ökad sjukdomsaktivitet postoperativt kan också vara ogynnsamt för infektionsrisk och sårläkning.
Postoperativ infektionsrisk
Generellt har patienter med reumatisk sjukdom en ökad förekomst av postoperativa infektioner vid ortopedkirurgiska ingrepp jämfört med personer utan reumatisk sjukdom (Taylor-Williams, 2020).
Studier av inverkan av läkemedelsbehandling på infektionsrisk har relativt samstämmigt inte kunnat påvisa någon säker generell riskökning kopplat till behandling med syntetiska antireumatiska läkemedel.
För biologiska läkemedel är bilden mer komplex. Tre metaanalyser som fokuserat på risken för postoperativa infektioner vid elektiv ortopedkirurgi hos TNF-hämmarbehandlade RA patienter (Clay, 2016; Goodman, 2016; Mabille, 2016) påvisade en cirka dubblerad risk för postoperativa infektioner jämfört med RA patienter som inte behandlats med TNF-hämmare före eller i anslutning till kirurgin.
Två av metaanalyserna utvärderade effekten av uppehåll/utsättning av TNF-hämmarbehandling före ingreppet. En visade en signifikant minskad risk för postoperativa infektioner efter utsättning jämfört med fortsatt TNF-hämmarbehandling, men den andra kunde inte påvisa någon signifikant riskminskning vid utsättning. Bedömningen av dessa resultat försvåras bl a av att man studerat olika typer av ingrepp och olika patientpopulationer som från början kan ha olika risk för infektion. Information om riskfaktorer som rökning och komorbiditet saknas i flertalet studier.
Tidpunkt för och längd på uppehållet med TNF-hämmare varierar mellan studier och enskilda studier visar delvis motstridiga resultat. I en tidigare studie jämfördes förekomsten av postoperativ infektion efter ortopedisk kirurgi hos patienter som gjort uppehåll med TNF-hämmare mer än 5 halveringstider före ingrepp med uppehåll mindre än 5 halveringstider utan att man kunde påvisa någon skillnad i infektionsförekomst (Ruyssen, 2007). I en annan studie var risken för postoperativ infektion 10 gånger högre hos de som opererats inom doseringsintervall för en TNF-hämmare jämfört med om ingreppet skett efter uppehåll under minst ett doseringsintervall (Scherrer, 2013). En bDMARD (vs uppehåll) och postoperativ protesinfektion (Carlson, 2021). I en retrospektiv kohortstudie baserad på U.S. Medicare data av patienter med bl a RA, AS och psoriasisartrit sågs ingen skillnad postoperativt avseende infektionsförekomst, inklusive protes-relaterad infektion kopplad till tidpunkt för sista behandling med infliximab (< 4 veckor jämfört med 8-12 veckor före kirurgi) (George, 2017). Vissa patienter med möjliga riskfaktorer för infektion var exkluderade från studien (t.ex patienter med ledinfektion sista året, proteskirurgi sista 6 mån). I en annan studie från samma grupp sågs ingen skillnad i förekomst av post-operativa infektioner efter höft- och knäplastik när behandling med olika bDMARDs jämfördes (abatacept, adalimumab, etanercept, infliximab, rituximab, tocilizumab) (George, 2019). I en studie från Lund sågs heller ingen säker koppling mellan pågående TNF-hämmarbehandling och en ökad förekomst av postoperativ protesinfektion hos 494 reumatiska patienter som genomgick elektiv höft- eller knäprotesoperation (Borgas, 2020). Av sju patienter med protesinfektion hade en patient TNF-hämmarbehandling.
I en studie av i.v abataceptbehandlade patienter som genomgått kirurgi var förekomsten av postoperativa komplikationer (varav hälften infektioner) allmänt relativt låg (7,2%), men signifikant vanligare efter ortopediska ingrepp (n=176), särskilt i nedre extremitet än efter övriga kirurgiska ingrepp (n= 107). Medeltiden mellan sista infusion och kirurgi var likartad hos de med och utan komplikation (ca 5 veckor) (Latourte, 2017). I en annan studie av iv abataceptbehandlade patienter sågs ingen skillnad i postoperativ infektionsförekomst mellan de som fått sista abataceptinfusion <4 veckor jämfört med 4-8 veckor före kirurgi (George, 2019). En nylig retrospektiv studie kunde inte observera någon säker skillnad avseende incidens av postoperativa komplikationer mellan RA patienter med abatacept (n=97) i jämförelse med matchade RA patienter med csDMARD och/eller kortikosteroider (n=97) (Ito, 2020).
För vissa bDMARDs finns bara enstaka studier som belyser infektionsrisk vid elektiv ortopedisk kirurgi (rituximab, tocilizumab) eller inga studier alls (belimumab, certolizumab, golimumab, apremilast, sekukinumab, ustekinumab).
För JAK-hämmarna (baracitinib, filgotinib, tofacitinib och upadacitinib) är studier om perioperativ risk och handhavande i samband med kirurgi begränsade. En nylig retrospektiv studie iakttog signifikant minskade lymfocytantal postoperativt hos RA patienter med tofacitinib (n=34) i jämförelse med matchade patienter med csDMARDs (n=34) (Akihiro, 2021). Ingen postoperativ infektion eller fördröjd läkningsprocess noterades hos dessa patienter med tofacitinib. I en annan retrospektiv studie av 32 patienter med RA behandlade med JAK-hämmare iakttogs inte heller någon postoperativ infektion i samband med totalt 49 ortopediska ingrepp, däremot ett fall av fördröjd läkningsprocess (Nishida, 2023). I en retrospektiv studie av patienter med RA som genomgått ortopedisk kirurgi och som behandlades med JAK-hämmare (n=62) eller bDMARDs (n=62) sågs förutom en ökad incidens av postoperativa skov vid behandling med JAK-hämmare inga signifikanta skillnader i postoperativa komplikationer mellan JAK-hämmare och bDMARDs (Bekki, 2024). Studier av tofacitinib visar en allmänt ökad risk för infektioner och allvarliga infektioner hos patienter med RA i jämförelse med kontroller behandlade med placebo eller csDMARDs (Cohen, 2014). I väntan på mer information föreslås uppehåll inför kirurgi. I likhet med nyligen uppdaterade guidelines från German Society for Rheumatology (Albrecht, 2022) och ACR för anti-reumatisk behandling vid höft- och knäplastik (Goodman, 2022) föreslås uppehåll 4 dagar före kirurgi med tanke på preparatens korta halveringstid.
Vår sammanvägda bedömning är att en ökad infektionsrisk i samband med elektiv ortopedisk kirurgi inte kan uteslutas hos patienter som behandlas med TNF-hämmare eller andra bDMARDs. Evidensen för att uppehåll med bDMARDs minskar risken för postoperativa komplikationer är fortsatt låg och bygger på registerbaserade studier.
En anpassning av behandling med bDMARDs i samband med kirurgi behöver övervägas där hänsyn också ska tas till faktorer som typ av ingrepp och individuella riskfaktorer. Vid låg risk för infektion är rimligen, även om formella studier saknas, behovet av att anpassa doseringen av biologiska läkemedel också låg.
Vi föreslår att en individuell bedömning av infektionsrisk alltid görs inför kirurgi och denna kan innebära avsteg från nedanstående föreslagna generella rekommendationer. Faktorer som kopplats till ökad risk för postoperativ infektion hos patienter med reumatisk sjukdom är armbågs- och fotkirurgi, revisionsplastik, hög ålder, samtidig kortisonbehandling, ryggkirurgi med inopererat instrumentarium och tidigare hud- och sårinfektion. Komorbiditet och bakomliggande sjukdom/sjukdomsaktivitet och risk med terapiuppehåll måste också vägas in.
Påverkan på läkningsprocessen
Flertalet studier som utvärderat läkemedelseffekt på den postoperativa läkningsprocessen har inte kunnat påvisa försämrad sårläkning kopplat till behandling med syntetiska eller biologiska immunmodulerande läkemedel. Undantag är cyklofosfamid och leflunomid där försämrad sårläkning finns rapporterat. Det finns i nuläget inte tillräckligt underlag för att rekommendera generellt behandlingsuppehåll av detta skäl. En individuell bedömning får göras om sårläkningskomplikation tillstöter.
Övrig problematik
Risk för annan postoperativ problematik (t.ex påverkad njur-, lever- eller blodbild eller risk för läkemedelsinteraktioner) måste bedömas individuellt. Vår uppfattning är att cyklofosfamid och klorambucil är två preparat som intar en särställning baserat på kraftig immunsuppressiv effekt och risk för toxicitet t.ex benmärgspåverkan, varför ett uppehåll med dessa preparat rekommenderas i samband med kirurgi.
Infektionsrisk: Principer för uppehållets längd
De vanligaste redovisade principerna som styr uppehållets längd före ortopedisk kirurgi är:
- Uppehåll under perioperativ period (1 vecka före och 1 vecka efter ingrepp)
- Uppehåll baserat på preparatets halveringstid (ofta 3-5 halveringstider)
- Uppehåll baserat på doseringsintervall för preparatet
Vid tidpunkten för 5 halveringstider bedöms ett preparat i stort sett vara eliminerat ur kroppen, men detta kemiska mått behöver inte vara kopplat till preparatets biologiska effekter.
För t.ex TNF-hämmare med en halveringstid på 10-14 dagar (certrolizumab, adalimumab, golimumab, infliximab) innebär ett uppehåll på 3-5 halveringstider att sista dos ska ges ca 30-70 dagar före planerat ingrepp.
Ett preparats doseringsintervall baseras på dos-responsstudier och relaterar till biotillgänglighet och biologisk effekttid.
Detta dokument ansluter sig till principen om uppehåll före kirurgi baserat på preparatets doseringsintervall och koppling till klinisk effekt, dvs i allmänhet betydligt kortare uppehåll än om hänsyn tas till läkemedlets halveringstid.
Principen för återinsättning av läkemedel efter ortopedisk kirurgi är:
- Återinsättning när risk för postoperativ infektion bedöms vara över (1-2 veckor efter ingrepp/vid sårläkning)
Detta förfarande vid återinsättning efter kirurgi rapporteras väsentligen samstämmigt i litteraturen liksom från flertalet svenska reumatologenheter.
För rituximab som ofta doseras med minst 6 månaders intervall kan kirurgi efter dosintervall bli praktiskt svår att alltid genomföra. I den studie som finns av rituximab och förekomst av postinfektiös komplikation/infektion (franska AIR-registret) (Godot 2013) sågs ingen koppling mellan tid sen senaste infusion av rituximab och risk vid kirurgi som utfördes under det första året efter infusion. Infektionerna inträffade ofta dagar-närmsta veckorna efter ingreppet i median 6.4 mån (3.7-8.8 mån) efter senaste infusion av rituximab. Inga uppgifter om betydelsen av återkomst av B-celler (vilket kan ta 6-12 mån efter behandling) eller förekomst av neutropeni redovisas. I andra studier förefaller medeltiden för ”late-onset neutropenia” vara ca 5 månader efter rituximab behandling, ibland med koppling till infektion, ibland inte.
Vårt förslag är att man skjuter på kirurgi så långt det är rimligt efter senaste infusion av rituximab utan att exakt tidsgräns kan anges. Bestämning av immunoglobulinnivåer kan övervägas hos högriskpatienter.
Kortikosteroider
Systemiska kortikosteroider
Långvarig systemisk kortisonterapi är sen länge kopplad till risk för toxicitet, bl a ökad risk för infektioner. Risken är kopplad till dos där en större litteraturgenomgång publicerad 2016 fann låg risk vid prednisolondoser upp till 5 mg/dag, intermediär risk för 5-10 mg och hög risk vid doser över 10 mg/dag (Strehl, 2016).
Det finns även visst stöd för att systemisk kortisonterapi specifikt ökar risken för post-operativa infektioner efter elektiv ortopedisk kirurgi. Två publicerade stora registerstudier från samma grupp visade en ökad förekomst av post-operativa protesrelaterade infektioner vid behandling med prednisolondoser >10 mg hos patienter med reumatisk sjukdom som genomgått höft- eller knäplastik. Jämförelsen gjordes med icke-kortisonbehandlade patienter, kortisondosen var uppskattad via registrerad receptförskrivning månaden före kirurgi, alla patienter hade samtidig behandling med något bDMARD (George, 2017; George, 2019). Cirka 80% av patienterna var 65 år eller äldre. I en tredje studie från samma grupp av i.v. abataceptbehandade patienter med bl a RA sågs en ökad förekomst av sjukhusvård för infektion hos patienter som haft peroralt kortison förskrivet i dos motsvarande prednisolon >7,5 mg före protesoperationen jämfört med icke-kortisonbehandlade (George, 2019).
I en annan stor registergenomgång av patienter som genomgått höftplastik var preoperativ kortisonterapi (>10 dagar månaden före ingreppet) signifikant kopplad till ökad risk för postoperativa infektioner (ytlig infektion i operationsområdet samt sjukhusvård för andra icke-protesrelaterade infektioner) (Boddapati, 2018).
En annan aspekt av steroidterapi i anslutning till kirurgi är påverkan på sårläkning. En studiesammanställning publicerad 2013 visade att kronisk kortikosteroidbehandling >30 dagar före kirurgi ökade sårkomplikationsförekomsten 2-5 ggr jämfört med patienter som inte behandlats med kortison. Komplikationerna varierade med dos och duration av steroidterapi, men även med komorbiditeter och typ av ingrepp. Kortvarig (upp till 10 dagar) ökning av steroiddosen i nära samband med kirurgi (vilket ofta ordineras av narkosläkare eller ortoped) förefaller inte ge ökad sårläkningsproblematik (Wang, 2013).
Sammanfattningsvis är en allmän rekommendation (som vid all långvarig systemisk steroidterapi) att sträva efter lägsta fungerande kortisondos i god tid före kirurgi, om möjligt motsvarande 10 mg prednisolon eller lägre. För detaljerade rekommendationer om handhavandet av steroider vid de olika reumatiska sjukdomarna ska SRFs separata behandlingsrekommendationer för respektive sjukdom alltid beaktas.
Intraartikulära kortikosteroider
Det finns visst vetenskapligt stöd för att avstå kortisoninjektion i led där proteskirurgi planeras. Tillgängliga studier är retrospektiva och omfattar i huvudsak artrospatienter som genomgått höft- eller knäplastik (Kaspar, 2005; Papavasiliou, 2006; McIntosh, 2006; Cancienne, 2015; Schairer, 2016; Bedard, 2017). Man har jämfört postoperativ infektionsförekomst i den opererade leden hos patienter som fått respektive inte fått intraartikulär injektion i den aktuella leden innan ingreppet. Tidsintervall mellan injektionen och ingreppet varierar, men flera studier har funnit en signifikant ökning av infektionsrisken om injektionen getts inom 3 månader före ingreppet (Cancienne, 2015; Schairer, 2016). En studie såg en signifikant ökning av infektioner om injektionen getts upp till 6 månader innan ingreppet (Bedard, 2017). De flesta enskilda studierna är små och metodologin varierar. I två metaanalyser av höft- och knäplastikoperationer (Charalambous, 2014; Pereira, 2016) kunde man inte konfirmera att preoperativ intraartikulär steroidinjektion var associerad med signifikant riskökning för infektion och man efterlyser hög-kvalitativa randomiserade studier för att säkrare kunna besvara denna fråga. Bland ortopedkirurger finns utbredd konsensus om att avstå kortisoninjektion inom 3 månader före kirurgi.
Annan kirurgi än elektiv ortopedisk kirurgi
Inför uppdateringen 2021 av detta dokument gjordes en systematisk litteratursökning avseende läkemedelsbehandling vid annan kirurgi än elektiv ortopedisk kirurgi. Här finns enbart ett fåtal identifierade observationsstudier (Morel, 2020; Ward, 2020) och en metaanalys av kirurgi hos patienter med läkemedelsbehandlad inflammatorisk tarmsjukdom varav en del patienter haft TNF-hämmare (Law, 2020). Ingen av dessa rapporterar någon säker koppling mellan pågående immunmodulerande terapi och komplikationer i samband med ingreppen, men det betonas att underlaget är litet och att fler studier behövs.
Sammantaget finns i nuläget inte underlag för rekommendationer specifikt kring annan kirurgi än elektiv ortopedisk kirurgi. Vad gäller återinsättning av läkemedel efter kirurgi ser vi ingen anledning till annan grundrekommendation än den som gäller elektiv kirurgi, dvs återinsättning av immunmodulerande terapi så snart sårläkning föreligger och risken för postoperativ infektion bedöms vara över.
Referenser
Referenser
Abdulkader R, Dharmapalaiah C, Rose G, et al. Late-onset neutropenia in patients with rheumatoid arthritis after treatment with rituximab. J Rheumatol. 2014;41:858-61.
Akihiro U, Matsumoto T, Maenohara Y, et al. Systemic inflammatory responses after orthopedic surgery in patients with rheumatoid arthritis treated with tofacitinib. Clinical rheumatology. 2021. Epub 2021/09/22
Akkara Veetil BM, Bongartz T. Perioperative care for patients with rheumatic diseases. Nat Rev Rheumatol. 2012; 8:32-41.Review.
Albrecht K, Poddubbny D, Leipe J, et al. Perioperative management of patients with inflammatory rheumatic diseases. Z Rheumatol. 2022. Epub 2022/03/03.
Baek SH. Identification and preoperative optimization of risk factors to prevent periprosthetic joint infection. World J Orthop. 2014 18;5:362-7.
Baker JF, George MD. Prevention of Infection in the Perioperative Setting in Patients with Rheumatic Disease Treated with Immunosuppression. Curr Rheumatol Rep. 2019 Mar 8;21(5):17.
Bedard NA, Pugely AJ, Elkins JM, et al. The John N.Insall Award: do intraarticular injections increase the risk of infection after TKA? Clin Orthop Relat Res. 2017;475:45-52.
Bekki H, Hashiguchi T, Kawamura S, et al. Complications after orthopaedic surgeries in patients with rheumatoid arthritis treated with Janus kinase inhibitors: A retrospective observational study. Modern rheumatology / the Japan Rheumatism Association 2024;34(5):954-9.
Berber O, Berber R, Back DL, Sandiford NA. Do Biologic Agents Increase the Risk of Infection in Patients undergoing Lower Limb Arthroplasty Surgery? Curr Rheumatol Rev. 2018 Apr 20;14(1):46-52. Review.
Berthold E, Geborek P, Gülfe A. Continuation of TNF blockade in patients with inflammatory rheumatic disease. An observational study on surgical site infections in 1,596 elective orthopedic and hand surgery procedures. Acta Orthop. 2013;84:495-501.
Bibbo C, Goldberg JW.Infectious and healing complications after elective orthopaedic foot and ankle surgery during tumor necrosis factor-alpha inhibition therapy. Foot Ankle Int. 2004 ;25:331-5.
Bongartz T, Halligan CS, Osmon DR, et al. Incidence and risk factors of prosthetic joint infection after total hip or knee replacement in patients with rheumatoid arthritis. Arthritis Rheum. 2008;59:1713-20.
Borgas Y, Gülfe A, Kindt M, Stefánsdóttir A.Anti-rheumatic treatment and prosthetic joint infection: an observational study in 494 elective hip and knee arthroplasties.
.BMC Musculoskelet Disord. 2020 Jun 29;21(1):410. doi: 10.1186/s12891-020-03459-z.
Breuer GS, Ehrenfeld M, Rosner I, et al. Late-onset neutropenia following rituximab treatment for rheumatologic conditions. Clin Rheumatol. 2014;33:1337-40.
Boddapati V, Fu MC, Su EP, et al. Preoperative Corticosteroid Use for Medical Conditions is Associated with Increased Postoperative Infectious Complications and Readmissions After Total Hip Arthroplasty: A Propensity-Matched Study. Am J Orthop (Belle Mead NJ). 2018 Dec;47(12).
Cancienne JM, Werner BC, Luetkemeyer LM, Browne JA.Does timing of previous intra-articular steroid injection affect the post-operative rate of infection in total knee arthroplasty? J Arthroplasty. 2015;30:1879-1882.
Carlson VR, Anderson LA, Lu CC, et al. Perioperative Continuation of Biologic Medications Increases Odds of Periprosthetic Joint Infection in Patients With Inflammatory Arthropathy. The Journal of arthroplasty. 2021;36(7):2546-50.
Charalambous CP, Prodromidis AD, Kwaees TA. Do intraarticular steroid injections increase infection rates in subsequent arthroplasty? A systematic review and meta-analysis of comparative studies. J Arthroplasty. 2014;29:2175-2180.
Clay M, Mazouyes A, Gilson M, Gaudin P, Baillet A. Risk of postoperative infections and the discontinuation of TNF inhibitors in patients with rheumatoid arthritis: A meta-analysis. Joint Bone Spine. 2016; S1297-319X(16)30004-5.
Cohen S, Radominski SC, Gomez-Reino JJ, Wang L, Krishnaswami S, Wood SP, et al. Analysis of infections and all-cause mortality in phase II, phase III, and long-term extension studies of tofacitinib in patients with rheumatoid arthritis. Arthritis Rheumatol. 2014;66(11):2924-37.
Compagnoni R, Gualtierotti R, Randelli P. Total Joint Arthroplasty in Patients with Inflammatory Rheumatic Diseases. Adv Ther. 2018 Apr;35(4):439-456.
Del Olmo L, Hernández B, Galindo-Izquierdo M, et al. Peri-operative management of disease modifying anti-rheumatic drugs: recommendations based on a meta-analysis. Rev Esp Cir Ortop Traumatol. 2012 ;56:393-412. Review.
den Broeder AA, Creemers MC, Fransen J, et al. Risk factors for surgical site infections and other complications in elective surgery in patients with rheumatoid arthritis with special attention for anti-tumor necrosis factor: a large retrospective study. J Rheumatol. 2007 ;34:689-95.
Diaper R, Wong E, Metcalfe SA. The implications of biologic therapy for elective foot and ankle surgery in patients with rheumatoid arthritis. Foot (Edinb). 2017;30:53-58.
Escalante A, Beardmore TD. Risk factors for early wound complications after orthopedic surgery for rheumatoid arthritis. J Rheumatol. 1995;22:1844-51.
Fuerst M, Möhl H, Baumgärtel K, Rüther W. Leflunomide increases the risk of early healing complications in patients with rheumatoid arthritis undergoing elective orthopedic surgery. Rheumatol Int. 2006 ;26:1138-42.
George MD, Baker JF, Yenchih Hsu J, et al.Perioperative timing of infliximab and the risk of serious infection after elective hip and knee arthroplasty. Arthritis Care Res (Hoboken). 2017;69:1845-1854.
George MD , Baker FD. Perioperative management of immunosuppression in patients with rheumatoid arthritis. Curr Opin Rheumatol . 2019 May;31(3):300-306.
George MD, Baker JF, Winthrop K et al. Risk of Biologics and Glucocorticoids in Patients With Rheumatoid Arthritis Undergoing Arthroplasty: A Cohort Study. Ann Intern Med. 2019 Jun 18;170(12):825-836.
George MD, Baker JF, Winthrop K et al. Timing of Abatacept Before Elective Arthroplasty and Risk of Postoperative Outcomes. Arthritis Care Res (Hoboken). 2019 Sep;71(9):1224-1233.
Giles JT, Bartlett SJ, Gelber AC, et al. Tumor necrosis factor inhibitor therapy and risk of serious postoperative orthopedic infection in rheumatoid arthritis. Arthritis Rheum. 2006 15;55:333-7.
Gilson M, Gossec L, Mariette X, et al. Risk factors for total joint arthroplasty infection in patients receiving tumor necrosis factor α-blockers: a case-control study. Arthritis Res Ther. 2010;12:R145.
Goodman SM, Springer BD, Chen AF, et al. 2022 American College of Rheumatology/American Association of Hip and Knee Surgeons Guideline for the Perioperative Management of Antirheumatic Medication in Patients With Rheumatic Diseases Undergoing Elective Total Hip or Total Knee Arthroplasty. Arthritis & Rheumatology. 2022; 74: 1464-1473.
Goodman SM, Bykerk VP, DiCarlo E, et al. Flares in Patients with Rheumatoid Arthritis after Total Hip and Total Knee Arthroplasty: Rates, Characteristics, and Risk Factors. J Rheumatol. 2018 May;45(5):604-611.
Goodman SM et al. 2017 American College of Rheumatology/American Association of Hip and Knee Surgeons Guideline for the Perioperative Management of Antirheumatic Medication in Patients With Rheumatic Diseases Undergoing Elective Total Hip or Total Knee Arthroplasty. Arthritis Care Res Hoboken. 2017;69:1111-1124.
Goodman SM, Menon I, Christos PJ, Smethurst R, Bykerk VP. Management of perioperative tumour necrosis factor α inhibitors in rheumatoid arthritis patients undergoing arthroplasty: a systematic review and meta-analysis. Rheumatology (Oxford). 2016 ;55:573-82.
Goodman SM. Rheumatoid arthritis: Perioperative management of biologics and DMARDs. Semin Arthritis Rheum. 2015 ;44:627-32.
Goodman SM. Optimizing perioperative outcomes for older patients with rheumatoid arthritis undergoing arthroplasty: emphasis on medication management. Drugs Aging. 2015;32:361-9.
Godot S, Gottenberg JE, Paternotte S, et al. Safety of surgery after rituximab therapy in 133 patients with rheumatoid arthritis: data from the autoimmunity and rituximab registry. Arthritis Care Res (Hoboken). 2013; 65:1874-9.
Goh L, Jewell T, Laversuch C, Samanta A. Should anti-TNF therapy be discontinued in rheumatoid arthritis patients undergoing elective orthopaedic surgery? A systematic review of the evidence. Rheumatol Int. 2012; 32:5-13.
Grennan DM, Gray J, Loudon J, Fear S. Methotrexate and early postoperative complications in patients with rheumatoid arthritis undergoing elective orthopaedic surgery. Ann Rheum Dis. 2001;60:214-7.
Gualtierotti R, Parisi M, Ingegnoli F. Perioperative Management of Patients with Inflammatory Rheumatic Diseases Undergoing Major Orthopaedic Surgery: A Practical Overview. Adv Ther. 2018 Apr;35(4):439-456.
Hirano Y, Kojima T, Kanayama Y, et al. Influences of anti-tumour necrosis factor agents on postoperative recovery in patients with rheumatoid arthritis. Clin Rheumatol. 2010 ;29:495-500.
Hirao M, Hashimoto J, Tsuboi H, et al. Laboratory and febrile features after joint surgery in patients with rheumatoid arthritis treated with tocilizumab. Ann Rheum Dis. 2009 ;68:654-7.
Härle P, Straub RH, Fleck M. Perioperative management of immunosuppression in rheumatic diseases–what to do? Rheumatol Int. 2010 ;30:999-1004. Review.
Ito H, Tsuji S, Nakayama M, et al. Does Abatacept Increase Postoperative Adverse Events in Rheumatoid Arthritis Compared with Conventional Synthetic Disease-modifying Drugs? The Journal of rheumatology. 2020;47(4):502-9.
Ito H, Murata K, Sobue Y, et al. Comprehensive risk analysis of postoperative complications in patients with rheumatoid arthritis for the 2020 update of the Japan College of Rheumatology clinical practice guidelines for the management of rheumatoid arthritis. Modern rheumatology / the Japan Rheumatism Association. 2021:1-11.
Iwasa T, Nakamura K, Ogino H, et al. Multiple ulcers in the small and large intestines occurred during tocilizumab therapy for rheumatoid arthritis. Endoscopy. 2011 ;43:70-2.
Jain A, Witbreuk M, Ball C, Nanchahal J. Influence of steroids and methotrexate on wound complications after elective rheumatoid hand and wrist surgery. J Hand Surg Am. 2002 ;27:449-55.
Johnson BK, Goodman SM, Alexiades MM, Figgie MP, Demmer RT, Mandl LA. Patterns and associated risk of perioperative use of anti-tumor necrosis factor in patients with rheumatoid arthritis undergoing total knee replacement. J Rheumatol. 2013 ;40:617-23.
Kaspar, S, et al Infection in hip arthroplasty after previous injection of steroid. J Bone Joint Surg 2005; Br 87(4): 454-457.
Kawakami K, Ikari K, Kawamura K, et al. Complications and features after joint surgery in rheumatoid arthritis patients treated with tumour necrosis factor-alpha blockers: perioperative interruption of tumour necrosis factor-alpha blockers decreases complications? Rheumatology (Oxford). 2010 ;49:341-7.
Koyama K, Ohba T, Ebata S, Haro H. Postoperativer surgical infection after spinal surgery in Rheumatoid arthritis. Orthopedics.2016 ;39:e430-3.
Krause ML, Matteson EL. Perioperative management of the patient with rheumatoid arthritis. World J Orthop. 2014 ;5:283-91. Review.
Latourte A, Gottenberg JE, Luxembourger C, et al. Safety of surgery in patients with rheumatoid arthritis treated by abatacept: data from the French Orencia in Rheumatoid Arthritis Registry. Rheumatology (Oxford). 2017;56:629-637.
Law CC, Bell C, Koh D, Bao Y, Jairath V, Narula N. Risk of postoperative infectious complications from medical therapies in inflammatory bowel disease. Cochrane Database Syst Rev. 2020 Oct 24;10:CD013256.
Loza E, Martinez-Lopez JA, Carmona L. A systematic review on the optimum management of the use of methotrexate in rheumatoid arthritis patients in the perioperative period to minimize perioperative morbidity and maintain disease control. Clin Exp Rheumatol. 2009 ;27:856-62. Review.
McIntosh AL, Hanssen AD, Wenger DE, Osmon DR. Recent intraarticular steroid injection may increase infection rates in primary THA. Clin Orthop Relat Res. 2006;451:50-54.
Mabille C, Degboe Y, Constantin A, et al. Infectious risk associated to orthopaedic surgery for rheumatoid arthritis patients treated by anti-TNFalpha. Joint Bone Spine. 2016; S1297-319X(16)30134-8.
Momohara S, Kawakami K, Iwamoto T, et al. Prosthetic joint infection after total hip or knee arthroplasty in rheumatoid arthritis patients treated with nonbiologic and biologic disease-modifying antirheumatic drugs. Mod Rheumatol. 201;21:469-75.
Momohara S, Hashimoto J, Tsuboi H, et al. Analysis of perioperative clinical features and complications after orthopaedic surgery in rheumatoid arthritis patients treated with tocilizumab in a real-world setting: results from the multicentre TOcilizumab in Perioperative Period (TOPP) study. Mod Rheumatol. 2013;23:440-9.
Murata K, Yasuda T, Ito H, Yoshida M, Shimizu M, Nakamura T. Lack of increase in postoperative complications with low-dose methotrexate therapy in patients with rheumatoid arthritis undergoing elective orthopedic surgery. Mod Rheumatol. 2006;16:14-9.
Morel J, Locci M, Banal F etal. Safety of surgery in patients with rheumatoid arthritis treated with tocilizumab: data from the French (REGistry -RoAcTEmra) Regate registry. Clin Exp Rheumatol. 2020 May-Jun;38(3):405-410.
Morrison TA, Figgie M, Miller AO, Goodman SM. Periprosthetic joint infection in patients with inflammatory joint disease: a review of risk factors and current approaches to diagnosis and management. HSS J. 2013;9:183-94.
Nishida K, Nasu Y, Hashizume K, et al. Abatacept management during the perioperative period in patients with rheumatoid arthritis: report on eight orthopaedic procedures. Mod Rheumatol. 2014;24:544-5.
Nishida K, Harada R, Nasu Y, et al. The clinical course of patients with rheumatoid arthritis who underwent orthopaedic surgeries under disease control by tofacitinib. Mod Rheumatol. 2018:1–3.
Nishida K, Harada R, Nasu Y, et al. Influence of Janus kinase inhibitors on early postoperative complications in patients with rheumatoid arthritis undergoing orthopaedic surgeries. Mod Rheumatol. 2023: 1-8
Papavasiliou, A. V., et al. (2006). ”Infection in knee replacements after previous injection of intra-articular steroid. J Bone Joint Surg Br 88(3): 321-323.
Pereira LC, Kerr J, Jolles BM. Intra-articular steroid injection for osteoarthritis of the hip prior to total hip arthroplasty: is it safe? A systematic review. Bone Joint J. 2016;98B:1027-1035.
Pieringer H, Stuby U, Biesenbach G. Patients with Rheumatoid Arthritis Undergoing Surgery: How Should We Deal with Antirheumatic Treatment? Sem Arthritis Rheum. 2007; 36: 278–86.
Pieringer H, Stuby U, Biesenbach G. The place of methotrexate perioperatively in elective orthopedic surgeries in patients with rheumatoid arthritis. Clin Rheumatol. 2008 ;27:1217-20.
Pieringer H, Danninger K, Tzaribachev N, Böhler N, Pohanka E, Herold M.Patients with arthritis undergoing surgery: how should we manage tumour necrosis factor blocking agents perioperatively?-A systematic literature review. 2013 ;54:253-7.
Ravi B, Escott B, Shah PS, et al. A systematic review and meta-analysis comparing complications following total joint arthroplasty for rheumatoid arthritis versus for osteoarthritis. Arthritis Rheum. 2012 ;64:3839-49.
Robert J. Thorsness, Warren C. Hammert. Perioperative Management of Rheumatoid Medications. J Hand Surgery 2012; 37:1928–31.
Rosandich PA, Kelley JT 3rd, Conn DL. Perioperative management of patients with rheumatoid arthritis in the era of biologic response modifiers. Curr Opin Rheumatol. 2004;16:192-8. Review.
Ruyssen-Witrand A, Gossec L, Salliot C, et al. Complication rates of 127 surgical procedures performed in rheumatic patients receiving tumor necrosis factor alpha blockers. Clin Exp Rheumatol. 2007;25:430-6.
Schairer WW, Nwachukwu BU, Mayman DJ, Lyman S, Jerabek SA.Preoperative Hip Injections Increase the Rate of Periprosthetic Infection After,Total Hip Arthroplasty. J Arthroplasty. 2016 Sep;31(9 Suppl):166-169.e1.
Scherrer CB, Mannion AF, Kyburz D, Vogt M, Kramers-de Quervain IA. Infection risk after orthopedic surgery in patients with inflammatory rheumatic diseases treated with immunosuppressive drugs. Arthritis Care Res (Hoboken). 2013 ;65:2032-40.
Strehl C, Bijlsma JW, de Wit M, et al. Defining conditions where long-term glucocorticoid treatment has an acceptably low level of harm to facilitate implementation of existing recommendations: viewpoints from an
EULAR task force. 2016;75(6):952-7.
Talwalkar SC, Grennan DM, Gray J, Johnson P, Hayton MJ. Tumour necrosis factor alpha antagonists and early postoperative complications in patients with inflammatory joint disease undergoing elective orthopaedic surgery. Ann Rheum Dis. 2005;64:650-1.
Tanaka N, Sakahashi H, Sato E, Hirose K, Ishima T, Ishii S. Examination of the risk of continuous leflunomide treatment on the incidence of infectious complications after joint arthroplasty in patients with rheumatoid arthritis.J Clin Rheumatol. 2003;9:115-8.
Taylor-Williams O, Nossent J, Inderjeeth CA.Incidence and Complication Rates for Total Hip Arthroplasty in Rheumatoid Arthritis: A Systematic Review and Meta-Analysis Across Four Decades. Rheumatol Ther. 2020 Sep 30. doi: 10.1007/s40744-020-00238-z.
Tebbutt N C, Giraud A S, Inglese M, et al. Reciprocal regulation of gastrointestinal homeostasis by SHP2 and STAT-mediated trefoil gene activation in gp130 mutant mice. Nat Med. 2002; 8:1089-1097.
Wang AS, Armstrong EJ, Armstrong AW. Corticosteroids and wound healing: clinical considerations in the perioperative period. Am J Surg. 2013 Sep;206(3):410-7.
Ward MW, Dasgupta A. Pre-operative withholding of infliximab and the risk of infections after major surgery in patients with rheumatoid arthritis. Rheumatology (Oxford).2020 Dec 1;59(12):3917-26.
Wendling D, Balblanc JC, Brousse A, et al. Surgery in patients receiving anti-tumour necrosis factor alpha treatment in rheumatoid arthritis: an observational study on 50 surgical procedures. Ann Rheum Dis. 2005;64:1378-9.
Wise DM. Suppressed wound healing in a patient with rheumatoid arthritis taking leflunomide (arava). Perm J. 2011;15:70-4.
Van Duren BH, et al. The effect of perioperative biologic disease-modifying anti-rheumatic drugs on the risk of perioperative complications. Surgical site infection, delayed wound healing, and disease flares following orthopaedic surgical procedures. The journal of bone and joint surgery. 2022; 104 (12): 1116-1126.
Guidelines:
Albrecht K, Poddubbny D, Leipe J, et al. Perioperative management of patients with inflammatory rheumatic diseases. Z Rheumatol. 2022. Epub 2022/03/03.
Ding T, Ledingham J, Luqmani R, et al; Standards, Audit and Guidelines Working Group of BSR Clinical Affairs Committee; BHPR BSR and BHPR rheumatoid arthritis guidelines on safety of anti-TNF therapies. Rheumatology (Oxford). 2010 ;49:2217-9.
Goodman SM et al. 2022 American College of Rheumatology/American Association of Hip and Knee Surgeons Guideline for the Perioperative Management of Antirheumatic Medication in Patients With Rheumatic Diseases Undergoing Elective Total Hip or Total Knee Arthroplasty. Arthritis Care Res (Hoboken). 2017 69:1111-1124.
Malaviya AP, Ledingham J, Bloxham J, et al; BSR Clinical Affairs Committee & Standards, Audit and Guidelines Working Group; BHPR. The 2013 BSR and BHPR guideline for the use of intravenous tocilizumab in the treatment of adult patients with rheumatoid arthritis. Rheumatology (Oxford). 2014 ;53:1344-6.
Pham T, Claudepierre P, Deprez X, et al; Club Rhumatismes et Inflammation, French Society of Rheumatology. Anti-TNF alpha therapy and safety monitoring. Clinical tool guide elaborated by the Club Rhumatismes et Inflammations (CRI), section of the French Society of Rheumatology (Société Française de Rhumatologie, SFR). Joint Bone Spine.2005 ;72 Suppl 1:S1-58.
Pham T, Bachelez H, Berthelot JM, et al. Abatacept therapy and safety management. Joint Bone Spine. 2012 ;79 Suppl 1:3-84.
Saag KG, Teng GG, Patkar NM, et al; American College of Rheumatology. American College of Rheumatology 2008 recommendations for the use of nonbiologic and biologic disease-modifying antirheumatic drugs in rheumatoid arthritis. 2008 ;59:762-84.

