Riktlinjer för behandling av systemisk lupus erytematosus (SLE)
På uppdrag av Svensk Reumatologisk Förening 2026
Arbetsgruppen: Aleksandra Antovic (Ordförande), Agneta Zickert, Dag Leonard, Marit Stockfelt, Martina Frodlund, Petrus Linge
Sammanfattning
Summering av SRF:s riktlinjer för behandling av SLE
- För att säkerställa diagnostik och behandling bör patienter med känd eller misstänkt SLE skötas på reumatologisk specialistmottagning.
- SLE-diagnos kan ställas av reumatolog, oavsett om patienten fyller klassifikationskriterier eller inte. Behandling får inte fördröjas p.g.a. att kriterier ännu inte uppfyllts.
- Man bör i möjligaste mån klargöra om patientens symtom/manifestation(er) är relaterade till sjukdomsaktivitet (reversibel) eller organskada (irreversibel).
- Ansvarig läkare bör kartlägga vilket/vilka organ som utgör målorgan för planerad behandling. Ofta föreligger engagemang från flera organsystem samtidigt, behandlingen ska då styras utifrån vilket organengagemang som är mest allvarligt.
- Behandling av ”serologisk aktivitet” (komplementkonsumtion och/eller påvisade DNA-antikroppar) i frånvaro av klinisk bild talande för sjukdomsaktivitet bör undvikas.
- Antifosfolipidsyndrom (APS) förekommer hos 15–20 % av SLE-patienter och diagnostiseras utifrån kliniska symtom (t.ex. trombos och/eller graviditetskomplikation) samt persisterande förekomst av fosfolipidantikroppar. Kontroll av fosfolipidantikroppar bör ingå i initial utredning av SLE. Waran utgör grunden för behandling av manifest APS.
- Hydroxiklorokin bör ges till alla SLE-patienter (maxdos 5 mg/kg kroppsvikt) oavsett organengagemang såtillvida inte kontraindikationer föreligger. Efter 5 års behandling finns viss risk för retinopati varför ögonundersökning därefter bör ske årligen.
- Tidig immunosupressiv behandling med övervägande av kombinationsterapier, ibland inkluderande biologisk behandling, rekommenderas redan vid diagnos beroende på organengagemang. Detta rekommenderas generellt vid nefrit.
- Kortison ingår, ibland i högdos, som initial behandling vid flera organmanifestationer. Dosen bör därefter trappas ned med mål hel utsättning, om detta inte är möjligt bör man eftersträva lägsta möjliga dos motsvarande prednisolon ≤ 5 mg/dag.
- Fortlöpande monitorering av ordinerade läkemedel är viktig för att säkerställa följsamhet till given ordination (compliance), utvärdera effekt på sjukdomsaktivitet, upptäcka eventuella biverkningar samt för att reducera dos kortikosteroider.
- Överväg bristande compliance vid terapisvikt.
- Oavsett tidigare organengagemang ska kontroll av blodtryck och urinsticka alltid ingå vid återbesök. Nytillkommen albuminuri ska inge misstanke om nefrit och njurbiopsi bör övervägas.
- Värdering av kardiovaskulära riskfaktorer ska göras regelbundet enligt SRF:s allmänna riktlinjer för prevention av kardiovaskulär sjukdom vid reumatisk sjukdom.
- Symtom från centrala och perifera nervsystemet är vanliga vid SLE, men de är långt ifrån alltid inflammatoriskt betingade. Utredning ska inriktas mot huruvida symptomen är uttryck för grundsjukdomen eller orsakade av andra faktorer såsom infektion, läkemedelsbiverkan, intoxikation, metabol rubbning, hypertoni eller reaktion på svår sjukdom.
- Kloka kliniska val” ska beaktas vid diagnostik och uppföljning av SLE, man bör till exempel undvika extensiv provtagning hos patienter i långvarig remission.
Introduktion
Detta dokument har tagits fram av en arbetsgrupp utsedd av Svensk Reumatologisk Förening (SRF) för att ge stöd åt den enskilde reumatologen och bidra till en enhetlig behandling av SLE i Sverige. Syftet är att sammanfatta aktuella principer för läkemedelsbehandling vid SLE utifrån publicerad evidens, internationella rekommendationer samt beprövad erfarenhet och konsensus.
SLE är en komplex sjukdom med många olika manifestationer. För att underlätta och skapa struktur har riktlinjerna därför delats upp efter de viktigaste manifestationerna, även om det i praktiken ofta är flera organsystem som kräver samtidig behandling. I dokumentet ingår också ett separat avsnitt om enskilda läkemedel.
Definitioner och övergripande principer
Diagnos och klassifikationskriterier
Formella diagnostiska kriterier för SLE saknas. I klinisk praxis tillämpas ofta Fries & Holmans diagnostiska princip(1), som anses praktisk för att ställa diagnos vid misstänkt SLE.
Enligt Fries & Holman krävs följande tre kriterier för SLE-diagnos:
- Förekomst av antinukleära antikroppar (ANA) vid minst ett tillfälle, samt
- Tecken på systemsjukdom med engagemang av minst två organsystem (t.ex. hud, leder, njurar, serosa, blod, lungor eller nervsystem), samt
- Frånvaro av annan sjukdom som bättre förklarar patientens symtom.
För klassifikation av SLE används i första hand EULAR/ACR:s klassifikationskriterier från 2019 (bilaga A)(2). Ett positivt ANA-test (≥1:80, eller motsvarande positivt test med lokal metod) utgör ett obligatoriskt ingångskriterium. Därefter tillämpas viktade kriterier inom tio olika domäner: allmänsymtom, hematologi, neuropsykiatri, mukokutan, serosa, muskuloskeletal, njurar, fosfolipidantikroppar, komplement och SLE-specifika antikroppar. För klassifikation som SLE krävs minst 10 poäng, och endast den högsta poänggivande manifestationen eller laboratorieavvikelsen inom varje domän räknas.
Tidigare klassifikationskriterier som fortfarande används i klinisk praxis är ACR-1982 (bilaga B) (3), ACR-1997 (4) och SLICC 2012 (bilaga C) (5). Ett viktigt tillägg i SLICC 2012 är att biopsiverifierad SLE-nefrit som enskilt kriterium i kombination med förekomst av antinukleära antikroppar (ANA och/eller anti-DNA) definieras som SLE.
Sjukdomsaktivitet
För bedömning av sjukdomsaktivitet rekommenderas i första hand användning av SLE Disease Activity Index (SLEDAI)(6). Instrumentet mäter global sjukdomsaktivitet under de senaste tio dagarna och omfattar 24 olika domäner. Definitionsmässigt ska symtom på sjukdomsaktivitet med säkerhet kunna tillskrivas SLE-sjukdomen. Regelbunden skattning av SLEDAI rekommenderas(7, 8).
Om komplementnivåer och anti-dsDNA-antikroppar inte är tillgängliga kan i stället klinisk SLEDAI användas, vilken exkluderar dessa variabler. Både SLEDAI och klinisk SLEDAI kan registreras och skattas i SRQ.
Låg sjukdomsaktivitet och remission
För att förbättra livskvaliteten och förebygga utveckling av organskada är det viktigt att patienten uppnår remission eller i andra hand låg sjukdomsaktivitet (9).
Låg sjukdomsaktivitet (Lupus Low Disease Activity State, LLDAS) definieras som ett tillstånd där sjukdomsaktiviteten är begränsad; SLEDAI ≤ 4 (samt ingen ny sjukdomsaktivitet i centrala organ och inga nya eller försämring av symtom), läkarens bedömning av sjukdomsaktivitet (PGA ≤ 1), dos prednisolon ≤ 7,5 mg/dag och stabil dos antimalariamedicin / DMARD / biologisk behandling (10).
Remission (Definition of Remission in SLE, DORIS) innebär frånvaro av klinisk sjukdomsaktivitet; klinisk SLEDAI = 0 (SLEDAI exklusive komplement och anti-dsDNA), läkarens bedömning av sjukdomsaktivitet (PGA ≤ 0,5), dos prednisolon ≤ 5 mg/dag (11). Observera att patienten får stå på behandling med antimalariamedicin / DMARDs / biologisk behandling, och positivt test för komplement och dsDNA antikroppar får föreligga.
Både LLDAS och DORIS kan skattas och registreras i SRQ.
Patientrapporterad sjukdomsaktivitet
Det finns flera instrument för att bedöma patientrapporterad hälsa vid SLE. Quick Systemic Lupus Activity Questionnaire (Q-SLAQ) rekommenderas som förstahandsval (12).
Q-SLAQ är ett självskattningsinstrument som mäter sjukdomsaktivitet ur patientens perspektiv och omfattar 18 olika domäner. Patienten besvarar frågorna via PER/SRQ, och resultaten blir tillgängliga för behandlande läkare i SRQ, där de kan användas som stöd vid den kliniska bedömningen. Syftet med användningen av Q-SLAQ är att möjliggöra systematisk uppföljning av patientrapporterad sjukdomsaktivitet och att öka patientens delaktighet i vården.
Prognostiskt ogynnsamma faktorer
Flera faktorer har identifierats som prognostiskt ogynnsamma vid SLE. Dessa inkluderar tidig sjukdomsdebut, engagemang av flera organsystem vid debut, njur- eller CNS-manifestationer, fosfolipidantikroppar, tidig utveckling av organskada, icke-kaukasisk etnicitet samt manligt kön (13, 14). Patienter med dessa faktorer kan ha högre risk för sjukdomsprogression och komplikationer, vilket motiverar täta uppföljningar och individuell anpassning av behandlingsstrategin.
Målorgan för behandling
Vid läkemedelsbehandling av SLE bör målorganet tydliggöras. Ofta finns flera organsystem engagerade samtidigt; i sådana fall prioriteras det organ eller den sjukdomsmekanism som är mest akut eller kliniskt betydelsefull. Behandlingsval styrs alltså av specifika manifestationer, inte av SLE-diagnosen i sig. Exempel: Behandling av ledengagemang underordnas samtidig behandling av allvarliga inre organengagemang som t.ex. nefrit.
Behandling
Målsättningen med behandlingen vid SLE är att nå remission och att dosen av kortikosteroider minimeras eller helst avslutas(8). Antimalariabehandling rekommenderas till alla patienter (15). Vidare rekommenderas särskild uppmärksamhet och tidig behandling av nefrit. Däremot avråds från aktiv behandling av enbart serologisk aktivitet i frånvaro av aktiva SLE-manifestationer (16). Vid remission rekommenderas övervägande av successiv reduktion av behandlingen, med i första hand reduktion av kortisondosen (15).
Organskada
Organskada vid SLE mäts med SLICC/ACR Damage Index (SDI), som registrerar skador i 12 organsystem och ger en totalpoäng(17). För att räknas som organskada ska symtomen vara persistenta ≥ 6 månader, men de behöver inte nödvändigtvis orsakas av sjukdomen SLE eller behandlingen av SLE.
Frånvaro av progress i SDI indikerar god behandlingskontroll eller lindrig sjukdom. Utveckling av organskada är starkt kopplad till prognos, överlevnad och hälsorelaterad livskvalitet varför regelbunden skattning rekommenderas (18). Skattning av skada (SDI) kan göras i SRQ.
God vård vid SLE
SRF rekommenderar i linje med EULAR följande fem övergripande principer för god vård av patienter med SLE(15):
- Behandling vid SLE kräver ett multidisciplinärt och individanpassat omhändertagande inkluderande patientutbildning och patientmedverkan vid beslut om behandling, samtidigt som kostnad för patient och samhälle tas i beaktande.
- Sjukdomsaktivitet bör skattas vid varje besök och organskada skattas minst en gång per år med validerade instrument.
- Icke farmakologisk intervention inkluderande solskydd, rökstopp, hälsosam balanserad diet, regelbunden träning och osteoporosförebyggande åtgärder är viktiga för att förbättra hälsan på lång sikt.
- Vid val av farmakologisk behandling ska patientens klinik, typ och svårighetsgrad av organmanifestation, potentiella biverkningar, förekomst av komorbiditeter, risk för progress av organskada och patientens preferenser beaktas.
- Tidig diagnos, regelbunden screening för organmanifestationer (framförallt nefrit), prompt initiering av behandling med mål att nå remission eller låg sjukdomsaktivitet och god compliance med behandlingen är viktigt för att förebygga skov, förhindra utveckling av organskador och förbättra prognosen och livskvaliteten.
Generella råd
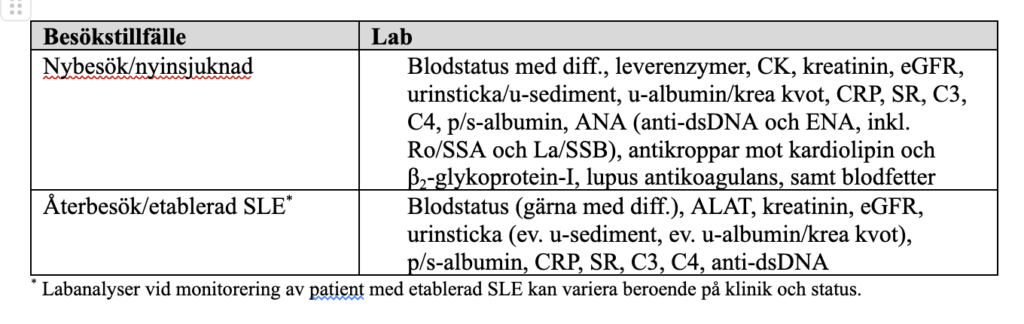
SRFs ger följande generella råd avseende vård och behandling av patienter med SLE. Bästa kliniska omhändertagande av patienter med SLE omfattar en genomgång av sjukdomshistoria inklusive hereditet och riskfaktorer, klinisk undersökning samt labutredning enligt tabell nedan.
Kortison
Kortikosteroider utgör, ibland i hög dos, en del av den initiala behandlingen vid flera SLE-manifestationer. Dosen bör därefter trappas ned successivt med målet att avsluta behandlingen helt. Om utsättning inte är möjlig bör lägsta effektiva underhållsdos eftersträvas, motsvarande prednisolon ≤ 5 mg/dag (8, 15).
Antimalariamedicin
Hydroxiklorokin rekommenderas till alla patienter med SLE, oavsett organengagemang, såvida inte kontraindikationer föreligger. Maximal dos är 5 mg/kg kroppsvikt per dag. Efter fem års behandling ökar risken för retinopati, varför årlig ögonundersökning därefter rekommenderas (Nationella kunskapsstöd | Sveriges ögonläkarförening) (19).
Kardiovaskulär screening
Bedömning av kardiovaskulära riskfaktorer ska göras vid nybesök och därefter regelbundet (20). Utöver SRF:s allmänna riktlinjer för prevention av kardiovaskulär sjukdom vid reumatisk sjukdom betonas vikten av att analysera förekomst av fosfolipidantikroppar då dessa är associerade med ökad risk för kardiovaskulär och cerebrovaskulär sjukdom. Anpassad kardiovaskulär screening för patienter med SLE kan göras i SRQ:s kardiovaskulära modul.
Vaccination
För vaccinationer hänvisas till SRF:s riktlinjedokument för vaccination vid inflammatoriska reumatiska sjukdomar. Risken för herpes zoster är särskilt ökad vid behandling med anifrolumab, varför vaccination med Shingrix® rekommenderas (21).
Cellprovtagning
Vid pågående och långvarig immunosuppression med exempelvis azatioprin (AZA) eller mykofenolat mofetil (MMF) hos kvinnor upp till 69 års ålder rekommenderas mer frekvent cellprovtagning, inkl. HPV-screening, än vad som erbjuds kvinnor i allmänhet (22).
Innehåll
Specifika organsystem – behandling och monitorering
Inledning
I detta avsnitt om specifika organsystem tas övergripande principer för behandling och monitorering upp. Dosering och mer specifik information om respektive läkemedel tas upp i avsnittet ”Läkemedel och dosering”.
Muskuloskeletala symtom
Klinisk bild
Symtom från rörelseapparaten förekommer hos minst 80% av patienter med SLE. Artrit är vanligt och förekommer som symmetrisk polyartrit, men kan också vara oligoartrit och monoartrit. Vid SLE är artriten i regel inte erosiv, men kan ändå ge upphov till felställningar med exempelvis ulnardeviation i händer och så kallad Jaccoud-deformitet. Erosiv artrit, så kallad ”rhupus”, är ovanligt och man bör då överväga möjligheten att RA föreligger samtidigt. Tenosynoviter, till exempel i händernas flexorsenor, är också vanligt förekommande. Myosit förekommer och är ofta mildare än vid polymyosit och dermatomyosit. Generaliserad fibromyalgiliknande smärta är vanligt vid SLE och är ofta associerad med trötthetsproblematik.
Utredning
Skelettröntgen och/eller ultraljud av drabbade leder kan ingå i en basal utredning. Utredning av SLE-relaterad myosit bör likna den vid polymyosit (se SRF:s separata behandlings-rekommendationer). Vid generaliserad trötthets- och smärtproblematik bör annan genes än SLE uteslutas, såsom tyreoidearubbning eller B12-brist.
Behandling
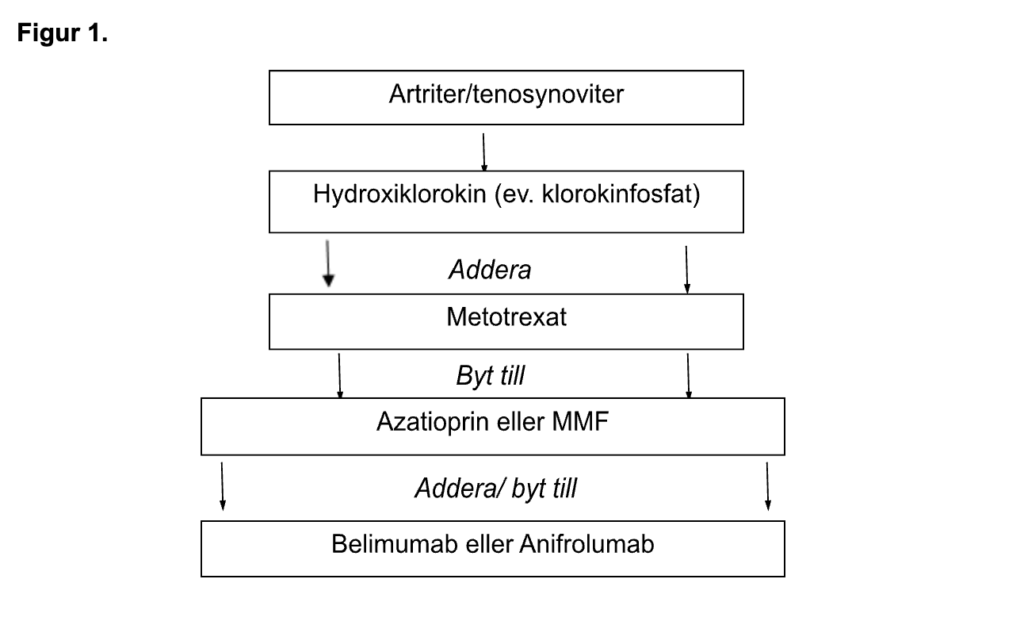
Muskuloskeletala manifestationer kan utgöra målorgan för behandling. En behandlingsalgoritm visas i Figur 1. Behandling med hydroxiklorokin (HCQ) ska alltid ges om inget särskilt skäl talar emot, och behålls då annan behandling adderas. Perorala kortikosteroider eller intra-artikulära injektioner kan ha sin plats som överbryggande behandling. Vid kvarstående artrit är nästa steg tillägg av metotrexat (MTX) (23). Om inte detta har tillräcklig effekt kan istället AZA eller MMF provas. Vid otillräcklig effekt eller biverkningar bör man överväga tillägg av/byte till biologisk behandling i form av belimumab (BEL) eller anifrolumab (ANI). Både BEL och ANI uppvisade effekt vid artrit, och för BEL särskilt i de fall när samtidig serologisk aktivitet (komplementkonsumtion och/eller anti-dsDNA antikroppar) förelåg (24-26). Behandling av SLE-relaterad myosit liknar den som ges vid artrit, dvs. kortikosteroider, MTX, AZA och MMF i första hand. Erfarenheten av biologisk behandling av SLE-myosit är begränsad. Vid generaliserad smärt-och trötthetsproblematik har fysisk aktivitet stor betydelse, se även SRF:s rekommendationer för modern reumarehabilitering (MORR).
Mukokutana manifestationer
SLE-manifestationer från hud och slemhinnor är vanligt, och kan dominera den kliniska bilden och utgöra målorgan för behandlingar. Det kan också vara del i en sjukdomsbild med symtom från flera olika organsystem där behandlingen får inriktas mot mer allvarliga manifestationer. I de fall där hudmanifestationer dominerar, kan patienten i vissa fall skötas av eller i samråd med hudspecialist.
Klinisk bild
Det finns en internationell gällande klassifikation av hudlesioner med histologi specifik för kutan lupus (27) vilken kan tjäna som underlag för hur man kan tänka även vid SLE. Det finns ett stort antal hudmanifestationer vid SLE, inkluderande olika typer av vaskulit och pannikulit, men vanligare är:
Akut kutan lupus med så kallat fjärilsexantem är den mest kända manifestationen (utslag över kinder och näsa).
Subakut kutan lupus, som ofta är associerat med mild SLE-sjukdom och Ro/SSA-antikroppar.
Olika typer av kronisk kutan lupus där diskoid lupus och alopeci är vanligast. DLE är ärrbildande, sitter ofta i ansikte och hårbotten, och bör behandlas aktivt för att förebygga ärr.
Det finns ett instrument för bedömning av aktivitet i och utbredning av hudlesionerna, inkluderande också skador i huden: CLASI (Cutaneous lupus activity and severity index) (28). Detta kan vara värdefullt men kräver vana och används främst inom forskning. Många andra symptom från huden som inte har lupus-specifik histologisk bild förekommer också. En mer eller mindre uttalad solöverkänslighet är mycket vanligt, det är dock viktigt att notera att ca 20 % av svensk befolkning får soleksem som oftast går att skilja ut med anamnes och klinisk bild. Återkommande, ibland smärtsamma slemhinnesår från mun, men även näsa och i sällsynta fall underlivet förekommer vid aktiv sjukdom.
Utredning
Även om hudmanifestationerna vid SLE kan ha ett typiskt utseende bör man ibland av differentialdiagnostiska skäl konfirmera den kliniska misstanken med hudbiopsi. Det finns också tillfällen då s.k. lupusband-test, vilket är ett immunofluorescenstest som tas från icke-UV-exponerad hud på lokal utan lesion, kan stärka SLE-diagnosen. Dock ingår Lupusband-test inte i rutinutredningen.
Behandling
SLE-patienter bör minimera den tid man vistas i solen då exposition för ultraviolett ljus kan utlösa eller försämra hudutslag, samt även bidra till en generell försämring av sjukdomen. Stark solskyddsfaktor och solråd bör alltid ges. Eftersom rökning är klart överrepresenterat vid kutan lupus och eventuellt kan utlösa eller aggravera SLE-manifestationer i huden är det angeläget att diskutera rökstopp (29). Vissa läkemedel (bl.a. terbinafine, TNF-hämmare, sulfa och antiepileptika) kan utlösa vissa former av kutan lupus och därför är noggrann läkemedelsanamnes viktig (30).
Lokalbehandling med kortikosteroider på lesioner kan prövas, men potent lokalbehandling med kortikosteroider eller takrolimus (TAK) ska ges i samråd med hudspecialist. Ofta krävs även systemisk behandling i första hand behandling med HCQ. Vid otillräcklig effekt kan konventionella immunosuppressiva preparat adderas. MTX, AZA, MMF och CS är möjliga alternativ och av dessa är MTX mest studerat.
I en meta-analys av MTX-behandling vid SLE identifierades tre RCT och sex observationsstudier sågs signifikant minskning av SLEDAI och kortikosteroider i behandlingsgruppen jämfört med placebogruppen (23).
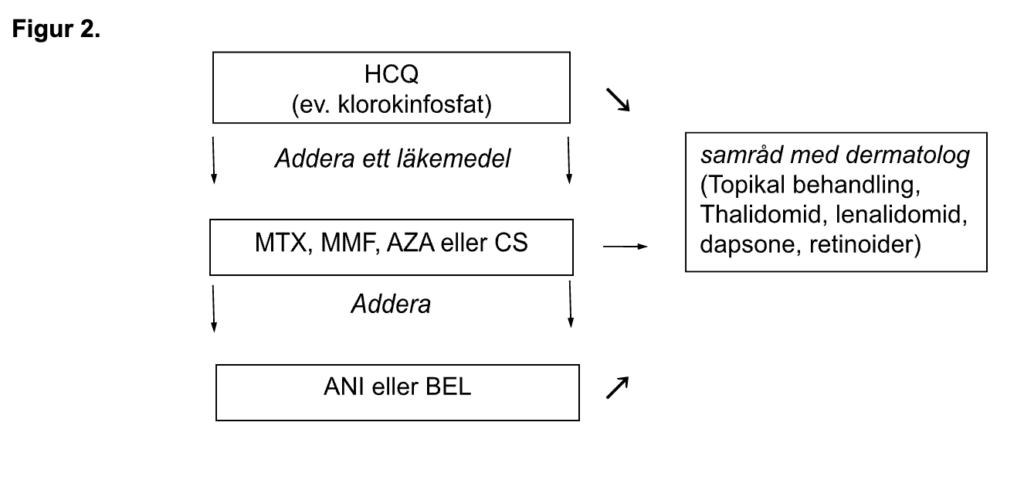
Vid mukokutana manifestationer finns också biologiska läkemedel som alternativ, BEL och ANI (Figur 2). I RCTs av BEL respektive ANI var hudmanifestationer vanligt förekommande. Båda preparaten uppvisade effekt på global SLE-aktivitet (25, 26). För både ANI och BEL sågs också effekt på kutan lupus, och för BEL särskilt när samtidig serologisk aktivitet (komplementkonsumtion och/eller anti-dsDNA antikroppar) förelåg. I observationsdata ses mycket god effekt av ANI vid svår hudlupus (31).
Alternativ till konventionella immunosuppressiva läkemedel när man särskilt vill inrikta sig mot mukokutan lupus är thalidomid, lenalidomid, dapsone och retinoider. Om dessa läkemedel ska användas bör det ske i samarbete med dermatolog och för thalidomid bör missbildningsrisk vid graviditet och risken för icke reversibel neuropati tas i beaktande.
Vid chill-blain lupus (pernio) kan kalciumflödeshämmare (Nifedipin) övervägas om lokala steroider och rökstopp är otillräcklig behandling (32).
Hematologiska manifestationer
Klinisk bild
Hematologiska manifestationer är vanliga vid SLE.
Anemi vid SLE kan ha många olika orsaker; inflammation orsakad av ökad sjukdomsaktivitet, järnbristanemi, njurinsufficiens, autoimmun hemolytisk anemi eller aplasi orsakad av benmärgssuppression av läkemedel eller antikroppar mot erytroblaster eller erytropoetin.
Leukopeni (<3,0×109/L) och neutropeni (<1,5×109/L) kan bero på immunologiska reaktioner, på behandling (till exempel AZA, cyklofosfamid [CYK], rituximab [RTX]), på benmärgsdysfunktion eller på hypersplenism. Lymfocytopeni (<1,0×109/L) kan orsakas av anti-lymfocytantikroppar, ökad apoptos eller behandling med kortikosteroider.
Lätt trombocytopeni (100–150×109/L) orsakas oftast av immunmedierad trombocytopeni (ITP), men kan också bero på nedsatt produktion beroende på läkemedelsbehandling (myelosuppressiva cytostatika, tiazider, karbamazepin, digitoxin, metyldopa, klopidogrel, glykoprotein IIb/III hämmare, heparin) eller i ovanliga fall bero på ökad konsumtion vid trombotisk mikroangiopati. Trombocytopeni är ofta associerat med andra immunologiskt betingade penier och med antifosfolipidsyndrom (APS). ITP kan vara den första sjukdomsmanifestationen vid SLE, såsom också Evans syndrom (kombination av autoimmun trombocytopeni och autoimmun hemolytisk anemi). Trombocytopeni är en negativ prognostisk faktor vid SLE (33).
Pancytopeni ses ibland vid SLE, men kan även bero på benmärgsinsufficiens vid aplastisk anemi, myelodysplastiskt syndrom, myelofibros och leukemier. Vidare förekommer makrofag-aktiveringssyndrom vid SLE.
Utredning
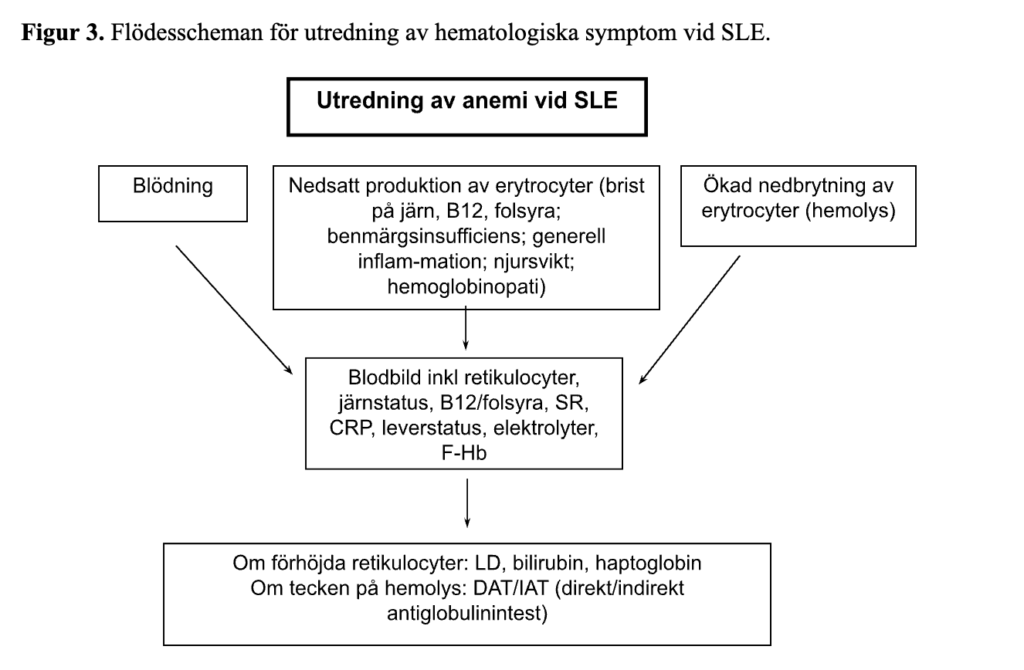
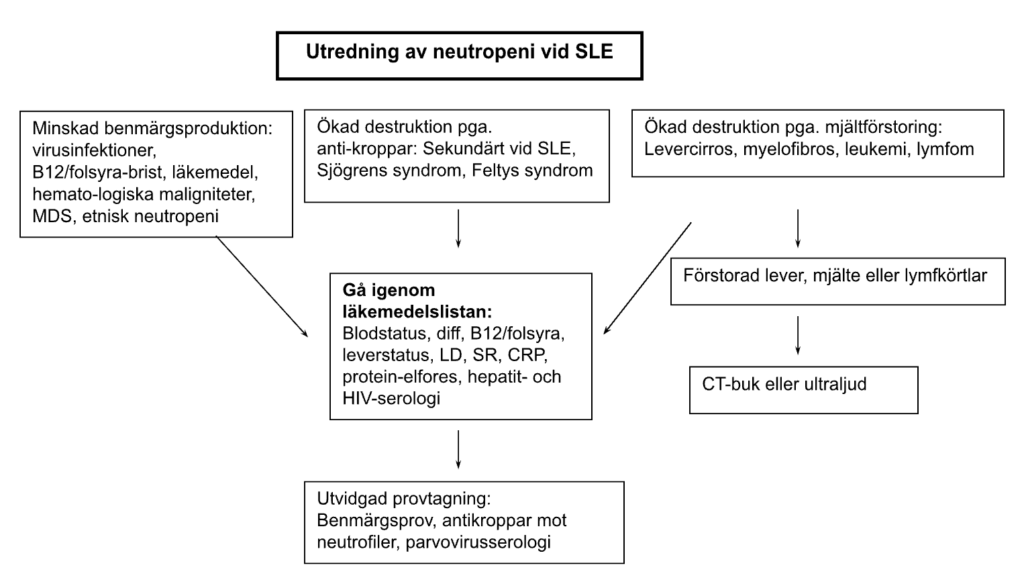
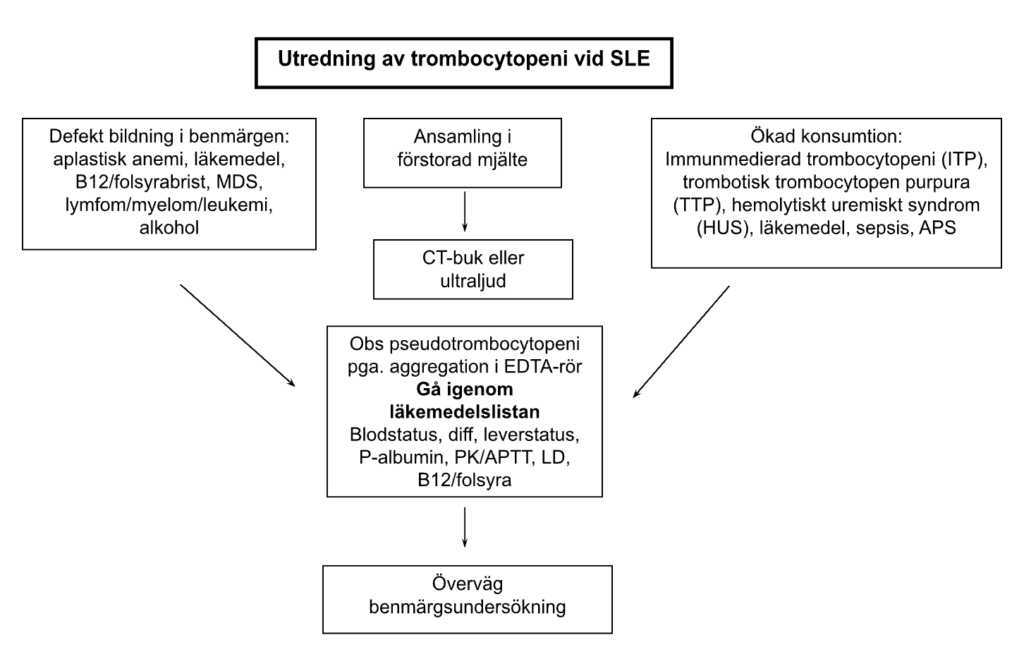
Den initiala utredningen av cytopenier bör inriktas på flera olika differentialdiagnoser (se flödesschema, Figur 3).
Behandling vid anemi
Behandling vid anemi orsakad av kronisk inflammation
Behandla grundsjukdomen. Kortikosteroider ger snabb effekt där man kan börja med medelhög dos (20–30 mg prednisolon per dygn) som trappas ned. Immunosuppressiva läkemedel kan också ge effekt men ökar risken för benmärgssuppression.
Behandling av anemi orsakad av njurinsufficiens
Överväg erytropoetin.
Behandling vid aplasi av erytrocyter
Kan bero på benmärgssuppression orsakad av behandling med läkemedel men kan också bero på antikroppar mot antigen på erytroblaster eller mot erytropoetin, vilket kan behandlas med kortikosteroider, CYK eller CS.
Behandling av autoimmun hemolytisk anemi
Evidens finns huvudsakligen för behandling av autoimmun hemolytisk anemi utan SLE (34). Behandlingen är akut och majoriteten av patienter med autoimmun hemolytisk anemi svarar på högdos kortikosteroider (1–2 mg/kg per dag av prednisolon) (35). Vid behandlingssvar kan steroiddosen snabbt sänkas (halvera dosen efter 14 dagar, sänk till 20 mg/dag inom en månad och trappa sedan ut helt inom 3–4 månader). Vid akuta situationer rekommenderas intravenösa pulsar med metylprednisolon tre dagar i följd. Om inte steroider har tillräcklig effekt ges RTX 1000 mg iv × 2 med 14 dagars intervall (36). Kortikosteroidsparande behandling är tillägg av AZA, MMF, CS eller BEL (34). Intravenöst immunglobulin (IvIg) kan ffa. vara ett alternativ till patienter som har stor infektionsrisk eller är gravida och ger en snabb men temporär effekt. Splenektomi bör vid SLE endast göras om annan behandling inte har effekt pga. risk för akuta svåra infektioner och för trombos (särskilt vid förekomst av aPL). Blodtransfusion bör undvikas pga. av risk för induktion av ytterligare antikroppsbildning mot erytrocytantigen, men kan ges på vitalindikation.
Behandling vid mikroangiopatisk hemolytisk anemi (MAHA)
Dessa patienter har förutom MAHA med schistocyter även trombocytopeni, njurengagemang, feber och neurologiska symtom. Liknar trombotisk trombocytopen purpura (TTP). Kan behandlas med högdos steroider och noggrann observans om sjukdomen är mindre allvarlig och med plasmabyten vid allvarlig sjukdom (37). Behandlas således på samma sätt som TTP eller hemolytiskt uremiskt syndrom (HUS).
Behandling vid leukopeni
Leukopeni vid SLE behöver oftast inte behandlas med undantag av svår neutropeni (<0,5×109 /L) tillsammans med upprepade bakteriella infektioner. I detta läge kan behandling med G-CSF ges i lägsta möjliga dos för att minimera risken för skov i SLE. Patienter med autoimmun neutropeni kan dock vara infektionsfria även vid svår neutropeni. Lymfopeni behöver inte behandlas, men är en markör för SLE med ökad risk för organskada (38). Behandling med AZA riskerar att försämra leukopenin via benmärgssuppression. Försiktig upptitrering av AZA kan göras under noggrann monitorering av leukocytnivåer i blodet. CS kan prövas då det ger mindre risk för leukopeni jämfört med AZA. I sällsynta fall kan behandling med IvIg ges. Behandling med ANI har visat positiv effekt avseende leukopeni (39).
Behandling vid trombocytopeni
Evidens finns huvudsakligen för behandling av primär ITP utan SLE (40). Trombocytpartikel-koncentration (TPK) över 50 behöver inte behandlas. Ökad risk för blödning finns vid TPK <50 men nivåer mellan 20 och 50 behandlas enbart om patienten har blödningssymptom. Nivåer <20 ska behandlas oavsett symptom då svåra blödningar kan inträffa.
Vid akut trombocytopeni är behandlingen främst högdos prednisolon 1–2 mg/kg/dag i upp till 14 dagar. Om en acceptabel stegring av TPK erhålls bör dosen prednisolon trappas ner med målet att sättas ut helt efter 2 månader (40). I akuta situationer och svåra fall med risk för blödning rekommenderas att prednisolon kombineras med IvIg. Om patienten inte svarar på kortikosteroider eller IvIg ges RTX 1000 mg iv med 14 dagars intervall (36). Som tredjehandsterapi ges AZA, MMF eller CS (40). Vilket läkemedel som väljs beror på om patienten har andra manifestationer av SLE som måste behandlas och andra faktorer såsom infektionsrisk och graviditet.
TTP eller trombotisk mikroangiopati behandlas med högdos steroider och noggrann observans om mindre allvarlig sjukdom och plasmabyten vid allvarlig sjukdom. CYK kan också utgöra ett alternativ.
Vid kronisk immunologiskt betingad trombocytopeni som svarar sämre på kortikosteroider kan thrombopoetin-receptor agonister ges (romiplastim eller eltrombopag) för att höja TPK över 50×109/L och därmed minska risken för blödning (41). Dock bör dessa preparat ges med försiktighet hos patienter med samtidig APS eller förekomst av aPL pga. av rapport om ökad risk för arteriell och venös trombos (42). BEL kan även övervägas vid kronisk trombocytopeni orsakad av SLE (25).
Serositer och myokardit
Klinisk bild
Inflammation i serösa organ (pleurit, perikardit och peritonit) drabbar upp till hälften av patienter med SLE åtminstone någon gång under sjukdomsförloppet och är ofta lindriga. Serosit med eller utan påvisbar utgjutning utgör debutsymtom hos ca 5-10%, särskilt hos de SLE-patienter som debuterar under senare delen av livet. Kliniska manifestationer av myokardit kan variera från takykardi till dyspné, bröstsmärta eller fulminant hjärtsvikt. Myokardit är mer ovanligt och uppträder ofta i kombination med annat organengagemang, ofta i anslutning till SLE-debut.
Utredning
Vid misstänkt pleurit kan konventionell lungröntgen i flankläge ibland men inte alltid identifiera pleuraexsudat. Vid oklarhet eller misstanke om annan diagnos som lungemboli eller infektion kan även datortomografi av thorax göras.
Vid misstänkt perikardit rekommenderas ultraljud av hjärtat. Vid misstänkt peritonit rekommenderas att ultraljud eller DT buk ingår i utredningen och ascites kan förekomma (43). Peritonit är ovanligare än andra SLE-orsakade serositer, och får ses som en uteslutningsdiagnos.
Klinisk misstanke om myokardit föranleder hjärtutredning, som brukar inkludera MR hjärta och görs i samråd med kardiolog.
Behandling
Behandlingen av serosit är likartad oavsett om det drabbar pleura, perikard eller peritoneum. Lindriga fall kan svara på NSAIDs, men ofta krävs behandling med perorala kortikosteroider. Fallrapporter indikerar att kolkicin kan ha effekt på serositer och används ofta vid perikardit (44). Immunsuppression med MTX, AZA eller MMF kan provas i kortisonsparande syfte men den vetenskapliga evidensen är låg. CYK kan prövas i terapiresistenta fall (45). Behandlingsstudier med biologiska läkemedel för SLE-relaterad serosit saknas, men en andel av patienter som erhöll BEL i BLISS-studierna uppvisade serosit vid baseline och gynnades av behandling med BEL (25).
Patienter med upprepade pleuriter kan ibland drabbas av kvarstående pleurala smärttillstånd som kan vara svåra att särskilja från nya pleuritepisoder. Även om kunskapen om detta är begränsad kan NSAIDs, gabapentin och amitriptylin prövas mot smärtorna.
Behandling av myokardit har inte utvärderats i kontrollerade studier. SLE-sjukdomen är ofta aktiv, och ofta ges initialt höga doser kortikosteroider följt av immunosuppression i form av CYK och MMF tillsammans med HCQ (45).
Lungor och luftvägar
Ungefär 50% SLE patienter får någon form av lungengagemang under sjukdomens förlopp. Faktorer som ökar risken för tidig och permanent lungskada är högre ålder och förekomst av anti-RNP-antikroppar. Lungmanifestationer vid SLE är kopplade till en högre dödlighet, vilket varierar beroende på typ och omfattning av lungpåverkan (46).
SLE-relaterad lungsjukdom uppdelas enligt följande:
- pleuralt engagemang (serosit)
- parenkymatöst engagemang (kronisk interstitiell lungsjukdom, akut lupus pneumonit, shrinking lung syndrome, diffus alveolär blödning)
- kärlengagemang (pulmonell arteriell hypertension – PAH, tromboembolisk sjukdom)
- bronkiellt engagemang
Utredning
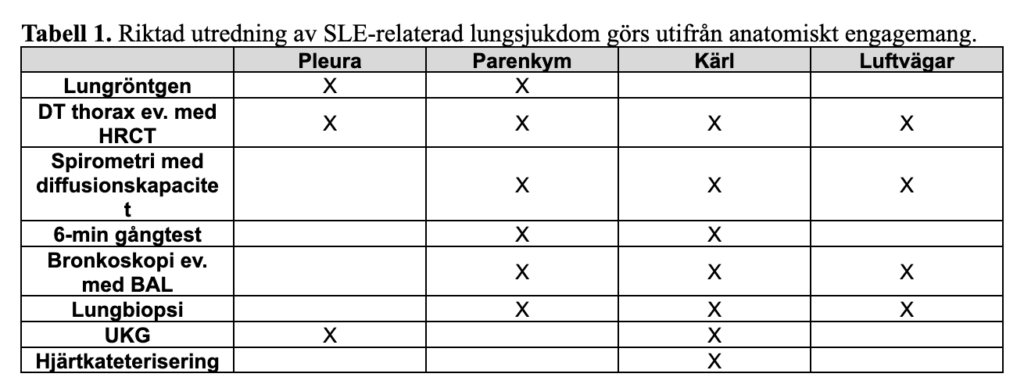
Förslag på utredning finns i Tabell 1.
Behandling
För de flesta typer av lungengagemang saknas kontrollerade behandlingsstudier, och behandlingsstrategierna baseras därför på klinisk erfarenhet och bästa tillgängliga kunskap. Nyligen publicerades ReCONNET–SLICC–SLEuro-expertkonsensus för behandling av sällsynta SLE-manifestationer, inklusive olika typer av lungengagemang (45).
Pleuralt engagemang (se separat avsnitt ”Serositer”)
Parenkymatöst engagemang
Kronisk interstitiell lungsjukdom (fibrotiserande lupus pneumonit) drabbar ca 4% av patienterna och är associerad till förekomst av Ro/SSA-antikroppar. Behandlingen innebär induktionsbehandling med kortikosteroider enbart eller i kombination med cyklofosfamid eller MMF, följt av underhållsbehandling med AZA eller MMF (45). Det finns inga studier som har undersökt effekten av antifibrotisk behandling vid interstitiell lungsjukdom hos patienter med SLE, men behandlingen kan möjligen ha en roll i att förebygga permanent lungskada. Fallrapporter finns där plasmabyten prövats med viss framgång.
Akut lupus pneumonit är en ovanlig manifestation med dyster prognos. Symtom utgörs ofta feber, hosta, pleuritsmärta, dyspné och ibland hemoptys. HRCT visar ofta bilateral pleuravätska med alveolära infiltrat, särskilt i nedre delen av lungorna. Expert Consensus föreslår behandling med metylprednisolon pulsar följt av prednisolon (1 mg/kg/dag, om möjligt nedtrappning under högst 6 månader) i kombination med cyklofosfamid (enligt EuroLupus-protokoll), därefter underhållsbehandling med MMF eller AZA (45).
Shrinking lung syndrome är en ovanlig manifestation och ger oförklarad dyspné, förhöjda diafragmavalv (i regel bilateralt) och sänkta lungvolymer utan tecken på interstitiell lungsjukdom. Prognosen är generellt sett god. Framgångsrik behandling med perorala kortikosteroider har beskrivits. Annan immunosuppression (AZA, MTX, CYK och RTX) har rapporterats kunna ha effekt i fall där kortikosteroider inte hjälpt (45).
Diffus alveolär blödning är ett sällsynt, men potentiellt livshotande tillstånd som kan ses vid SLE särskild vid förekomst av antifosfolipidantikroppar. Höga doser kortikosteroider används ofta med framgång. Plasmabyten har även visat sig öka överlevnaden hos patienter med ofullständigt svar på behandling med steroider. Även RTX har föreslagits vara verksamt (46).
Kärlengagemang
Pulmonell arteriell hypertension (PAH) är en ovanlig och potentiellt livshotande manifestation vid SLE och ger i regel dyspné. Majoriteten av SLE-patienter som drabbas av PAH har anti-ribonukleoprotein antikroppar och/eller reumatoid faktor. PAH ska utredas och behandlas av PAH-specialist. Diagnosen bekräftas slutligen definitivt med hjälp av hjärtkateterisering.
Tromboembolisk sjukdom, var god se stycke om APS.
Luftvägsengagemang
Övre luftvägsengagemang förekommer hos färre än 25 % av SLE-patienter någon gång under sjukdomen. Manifestationerna omfattar alltifrån orala ulcera (vanligt) och laryngit med ödem och milda ulcerationer, till rariteter som cricoarytenoidit, stämbandspares och nekrotiserande vaskulit. Prognosen är högst varierande, men många fall svarar bra på perorala kortikosteroider.
Ett fåtal fall med bronkiolitis obliterans och kryptogen organiserande pneumoni associerad med SLE har beskrivits. Varierande grad av framgång med steroider enbart eller i kombination med CYK finns rapporterat (46).
Nefrit
Klinisk bild
Nefrit är en vanlig och allvarlig organmanifestation som förekommer hos ca 50 % av patienter med SLE. Patienter med nefrit har ökad morbiditet och mortalitet jämfört med icke-nefrit patienter, främst på grund av ökad risk för hjärt-kärlsjukdom (15, 47). Lupusnefrit (LN) är en ”tyst manifestation” och ger i sig vanligen inga symtom. Därför bör urinstatus tas som rutin vid varje återbesök. Kardinalfynd vid nefrit är proteinuri.
Enligt SLICC-klassifikationen (5) (Bilaga C) definieras nefrit som:
- Proteinuri motsvarande >0,5 g/dygn (dU-albumin ca 300 mg eller U-protein/krea kvot ca 50 mg/mmol)
och/eller
- Förekomst av erytrocytcylindrar i urinsediment
Enligt de nyaste SLE-kriterierna från ACR/EULAR (2) där ANA i kombination med totalt minst 10 poäng krävs för att uppfylla klassifikation (Bilaga A) poängsätts nefritrelaterade fynd enligt nedan:
- Proteinuri >0,5 gram/24 timmar 4 poäng
- Biopsi med fynd av klass II eller V 8 poäng
- Biopsi med fynd av klass III eller IV 10 poäng
Utredning
Vid misstanke om nefrit bör utredning ske utan dröjsmål enligt nedan:
Urinprov för kvantifiering av proteinuri/albuminuri samt urinsediment.
Blodprover innefattande elektrolytstatus, p-albumin och blodfetter samt kartläggning av serologisk aktivitet med antikroppar mot dsDNA och komplementfaktorerna C3, C4 och C1q. Fosfolipidantikroppar bör kontrolleras om ej nyligen gjort. Kontroll av blodtryck är centralt.
För kvantifiering av proteinuri rekommenderas mätning av albumin/kreatinin-kvot i urin (U-A/C), helst i morgonurin.
I studier används ofta U-protein/kreatinin-kvot (U-P/C). Då albumin endast är en del av proteinurin behöver mängderna omräknas beroende av den metod som har använts. U-P/C >50 mg/mmol motsvaras av U-A/C >30 mg/mmol eller proteinuri på >0,5 g/dygn (48).
Vid misstanke om nefrit ska njurbiopsi utföras om inte kontraindikation föreligger. Generell rekommendation är att njurbiopsi ska utföras vid proteinuri U-P/C ≥50 mg/mmol (motsvararand U-A/C ≥30 mg/mmol), vid fynd av erytrocyter/erytrocytcylindrar i urinsediment samt vid försämrat GFR som inte kan förklaras av annan anledning (49, 50). Observera att det kan vara aktuellt med biopsi även vid lägre grad av proteinuri.
Njurbiopsi behövs för klassifikation av nefrit och ställningstagande till behandling, samt för att utesluta annan orsak till njurpåverkan. Utvärdering av biopsin bör ske med International Society of Nephrology/Renal Pathology Society (ISN/RPS) klassifikation (Tabell 2) (51) samt bedömning av aktivitets- och kronicitetsindex (52).

Utöver nefrittecken kan kärlförändringar indikerande APS med nefropati (APSN) och/eller interstitiella förändringar föreligga. Även dessa ska bedömas vid histopatologisk utredning och har betydelse för prognos och behandling (53). Ytterligare information om APSN finns under avsnittet om APS. Ställningstagande till antikoagulantiabehandling i dessa fall är av vikt.
Behandling
Höga doser kortikosteroider under längre tid bör undvikas och individualisering rekommenderas.
Både EULAR och ACR har under 2025 utarbetat uppdaterade behandlingsriktlinjer för SLE-nefrit (49, 50). Nytt i dessa riktlinjer är framförallt rekommendationer kring tidig kombinations-behandling, inklusive biologisk medicinering. De innefattar även rekommendationer kring övrig behandling, “non-immune treatment”.
Senare års rekommendationer har inneburit ett paradigmskifte avseende behandling av LN från att tidigare ha indelat behandlingen i 2 faser, induktions- respektive remissionsbehandling, till att nu rekommendera en mer kontinuerlig immunosuppressiv behandling under minst 3 år. Målet är dock som tidigare att uppnå ett snabbt svar på behandling, vilket har visats ge bättre prognos på sikt (54).
Behandling vid biopsiverifierad SLE-nefrit klass III/IV + klass V eller klass V med proteinuri >1 g/dygn (U-Albumin/kreatinin > 60):
Flera behandlingsalternativ föreligger. Generellt gäller att immundämpande medicin ska startas direkt vid diagnos och innehålla antingen MMF eller CYK tillsammans med kortikosteroider samt med ställningstagande till tilläggsbehandling av BEL eller calcineurinhämmare (CNI) i form av takrolimus (TAK) eller voklosplosplosporin (VOK). I enstaka fall med flera negativa prognostiska faktorer kan även obinutuzumab (OBI) övervägas som alternativ till BEL/CNI redan initialt. Vid avsaknad av prognostiskt ogynnsamma faktorer är ett alternativ att vänta med tilläggsbehandling BEL/CNI, under tät uppföljning och ställningstagande till tilläggsbehandling vid otillräcklig effekt. Följande behandling rekommenderas:
- HCQ
- ReninAngiotensinAldosteronSystem (RAAS)-blockad
- Kortison
- Ett av följande alternativ:
- MMF eller CYK + BEL
- MMF + kalcineurinhämmare (CNI)
- MMF + OBI
- MMF eller CYK i monoterapi
HCQ: Behandling med HCQ ska alltid ges, oavsett nefritklass, om inte kontraindikationer föreligger. HCQ har visats minska risken för skov och uppkomst av njurskada (55).
RAAS-blockad: ACEi/ARB ska ges för att reducera proteinuri och sänka blodtrycket.
MMF och CYK: MMF och CYK har bedömts som likvärdiga alternativ som inledande behandling (15, 56) men i de nya ACR-riktlinjerna rekommenderas MMF före CYK (50).
MMF ges peroralt i måldos 3 g/dygn. Till patienter som inte tolererar MMF kan man ge natriummykofenolat (360 mg natriummykofenolat motsvarar 500 mg MMF).
CYK ges intravenöst 500 mg varannan vecka i tre månader enligt Euro-Lupus-protokollet (54, 57), se bilaga D.
Efter 3 månaders behandling med CYK rekommenderas i första hand MMF (49), alternativt azathioprin (AZA). En jämförelse mellan MMF och AZA utfördes i MAINTAIN-studien där man visade numerärt färre skov vid MMF (dock ej signifikant) och något ökad förekomst av cytopenier vid AZA (54).
Vid snabbt progredierande glomerulonefrit, eller vid förekomst av många prognostiskt ogynnsamma faktorer (manligt kön, icke-kaukasiskt ursprung, hypertoni, sänkt njurfunktion, högt histopatologiskt aktivitets- och kronicitetsindex på biopsin) kan även behandling med högdos CYK iv övervägas men rekommenderas inte generellt (NIH-protokoll, se bilaga D) (49,58).
Terapi med endast MMF/CYK utan tilläggsbehandling kan övervägas vid gynnsamma faktorer som förstagångsnefrit, låggradig proteinuri, normalt GFR och mild histopatologisk bild. Då bör tät och regelbunden uppföljning ske, med beredskap för insättning av tilläggsbehandling vid otillräcklig effekt.
BEL i kombination med MMF har visat bättre behandlingssvar (59) och färre njurskov på sikt (60) jämfört med MMF i monoterapi. Kombinationsbehandling med BEL ska övervägas till patienter med extrarenala manifestationer eller negativa prognostiska markörer för nefrit såsom hög titer anti-dsDNA och uttalad komplementkonsumtion.
Initiala studier av behandling med CYK i kombination med BEL talade för bättre svar på behandling än CYK+placebo, men resultaten nådde inte statistisk signifikans. Post-hoc-analyser har dock visat att gruppen som fick CYK+BEL hade färre skov och mindre risk för nedsatt njurfunktion på sikt jämfört med gruppen som fick CYK+placebo (59,60).
VOK är en ny kalcineurinhämmare som har registrerats som tilläggsbehandling vid aktiv SLE-nefrit (klass III, IV och V) i kombination med MMF. Behandling med VOK har visats snabbt reducera graden av proteinuri. VOK påverkade dock inte den serologiska aktiviteten (61). Treårsuppföljning av studien har visat högre förekomst av renal respons i VOK-gruppen (62).
TAK i singelterapi har tidigare visats ha likvärdig effekt som MMF vid klass III/IV/V som induktionsterapi (63). TAK eller VOK kan övervägas som monoterapi vid ren LN klass V om proteinuri < 1 g/dygn men rekommenderas i övrigt ges i kombination med MMF enligt ovan (50).
Vid GFR<45, påtaglig blodtryckssteging eller högt kronicitetsindex på njurbiopsin bör BEL ges som tilläggsbehandling istället för VOK eller TAK med tanke på potentiell nefrotoxicitet av CNI (50).
OBI är en monoklonal humaniserad och glykomodifierad anti-CD20-antikropp. Den har som tillägg till standardbehandling med MMF i två stora studier vid SLE-nefrit visat signifikant bättre behandlingssvar än placebo (64,65). Störst skillnad mellan behandlings- och placebogrupp sågs hos patienter med hög sjukdomsaktivitet (proteinuri >3 g, högt anti-dsDNA, lågt C3, C4 samt nefrit klass IV och/eller III/VI +V (65). Obinutuzumab är med i de senaste riktlinjerna från EULAR, och kan övervägas redan initialt vid hög sjukdomsaktivitet, vid flera negativa prognostiska faktorer (som manligt kön, icke-kaukasiskt ursprung, hypertoni, sänkt njurfunktion, samt högt histopatologiskt aktivitets- och kronicitetsindex på biopsin) eller vid otillräcklig respons på initial terapi. Det finns ännu inte tillräcklig erfarenhet av OBI vid LN för att ge rekommendationer kring återbehandling och infektionsrisk bör beaktas.
RTX visade i en RCT (LUNAR) inte bättre effekt än konventionell terapi vid SLE-nefrit (66). Flera registerstudier har dock talat för gynnsam effekt av RTX vid nefrit. Trots avsaknad av dokumenterad effekt i RCTs kan RTX ges framförallt vid utebliven effekt av konventionell terapi vid ISN klass III-IV med eller utan klass V. Data kring återbehandling med RTX vid LN saknas idag.
Samt:
Kortikosteroider iv/po i nedtrappningsdos.
Enligt de senaste EULAR-rekommendationerna föreslås iv metylprednisolon initialt 500-2500 mg uppdelat på 3 dagar följt av prednisolon 0,3-0,7 mg/kg med gradvis nedtrappning till max 5 mg/dag efter 4-6 månader. Vid LN klass V nefrit utan nefros (proteinuri < 3 g/dygn) kan lägre initiala kortisondoser ges (49).
Alternativa scheman för kortison finns enligt Euro-Lupus, KDIGO och ACR (50, 57, 58).
Vid SLE-nefrit klass V med proteinuri <1 g/dygn
För LN klass V med relativt låggradig proteinuri finns färre studier och rekommendationer, men föreslås immundämpande terapi (50) enligt nedan:
- Kortikosteroider
och
- MMF
eller
- AZA eller TAK/VOK
Övriga behandlingsrekommendationer vid samtliga nefritklasser:
- Blodtryck bör ligga <130/80 mm Hg.
- Beakta behov av blodfettssänkande terapi vid hyperlipidemi.
- Kalk och vitamin D ska ges vid kortisonbehandling, överväg även bisfosfonat.
- Lågmolekylärt heparin alternativt warfarin om nefros med p-albumin <20–25 g/L.
- Acetylsalicylsyra (ASA) vid förekomst av fosfolipidantikroppar
- Beakta eventuell erytropoetinbrist vid anemi.
- Tillägg av SGLT2 hämmare kan övervägas vid stabil sjukdom, eventuellt i samråd med njurmedicin.
Observera att all behandling bör ske i samråd med patienten samt vara individualiserad med hänsyn tagen till fertilitet, följsamhet till behandling och samsjuklighet.
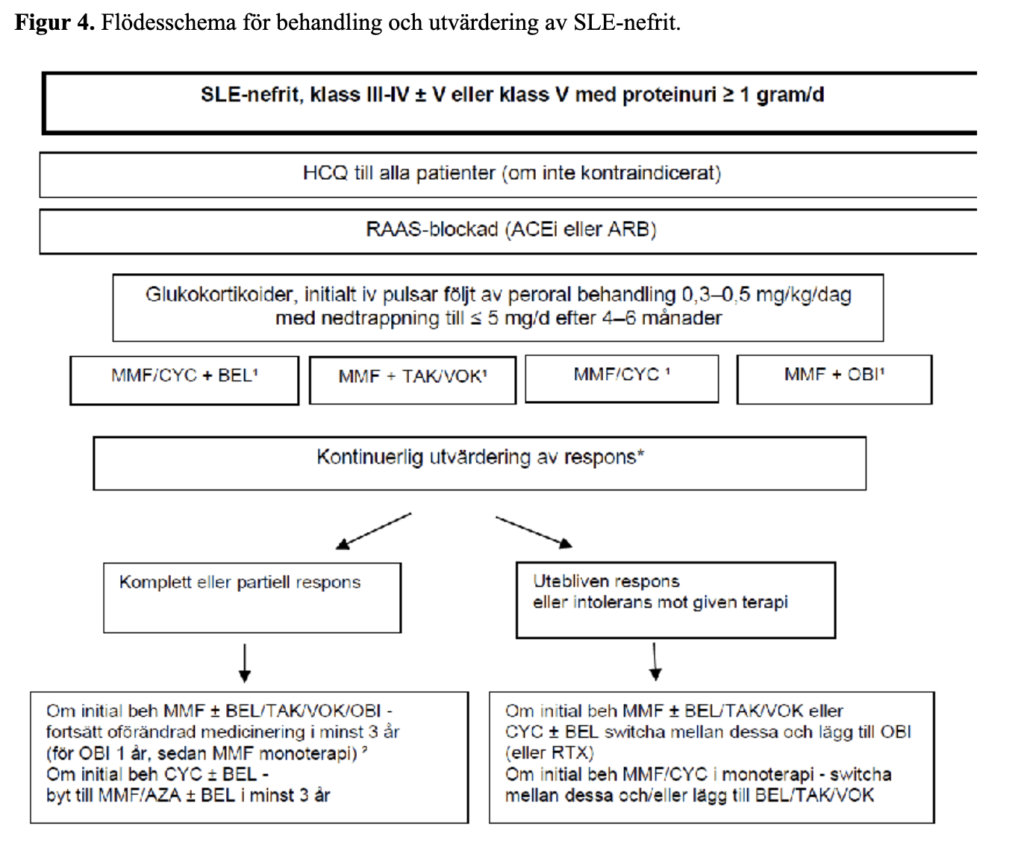
Se flödesschemat i Figur 4 för behandling.
Monitorering
Tät monitorering (var 2–4:e vecka i 2–4 månader, därefter glesare beroende på allvarlighetsgrad och behandlingssvar) rekommenderas med successiv och aktiv steroidnedtrappning samt kontroll av blodtryck, elektrolytstatus, p-albumin, grad av proteinuri och förekomst av urincylindrar. Även serologisk aktivitet (komplement och anti-dsDNA antikroppar) bör kontrolleras beroende på nefrittyp och svårighetsgrad, förslagsvis efter 3, 6 och 12 månader.
Koncentrationsbestämning av MMF och TAK kan vara av värde för monitorering av behandlade patienter men rekommendationer kring optimalt terapeutiskt intervall saknas. VOK kräver inte koncentrationsbestämningar.
Utvärdering av respons
Fler olika responskriterier för behandlingssvar finns, huvudsakligen baseras dessa responskriterier på grad och minskning av proteinuri, avsaknad av aktivt sediment i kombination med njurfunktionspåverkan. Då graden av proteinuri varierar bör upprepade mätningar av U-A/C utföras.
Utvärdering av behandlingssvar bör ske kontinuerligt och vid utebliven effekt bör byte av förstalinjebehandling övervägas, se figur 4. Observera att alltid överväga bristande compliance vid uteblivet/otillräckligt behandlingssvar.
Vid utvärdering av respons bör man även beakta de effekter på proteinurin som uppnås av behandling med ACEi och ARB.
Studier har visat bättre njurfunktion vid långtidsuppföljning om man uppnår proteinuri <0,7 g/dygn efter 12 månaders terapi (67). De idag befintliga responskriterierna utgår från proteinuri och njurfunktion och (Tabell 3) delas upp i komplett och partiell respons (47, 49, 50). Rebiopsi efter 6–12 månader kan vara värdefull vid utvärdering av terapieffekt då studier visat diskrepans mellan klinisk och histopatologisk respons (68, 69) och bör särskilt beaktas vid tveksamhet kring behandlingssvar.

Fortsatt behandling
Efter att ha uppnått stabil respons, antingen med initial immundämpande medicin eller efter byte och/eller tillägg av medicinering enligt figur 4, bör medicineringen fortgå minst 3 år. Behandlingen bör därefter individualiseras. Hos patienter med komplett respons kan man överväga att successivt minska immunosuppressionen med noggrann uppföljning för att upptäcka tecken till skov (49). Man bör balansera behandlingen med mål att behålla patienten i remission, undvika skov och njurfunktionsnedsättning men även att fullfölja behandling med minimal toxicitet. För fortsatt behandling bör man även beakta eventuell extra-renal sjukdomsaktivitet, adherens till läkemedelsbehandling, användande av HCQ samt (om rebiops har gjorts) kvarvarande histopatologisk aktivitet i njurvävnad trots inaktiv sjukdomsbild kliniskt (49). Patienter som recidiverat i nefritskov bör vanligen ha förlängd behandling.
Observera att HCQ har visats förebygga nefritskov och ska inte sättas ut såtillvida inte kontraindikationer föreligger (55).
Vid kvarstående njurfunktionspåverkan (GFR 20-60), ihållande proteinuri eller andra riskfaktorer för progredierande njursvikt, överväg tillägg SGLT2-hämmare, eventuellt i samråd med njurmedicin.
Njurinsufficiens
Patienter som utvecklar njurinsufficiens bör skötas i samarbete med specialist i njurmedicin. Behandling mot rubbningar i kalk-fosfatbalans, behov av erytropoetin och annan konservativ njursviktsterapi ska i första hand handläggas via njurmedicin. Vid terminal njursvikt kan såväl peritoneal- som hemodialys bli aktuell. Risken för återfall i nefrit efter njurtransplantation är förhållandevis låg vid SLE-nefrit (70).

Nervsystemet
Klinisk bild
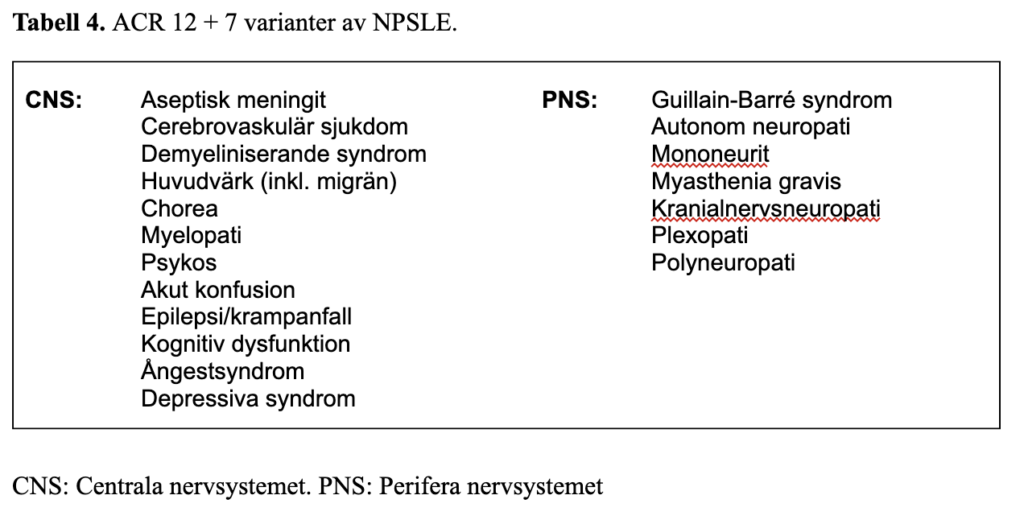
Exakt definition av neuropsykiatrisk SLE (NPSLE) saknas, men ACR:s kommitté publicerade 1999 förslag på 19 manifestationer från det centrala och perifera nervsystemet som bör ingå (71) (Tabell 4). Från dessa ingår psykos och kramper i ACR/EULAR klassifikationskriterier från 2019 (2), där också delirium lagts till som kriterium.
Engagemang av nervsystemet är vanligt vid SLE, men den rapporterade incidensen (12–95 %) varierar kraftigt mellan olika studier (). Variationerna förklaras sannolikt av skillnader i studiedesign och svårigheter att identifiera NPSLE som primär orsak till mildare neuropsykiatriska manifestationer såsom mild kognitiv dysfunktion, depression, huvudvärk, ångest och perifer neuropati. Svårare CNS-manifestationer är mer sällsynta. I en prospektiv studie av 370 patienter (medelålder 32±14 år), hade 4,3% en allvarlig CNS manifestation under 3 års uppföljning (72). Men, patienter med tidigare NPSLE uteslöts och eftersom sjukdomsdurationen var 9 år i medeltal, finns risk för viss underskattning då CNS-manifestationer är vanligare tidigt i sjukdomsförloppet (73). NPSLE-skov tenderar att öka kumulativt över tid (74) och är associerade med försämrad livskvalitet och en klart ökad mortalitet (75).
Utredning och attribuering
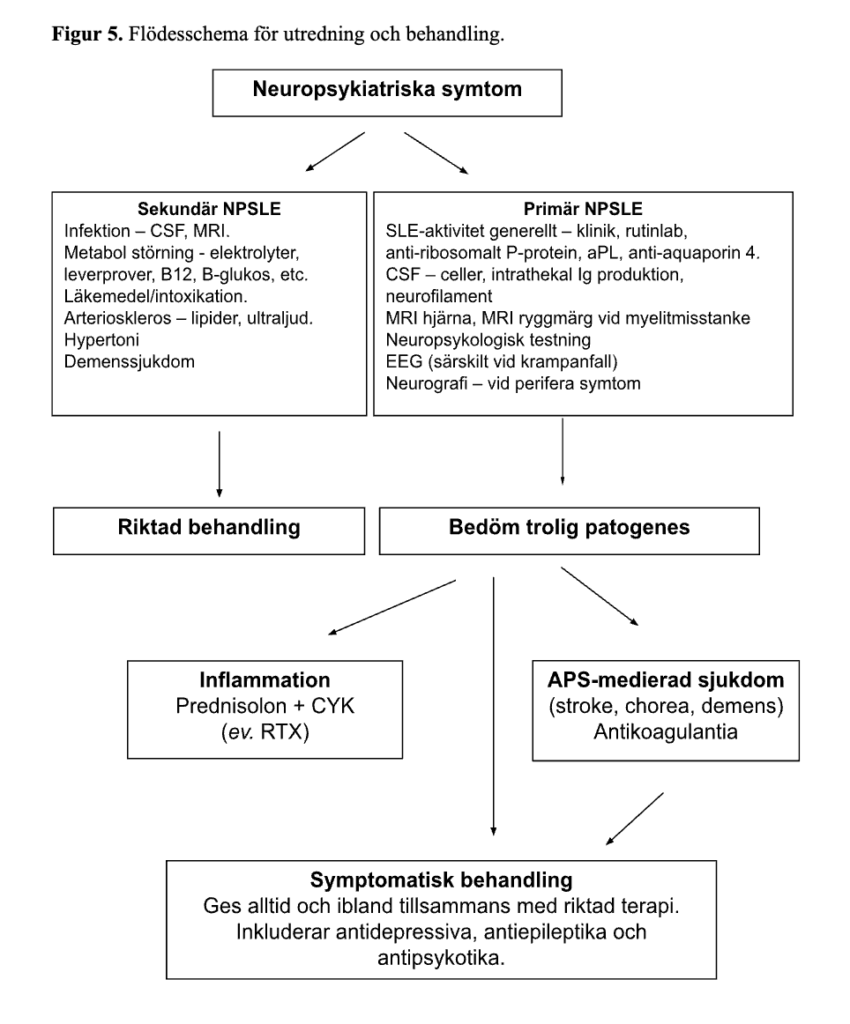
Flera översikter har publicerats med förslag på hur NPSLE ska diagnosticeras och behandlas där EULAR kom med sina rekommendationer 2010 (76). Utredningen styrs av den kliniska bilden och gjorda fynd vid initial undersökning av patienten (fokalt eller diffust NS-engagemang). Attribuering vid NPSLE är ofta en klinisk utmaning – att avgöra om NP-manifestationer är uttryck för grundsjukdomen (primär NPSLE) eller om det finns andra orsaker såsom infektion, läkemedelsbiverkan, intoxikation, metabol rubbning, hypertoni, primär neurologisk eller psykiatrisk sjukdom (sekundär NPSLE).
Vid attribuering av misstänkt NPSLE är det viktigt att beakta i vilket sammanhang den neuropsykiatriska händelsen uppträder (77). Samtidig klinisk och serologisk SLE-aktivitet i andra organ talar för primär NPSLE, medan förekomst av tydliga konkurrerande orsaker, exempelvis infektion, läkemedelsbiverkan eller metabol rubbning, talar emot. Vidare minskar en symtombild dominerad av ospecifika neuropsykiatriska symtom med hög förekomst i bakgrundsbefolkningen, såsom huvudvärk, ångest, mild depression eller lindrig kognitiv svikt, i frånvaro av annan SLE-aktivitet, sannolikheten för primär NPSLE . Upprepad multidisciplinär bedömning är ofta avgörande (78). Det är generellt vanligare att neuropsykiatriska symtom har sekundär orsak än tvärt om och fördelningen brukar uppskattas till 2/3 sekundär NPSLE och 1/3 primära fall (79). Kända riskfaktorer för primär NPSLE är hög sjukdomsaktivitet eller förekomst av organskador, tidigare NPSLE manifestationer och förekomst av aPL (särskilt stroke, chorea och epilepsi) samt lymfopeni (38). Således är uteslutande av infektion, läkemedelsbiverkan, metabola orsaker, cerebrovaskulär sjukdom, primär neurologisk/psykiatrisk sjukdom och läkemedelsinducerad neurotoxicitet en viktig del av utredningen.
Basal provtagning: CRP, blodstatus, elektrolyter, U-sticka, B-glukos, aPL, anti-dsDNA och komplement. Ytterligare provtagning anpassas till den kliniska situationen. Neurofilament light (NfL) i likvor eller plasma kan i vissa fall bidra med information om grad av axonal skada, men är ospecifikt och bör tolkas med försiktighet. Undersökning av likvor (celler, intratekal immunglobulinproduktion, odling, virus-PCR) och bilddiagnostik med magnetkameraundersökning (MRI) av CNS eller ryggmärg ingår i de flesta fall i basutredningen (Tabell 5). Några radiologiska förändringar specifika för SLE finns inte och i ett publicerat material med patienter som uppvisade klara neuropsykiatriska manifestationer hade omkring 50% helt normal MRI (80).
Opticusneurit och akut myelit är kända manifestationer inom s.k. Neuromyelitis Optica Spectrum Disorders (NMOSD) (81). Vid opticusneurit och myelit som del i NPSLE överlappar diagnostiskt med NMOSD och en betydande andel SLE patienter har också ökad förekomst av antikroppar mot aquaporin-4 (AQP-4), likt de med demyeliniserande NMOSD (82). Förekomst av AQP-4 är inte alltid associarat med en demyeliniserande sjukdom vid SLE, men förekomst av antikroppar kan ha betydelse för val av behandling (se nedan) och bör därför ingå i utredning av dessa tillstånd.
Vid tidig debut, atypiska CNS manifestationer eller uttalad behandlingsresistens bör även sällsynta monogena interferonmedierade sjukdomar (tex Aicardi-Goutieres syndrom) beaktas, då den kliniska bilden delvis kan överlappa NPSLE. Kliniskt användbar mätning av interferonaktivitet saknas idag, men DT av CNS påvisar ofta typiska förkalkningar i sjukdomsgruppen.

Behandling
Terapin vid primär NPSLE bör riktas mot identifierad orsak och kan därför innefatta allt från antikoagulantia (till exempel aPL-medierad stroke) till immunosuppression med kortikosteroider i kombination med cytostatika (till exempel immunmedierad konfusion, myelit, mononeurit), se flödesschema i Figur 5.
Flera översiktsartiklar diskuterar behandlingen vid NPSLE (83), men bara en randomiserad studie med immunosuppressiv behandling specifikt avseende NPSLE har publicerats (84). Här inkluderades 32 patienter med varierande men allvarliga NPSLE-manifestationer. Behandlingen pågick i 2 år, antingen med enbart steroidpulsar (metylprednisolon 1 g/dygn×3 följt av månatlig steroidpulsar i 4 månader och därefter glesare steroidpulsar) eller med iv CYK (0.75 g/m2 månatligen i 1 år och sedan varannan månad i ytterligare 1 år). Samtliga fick steroider 1 mg/kg/dygn i nedtrappande dos under 3 månader. Resultatet från studien visade ett klart bättre utfall för CYK tillägg (respons med CYK 95% versus steroider 54%). Enskilda fallbeskrivningar har rapporterat god effekt av RTX vid NPSLE och RTX används i praktiken vid terapirefraktär NPSLE, men systematisk genomgång anger svag evidens (83, 85101). Studieunderlaget för behandling av överlappande AQP-4 positiv NMOSD vid SLE är bristfälligt, men extrapolering av NMOSD studier talar för RTX, MMF eller azatiprin som steroidsparande behandling (86).
Depression behandlas symptomatiskt, efter uteslutning av eventuell kognitiv rubbning och behandlande läkare bör vara medveten om att ökad mortalitet i suicid rapporterats bland SLE patienter (87).
Antiepileptika används vid upprepade krampanfall men viktigt att beakta ev. tecken på inflammatoriskt CNS-engagemang, som kräver utredning. Det är centralt med tät uppföljning och kontakt med anhöriga vid NPSLE då inte sällan patienten själv har svårt att redogöra för sjukdomens utveckling. Vid sekundär NPSLE blir behandlingen inriktad mot orsaken till sjukdomsbilden, som exempelvis infektion, metabol rubbning eller spänningshuvudvärk.
En viktig aspekt av bedömningen av NPSLE är att göra uppföljande utvärderingar av tillståndet. Ofta behövs ett multidisciplinära omhändertagande, inkluderande neurolog, neuroradiolog, neuropsykolog och psykiatriker i både inledningsskede och vid uppföljning. Men, även med multidisciplinärt omhändertagande i ett högspecialiserat center för NPSLE sågs att 14.6 % av patienterna klassificerades om från primär NPSLE till ”sekundär” SLE vid uppföljning (78).
Ett problem vid primär NPSLE är att det ibland är svårt, eller t.o.m. omöjligt, att avgöra om organskadan är stationär, och således ett uttryck för tidigare NPSLE-skov, eller progressiv. Den sammantagna kliniska bilden, även här med återkommande utvärderingar av patienten, blir då avgörande för bedömningen.
Antifosfolipidsyndrom
Klinisk bild och utredning
APS förekommer hos cirka 15–20 % av patienter med SLE och benämns då sekundärt APS, till skillnad från primärt APS som uppträder isolerat. APS klassificeras vid förekomst av trombos och/eller graviditetskomplikation i kombination med persisterande antifosfolipidantikroppar (aPL) (88), Tabell 6. De nya ACR/EULAR-kriterierna från 2023 inkluderar även klaffsjukdom och trombocytopeni samt mer precisa definitioner av kliniska och serologiska kriterier (89). Kriterierna är främst avsedda för forskning och behöver utvärderas i klinisk praxis innan de kan användas rutinmässigt.
Tabell 6. Klassifikation av APS.
APS föreligger vid minst ett kliniskt symptom och upprepad positivitet, med minst 12 veckors mellanrum, i ett av laboratoriefynden.
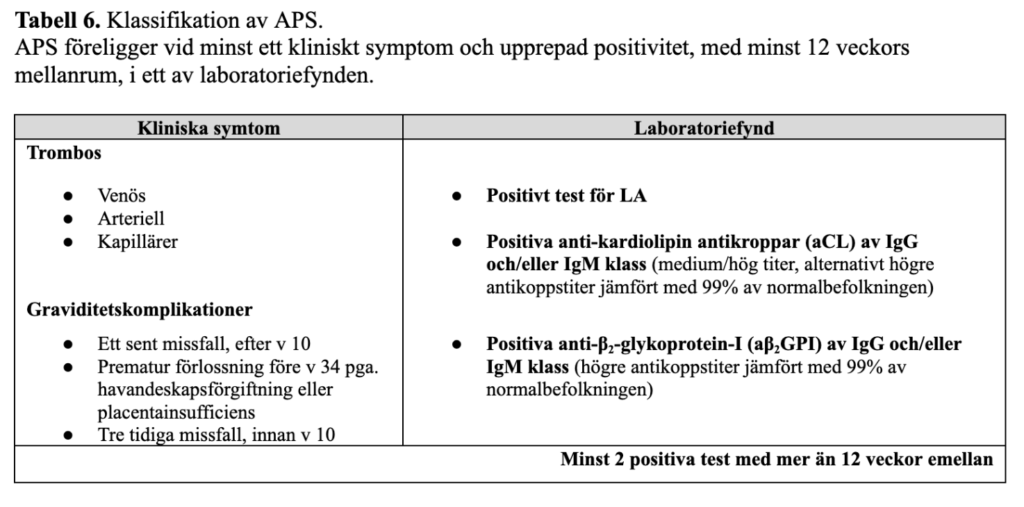
Tromboser vid APS kan engagera alla kärlbäddar. Djup ventrombos och lungemboli är vanligaste, medan stroke är den vanligaste arteriella manifestationen. Även mikrovaskulära tromboser, exempelvis i hud eller njure, kan förekomma. Vid graviditet kan APS orsaka komplikationer såsom tidiga och sena missfall, intrauterin fosterdöd, havandeskapsförgiftning, prematur förlossning och placentainsufficiens. Alla SLE patienter bör testas för aPL, med upprepad provtagning efter 12 veckor vid positivt fynd eller inför planerad graviditet.
Det viktigaste testet för aPL är det funktionella lupusantikoagulans (LA) testet, som har den starkaste kopplingen till både trombotiska manifestationer och graviditetskomplikationer (90). Eftersom behandling med antikoagulantia kan ge falskt positiva resultat är det viktigt att sådan behandling anges på remissen. Antikardiolipinantikroppar (aCL) och anti-β2glykoprotein-I antikroppar (aβ2GPI) analyseras med ELISA-teknik. Enligt APS-kriterierna ingår aCL och aβ2GPI av IgG- och IgM-isotyp (Tabell 6). Även IgA antikroppar mäts ofta, men ingår inte i APS-klassifikationskriterierna. Däremot omfattar både SLICC- och EULAR/ACR-kriterierna för SLE alla tre isotyper: IgG, IgM och IgA (2, 5).
Patienter som är positiva för samtliga tre tester – LA, aCL och aβ2GPI har s.k. trippelpositivitet, vilket innebär den högsta risken för trombos (91, 92). Även isolerad LA-positivitet och höga nivåer av aCL eller aβ2GPI definierar en högrisk aPL-profil (91) (Tabell 7).
Katastrofalt APS (CAPS)
En sällsynt variant av APS (ca 1%) är CAPS som inom några dagar till veckor drabbar flera organ, oftast med mikrotromboser. Det är vanligt att njurar, lever, lungor, nervsystem och hjärta engageras där minst tre organ ska vara påverkade enligt definitionen för ”definitivt CAPS” (93). I de flesta fall kan man definiera bakomliggande orsak till CAPS, till exempel infektion, kirurgiskt ingrepp, graviditetskomplikation eller nyligen avslutad warfarinbehandling. CAPS är viktigt att snabbt diagnostisera då det har hög mortalitet och kräver intensivvård.

Generellt bör man beakta att SLE i sig medför en ökad risk för kliniska komplikationer.
Andra symtom som associerats med positiva aPL
Utöver de symtom som ingår i APS definitionen finns ett flertal tillstånd som år associerade med aPL och är förtydligade i de nya EULAR/ACR kriterierna (Tabell 8) (89).

Behandling
Rekommendationerna nedan bygger på EULARs behandlingsrekommendationer för primär och sekundär APS och för handläggning av familjeplanering, graviditet och menopaus vid SLE och APS (94, 22).
Primär trombosprofylax (aPL bärare)
- Undvik östrogeninnehållande p-piller och peroral östrogensubstitution. Vaginala beredningar/plåster kan övervägas men med försiktighet.
- Behandla och optimera övriga riskfaktorer: rökning, hypertoni, diabetes, hyperlipidemi.
- Ge lågmolekylärt heparin (LMH) profylax vid tillfälligt ökad risk (kirurgi, immobilisering):
Fragmin 5000IE s.c.×1 eller Innohep 4500IE s.c.×1 (justera dos vid vikt <50 kg eller>90 kg) - Till patienter med aPL av hög riskprofil (Tabell 7), rekommenderas lågdos ASA (ldASA, Trombyl® 75 mg×1), om det inte föreligger några kontraindikationer.
- Till patienter med låg risk aPL profil kan ldASA övervägas.
Sekundär trombosprofylax
- Patienter med SLE och APS bör få oral antikoagulation med warfarin. Terapeutiskt målintervall är INR 2.0–3.0. Grundregeln är livslång behandling.
- För vissa patienter med låg risk (Tabell 7) kan utsättning av antikoagulantia övervägas efter 3–6 månader.
- Direct Oral AntiCoagulants (DOAK) ska inte ges till APS patienter med hög riskprofil, pga. ökad risk för arteriella tromboser, fr.a. stroke, jämfört med warfarinbehanling (95). I enskilda fall efter att andra möjliga behandlingar uteslutits kan DOAK-behandling övervägas. Handläggning ska i dessa fall ske i samråd med erfaren koagulationsspecialist.
Vid trombosrecidiv med terapeutiskt INR (2.0–3.0) finns flera behandlingsalternativ, se nedan, men inget av dessa är evidensbaserat. Behandling bör ske i samråd med koagulationsspecialister.
1) Öka INR målintervallet till 3.0–4.0.
2) Tillägg av ldASA (Trombyl® 75 mg×1) till warfarin (INR 2.0–3.0)
3) Byte till LMH till exempel Inj. dalteparin (Fragmin®) 200 IE/kg×1 s.c, tinzaparin (Innohep®) 175 IE/kg×1 s.c. (justera dos vid nedsatt njurfunktion).
Behandling av CAPS
CAPS är ett akut, livshotande tillstånd som kräver snabbt, multiprofessionellt omhändertagande på intensivvårdsavdelning. Mortalitet har minskat från >50 % till ~30 % med kombinationsbehandling (96):
- Antikoagulation (iv heparin eller LMH)
- Kortikosteroider (iv Solu-Medrol pulsar och peroral Prednisolon i nedtrappning)
- Plasmaferes och/eller IVIG
- Fallrapporter visar effekt av rituximab och euclizumab (Soliris®) (.
Behandling vid graviditet
Alla kvinnor aPL-bärare ska följas i specialistmödravården under graviditeten. Det är angeläget med planering av graviditet till en period då SLE-sjukdomens aktivitet är lägsta möjliga.
Före graviditet
- Remiss till specialistmödravård för prekonceptionell rådgivning.
- HCQ och ldASA bör ges inför en planerad graviditet för att förebygga missfall.
- Warfarin är teratogent och ska ersättas av LMH i samband med planering av graviditet.
Under graviditet
- Om det inte är gjort innan graviditeten ska warfarin-behandling avslutas så snart positivt graviditetstest konstaterats.
- Behandling med HCQ, ldASA och LMH ska fortsätta under hela graviditeten. LMH doseras som högdos profylax till patienter med tidigare trombos eller högriskprofil, dvs. Inj. dalteparin (Fragmin®) 5000 E×2 s.c. (viktjusteras vid behov) eller Inj. tinzaparin 175E/kg s.c. (Innohep®), där en alltid mätbar koncentration av LMH eftersträvas. LMH-koncentration mäts som aktivitet för hämning av Faktor Xa, dvs. antifaktor Xa, den ska ligga mellan 0,1–0,2 IE/ml som dalvärde (före given dos). Dosjustering och kontroller sköts med fördel i samråd med specialistmödravården.
Vid behandlingsresistent APS med upprepade graviditetskomplikationer, trots behandling enligt ovan, kan tillägg med prednisolon 10 mg, intravenöst gammaglobulin (IvIg) och/eller plasmaferes övervägas.
Efter graviditeten
Fortsätt med LMH och ldASA i minst 6 veckor för att förebygga trombos hos kvinnan, alternativt gå tillbaka till warfarin i de fall detta är aktuellt.
Vid nytt insjuknande i trombos/lungemboli under graviditet:
Behandlingsdos med LMH (dalteparin 250 E/kg/kroppsvikt/dygn uppdelat på 2 doser), och för tizaparin 25 % högre behandlingsdos än till icke gravida patienter. En nivå av faktor Xa före Inj på 0,2–0,3 eftersträvas och 3 timmar efter injektion 0,6–1,0. Behandlingsdos pågår i minst 4 veckor och efter det kan dosen sänkas till en antifaktor Xa nivå på 0,1–0,2 för injektion (motsvarande profylax i högdos).
Behandlingsalternativ som saknar evidens vid APS, men som kan övervägas i vissa situationer
Direct Oral Anti Coagulants (DOAK)
Faktor Xa- (rivaroxaban, apixban, endoxaban) och trombinhämmare (dabigatran).
Studier har visat att risken för ffa. arteriella komplikationer, särskilt stroke, är stor hos patienter med APS som behandlas med DOAK. Det gäller särskilt patienter som är aPL trippelpositiva. DOAK bör därför inte ges till APS patienter (95).
Övriga preparat
Det finns nu många fallrapporter där man använt RTX framgångsrikt vid både primärt och sekundärt APS. Ofta har RTX använts i akuta CAPS-situationer, men det finns även rapporter om långtidsanvändning (97).
Några mindre studier har visat att statinbehandling minskar pro-inflammatoriska cytokiner och markörer för endotelaktivering i blodet hos patienter med APS. En mindre studie visade att pravastatin skyddade ”högrisk APS kvinnor” mot obstetriska komplikationer (98).
Det finns fallrapporter där C5a-hämmare, eculizumab (Soliris®) varit effektivt som behandling av refraktär CAPS samt vid trombotisk mikroangiopati, njurtransplantation och vid graviditet (99, ). Vid svår APS med rekurrenta trombosepisoder kan man överväga profylax med hydroxiklorokin (Plaquenil®).
Graviditet
Definitioner
Kvinnor med SLE har en ökad risk att drabbas av graviditetskomplikationer jämfört med friska kvinnor. Att föda för tidigt och att föda barn som är små för tiden är drygt dubbelt så vanligt vid SLE (100). Havandeskapsförgiftning kan debutera efter vecka 20, med hypertoni, proteinuri och huvudvärk och i svårare fall tecken till försämrad organfunktion. Risken att drabbas av havandeskapsförgiftning är ca tre gånger större vid SLE (100). Risken för missfall och intrauterin fosterdöd är också ökad jämfört med friska kvinnor (100). Kvinnor med SLE har under graviditeten också ökad risk att drabbas av arteriell och venös trombos (101).
Prognosen vid SLE-graviditet har dock förbättrats avsevärt med hjälp av prekonceptionell rådgivning och modern behandling, och de flesta kvinnor med SLE kan idag gå igenom en komplikationsfri graviditet (102).
Utredning inför graviditet
Önskemål om graviditet bör diskuteras ofta och tidigt, eftersom graviditetskomplikationer är vanligare vid oplanerade graviditeter jämfört med planerade (103). Med fördel efterfrågas graviditetsönskemål vid varje återbesök. Om kvinnan inte vill bli gravid kan preventivmedel diskuteras för att minska risken för en oplanerad graviditet. Preventivmedel bör också sättas in när behandling med potentiellt teratogena läkemedel som MTX och MMF startas.
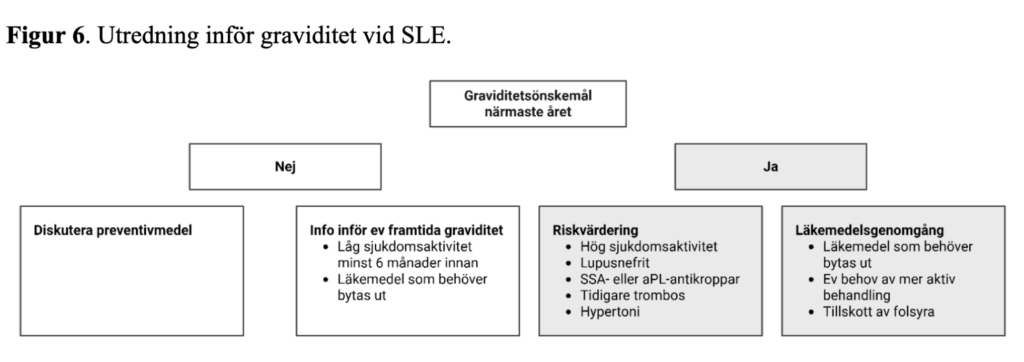
Vid önskemål om graviditet bör förekomst av sjukdomsrelaterade riskfaktorer utvärderas tidigt (Figur 6). I en prospektiv studie hade 8% av kvinnor utan starka riskfaktorer någon graviditetskomplikation jämfört med 58% av kvinnor med en eller flera starka riskfaktorer (104). En tydlig riskfaktor för utveckling av graviditetskomplikationer är hög sjukdomsaktivitet inför graviditet och vid befruktning (105). Ett riktmärke kan vara att sjukdomen ska vara lågaktiv, helst med behandling som fungerar vid graviditet, minst sex månader innan konception. Lupusnefrit och APS är andra starka riskfaktorer för graviditetskomplikationer (105). Detsamma gäller högrisk aPL-profil samt hypertoni, som får kontrolleras med läkemedel som är kompatibla med graviditet.
Om modern har anti-SSA-antikroppar kan de passivt föras över till fostret. Det kan orsaka neonatal lupus, som kan ge tillfälliga hudutslag, penier, förhöjda transaminaser och förstorad lever och mjälte. Den allvarligaste manifestationen är dock kongenitalt AV-block, som medför ökad dödlighet och ofta behov av pacemaker. Risken för komplett AV-block har beräknats till 2% om modern har antikroppar mot SSA (106), och ökar till 17% om ett syskon tidigare har drabbats (107). Kvinnor med känd förekomst av anti-SSA-antikroppar monitoreras ofta med ultraljud vid specialistmödravården för att möjliggöra tidig upptäckt.
Behandling innan graviditet
Kvinnor som inte önskar bli gravida bör uppmuntras att använda ett säkert preventivmedel. Kombinerad hormonell antikonception innehåller både östrogener och gestagener, och innebär en ökad risk för trombos. Kvinnor med SLE rekommenderas i första hand att undvika kombinerad hormonell antikonception. Gestagena metoder som minipiller och p-spruta, samt koppar- och hormonspiral, är säkrare val med avseende på trombosrisk. Dagen-efter-piller, som innehåller gestagen, går bra att använda vid SLE.
Vid önskemål om graviditet bör MTX sättas ut minst 3 månader innan konception och MMF minst 6 veckor innan konception (se även SRF:s riktlinjer för läkemedel vid graviditet och amning). Efter avslutad behandling med MTX bör folsyra i dosen 2,5 mg/dag intas under hela graviditeten. Cyklofosfamid är kontraindicerat under graviditet och bör avslutas 3 månader innan planerad graviditet.
Fertiliteten verkar inte påverkas av SLE-sjukdomen i sig, men läkemedel som CYK kan minska ovarialreserven. Även NSAID kan påverka fertiliteten och kan sättas ut vid svårighet att bli gravid. Assisterad reproduktion innebär en hormonell stimulering, men brukar anses genomförbart vid lågaktiv och välbehandlad sjukdom (22, 108).
Utredning under graviditet
Fysiologiska graviditetsförändringar som andfåddhet, trötthet och håravfall kan härma skov i SLE. Vid normal graviditet ökar den totala blodvolymen och det blir vanligare med anemi och trombocytopeni, ökad sänka och mild proteinuri. Kreatinin och albumin sjunker normalt under graviditeten. Komplementnivåer kan öka något under en graviditet, och kan te sig normala trots aktiv SLE.
Det kan vara svårt att skilja havandeskapsförgiftning från lupusnefrit, då båda kan orsaka proteinuri, hypertoni och försämrad njurfunktion. För faktorer som talar för SLE respektive havandeskapsförgiftning, se Tabell 9.

Monitorering och behandling under graviditet
Inför planerad graviditet erbjuds kvinnor med SLE och deras partner gärna ett prekonceptionellt besök hos Specialistmödravården. Uppföljning under graviditeten ska ske både hos Reumatolog och Specialistmödravård, i nära samarbete. Uppföljning hos reumatolog med provtagning en gång per trimester kan vara ett riktmärke, tätare vid behov.
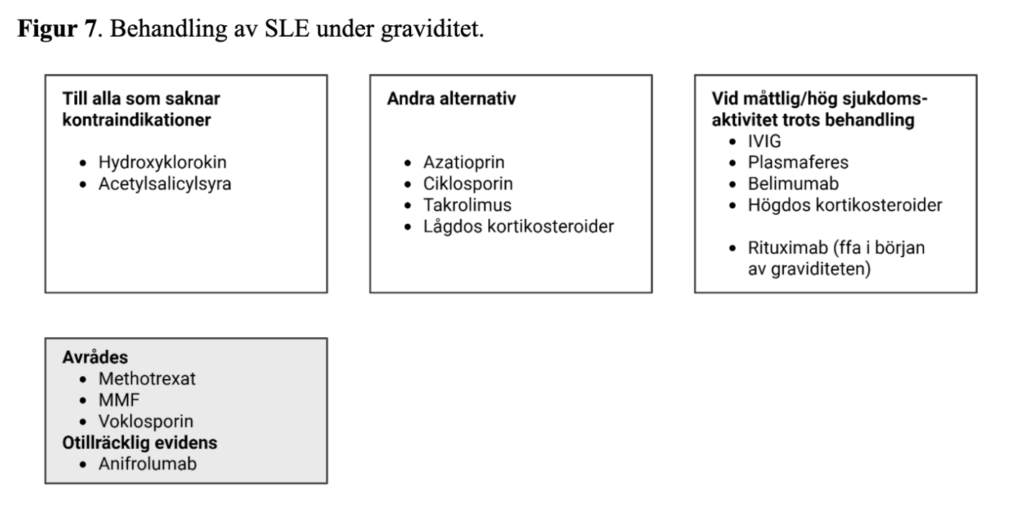
Sjukdomsaktiviteten ska hållas låg med läkemedel som är så säkra som möjligt under graviditeten (Figur 7). Patienten bör tidigt, gärna innan en planerad graviditet, vara införstådd med att en välbehandlad sjukdom är fördelaktigt för både henne och fostret. Precis som hos icke-gravida patienter med SLE styrs behandlingen av sjukdomens organengagemang och allvarlighetsgrad. Klorokin ska förskrivas om inte kontraindikationer finns, eftersom behandling minskar sjukdomsaktiviteten och förebygger skov och graviditetskomplikationer (109). AZA i doser ≤2 mg/kg/dygn kan läggas till vid kvarvarande sjukdomsaktivitet.
Andra immunosupprimerande läkemedel som kan användas under graviditet är CS och TAK. Vid måttlig eller hög sjukdomsaktivitet trots behandling är högdos glukokortikoider, IvIg och plasmaferes möjliga alternativ. Även om inget klart mönster av malformationer visats vid behandling med BEL under graviditet (110-112) så är kunskapsläget fortfarande begränsat. Behandling med BEL kan fortgå fram till påvisad graviditet, och om det behövs för att effektivt kontrollera moderns sjukdom kan fortsatt behandling under graviditeten också övervägas (se SRF:s riktlinjer för läkemedel vid graviditet och amning). Vid stark medicinsk indikation kan RTX övervägas, framför allt i början av graviditeten.
Vid behandling med kortikosteroider (KS) har samband rapporterats till för tidig födsel och preterm premature rupture of the membranes (PPROM), även vid lägre doser. Därför bör lägsta effektiva dos eftersträvas (113).
Lågdos ASA förskrivs rutinmässigt till kvinnor med SLE för att minska risken för havandeskapsförgiftning. Insatt tidigt i graviditeten till kvinnor med förhöjd risk för havandeskapsförgiftning minskar ASA risken för havandeskapsförgiftning, perinatal mortalitet, för tidig födsel och att föda ett barn som är litet för tiden (114, 115). Vid APS och förekomst av aPL kan behandling med LMWH bli aktuellt, se avsnittet om APS i detta dokument.
Förlossning, postpartum och amning
Spontan vaginal förlossning i fullgången tid brukar eftersträvas. Amning kan uppmuntras hos de flesta kvinnor med SLE som så önskar. Man bör då sträva efter att hålla sjukdomsaktiviteten låg med hjälp av läkemedel som är kompatibla med amning. Om det inte går får en individuell risk-nytta-bedömning göras, där det kan vägas in att prematura och sjuka spädbarn kan vara mer läkemedelskänsliga. Läkemedel som anses kompatibla med amning innefattar HCQ, AZA, CS, TAK, NSAID, IvIg, plasmaferes och kortikosteroider i doser <20 mg prednisolon-ekvivalent. Vid kortikosteroider ≥20 mg prednisolon-ekvivalent bör man vänta med amning 4 timmar efter intag. Postpartum är en period med ökad risk för skov, även om frekvensen varierar mellan olika studier. Därför är det fördelaktigt att redan under graviditeten diskutera amning och postpartum-perioden med patienten, och ungefär 6–10 veckor efter förlossningen kan patienten bedömas av reumatolog.
Läkemedel
Inledning
Endast prednisolon, AZA, klorokin, CYK, BEL, ANI och VOK har SLE som godkänd indikation enligt FASS. Trots att specifik indikation för SLE saknas används en lång rad andra läkemedel ändå. Nedan följer sammanfattningar av de läkemedel som är aktuella för behandling av SLE i Sverige, inkluderande användningsområde, biverkningar, verkningsmekanism och studier som är gjorda. Avseende säkerhetsprover hänvisas till SRF:s särskilda rekommendationer. Sviktande eller otillräcklig terapieffekt är vanligt och riskfaktorer för detta är hög sjukdomsaktivitet, neuropsykiatriska manifestationer, låg utbildning, bristande socialt stöd förutom klassiska riskfaktorer som polyfarmaci och många doseringstillfällen (116,117). Det är också angeläget att beakta möjligheten av bristande följsamhet (dvs. adherence) hos patienten.
Klorokin (hydroxiklorokin och klorokinfosfat)
Indikation
Båda substanserna har i tillägg till RA indikation systemisk och diskoid lupus erytematosus (FASS). HCQ har särskilt god effekt mot hud- och muskuloskeletala manifestationer men rekommenderas till alla patienter med SLE, om inte kontraindicerat, på grund av en rad långsiktiga positiva effekter bland annat på skovfrekvens, organskada och överlevnad (118).
Dosering
Med anledning av en gynnsammare biverkningsprofil rekommenderas i första hand HCQ framför klorokinfosfat. Startdosen av HCQ kan variera mellan 200 mg varannan dag till den vanligaste underhållsdosen som är 200 mg dagligen. Vid särskilt behandlingsresistent kutan lupus kan dosen under en period höjas till 400 mg dagligen. En dosering som understiger 5 mg/kg per dag anses gynnsamt avseende biverkningar. Koncentrationsbestämning av HCQ används inte i klinisk praxis, men kan övervägas vid terapisvikt eller misstänkt biverkan.
Biverkningar
De vanligaste biverkningarna utgörs av illamående, exantem och huvudvärk. Neurogen hörselnedsättning, mental påverkan (till exempel mardrömmar och psykos), myopati, arytmi och benmärgspåverkan är ovanliga biverkningar.
Risken för retinopati är störst för klorokinfosfat, men finns även för HCQ (efter >5 års exposition). Det finns riktlinjer för ögonkontroller utarbetade i samråd mellan SRF och Svenska Ögonläkarföreningen (var god se dessa riktlinjer). Klorokin bör undvikas vid misstankar om psoriasis, samt vid redan känd syn- eller hörselnedsättning. De gastrointestinala biverkningarna kan ibland reduceras genom att ge lägre dos under en period.
Verkningsmekanismer
HCQ ökar pH i lysosomer och minskar därigenom inflammation medierad via Toll-lika receptorer (TLR) 7 och 9 i antigenpresenterande celler. Detta medför att den interferonstimulerande effekten av DNA och RNA innehållande immunkomplex som tas upp av plasmacytoida dendritceller minskas.
Bakgrund/studier
Sedan klorokinbehandling introducerades på 50-talet i syfte att minska hud- och ledengagemang och att vara skovförebyggande har ett flertal studier kunnat belägga denna positiva effekt. I metaanalyser har man kunnat påvisa effekter även på lång sikt på minskad sjukdomsaktivitet, minskad organskada och förbättrad överlevnad (118, 119). Dessutom har man i samma studier sett positiva effekter av behandling med HCQ på blodfetter (sänker LDL) och på risken för trombos. Vid graviditet bör man fortsätta behandling med HCQ då risken för försämring i grundsjukdomen annars ökar, prognosen för lyckad graviditet ökar och dessutom finns det data som tyder på att HCQ kan skydda mot kongenitalt hjärtblock (120).
Kortikosteroider
Indikation
Prednisolon har indikation enligt FASS som ospecifik terapi vid exempelvis SLE. Kortikosteroider reducerar snabbt inflammation och används som akut behandling vid skov av SLE oavsett organmanifestation. De bör ges i lägsta möjliga dos under kortast möjliga tid tillsammans med mer specifik sjukdomsmodifierande behandling med målet att sätta ut kortikosteroiderna på sikt. För peroral behandling rekommenderas prednisolon och för intravenös behandling metylprednisolon.
Dosering
Dosering av kortikosteroider beror på sjukdomsaktivitet och vilket organ som primärt är engagerat. Vid milda skov med mukokutana eller muskuloskeletala symtom kan låga doser prednisolon ges (5–15 mg/dygn po). Vid medelsvåra skov med serosit eller hematologiska manifestationer ges medelhög dos prednisolon (20–30 mg/dygn po). Vid svåra skov med större inre organengagemang (t.ex. nefrit eller neuropsykiatriska manifestationer) kan metylprednisolon ges (0,5–1 g iv) under 3 dagar i följd som pulsterapi följt av lägre doser peroral terapi. Även vid medelsvåra skov kan pulsterapi med lägre doser metylprednisolon (0,125–0,25 g) ges följt av låga doser peroral terapi, då detta kan ge god antiinflammatorisk effekt med lägre totaldoser kortison.
När effekt erhållits reduceras dygnsdosen, hastigare vid högre doser, till fullständig utsättning eller minsta möjliga underhållsdos. Det är fördelaktigt att ge hela underhållsdosen på morgonen, eftersom prednisolon då verkar i takt med binjurebarkens naturliga dygnsrytm vilket minskar risken för binjurebarkshämning. Utsättning bör ske gradvis och ökad dos kan behöva ges vid feber, inför kirurgi och andra stresstillstånd.
Biverkningar
Behandling med kortikosteroider under längre tid ger svåra biverkningar som bidrar väsentligt till den organskada som uppstår vid SLE . Risken är ökad för bland annat diabetes, fetma, hypertoni, osteoporos, osteonekros, katarakt, glaukom, hudatrofi med blödningar och försämrad sårläkning, muskelatrofi, myopati, cushing-liknande symtom, aktivering av tidigare psykisk sjukdom och sömnsvårigheter (121,122145, 146). Infektionsförsvaret hämmas även av en låg dos kortikosteroider, med ökad risk för infektioner, och den egna ACTH- och kortisolutsöndringen hämmas (123). Vid behandling av barn och unga ska risken för tillväxthämning särskilt beaktas.
Enligt en studie var risken för Pneumocystisinfektion endast måttligt ökad vid SLE, även vid behandling med högdos kortikosteroider under längre tid (124). Då behandling med trimetoprim-sulfa ger en ökad förekomst av biverkningar, framför allt från huden, hos just patienter med SLE, rekommenderas inte rutinmässig profylax med detta preparat (125). Om omständigheter indikerar högre risk för Pneumocystis, som vid samtidig behandling med CYK och hög ålder, rekommenderas istället pentamidin-inhalationer eller atovakvon (oral suspension 150 mg/ml i dosering 5 mL x 2) som profylax.
Patienter som ska behandlas med daglig dos om minst 5 mg prednisolon i minst tre månader bör erhålla tillskott av kalk/vitamin D. DXA-mätning bör göras, och ofta ges också benspecifik behandling med bisfosfonater enligt lokala riktlinjer. Frakturrisken ökar omgående vid kortisonbehandling.
Verkningsmekanismer
Vid behandling med prednisolon i doser under 30 mg/dag beror de antiinflammatoriska effekterna av kortikosteroider på genomiska mekanismer. Steroiderna binder till kortikosteroid-receptorer i cytosolen och detta komplex inducerar eller undertrycker transkription av multipla gener. Vid behandling med kortikosteroider i högre doser uppstår även effekter som beror på icke genomiska mekanismer, sannolikt via kortikosteroidreceptorer i cellmembran och direkta effekter på cellmembranet. Dessa effekter uppstår inom minuter. Kortikosteroider har således en mycket bred effekt och påverkar ett flertal komponenter både i medfödda och i förvärvade immunsystemet och även i det metabola systemet.
Bakgrund/studier
Tidiga RCT både vid nefrit och neuropsykiatriska manifestationer har visat att månatliga pulsdoser med intravenöst metylprednisolon ger signifikant sämre behandlingseffekt än månatliga pulsdoser med intravenöst CYK (84). Kombinationen av metylprednisolon och CYK gav dock vid nefrit bättre långtidsresultat vad gäller njurfunktion jämfört med enbart CYK (126). Därmed ingår kortikosteroider i kombination med annan immunmodulerande behandling i senare RCTs vid SLE-nefrit. Behandling med medelhöga doser prednisolon har också visats kunna förebygga svåra skov hos patienter med kliniskt stabil SLE men med serologiska riskfaktorer i en liten RCT, men risken för långsiktiga biverkningar med organskada måste noga vägas mot nyttan (127).
I övrigt har behandling med kortikosteroider visat goda resultat vid mindre observationella icke kontrollerade studier vid flertalet organmanifestationer. Olika doseringar av kortikosteroider har använts i olika studier och kontrollerade jämförelser saknas. Evidens saknas även vad gäller dosering under nedtrappning och klinisk praktik varierar (128). En mindre observationsstudie indikerar dock att underhållsbehandling med kortikosteroider kan undvikas vid nefrit som behandlas med RTX och metylprednisolon för induktion och med MMF som underhållsbehandling (129). Således är evidens för användandet av kortikosteroider ej optimal, men det finns mycket stor erfarenhet och kortikosteroider har en viktig roll för behandling av skov i det akuta skedet.
Azatioprin (AZA)
Indikation
Vid sidan av sin användning som profylax mot transplantatavstötning kan AZA enligt FASS ge klinisk effekt hos en andel av patienter med SLE. I praktiken används AZA som remissionsbevarande behandling efter induktionsbehandling vid nefrit (54), och som steroidsparande läkemedel vid flera olika SLE-manifestationer.
Dosering
Vid SLE används AZA i regel med startdos 1–3 mg/kg kroppsvikt/dag. Dosen ska justeras i enlighet med terapisvar, vilket kanske inte är märkbart förrän efter flera veckor eller månader. Underhållsdosen ligger vanligtvis på 2-2,5 mg/kg kroppsvikt/dag och justeras i enlighet med kliniskt behov och hematologisk tolerans.
Genetiskt låg eller avsaknad aktivitet hos enzymet thiopurin S-metyltransferas (TPMT) kan orsaka ackumulering av AZA-metaboliter med hematologisk toxicitet som följd. Vid behandlingsstart kan utredning omfattande TPMT-enzymaktivitet och TPMT-genotypning övervägas för vägledning om behandling med AZA bör undvikas, inledas försiktigt eller ges med normal dosering (se också SRF:s riktlinje om provtagning och kontroller vid antireumatisk behandling). Tiopurin-metaboliter kan analyseras för att följa upp insatt behandling.
Biverkningar
Illamående är den vanligaste biverkningen vid användning av AZA. Risken för hematologisk påverkan med leukopeni och trombocytopeni motiverar regelbunden provtagning. Mindre vanliga biverkningar är hudtumörer, samt leverpåverkan som ibland kan ha snabbt förlopp. Resultat från svenska register indikerar att behandling med AZA till patienter med SLE ger en förhöjd risk för infektioner som kan kräva sjukhusvård (130).
Verkningsmekanismer
AZA absorberas från magtarmkanalen och bryts snabbt ner till bland annat 6-merkaptopurin (6-MP). Denna metaboliseras till 6-thioinosinsyra och vidare till 6-thioguaninnukleotider (6-TGN), vilka antas stå för preparatets immunosuppressiva och cytotoxiska effekt. Hos patienter som saknar det enzym som metaboliserar 6-MP till 6-thioinosinsyra har AZA ingen effekt.
Bakgrund/studier
För behandling med AZA vid renal SLE hänvisas till avsnittet om nefrit.
Avseende AZA för behandling av icke-renal SLE finns endast ett fåtal publikationer. I en kohortstudien ledde kombinationen av AZA och prednisolon till en betydande minskning av antalet skov jämfört med en föregående period med prednisolon, NSAIDs och/eller klorokin (131). I en icke-blindad RCT var den steroidsparande effekten liknande för AZA och CS (132).
Sammanfattningsvis föreligger begränsad evidens men god erfarenhet av att använda AZA vid icke-renal SLE, t.ex. vid manifestationer från hud och leder. Det gör att AZA har stor betydelse för patienter som behöver steroidsparande behandling.
Metotrexat (MTX)
Indikation
MTX har enligt FASS indikation aktiv RA hos vuxna, hudpsoriasis samt svår psoriasisartrit. Läkemedlet har således inte registrerad indikation för SLE, men har en dokumenterad effekt främst på manifestationer från hud och leder.
Dosering
MTX doseras på motsvarande sätt som vid RA, dvs. med veckodoser om 7,5–30 mg en gång/vecka peroralt eller subkutant.
Biverkningar
De vanligaste subjektiva biverkningarna är huvudvärk och illamående, vilka precis som leverpåverkan, kan motverkas med tillförsel av folsyra. Hematologisk påverkan med leukopeni och trombocytopeni förekommer mindre ofta, men motiverar monitorering.
Verkningsmekanismer
MTX är en folsyraantagonist men den anti-inflammatoriska effekten medieras via andra mekanismer såsom hämning av cytokinproduktion, påverkan på T-cellsfunktion och påverkan på adenosin-nivåer.
Bakgrund/studier
I en metaanalys kunde tre RCT och sex observationella studier identifieras (23) och det var huvudsakligen aktiva symptom från hud och leder som behandlades. En signifikant minskning av SLEDAI och kortikosteroider kunde ses i behandlingsgruppen jämfört med placebo (23).
Anifrolumab (ANI)
Indikation
Anifrolumab (ANI, Saphnelo®) har enligt FASS indikation som tilläggsbehandling hos vuxna patienter med måttlig till svår, aktiv, autoantikroppspositiv SLE, trots standardbehandling.
Dosering
Rekommenderad dos är 300 mg, administrerad som intravenös infusion under en 30-minutersperiod var fjärde vecka.
Biverkningar
De vanligaste biverkningarna är övre luftvägsinfektion, bronkit, infusionsrelaterade reaktioner och herpes zoster (133). I de 52 veckor långa kliniska studierna var incidensen av infektioner av herpes zoster 6,4 % i ANI-gruppen och 1,4 % i placebogruppen (21,134). Incidensen minskade därefter över tid i den 3-åriga förlängningsstudien. Under år 2–4 fick ANI-gruppen 3,4 och placebogruppen 2,8 herpes zoster infektioner per 100 patientår (135). Vaccination mot bältros rekommenderas därför vid behandling med ANI.
Verkningsmekanismer
ANI är en human monoklonal antikropp som binder till typ I interferonreceptorn (IFNAR1). Denna bindning internaliserar IFNAR1 och hämmar typ I IFN-signaleringen och således IFN-driven genexpression samt inflammatoriska och immunologiska processer nedströms. Typ I IFN har en central betydelse för patogenesen vid SLE (136, 137).
Bakgrund/studier
ANI utvärderades i tre randomiserade, dubbelblinda, placebokontrollerade multicenterstudier; en fas IIb studie (MUSE) (164) och två fas III studier (TULIP-1 och -2) (24, 134). De tre studierna inkluderade vuxna patienter av båda könen med måttlig till svår antikroppspositiv (ANA, anti-dsDNA eller anti-Sm) SLE med otillräckligt svar på standardbehandling. De flesta patienter hade engagemang av hud och leder.
I MUSE (n=305) utvärderades ANI 300 mg och 1000 mg iv var fjärde vecka (138). Det primära utfallsmåttet var SRI (4)-respons vid vecka 24. SRI (4) samt BICLA vid vecka 52 var sekundära effektmått. SRI (4) vid 24 veckor uppnåddes av 34 % (300 mg), 29 % (1000mg) och 18% (placebo), p=0,014 (300 mg/placebo) och p=0,063 (1000 mg/placebo). SRI (4) vid 52 veckor uppnåddes av 63 % (300 mg) och 40 % (placebo), p<0,001. BICLA-respons vid 52 veckor uppnåddes av 54 % (300 mg) och 26 % (placebo), p<0,001.
I TULIP-1 (n=457) utvärderades ANI 150 mg och 300 mg iv var fjärde vecka (134). Det primära utfallsmåttet var SRI (4) vid 52 veckor och ett sekundärt utfallsmått var BICLA vid 52 veckor. SRI (4) vid 52 veckor uppnåddes av 48 % (150 mg), 47 % (300 mg) och 43 % (placebo), p=0,45 (300 mg/placebo). BICLA-respons vid 52 veckor uppnåddes av 46 % (300 mg) och 30 % (placebo), p<0,001.
I TULIP-2 (n=362) utvärderades ANI 300 mg iv var fjärde vecka (24). Baserat på resultatanalyser från MUSE och TULIP-1 ändrades det primära utfallsmåttet för TULIP-2 från SRI (4) till BICLA vid 52 veckor. Ändringen gjordes medan data för TULIP-2 fortfarande var blindad. Resultatet visar att BICLA vid 52 veckor uppnåddes av 48 % (300 mg) och 32 % (placebo), p<0,001. SRI (4) vid 52 veckor uppnåddes av 56 % (300 mg) och 37 % (placebo), p<0,001.
Behandlingsrespons för ANI vid olika manifestationer av SLE har bl.a. studerats via sammanslagning av data från studierna TULIP-1 och -2 (39). Denna post-hoc analys inkluderade 360 patienter som fått ANI 300 mg och 360 patienter som fått placebo. Vid inklusion hade 89 % av patienterna muskuloskeletalt engagemang och 86 % mukokutant engagemang. Efter 52 veckor sågs en förbättring avseende muskuloskeletalt engagemang hos 56 % i gruppen som fått ANI och hos 44 % i gruppen som fått placebo, p=0,0025. Vidare sågs en signifikant förbättring avseende mukokutant engagemang hos 54 % i gruppen som fått ANI och hos 38 % som fått placebo, p<0,0001. Utöver detta observerades en förbättring av hematologiska manifestationer hos 56 % (ANI) mot 31 % (placebo), p=0,028 samt immunologiska manifestationer hos 19 % (ANI) mot 11 % (placebo), p=0,037. I denna post-hoc analys kunde patienter som fått ANI pga. artriter och hudengagemang reducera dosen kortison mer än patienter som fått placebo. Liknande resultat sågs i en annan post-hoc analys där andelen patienter i TULIP-1 och -2 som varaktigt kunnat reducera dosen prednisolon studerades (139). Denna studie inkluderade patienter som vid studiestart behandlades med ≥10 mg prednisolon (n=375) och visade att 51 % (ANI) och 32 % (placebo) kunnat reducera dosen prednisolon till ≤7,5 mg vecka 40 till 52, p<0,001.
En ”real life” studie från Danmark inkluderande 16 patienter som fått behandling med Anifrolumab visade reduktion av sjukdomsaktivitet inkluderande förbättring av hudengagemang, reduktion av kortisonbehandling och förbättring av patientrapporterad hälsa (140). Tani et al. visade att 80 % av patienterna som behandlats med ANI uppnådde LLDAS efter 6 månader, och att dosen kortison kunde reduceras signifikant (141). Ytterligare en studie har visat att patienter som behandlats med ANI + standardbehandling efter 4 år utvecklat färre organskador jämfört med en ”real-world” kontrollgrupp (142).
ANI har studerats i en fas II studie (TULIP-LN) inkluderande 147 patienter med SLE-nefrit klass III/IV ±V (143). Utöver MMF och kortison fick patienterna i denna studie antingen 300 mg ANI var fjärde vecka, 900 mg ANI var fjärde vecka 3 gånger följt av 300 mg var fjärde vecka eller placebo. Studien nådde inte sin primära endpoint, men numeriskt fler patienter som fick ANI (46 %) uppnådde komplett renal response jämfört med placebo (33 %) efter 52 veckor. Anifrolumab saknar idag indikation för SLE-nefrit. En fas III-studie med ANI vid SLE nefrit pågår.
Belimumab (BLM)
Indikation
BEL är enligt FASS godkänt som tilläggsbehandling hos vuxna med aktiv, autoantikroppspositiv SLE med hög sjukdomsaktivitet (t.ex. anti-dsDNA-positivitet, lågt komplement) trots standardterapi.
BEL är ett alternativ som kan övervägas som tillägg vid SLE-nefrit (se separat stycke) (60). BEL kan också vara ett alternativ vid medelsvår terapiresistent SLE, främst vid symptom från hud, slemhinnor och leder, och i viss mån hematologiska manifestationer.
I FASS-textens formulering kring behandlingsindikation anges exempel på sjukdomsaktivitet som positiva antikroppstest och lågt komplement. Det bör påpekas att behandlingsindikationerna primärt är kliniskt relevanta symptom, inte enbart laboratoriefynd, även om förekomst av serologisk aktivitet talar för behandling.
Dosering
Subkutan dosering är 200 mg/vecka oberoende av vikt, enligt FASS, men intravenös infusion ges i dosen 10 mg/kg. Iv-behandling inleds med 3 doser med två veckors mellanrum och därefter med intervallet 4 veckor.
Biverkningar
Inga betydelsefulla oväntade biverkningar har redovisats i de studier som anges ovan. Infusionsreaktioner, varav i några fall allvarliga, har rapporterats.
Verkningsmekanismer
BEL är en human monoklonal antikropp riktad mot B-lymfocytstimulator (BAFF/BLyS) vars effekter är centrala för B-cellers differentiering och aktivering. Genom blockad av lösligt BAFF/BLyS hämmas B-cellers förmåga till vidare differentiering till plasmaceller.
Bakgrund/studier
Två RCT, fas III-studier, med i princip samma upplägg, BLISS-52 (144) och BLISS-76 (25), är genomförda med positiva resultat vilket legat till grund för godkännande av detta läkemedel. Dokument finns fritt tillgängligt från flera av de granskningsprocesser dessa studier genomgått där man kan skapa sig en uppfattning om evidensstyrkan bl.a. från EMA.
I bägge RCT användes SLE-responder Index (SRI) vid 52 veckors behandling som primärt utfallsmått. För att klassas som SRI responder krävs att samtliga av följande kriterier uppnås: 1) = 4 poäng minskning av SLEDAI 2) Inga nya BILAG A och inte mer än 1 ny BILAG B domänscore 3) Ingen försämring av ”Physician’s Global Assessement”. Aktiv allvarlig SLE-nefrit, CNS-lupus och annan allvarlig SLE exkluderades. Bägge studierna uppnådde primär endpoint efter 52 veckor. I BLISS-52 uppnådde 57.6% i behandlingsgruppen SRI jämfört med 43.6% i placebogruppen (p=0.0006) medan 43.2% i behandlingsgruppen och 33.8% i placebogruppen uppnådde SRI i BLISS-76 studien (p=0.021). Flera sekundära effektvariabler har studerats, där man sett effekt på sänkning av dos kortikosteroider, tid till första skov, antalet allvarliga skov, liksom viktiga livskvalitetsvariabler såsom trötthet. Patienter med hög sjukdomsaktivitet (SLEDAI>10), höga doser kortikosteroider, förekomst av anti-dsDNA antikroppar i kombination med låga komplementnivåer har identifierats som de subgrupper som svarat bäst .
Det har också publicerats data vid SLE-nefrit där BEL som tillägg till standardbehandling gav signifikant bättre njurrespons jämfört med enbart standardbehandling (60). Dock uppnåddes statistisk signifikans enbart för den grupp som fått MMF och inte för de som erhöll CYK följt av AZA (60). I studien inkluderades patienter med duration av SLE-nefrit upp till 2 månader och även recidivnefriter kunde inkluderas. För rekommendationer avseende användning av BEL vid SLE-nefrit hänvisas till den sektionen.
Uppföljning och monitorering
Behandling start rekommenderas föregås av diskussion vid behandlingskonferens eller motsvarande lokal rutin. Utvärdering av respons måste ske av behandlande läkare på individuell bas. De responskriterier som använts i studierna är komplicerade, men delar av dessa är möjliga att registrera och följa i SRQ där alla patienter som startas på BEL ska registreras. Utifrån studierna som genomförts är det rimligt att förvänta signifikanta behandlingseffekter inom 6 månader. Utvärdering om fortsatt behandling eller ej bör därför sker efter 6–12 månader. Under första behandlingsåret bör läkarbesök ske minst var 3:e månad. Regelbunden provtagning med prover avsedda för monitorering av eventuella biverkningar liknande de som tas vid annan behandling med biologiska läkemedel rekommenderas.
Cyklofosfamid
Indikation
CYK är ett cytostatikum som är registrerat för användning vid ”särskilda fall av SLE” vilket i praktiken innebär att preparatet ges vid aktiv SLE med hotande förlust av funktionen hos vitala organ (CNS, hjärta, lungor, njurar och benmärg).
Dosering
Både peroral och intravenös terapi kan användas vid SLE men intravenös pulsbehandling är att föredra framför kontinuerlig tablettbehandling pga. klart mindre risk för biverkningar. Idag används ffa. den så kallade Euro-Lupus regimen. Ett undantag är NPSLE där högre doser ofta är motiverat. Euro-Lupus regimen innebär att 500 mg CYK ges iv varannan vecka i 3 månader (totalt 6 doser) tillsammans med kortikosteroider (57). Se bilaga D för detaljer.
Biverkningar
CYK har en omfattande lista med biverkningar, men kortsiktigt ger intravenös lågdosbehandling få problem. Vanligast är illamående. Vid långvarig behandling ses ökad risk för infektioner (bakterier, virus, svamp och protozoer), benmärgshämning, infertilitet och ökad incidens av maligniteter. Vid ffa. peroral behandling är hemorragisk cystit och blåscancer fruktade komplikationer. Ju äldre patienten är ju större är risken för permanent infertilitet och denna risk är dosberoende, vilket gäller för de flesta biverkningar av CYK. Risken för infertilitet gäller både män och kvinnor. Vid en kumulativ dos >23 g hos kvinnor som är äldre än 29 år sågs amenorré hos 100 % (). Behandling med GnRH-antagonist innan och under behandling med CYK har visats minska risken för amenorré (145). Kryopreservation av ovarialvävnad eller reproduktiva celler inför behandling med CYK till kvinnor som närmar sig menopaus kan övervägas (22). Yngre manliga patienter kan erbjudas nedfrysning av sperma före behandling med CYK.
Verkningsmekanismer
Preparatet är kemiskt besläktat med kvävesenapsgas och är en pro-drug som kräver bioaktivering av cytokrom P450 systemet för att farmakologiskt aktiva metaboliter ska bildas. Viktigast är fosforamidsenapsgas som ger alkylering av DNA vilket leder till brott av DNA-strängen. Detta hämmar både medfödd och förvärvad immunitet, men kan också förklara många av de biverkningar som ses vid långtidsanvändning av preparatet (till exempel benmärgshämning, infertilitet, ökad risk för malignitet).
Bakgrund/studier
Det finns ett mycket stort antal studier av patienter med SLE där CYK har administrerats på olika sätt i varierande doser. Ur den digra litteraturen kan man dra några klara slutsatser:
- CYK är som regel mycket effektivt vid aktiv SLE och detta läkemedel har medfört en klart förbättrad överlevnad för patienter med engagemang av vitala organ.
- Pulsbehandling är att föredra framför peroral terapi pga. klart mindre risk för biverkningar enligt vad som sagts ovan.
- Lågdosbehandling med CYK vid proliferativ SLE-nefrit har vid långtidsuppföljning inte visat sämre utfall än tidigare högdosregimer (57).
- CYK ska inte användas i remissionsbevarande syfte, dvs. som underhållsbehandling.
Mykofenolat mofetil (MMF) och natriummykofenolat
Indikation
MMF kan vara ett förstahandsval vid behandling av nefrit (se också detta avsnitt) eller som steroidsparare vid icke-renal SLE. Registrerad indikation enligt FASS: profylax mot transplantationsavstötning.
Dosering
MMF doseras vanligen 1–1,5 g×2 och motsvarande dos natriummykofenolat är 720 mg×2. Dosen kan justeras efter koncentrationsbestämning före och två gånger efter dos med påföljande beräkning av area under the curve (AUC) vilket kan bidra till bättre kontroll av sjukdomsaktiviteten (146), se lokala riktlinjer. Som underhållsdos vid långtidsbehandling kan dosen ibland trappas ned.
Biverkningar
Biverkningar innefattar ökad risk för infektioner (bakterier, virus, svamp och protozoer), leukopeni, trombocytopeni och anemi, gastrointestinala biverkningar, samt, i kombination med andra immunosuppressiva, ökad risk för hudmaligniteter och lymfom och ren erytrocytaplasi.
Verkningsmekanismer
MMF metaboliseras presystemiskt till den aktiva metaboliten mykofenolsyra (MPA) som selektivt hämmar inosin-monofosfat-dehydrogenas och hämmar därigenom nysyntesen av guanosin-nukleotid utan att införlivas i DNA. T- och B-celler kan till skillnad från andra celltyper inte använda alternativa syntesvägar vilket leder till en kraftigare cytostatisk effekt på lymfocyter än på andra celler. Både cellproliferationen och produktionen av antikroppar hämmas. Dessutom kan produktionen av IFN-α och IL-12 från dendritiska celler hämmas. Natriummykofenolat är natriumsaltet av den aktiva metaboliten MPA och har samma verkningsmekanism.
Bakgrund/studier
Randomiserade studier har visat att MMF är lika effektivt som intravenösa cyklofosfamid-pulsar vid induktionsbehandling av SLE-nefrit med färre biverkningar som alopeci och amenorré, och utan större skillnad vad gäller infektioner, leukopeni eller gastrointestinala biverkningar (56, 147). Den största studien visade bättre effekt av MMF, och i denna studie var en majoritet av patienterna afroamerikaner (147). En efteranalys av effekten på icke-renala manifestationer har visat att MMF hade likvärdig effekt som CYK iv, även vid mukokutana och muskuloskeletala manifestationer (148).
Två randomiserade kontrollerade studier har jämfört MMF med AZA som underhållsbehandling vid nefrit. Den studie som utfördes på patienter med kaukasiskt ursprung visade att MMF är ett likvärdigt alternativ till AZA vid underhållsbehandling av SLE-nefrit medan studien som utfördes på en majoritet icke-kaukasisk befolkning visade signifikant bättre underhållseffekt av MMF (54, 149). Slutligen har en randomiserad, kontrollerad öppen studie hos patienter med kaukasiskt ursprung visat att natriummykofenolat är mer effektivt än AZA för att inducera långvarig klinisk remission och förebygga skov hos patienter med aktiv icke-renal SLE (150). En longitudinell observationsstudie visade att 75 % av patienterna som behandlades med MMF vid artrit kvarstod på behandling efter 5 år vilket stödjer god klinisk effekt vid denna manifestation (151).
Ciklosporin (CS)
Indikation
Ciklosporin (CS) saknar registrerad SLE-indikation för SLE, men har indikation: steroidberoende nefrotiskt syndrom, aktiv RA, psoriasis och atopisk dermatit. CS kan dock i särskilda fall även ha en plats i behandlingsarsenalenövervägas vid icke-renal SLE.
Dosering
Vid icke-renal SLE används CS oftast i doser motsvarande 2–3 mg/kg kroppsvikt/dag.
Biverkningar
De vanligaste biverkningarna vid användning av CS utgörs av nedsatt njurfunktion, cytopenier, tremor, hirsutism, hypertoni, diarré, anorexi, illamående och kräkningar.
Verkningsmekanismer
CS består av en cyklisk polypeptid innehållande 11 aminosyror som hämmar utveckling av cellmedierade reaktioner, och T-cellsberoende antikroppsbildning. CS hämmaroch produktion och frisättning av cytokiner, inklusive IL-2, och förefaller CS tros blockera vilande lymfocyter i G0- eller tidig G1-fas i cellcykeln. CS och gerhar en specifik och reversibel verkan på lymfocyter. Till skillnad från cytostatika hämmas inte hematopoesen eller fagocytfunktionen.
Bakgrund/studier
Evidensen för CS vid icke renal SLE är begränsad. Den baseras på två blindade RCT, varav en prospektiv ’open label’-karaktär, och fem kohortstudier som totalt inkluderat 319 patienter. I ’open label’-studien undersöktes effekten av CS (2,5–5 mg/kg kroppsvikt/dag) hos 16 patienter med aktiv icke-renal SLE under en genomsnittlig behandlingstid av drygt 30 månader (152). European Consensus Lupus Activity Measurement (ECLAM) score minskade signifikant (p<0.005) efter 6 månader, men inte i slutet av observationstiden. De vanligaste biverkningarna utgjordes av hypertoni och försämrad njurfunktion (3/16 patienter). CS förefaller ha en jämförbar steroidsparande effekt som AZA, men säkerhetsprofilen är mindre fördelaktig (153).
CS kan utgöra ett behandlingsalternativ under graviditet, men kontinuerlig monitorering av bl.a. njurfunktion och blodtryck är viktig (154).
För behandling med CS av renal SLE hänvisas till avsnittet om nefrit.
Takrolimus (TAK)
Indikation
TAK har indikationen profylax mot transplantatavstötning och saknar registrerad indikation för SLE. I vissa fall av framförallt renal, SLE kan dock TAK utgöra ett alternativ i behandlingsarsenalen.
Dosering
Doseringen är individuell, vanligen 0,05 mg/kg/dag initialt, dosen justeras sedan efter koncentrationsbestämning (varje vecka första månaden vilket sedan glesas ut, se SRF:s Riktlinjer för provtagning och kontroller vid antireumatisk behandling).
Vid nefrit föreslås en låg initialdos 1 mg x 2 vilket sedan dosjusteras efter konc.bestämningar enligt ovan.
Biverkningar
De vanligaste biverkningarna vid användning av TAK utgörs av nedsatt njurfunktion, hypertoni, tremor, huvudvärk, illamående, diarré samt cytopenier.
Verkningsmekanismer
TAK har endast delvis kända effekter på immunsystemet. Verkningsmekanismen för TAK medieras via bindning till ett cytosoliskt protein (FKBP12), vilket också svarar för den intracellulära ackumuleringen av substansen. Komplexet mellan FKBP12 och TAK binds specifikt och kompetetivt till (samt hämmar) kalcineurin vilket leder till en kalciumberoende hämning av T-cellsmedierade reaktioner och hindrar därmed transkriptionen av ett antal interleukin-gener. Särskilt hämmas bildningen av cytotoxiska lymfocyter, som huvudsakligen orsakar avstötning av transplantat. TAK undertrycker aktiveringen av T-lymfocyter och T-hjälparcell-beroende proliferation av B-celler, liksom bildningen av IL-2, IL-3 och IFN-γ samt uttryck av IL-2 receptorn.
Bakgrund/studier
Ett fåtal studier har utvärderat effekt och/eller säkerhet av TAK i behandlingen av icke-renal SLE. I en prospektiv ”open-label”-kohortstudie över 24 veckor behandlades 21 patienter med olika typer av inflammatorisk systemsjukdom (varav 2 hade icke-renal SLE med måttlig aktivitet) med TAK (2–4 mg/dag). Medel-SLEDAI minskade signifikant vid 24 veckor (p <0.01). I 8 fall avbröts behandlingen inom 24 veckor på grund av bristande effekt (6 fall) och biverkningar (2 fall) (155).
I en”open-label” RCT jämfördes effekten av TAK med MMF för såväl induktions- som underhållsbehandling hos SLE-patienter med aktiv nefrit, även effekter på extrarenal sjukdomsaktivitet SLE studerades. Viss effekt på sjukdomsaktivitet noterades för TAK initialt men vid 1-årsuppföljningen hade endast MMF-gruppen en signifikant lägre extrarenal sjukdomsaktivitet jämfört med baseline (156).
Sammanfattningsvis saknas evidens för att använda TAK vid icke-renal SLE. En relativt stor andel patienter har i studierna tvingats avbryta behandling med TAK på grund av en bristande effekt eller biverkningar.
För behandling med TAK av renal SLE hänvisas till avsnittet om nefrit.
Voklosporin (VOK)
Indikation
Voklosporin (Lupkynis®) är registrerad för behandling av lupusnefrit. Indikationen enligt FASS är behandling av vuxna patienter med aktiv SLE-nefrit av klass III, IV eller V (inklusive blandad klass III/V och IV/V) i kombination med MMF.
Dosering
VOK ges som tablett i fast dos om 23,7 mg 2 gånger dagligen (tre kapslar à 7,9 mg x 2).
Biverkningar
De vanligaste rapporterade biverkningarna är infektioner i övre luftvägar, anemi, huvudvärk, hypertoni, hosta, diarré och buksmärta. De fyra första veckornas behandling är det vanligt med hemodynamisk minskning av eGFR, vilket sedan stabiliseras vid fortsatt behandling.
Verkningsmekanismer
VOK är en calcineurininhibitor och immunosuppressor. Kalcineurin är ett kalcium/kalmodulin-beroende fosfatas vars aktivitet är nödvändig för igångsättningen av T-cellernas lymfokinproduktion och tillväxt. Den immunhämmande aktiviteten medför en hämning av lymfocytproliferationen, T-cellernas cytokinproduktion liksom uttrycket av T-cellsaktiverande ytantigener. VOK har även en stabiliserande effekt på podocyter och har en relativt snabbt insättande effekt med minskning av proteinurigraden. VOK kräver inte koncentrationsbestämningar och har en mer gynnsam effekt på lipider och glukoskoncentrationer jämfört med andra calcineurininhibitorer
Bakgrund/studier
Godkännandet av VOK utgår från AURORA-I (61) där man studerat effekten av MMF + VOK på biopsiverifierad LN klass III, IV och V (eller kombinationer av klasser) i jämförelse med placebo tillsammans med MMF och med snabb nertrappning av steroider. Effekterna utvärderades efter 52 veckor där andelen patienter som uppnått en komplett renal respons jämfördes med placebo.
Studien visade att patienter i VOK-gruppen uppnådde en signifikant ökad andel med komplett renal respons jämfört med placebogruppen (73 [41%] av 179 patienter vs 40 [23%] av 178 patienter; OR 2.65; 95% CI 1.64–4.27; p <0,0001 (18% skillnad). Övriga kombinerade utfallsmått avseende på komplett renal response var vanligare i VOK-grupppen men bara statistiskt signifikanta i gruppen med U-PCR på 0·5 mg/mg eller mindre. VOK påverkade inte den serologiska aktiviteten (anti-dsDNA/komplementkonsumtion).
I den uppföljande placebokontrollerade studien AURORA 2 studerades långtidseffekter (3-årsdata) av VOK i kombination med MMF och lågdossteroider där >80% av patienterna från AURORA-1 studien inkluderades (62). Man rapporterade förbättring avseende proteinuri och en ökad förekomst av komplett renal respons i VOK-gruppen jämfört med placebo (50,9% vs 39,0%; odds ratio 1.74; 95% CI 1.00–3.03). Dock hade VOK-gruppen lägre grad av proteinuri redan vid studiestart jämfört med placebogruppen. Det var ingen skillnad i njurskov mellan grupperna men ca 25% av patienterna hade nya njurskov under behandlingstiden. Vid studiens slut var biverkningsprofilen i de två behandlingsgrupperna likartad och några nya säkerhetssignaler noterades ej. För behandling med VOK hänvisas även till avsnittet om nefrit.
Obinutuzumab (OBI)
Indikation
OBI har indikation för behandling av kronisk lymfatisk leukemi samt follikulärt lymfom. Registrerad indikation för SLE saknas i Sverige men är sedan oktober 2025 godkänd av FDA för behandling av aktiv lupusnefrit hos vuxna.
I Sverige har OBI dock använts sedan flera år, framför allt vid svårbehandlad nefrit med intolerans mot RTX pga utveckling av antikroppar (se avsnitt RTX under biverkningar).
Dosering
Doseringen är vanligen 1000 mg x 2 givet med 2 veckors mellanrum. Premedicinering ska ges med paracetamol, antihistamin samt kortikosteroider enligt lokala PM, se RTX. Återbehandling kan ske tidigast efter 6 månader efter individuell bedömning.
I studien som legat till grund för FDA:s godkännande gavs OBI (i kombination med MMF) 1000 mg x 2 med 2 veckors mellanrum initialt, med återbehandling (1000 mg x2) efter 6 månader samt därefter ytterligare en dos (1000 mg x 1) 12 månader efter första dosen. Det finns inte studier med data för återbehandling efter vecka 52 (65).
Biverkningar
I REGENCY studien var den vanligaste biverkan infektioner (inkluderande covid-19 samt covid-19 relaterad svår sjukdom, urinvägs- och luftvägsinfektioner). Studien pågick under covidpandemin, vilket sannolikt påverkat både förekomst och grad av covidrelaterade biverkningar. I övrigt var de vanligast förekommande biverkningarna infusionsreaktioner och neutropeni (65). I FASS-texten om OBI vid behandling av hematologisk sjukdom står som mycket vanliga biverkningar infektioner (bland annat ÖLI, UVI, sinuit, pneumoni och HZV) samt som mindre vanlig biverkan reaktivering av hepatit-B. Som mycket vanliga eller vanliga biverkningar står även bland annat infusionsreaktioner, allmänna symtom (såsom trötthet, ledvärk, huvudvärk och sömnsvårigheter), anemi, leukopeni/neutropeni samt ökad förekomst av skivepitelcancer. Dessutom beskrivs fall av arytmier samt andra kardiovaskulära händelser framförallt hos personer med redan existerande hjärtsjukdom. Observera dock att FASS-texten baseras på behandling av patienter med hematologisk malignitet, inte SLE.
Verkningsmekanism
OBI är en monoklonal humaniserad och glykomodifierad anti-CD20-antikropp. OBI är riktad mot CD20 vilken uttrycks på olika B-cellspopulationer, och har visats ge högre grad av B-cellsdepletion än RTX (65,157). Glykomodifieringen av OBI medför högre grad av direkt påverkan på B-celler med åtföljande celldöd, ökad Fc-receptor-medierad B-cells toxicitet och även ökad antikroppsmedierad fagocytos än RTX. Studier har, förutom höggradig B-cellsdepletion i cirkulationen, även visat depletion av B-celler i vävnad.
Bakgrund/studier
OBI som tillägg till standardbehandling med MMF har i två stora studier visat signifikant bättre behandlingssvar än placebo vid SLE-nefrit (64, 65). NOBILITY, en fas 2 randomiserad och placebokontrollerad studie av LN, visade en högre andel komplett respons vecka 52, 76 och 104 i gruppen som fått MMF+OBI jämfört med MMF+placebo (64). Post hoc analyser visade även längre tid till nytt nefritskov, samt lägre risk för försämrad njurfunktion och död.
I fas 3 studien REGENCY randomiserades 271 patienter med biopsiverifierad aktiv nefrit klass III eller IV +/- klass V till behandling med OBI eller placebo som tillägg till MMF och kortison (med måldos prednisolon 5 mg vecka 24) (65). 135 patienter erhöll OBI. Primary endpoint var complete renal response vecka 76, definierat som U-P/C <0,5 samt GFR inom 85% från baseline (utan behov av annan tilläggsbehandling, tidigt avbrytande av studien eller död). Secondary endpoint var komplett respons med prednisolondos 7,5 mg eller lägre vecka 64–72. Signifikant fler patienter i OBI-gruppen nådde komplett respons vecka 76 (46,4%) jämfört med i placebogruppen (33,1 %), och fler nådde även secondary endpoint (42,7 vs. 30,9 %. Störst skillnad mellan behandlings- och placebogrupp sågs hos patienter med hög sjukdomsaktivitet (proteinuri >3 g, högt anti-dsDNA, lågt C3, C4 samt nefrit klass IV och/eller III/VI +V (65).
Rituximab (RTX)
Indikation
RTX kan vara ett behandlingsalternativ vid svår och refraktär SLE där störst erfarenhet finns vid behandling av nefrit. RTX kan även övervägas vid svåra hematologiska-och CNS-manifestationer, men har idag ingen plats vid mild till moderat sjukdomsbild. Data kring återbehandling med RTX är begränsade.
RTX är idag registrerat för RA, granulomatos polyangit, mikroskopisk polyangit, non-Hodgkin lymfom och kronisk lymfatisk leukemi. Registrerad indikation för SLE saknas enligt FASS. Sedan 2018 finns flera RTX-biosimilarer på den svenska marknaden.
Dosering
Inget standardiserat behandlingsprotokoll finns vid behandling med RTX vid SLE. Det mest använda protokollet är 1g×2 givet med 2 veckors mellanrum. Så kallat ”lymfomprotokoll” där man ger RTX i en dos på 375 mg/m2 en gång per vecka i 4 veckor används i vissa fall.
Kunskapsläget är ofullständigt avseende samtidig användning av CYK eller annan DMARD, men samtidigt användande av MMF har inte visat ökad biverkningsrisk (66). Premedicinering med antihistamin, paracetamol och steroider används oftast före infusion (se lokala PM). Patienter rekommenderas om möjligt vaccineras mot pneumokocker, covid och influensa före behandlingsstart med RTX (se SRF:s riktlinjer för vaccination av patienter med inflammatoriska reumatiska sjukdomar).
Biverkningar
Infusionsrelaterade biverkningar är vanligast. Fall av reaktivering av hepatit B och JC-virusreaktivering/progressiv multifokal encefalopati (PML) finns rapporterade. Utveckling av sent uppträdande leukopeni (late onset neutropenia) har visats efter behandling vid SLE (158) och observans på neutrofilnivåer bör beaktas hos RTX-behandlade patienter. Antikroppsutveckling mot RTX har rapporterats i relativt hög frekvens (37%), ffa hos yngre patienter med aktiv sjukdom och nefrit, men eventuella kliniska konsekvenser är i övrigt okända (159,160). Uppkomst av infusionsreaktioner och serum sickness kan förekomma hos antikroppspositiva individer. Samtidig behandling med högdos steroider eller CYK har inte visat minskad uppkomst av antikroppsutveckling mot RTX (190). Hypogammaglobulinemi kan uppträda efter behandling med RTX och Ig-nivåer bör monitoreras innan återbehandling.
Verkningsmekanismer
RTX är en monoklonal antikropp riktad mot CD20 som uttrycks på olika B-cellspopulationer. Behandlingen ges intravenöst och medför att CD20-uttryckande B-celler elimineras ur cirkulationen under en varierande tidsperiod, vanligen cirka 6 månader.
Bakgrund/studier
Två stora randomiserade kontrollerade studier (RCTs) har hittills publicerats kring effekter av RTX vid SLE. I EXPLORER-studien utvärderades effekter av RTX vid svår till medelsvår icke-renal SLE (161. LUNAR-studien rapporterade effekter av RTX vid renal SLE (ISN/RPS klass III/IV) (66). Ingen av studierna kunde visa bättre effekt av RTX jämfört med placebo (MMF i LUNAR och MMF/MTX/AZA i EXPLORER) och RTX är därför idag inte registrerat för behandling av SLE.
Orsakerna till de negativa resultaten av studierna har varit föremål för debatt och kritik har riktats mot studieuppläggen med avseende på parallell terapi, uppföljningstiden och hur endpoints definierades.
I de randomiserade kontrollerade studierna har RTX använts i kombination med annan DMARD samt steroider i nedtrappande dosering. RTX har givits i initial dos av 1g×2 givet med 2 veckor mellanrum. Återbehandling utfördes vid 24 veckor i samma dosering. Ingen ökad säkerhetsrisk noterades vid kombination RTX med DMARD jämfört med DMARD i monoterapi (66).
Trots att RCTs inte visat effekt vid SLE har terapin kommit till allt större användande vid terapirefraktär SLE, och data från observationsstudier och registerstudier (162, 163191-194) har kunnat påvisa gynnsam effekt.
Störst erfarenhet av RTX-terapi finns vid SLE med njurengagemang där data på över 400 patienter finns publicerade och där 67–77% av patienterna uppnått komplett eller partiell respons (164). Vid hematologiska manifestationer finns data vid hemolys och trombocytopeni med goda resultat, men kontrollerade studier saknas. Begränsade observationella data finns vid NPSLE (163).
Trots avsaknad av evidens i RCTs kan RTX vara ett behandlingsalternativ givet som monoterapi eller i kombinationsterapi med av MMF eller CYK vid SLE-nefrit klass III–IV ± klass V med nefros. I riktlinjer omnämns RTX fortfarande som ett behandlingsalternativ vid utebliven effekt eller försämrad bild vid 6 månaders uppföljning eller vid terapisvikt på MMF och CYK (8, 50). Studier kring återbehandling eller underhållsbehandling med RTX utgörs idag av fallrapporter och fall-serier och har hittills inte medfört någon indikation för säkerhetsrisker.
Övriga biologiska preparat och JAK-hämmare
En metaanalys har rapporterat data från 10 randomiserade studier och 20 fallrapporter som inkluderade 2460 SLE patienter behandlade med olika JAK-hämmare. Resultaten tyder på bättre effekt av JAK-hämmare jämfört med placebo för behandling av muskuloskeletala manifestationer. JAK-hämmare och placebo hade liknande incidens av biverkningar (165). Baserat på tillgängliga data från patienter med RA bör riskfaktorer för trombos och malignitet beaktas före användning av JAK-hämmare hos patienter med SLE. Med nuvarande kunskap bör JAK-hämmare undvikas hos patienter med APS.
Infliximab, tocilizumab, abatacept, anakinra och sekukinumab har givits till patienter med SLE, men inget av preparaten har uppvisat en klinisk effekt som gör att de i nuläget kan rekommenderas vid SLE annat än inom ramen för kliniska prövningar. TNF-blockad har visserligen haft en god effekt vid korttidsbehandling av SLE-nefrit, men långsiktigt har allvarliga biverkningar noterats (166). Det finns även resultat från fas-2 prövning med ustekinumab, vilken som visade viss effekt på sjukdomsaktivitet på icke-allvarlig SLE (167). En fas 2-prövning med deucravacitinib, en selektiv TYK-2 hämmare, som involverade 363 SLE patienter med aktiv sjukdom, påvisade minskning av sjukdomsaktivitet i flera domäner jämfört med placebo, med en acceptabel säkerhetsprofil (168).
Intravenöst immunoglobulin (IvIg)
Indikation
Intravenöst immunoglobulin (IvIg) används vid immunmedierad trombocytopeni och autoimmun hemolytisk anemi samt vid svåra former av APS.
Indikation enligt FASS: Primär immuncytotrombocytopeni (ITP), hypogammaglobulinemi med infektionsbenägenhet, Kawasakis sjukdom och Guillain-Barré syndrom, multifokal motorisk neuropati.
Dosering
Vid autoimmun trombocytopeni och autoimmun hemolytisk anemi ges IvIg antingen som 1000 mg/kg intravenöst som upprepas en gång inom 3 dagar eller 400 mg/kg intravenöst dagligen under 3–5 dagar.
Biverkningar
Biverkningar är överkänslighetsreaktioner, huvudvärk, illamående, feber, trötthet och reaktioner vid infusionsstället. Reaktionerna brukar vara relaterade till dos och infusionshastighet.
Verkningsmekanismer
IvIg har föreslagits modulera B-celler på ett flertal olika sätt. Patogena autoantikroppar kan neutraliseras av anti-idiotypa antikroppar i IvIg, immunkomplex av IgG kan binda till den inhibitoriska receptorn FcγRIIB som nedreglerar den aktiverande signalen via B-cells receptorer, Fc-receptorer på fagocyter kan blockeras (169), och IvIg kan påverka B-cellernas intracellulära signalering så att ett tillstånd av reversibel anergi uppstår (170).
Bakgrund/studier
IvIg visades initialt kunna öka antalet trombocyter vid idiopatisk trombocytopen purpura. Därefter har effekt visats vid immunmedierad trombocytopeni associerad med SLE, autoimmun hemolytisk anemi i samband med SLE och vissa svåra former av APS. Kan ges vid graviditet och vara till fördel vid samtidig infektion (171). IvIg var dock också associerat med både ökad trombosrisk och försämrad njurfunktion, särskilt hos äldre patienter (172) som måste tas i beaktandet vid behandlingsval.
Stamcellstransplantation
Stamcellstransplantation har provats vid svår terapiresistent SLE, men randomiserade kontrollerade studier saknas. Erfarenheter av stamcellstransplantation i Sverige är mycket begränsade, och idag finns många andra behandlingsalternativ vid svår terapirefraktär SLE.
Verkningsmekanismerna vid autolog stamcellstransplantation tros primärt inte utgå från transplantationen i sig utan snarare från den tunga immunosuppressiva terapi som ges före transplantationen och som eliminerar autoreaktiva lymfocyter, sänker eller tar bort autoantikroppar och möjliggör en rekonstitution av immunsystemet (173).
Behandlingen bör utföras vid centra med erfarenhet av både stamcellstransplantation och SLE i nära samarbete mellan berörda specialister. Stamcellstransplantation bör främst övervägas till patienter med ökad mortalitetsrisk från SLE, är refraktära till konventionell terapi och utföras före det att svåra organskador uppstått (174).
CAR-T celler behandling
CAR T celler diskuteras som möjlig behandling vid svår SLE, och fallrapporter har visat goda resultat (175). Större studier saknas i nuläget, och behandling sker inom ramen för kliniska studier.
Non-Steroidal Anti-Inflammatory Drugs (NSAID)
Non-Steroidal Anti-Inflammatory Drugs (NSAID) är inhibitorer av cyklooxygenas Cox-1 och Cox-2. De flesta NSAID preparat är icke selektiva COX hämmare eller har en profil med mer COX-1 hämning och några är selektiva Cox-2 hämmare med mindre påverkan på trombocyter.
Inga större kontrollerade studier där effekt specifikt studerats vid SLE har gjorts, men biverkningar är däremot mer studerat. Denna grupp av läkemedel kan ha en plats vid ej allvarlig SLE där man kan få effekt på muskuloskeletala symptom och serositer. Med tanke på biverkningsprofilen generellt för NSAID med ökad risk för kardiovaskulära händelser, njurpåverkan, hypertension kan dock NSAID vid mer allvarlig SLE vara olämpligt, och just dessa möjliga biverkningar bör särskilt uppmärksammas. Ett samband mellan NSAID, särskilt ibuprofen, och aseptisk meningit vid SLE och andra autoimmuna sjukdomar är beskrivet hos ett litet antal fall (176).
Referenser
Referenser
- Fries JF, Holman HR. Systemic lupus erythematosus: a clinical analysis. Major Probl Intern Med. 1975;6:v-199.
- Aringer M, Costenbader K, Daikh D, Brinks R, Mosca M, Ramsey-Goldman R, et al. 2019 European League Against Rheumatism/American College of Rheumatology Classification Criteria for Systemic Lupus Erythematosus. Arthritis Rheumatol. 2019;71(9):1400-12.
- Tan EM, Cohen AS, Fries JF, Masi AT, McShane DJ, Rothfield NF, et al. The 1982 revised criteria for the classification of systemic lupus erythematosus. Arthritis Rheum. 1982;25(11):1271-7.
- Hochberg MC. Updating the American College of Rheumatology revised criteria for the classification of systemic lupus erythematosus. Arthritis Rheum. 1997;40(9):1725.
- Petri M, Orbai AM, Alarcon GS, Gordon C, Merrill JT, Fortin PR, et al. Derivation and validation of the Systemic Lupus International Collaborating Clinics classification criteria for systemic lupus erythematosus. Arthritis Rheum. 2012;64(8):2677-86.
- Gladman DD, Ibanez D, Urowitz MB. Systemic lupus erythematosus disease activity index 2000. J Rheumatol. 2002;29(2):288-91.
- Bruce IN, O’Keeffe AG, Farewell V, Hanly JG, Manzi S, Su L, et al. Factors associated with damage accrual in patients with systemic lupus erythematosus: results from the Systemic Lupus International Collaborating Clinics (SLICC) Inception Cohort. Ann Rheum Dis. 2015;74(9):1706-13.
- Sammaritano LR, Askanase A, Bermas BL, Dall’Era M, Duarte-Garcia A, Hiraki LT, et al. 2025 American College of Rheumatology (ACR) Guideline for the Treatment of Systemic Lupus Erythematosus. Arthritis Rheumatol. 2025.
- Parra Sanchez AR, van Vollenhoven RF, Morand EF, Bruce IN, Kandane-Rathnayake R, Weiss G, et al. Targeting DORIS Remission and LLDAS in SLE: A Review. Rheumatol Ther. 2023;10(6):1459-77.
- Franklyn K, Lau CS, Navarra SV, Louthrenoo W, Lateef A, Hamijoyo L, et al. Definition and initial validation of a Lupus Low Disease Activity State (LLDAS). Ann Rheum Dis. 2016;75(9):1615-21.
- van Vollenhoven RF, Bertsias G, Doria A, Isenberg D, Morand E, Petri MA, et al. 2021 DORIS definition of remission in SLE: final recommendations from an international task force. Lupus Sci Med. 2021;8(1).
- Svenungsson E, Gunnarsson I, Illescas-Backelin V, Trysberg E, Jonsen A, Leonard D, et al. Quick Systemic Lupus Activity Questionnaire (Q-SLAQ): a simplified version of SLAQ for patient-reported disease activity. Lupus Sci Med. 2021;8(1).
- Nived O, Jonsen A, Bengtsson AA, Bengtsson C, Sturfelt G. High predictive value of the Systemic Lupus International Collaborating Clinics/American College of Rheumatology damage index for survival in systemic lupus erythematosus. J Rheumatol. 2002;29(7):1398-400.
- Rahman P, Gladman DD, Urowitz MB, Hallett D, Tam LS. Early damage as measured by the SLICC/ACR damage index is a predictor of mortality in systemic lupus erythematosus. Lupus. 2001;10(2):93-6.
- Fanouriakis A, Kostopoulou M, Andersen J, Aringer M, Arnaud L, Bae SC, et al. EULAR recommendations for the management of systemic lupus erythematosus: 2023 update. Ann Rheum Dis. 2024;83(1):15-29.
- van Vollenhoven RF, Mosca M, Bertsias G, Isenberg D, Kuhn A, Lerstrom K, et al. Treat-to-target in systemic lupus erythematosus: recommendations from an international task force. Ann Rheum Dis. 2014;73(6):958-67.
- Gladman D, Ginzler E, Goldsmith C, Fortin P, Liang M, Urowitz M, et al. The development and initial validation of the Systemic Lupus International Collaborating Clinics/American College of Rheumatology damage index for systemic lupus erythematosus. Arthritis Rheum. 1996;39(3):363-9.
- Alarcon GS, Roseman JM, McGwin G, Jr., Uribe A, Bastian HM, Fessler BJ, et al. Systemic lupus erythematosus in three ethnic groups. XX. Damage as a predictor of further damage. Rheumatology (Oxford). 2004;43(2):202-5.
- Rosenbaum JT, Costenbader KH, Desmarais J, Ginzler EM, Fett N, Goodman SM, et al. American College of Rheumatology, American Academy of Dermatology, Rheumatologic Dermatology Society, and American Academy of Ophthalmology 2020 Joint Statement on Hydroxychloroquine Use With Respect to Retinal Toxicity. Arthritis Rheumatol. 2021;73(6):908-11.
- Drosos GC, Vedder D, Houben E, Boekel L, Atzeni F, Badreh S, et al. EULAR recommendations for cardiovascular risk management in rheumatic and musculoskeletal diseases, including systemic lupus erythematosus and antiphospholipid syndrome. Ann Rheum Dis. 2022;81(6):768-79.
- Tummala R, Abreu G, Pineda L, Michaels MA, Kalyani RN, Furie RA, et al. Safety profile of anifrolumab in patients with active SLE: an integrated analysis of phase II and III trials. Lupus Sci Med. 2021;8(1).
- Andreoli L, Bertsias GK, Agmon-Levin N, Brown S, Cervera R, Costedoat-Chalumeau N, et al. EULAR recommendations for women’s health and the management of family planning, assisted reproduction, pregnancy and menopause in patients with systemic lupus erythematosus and/or antiphospholipid syndrome. Ann Rheum Dis. 2017;76(3):476-85.
- Sakthiswary R, Suresh E. Methotrexate in systemic lupus erythematosus: a systematic review of its efficacy. Lupus. 2014;23(3):225-35.
- Morand EF, Furie R, Tanaka Y, Bruce IN, Askanase AD, Richez C, et al. Trial of Anifrolumab in Active Systemic Lupus Erythematosus. N Engl J Med. 2020;382(3):211-21.
- Manzi S, Sanchez-Guerrero J, Merrill JT, Furie R, Gladman D, Navarra SV, et al. Effects of belimumab, a B lymphocyte stimulator-specific inhibitor, on disease activity across multiple organ domains in patients with systemic lupus erythematosus: combined results from two phase III trials. Ann Rheum Dis. 2012;71(11):1833-8.
- Vital EM, Merrill JT, Morand EF, Furie RA, Bruce IN, Tanaka Y, et al. Anifrolumab efficacy and safety by type I interferon gene signature and clinical subgroups in patients with SLE: post hoc analysis of pooled data from two phase III trials. Ann Rheum Dis. 2022;81(7):951-61.
- Kuhn A, Landmann A. The classification and diagnosis of cutaneous lupus erythematosus. J Autoimmun. 2014;48-49:14-9.
- Bein D, Kuehn E, Meuth AM, Amler S, Haust M, Nyberg F, et al. Evaluation of disease activity and damage in different subtypes of cutaneous lupus erythematosus using the CLASI. Journal of the European Academy of Dermatology and Venereology : JEADV. 2011;25(6):652-9.
- Szczech J, Samotij D, Werth VP, Reich A. Trigger factors of cutaneous lupus erythematosus: a review of current literature. Lupus. 2017;26(8):791-807.
- Vaglio A, Grayson PC, Fenaroli P, Gianfreda D, Boccaletti V, Ghiggeri GM, et al. Drug-induced lupus: Traditional and new concepts. Autoimmun Rev. 2018;17(9):912-8.
- Tani C, Cardelli C, Zen M, Moroni L, Piga M, Ceccarelli F, et al. Anifrolumab in Refractory Systemic Lupus Erythematosus: A Real-World, Multicenter Study. J Rheumatol. 2024;51(11):1096-1101.
- Pratt M, Mahmood F, Kirchhof MG. Pharmacologic Treatment of Idiopathic Chilblains (Pernio): A Systematic Review. J Cutan Med Surg 2021; 25:530.
- Costa Pires T, Caparrós-Ruiz R, Gaspar P, Isenberg DA. Prevalence and outcome of thrombocytopenia in systemic lupus erythematous: single-centre cohort analysis. Clin Exp Rheumatol. 2021; 39(3):601-605.
- Jager U, Barcellini W, Broome CM, Gertz MA, Hill A, Hill QA, et al. Diagnosis and treatment of autoimmune hemolytic anemia in adults: Recommendations from the First International Consensus Meeting. Blood Rev. 2020;41:100648.
- Gomard-Mennesson E, Ruivard M, Koenig M, Woods A, Magy N, Ninet J, et al. Treatment of isolated severe immune hemolytic anaemia associated with systemic lupus erythematosus: 26 cases. Lupus. 2006;15(4):223-31.
- Serris A, Amoura Z, Canoui-Poitrine F, Terrier B, Hachulla E, Costedoat-Chalumeau N, et al. Efficacy and safety of rituximab for systemic lupus erythematosus-associated immune cytopenias: A multicenter retrospective cohort study of 71 adults. Am J Hematol. 2018;93(3):424-9.
- Rock GA, Shumak KH, Buskard NA, Blanchette VS, Kelton JG, Nair RC, et al. Comparison of plasma exchange with plasma infusion in the treatment of thrombotic thrombocytopenic purpura. Canadian Apheresis Study Group. N Engl J Med. 1991;325(6):393-7.
- Yavuz S, Cansu DU, Nikolopoulos D, Crisafulli F, Antunes AM, Adamichou C, et al. Lymphopenia as a risk factor for neurologic involvement and organ damage accrual in patients with systemic lupus erythematosus: A multi-center observational study. Semin Arthritis Rheum. 2020; 50(6):1387-93.
- Morand EF, Furie RA, Bruce IN, Vital EM, Dall’Era M, Maho E, et al. Efficacy of anifrolumab across organ domains in patients with moderate-to-severe systemic lupus erythematosus: a post-hoc analysis of pooled data from the TULIP-1 and TULIP-2 trials. Lancet Rheumatol. 2022;4(4):e282-e92.
- Provan D, Arnold DM, Bussel JB, Chong BH, Cooper N, Gernsheimer T, et al. Updated international consensus report on the investigation and management of primary immune thrombocytopenia. Blood Adv. 2019;3(22):3780-817.
- Rodeghiero F, Stasi R, Giagounidis A, Viallard JF, Godeau B, Pabinger I, et al. Long-term safety and tolerability of romiplostim in patients with primary immune thrombocytopenia: a pooled analysis of 13 clinical trials. Eur J Haematol2013;91(5):423-36.
- Guitton Z, Terriou L, Lega JC, Nove-Josserand R, Hie M, Amoura Z, et al. Risk of thrombosis with anti-phospholipid syndrome in systemic lupus erythematosus treated with thrombopoietin-receptor agonists. Rheumatology. 2018;57(8):1432-8.
- Frittoli RB, Vivaldo JF, Costallat LTL, Appenzeller S. Gastrointestinal involvement in systemic lupus erythematosus: A systematic review. J Transl Autoimmun. 2021;4:100106.
- Morel N, Bonjour M, Le Guern V, Le Jeunne C, Mouthon L, Piette JC, et al. Colchicine: a simple and effective treatment for pericarditis in systemic lupus erythematosus? A report of 10 cases. Lupus. 2015;24(14):1479-85.
- Arnaud L, Ruiz-Irastorza G, Aranow C, Bernatsky S, Dall’Era M, Adelowo O, et al. ERN ReCONNET-SLICC-SLEuro expert consensus on the therapeutic management of rare systemic lupus erythematosus manifestations. Lancet Rheumat. 2025;7(7):e505-e18.
- Amarnani R, Yeoh SA, Denneny EK, Wincup C. Lupus and the Lungs: The Assessment and Management of Pulmonary Manifestations of Systemic Lupus Erythematosus. Front Med (Lausanne). 2021 Jan 18;7:610257.
- Bertsias GK, Tektonidou M, Amoura Z, Aringer M, Bajema I, Berden JH, et al. Joint European League Against Rheumatism and European Renal Association-European Dialysis and Transplant Association (EULAR/ERA-EDTA) recommendations for the management of adult and paediatric lupus nephritis. Ann Rheum Dis. 2012;71(11):1771–82.
- Lamb EJ, MacKenzie F, Stevens PE. How should proteinuria be detected and measured? Ann Clin Biochem. 2009;46(Pt 3):205–17.
- Fanouriakis A, Kostopoulou M, Anders HJ, Andersen J, Aringer M, Beresford MW, et al. EULAR recommendations for the management of systemic lupus erythematosus with kidney involvement: 2025 update. Ann Rheum Dis. 2025.
- Sammaritano LR, Askanase A, Bermas BL, Dall’Era M, Duarte-Garcia A, Hiraki LT, et al. 2024 American College of Rheumatology (ACR) Guideline for the Screening, Treatment, and Management of Lupus Nephritis. Arthritis Rheumatol. 2025;77(9):1115–35.
- Weening JJ, D’Agati VD, Schwartz MM, Seshan SV, Alpers CE, Appel GB, et al. The classification of glomerulonephritis in systemic lupus erythematosus revisited. J Am Soc Nephrol. 2004;15(2):241–50.
- Bajema IM, Wilhelmus S, Alpers CE, Bruijn JA, Colvin RB, Cook HT, et al. Revision of the International Society of Nephrology/Renal Pathology Society classification for lupus nephritis: clarification of definitions, and modified National Institutes of Health activity and chronicity indices. Kidney Int. 2018;93(4):789–96.
- Tektonidou MG, Sotsiou F, Nakopoulou L, Vlachoyiannopoulos PG, Moutsopoulos HM. Antiphospholipid syndrome nephropathy in patients with systemic lupus erythematosus and antiphospholipid antibodies: prevalence, clinical associations, and long-term outcome.
- Houssiau FA, D’Cruz D, Sangle S, Remy P, Vasconcelos C, Petrovic R, et al. Azathioprine versus mycophenolate mofetil for long-term immunosuppression in lupus nephritis: results from the MAINTAIN Nephritis Trial. Annals of the rheumatic diseases. 2010;69(12):2083-9.
- Pons-Estel GJ, Alarcon GS, McGwin G, Jr., Danila MI, Zhang J, Bastian HM, et al. Protective effect of hydroxychloroquine on renal damage in patients with lupus nephritis: LXV, data from a multiethnic US cohort. Arthritis Rheum. 2009;61(6):830–9.
- Appel GB, Contreras G, Dooley MA, Ginzler EM, Isenberg D, Jayne D, et al. Mycophenolate mofetil versus cyclophosphamide for induction treatment of lupus nephritis. J Am Soc Nephrol. 2009;20(5):1103–12.
- Houssiau FA, Vasconcelos C, D’Cruz D, Sebastiani GD, Garrido Ed Ede R, Danieli MG, et al. Immunosuppressive therapy in lupus nephritis: the Euro-Lupus Nephritis Trial, a randomized trial of low-dose versus high-dose intravenous cyclophosphamide. Arthritis Rheum. 2002;46(8):2121–31.
- Kidney Disease: Improving Global Outcomes Lupus Nephritis Work G. KDIGO 2024 Clinical Practice Guideline for the management of LUPUS NEPHRITIS. Kidney Int. 2024;105(1S):S1–S69.
- Furie R, Rovin BH, Houssiau F, Malvar A, Teng YKO, Contreras G, et al. Two-Year, Randomized, Controlled Trial of Belimumab in Lupus Nephritis. N Engl J Med. 2020;383(12):1117–28.
- Rovin BH, Furie R, Teng YKO, Contreras G, Malvar A, Yu X, et al. A secondary analysis of the Belimumab International Study in Lupus Nephritis trial examined effects of belimumab on kidney outcomes and preservation of kidney function in patients with lupus nephritis. Kidney Int. 2022;101(2):403–13.
- Rovin BH, Teng YKO, Ginzler EM, Arriens C, Caster DJ, Romero-Diaz J, et al. Efficacy and safety of voclosporin versus placebo for lupus nephritis (AURORA 1): a double-blind, randomised, multicentre, placebo-controlled, phase 3 trial. Lancet. 2021;397(10289):2070–80.
- Saxena A, Ginzler EM, Gibson K, Satirapoj B, Santillan AEZ, Levchenko O, et al. Safety and Efficacy of Long-Term Voclosporin Treatment for Lupus Nephritis in the Phase 3 AURORA 2 Clinical Trial. Arthritis Rheumatol. 2024;76(1):59–67.
- Mok CC, Ying KY, Yim CW, Siu YP, Tong KH, To CH, et al. Tacrolimus versus mycophenolate mofetil for induction therapy of lupus nephritis: a randomised controlled trial and long-term follow-up. Ann Rheum Dis. 2016;75(1):30–6.
- Furie RA, Aroca G, Cascino MD, Garg JP, Rovin BH, Alvarez A, et al. B-cell depletion with obinutuzumab for the treatment of proliferative lupus nephritis: a randomised, double-blind, placebo-controlled trial. Ann Rheum Dis. 2022;81(1):100–7.
- Furie RA, Rovin BH, Garg JP, Santiago MB, Aroca-Martinez G, Zuta Santillan AE, et al. Efficacy and Safety of Obinutuzumab in Active Lupus Nephritis. N Engl J Med. 2025;392(15):1471–83.
- Rovin BH, Furie R, Latinis K, Looney RJ, Fervenza FC, Sanchez-Guerrero J, et al. Efficacy and safety of rituximab in patients with active proliferative lupus nephritis: the Lupus Nephritis Assessment with Rituximab study. Arthritis Rheum. 2012;64(4):1215–26.
- Tamirou F, Lauwerys BR, Dall’Era M, Mackay M, Rovin B, Cervera R, et al. A proteinuria cut-off level of 0.7 g/day after 12 months of treatment best predicts long-term renal outcome in lupus nephritis: data from the MAINTAIN Nephritis Trial. Lupus Sci Med. 2015;2(1):e000123.
- Zickert A, Sundelin B, Svenungsson E, Gunnarsson I. Role of early repeated renal biopsies in lupus nephritis. Lupus Sci Med. 2014;1(1):e000018.
- Parodis I, Adamichou C, Aydin S, Gomez A, Demoulin N, Weinmann-Menke J, et al. Per-protocol repeat kidney biopsy portends relapse and long-term outcome in incident cases of proliferative lupus nephritis. Rheumatology (Oxford). 2020;59(11):3424–34.
- Goral S, Ynares C, Shappell SB, Snyder S, Feurer ID, Kazancioglu R, et al. Recurrent lupus nephritis in renal transplant recipients revisited: it is not rare. Transplantation. 2003;75(5):651–6.
- The American College of Rheumatology nomenclature and case definitions for neuropsychiatric lupus syndromes. Arthritis Rheum. 1999;42(4):599-608.
- Kampylafka EI, Alexopoulos H, Kosmidis ML, Panagiotakos DB, Vlachoyiannopoulos PG, Dalakas MC, et al. Incidence and prevalence of major central nervous system involvement in systemic lupus erythematosus: a 3-year prospective study of 370 patients. PloS one. 2013;8(2):e55843.
- Hanly JG, Urowitz MB, Gordon C, Bae SC, Romero-Diaz J, Sanchez-Guerrero J, et al. Neuropsychiatric events in systemic lupus erythematosus: a longitudinal analysis of outcomes in an international inception cohort using a multistate model approach. Ann Rheum Dis. 2020;79(3):356-62.
- Hanly JG, Gordon C, Bae SC, Romero-Diaz J, Sanchez-Guerrero J, Bernatsky S, et al. Neuropsychiatric Events in Systemic Lupus Erythematosus: Predictors of Occurrence and Resolution in a Longitudinal Analysis of an International Inception Cohort. Arthritis Rheumatol. 2021;73(12):2293-302.
- Zirkzee EJ, Huizinga TW, Bollen EL, van Buchem MA, Middelkoop HA, van der Wee NJ, et al. Mortality in neuropsychiatric systemic lupus erythematosus (NPSLE). Lupus. 2014;23(1):31-8.
- Bertsias GK, Ioannidis JP, Aringer M, Bollen E, Bombardieri S, Bruce IN, et al. EULAR recommendations for the management of systemic lupus erythematosus with neuropsychiatric manifestations: report of a task force of the EULAR standing committee for clinical affairs. Ann Rheum Dis. 2010;69(12):2074-82.
- Fanouriakis A, Pamfil C, Rednic S, Sidiropoulos P, Bertsias G, Boumpas DT. Is it primary neuropsychiatric systemic lupus erythematosus? Performance of existing attribution models using physician judgment as the gold standard. Clinical and experimental rheumatology. 2016;34(5):910-7.
- Magro-Checa C, Zirkzee EJ, Beaart-van de Voorde LJJ, Middelkoop HA, van der Wee NJ, Huisman MV, et al. Value of multidisciplinary reassessment in attribution of neuropsychiatric events to systemic lupus erythematosus: prospective data from the Leiden NPSLE cohort. Rheumatology (Oxford). 2017;56(10):1676-83.
- Hanly JG, Su L, Farewell V, McCurdy G, Fougere L, Thompson K. Prospective study of neuropsychiatric events in systemic lupus erythematosus. J Rheumatol. 2009;36(7):1449-59.
- Steup-Beekman GM, Zirkzee EJ, Cohen D, Gahrmann BM, Emmer BJ, Steens SC, et al. Neuropsychiatric manifestations in patients with systemic lupus erythematosus: epidemiology and radiology pointing to an immune-mediated cause. Ann Rheum Dis. 2013;72 Suppl 2:ii76-9.
- Wingerchuk DM, Banwell B, Bennett JL, Cabre P, Carroll W, Chitnis T, et al. International consensus diagnostic criteria for neuromyelitis optica spectrum disorders. Neurology. 2015;85(2):177-89.
- Williams JN, Speyer CB, Kreps DJ, Kimbrough DJ, Costenbader K, Bhattacharyya S. Spinal cord syndromes in patients with systemic lupus erythematosus: differentiating lupus myelitis, neuromyelitis optica, and multiple sclerosis. Lupus. 2019;28(14):1656-62.
- Papachristos DA, Oon S, Hanly JG, Nikpour M. Management of inflammatory neurologic and psychiatric manifestations of systemic lupus erythematosus: A systematic review. Semin Arthritis Rheum. 2021;51(1):49-71.
- Barile-Fabris L, Ariza-Andraca R, Olguin-Ortega L, Jara LJ, Fraga-Mouret A, Miranda-Limon JM, et al. Controlled clinical trial of IV cyclophosphamide versus IV methylprednisolone in severe neurological manifestations in systemic lupus erythematosus. Ann Rheum Dis. 2005;64(4):620-5.
- Cobo-Ibanez T, Loza-Santamaria E, Pego-Reigosa JM, Marques AO, Rua-Figueroa I, Fernandez-Nebro A, et al. Efficacy and safety of rituximab in the treatment of non-renal systemic lupus erythematosus: a systematic review. Semin Arthritis Rheum. 2014;44(2):175-85.
- Kopp CR, Prasad CB, Naidu S, Sharma V, Misra DP, Agarwal V, et al. Overlap syndrome of anti-aquaporin-4 positive neuromyelitis optica spectrum disorder and systemic lupus erythematosus: A systematic review of individual patient data. Lupus. 2023;32(10):1164-72.
- Tang KT, Lin CH, Chen HH, Chen YH, Chen DY. Suicidal drug overdose in patients with systemic lupus erythematosus, a nationwide population-based case-control study. Lupus. 2016;25(2):199-203.
- Miyakis S, Lockshin MD, Atsumi T, Branch DW, Brey RL, Cervera R, et al. International consensus statement on an update of the classification criteria for definite antiphospholipid syndrome (APS). J Thromb Hemost 2006;4(2):295-306.
- Barbhaiya M, Zuily S, Naden R, Hendry A, Manneville F, Amigo MC, et al. The 2023 ACR/EULAR Antiphospholipid Syndrome Classification Criteria. Arthrit Rheum. 2023;75(10): 1687-702.
- Galli M, Luciani D, Bertolini G, Barbui T. Lupus anticoagulants are stronger risk factors for thrombosis than anticardiolipin antibodies in the antiphospholipid syndrome: a systematic review of the literature. Blood. 2003;101(5):1827-32.
- Pengo V, Ruffatti A, Legnani C, Testa S, Fierro T, Marongiu F, et al. Incidence of a first thromboembolic event in asymptomatic carriers of high-risk antiphospholipid antibody profile: a multicenter prospective study. Blood. 2011;118(17):4714-8.
- Saccone G, Berghella V, Maruotti GM, Ghi T, Rizzo G, Simonazzi G, et al. Antiphospholipid antibody profile based obstetric outcomes of primary antiphospholipid syndrome: the PREGNANTS study. Am J Obstet Gynecol. 2017;216(5):525 e1- e12.
- Cervera R, Rodriguez-Pinto I, Colafrancesco S, Conti F, Valesini G, Rosario C, et al. 14th International Congress on Antiphospholipid Antibodies Task Force Report on Catastrophic Antiphospholipid Syndrome. Autoimmun Rev. 2014;13(7):699-707.
- Tektonidou MG, Andreoli L, Limper M, Amoura Z, Cervera R, Costedoat-Chalumeau N, et al. EULAR recommendations for the management of antiphospholipid syndrome in adults. Ann Rheum Dis. 2019;78(10):1296-304.
- Pengo V, Denas G, Zoppellaro G, Jose SP, Hoxha A, Ruffatti A, et al. Rivaroxaban vs warfarin in high-risk patients with antiphospholipid syndrome. Blood. 2018;132(13):1365-71.
- Rodriguez-Pinto I, Espinosa G, Cervera R. Catastrophic antiphospholipid syndrome: The current management approach. Best Pract Res Clin Rheumatol. 2016;30(2):239-49.
- Wang CR, Liu MF. Rituximab usage in systemic lupus erythematosus-associated antiphospholipid syndrome: A single-center experience. Semin Arthrit Rheum. 2016;46(1):102-8.
- Costantine MM. Pravastatin to prevent obstetrical complications in women with antiphospholipid syndrome. J Clin Invest. 2016;126(8):2792-4.
- Kello N, Khoury LE, Marder G, Furie R, Zapantis E, Horowitz DL. Secondary thrombotic microangiopathy in systemic lupus erythematosus and antiphospholipid syndrome, the role of complement and use of eculizumab: Case series and review of literature. Semin Arthritis Rheum. 2019;49(1):74-83.
- He WR, Wei H. Maternal and fetal complications associated with systemic lupus erythematosus: An updated meta-analysis of the most recent studies (2017-2019). Medicine. 2020;99(16):e19797.
- Clowse ME, Jamison M, Myers E, James AH. A national study of the complications of lupus in pregnancy. Am J Obstet Gynecol. 2008;199(2):127 e1-6.
- Mehta B, Luo Y, Xu J, Sammaritano L, Salmon J, Lockshin M, et al. Trends in Maternal and Fetal Outcomes Among Pregnant Women With Systemic Lupus Erythematosus in the United States: A Cross-sectional Analysis. Ann Intern Med. 2019;171(3):164-71.
- Rajendran A, Eudy AM, Balevic SJ, Clowse MEB. The importance of pregnancy planning in lupus pregnancies. Lupus. 2021;30(5):741-51.
- Buyon JP, Kim MY, Guerra MM, Laskin CA, Petri M, Lockshin MD, et al. Predictors of Pregnancy Outcomes in Patients With Lupus: A Cohort Study. Ann Intern Med. 2015;163(3):153-63.
- Wind M, Fierro JJ, Bloemenkamp KWM, de Leeuw K, Lely AT, Limper M, et al. Pregnancy outcome predictors in systemic lupus erythematosus: a systematic review and meta-analysis. Lancet Rheumatol. 2024; 6(10):e667-e683.
- Brucato A, Frassi M, Franceschini F, Cimaz R, Faden D, Pisoni MP, et al. Risk of congenital complete heart block in newborns of mothers with anti-Ro/SSA antibodies detected by counterimmunoelectrophoresis: a prospective study of 100 women. Arthrit Rheum. 2001;44(8): 1832-5.
- Llanos C, Izmirly PM, Katholi M, Clancy RM, Friedman DM, Kim MY, et al. Recurrence rates of cardiac manifestations associated with neonatal lupus and maternal/fetal risk factors. Arthrit Rheum. 2009;60(10):3091-7.
- Sammaritano LR, Bermas BL, Chakravarty EE, Chambers C, Clowse MEB, Lockshin MD, et al. 2020 American College of Rheumatology Guideline for the Management of Reproductive Health in Rheumatic and Musculoskeletal Diseases. Arthritis Care Res. 2020;72(4):461-88.
- Clowse ME, Magder L, Witter F, Petri M. Hydroxychloroquine in lupus pregnancy. Arthrit Rheum. 2006;54(11):3640-7.
- Juliao P, Wurst K, Pimenta JM, Gemzoe K, Landy H, Moody MA, et al. Belimumab use during pregnancy: Interim results of the belimumab pregnancy registry. Birth Defects Res. 2023; 115(2):188-204.
- Vela-Casasempere P, Caño Alameda R, Gómez Sabater S, Cortell Aznar S, Pérez Pascual E. Considering belimumab during pregnancy: A more viable option over time. Lupus. 2024;33(7):700-715.
- Petri M, Landy H, Clowse MEB, Gemzoe K, Khamashta M, Kurtinecz M, et al. Belimumab use during pregnancy: a summary of birth defects and pregnancy loss from belimumab clinical trials, a pregnancy registry and postmarketing reports. Ann Rheum Dis. 2023;82(2):217-225.
- Shimada H, Wakiya R, Kanenishi K, Miyatake N, Nakashima S, Mansour MMF, et al. Preterm birth is strongly affected by the glucocorticoid dose during pregnancy in women complicated by systemic lupus erythematosus. Arthritis Research Ther. 2022;24(1):10.
- ACOG Committee Opinion No. 743: Low-Dose Aspirin Use During Pregnancy. Obstet Gynecol. 2018;132(1):e44-e52.
- Force USPST, Davidson KW, Barry MJ, Mangione CM, Cabana M, Caughey AB, et al. Aspirin Use to Prevent Preeclampsia and Related Morbidity and Mortality: US Preventive Services Task Force Recommendation Statement. JAMA. 2021;326(12):1186-91.
- Costedoat-Chalumeau N, Pouchot J, Guettrot-Imbert G, Le Guern V, Leroux G, Marra D, et al. Adherence to treatment in systemic lupus erythematosus patients. Best practice & research Clinical rheumatology. 2013;27(3):329-40.
- Nguyen Y, Blanchet B, Urowitz MB, Hanly JG, Gordon C, Bae SC, et al. Association Between Severe Nonadherence to Hydroxychloroquine and Systemic Lupus Erythematosus Flares, Damage, and Mortality in 660 Patients From the SLICC Inception Cohort. Arthritis Rheumatol. 2023;75(12):2195-206.
- Akhavan PS, Su J, Lou W, Gladman DD, Urowitz MB, Fortin PR. The early protective effect of hydroxychloroquine on the risk of cumulative damage in patients with systemic lupus erythematosus. J Rheumatol. 2013;40(6):831-41.
- Peart E, Clowse ME. Systemic lupus erythematosus and pregnancy outcomes: an update and review of the literature. Curr Opin Rheumatol. 2014;26(2):118-23.
- Sciascia S, Hunt BJ, Talavera-Garcia E, Lliso G, Khamashta MA, Cuadrado MJ. The impact of hydroxychloroquine treatment on pregnancy outcome in women with antiphospholipid antibodies. Am J Obstet Gynecol. 2015.
- Al Sawah S, Zhang X, Zhu B, Magder LS, Foster SA, Iikuni N, et al. Effect of corticosteroid use by dose on the risk of developing organ damage over time in systemic lupus erythematosus-the Hopkins Lupus Cohort. Lupus Sci Med. 2015;2(1):e000066.
- Ugarte-Gil MF, Mak A, Leong J, Dharmadhikari B, Kow NY, Reategui-Sokolova C, et al. Impact of glucocorticoids on the incidence of lupus-related major organ damage: a systematic literature review and meta-regression analysis of longitudinal observational studies. Lupus Sci Med. 2021;8(1).
- Abe K, Ishikawa Y, Kita Y, Yajima N, Inoue E, Sada KE, et al. Association of low-dose glucocorticoid use and infection occurrence in systemic lupus erythematosus patients: a prospective cohort study. Arthritis Res Ther. 2022;28(1):179.
- Kapoor TM, Mahadeshwar P, Nguyen S, Li J, Kapoor S, Bathon J, et al. Low prevalence of Pneumocystis pneumonia in hospitalized patients with systemic lupus erythematosus: review of a clinical data warehouse. Lupus. 2017;26(14):1473-82.
- Pope J, Jerome D, Fenlon D, Krizova A, Ouimet J. Frequency of adverse drug reactions in patients with systemic lupus erythematosus. J Rheum. 2003;30(3):480-4.
- Illei GG, Austin HA, Crane M, Collins L, Gourley MF, Yarboro CH, et al. Combination therapy with pulse cyclophosphamide plus pulse methylprednisolone improves long-term renal outcome without adding toxicity in patients with lupus nephritis. Ann Intern Med. 2001;135(4):248-57.
- Tseng CE, Buyon JP, Kim M, Belmont HM, Mackay M, Diamond B, et al. The effect of moderate-dose corticosteroids in preventing severe flares in patients with serologically active, but clinically stable, systemic lupus erythematosus: findings of a prospective, randomized, double-blind, placebo-controlled trial. Arthrit Rheum. 2006;54(11):3623-32.
- Walsh M, Jayne D, Moist L, Tonelli M, Pannu N, Manns B. Practice pattern variation in oral glucocorticoid therapy after the induction of response in proliferative lupus nephritis. Lupus. 2010;19(5):628-33.
- Condon MB, Ashby D, Pepper RJ, Cook HT, Levy JB, Griffith M, et al. Prospective observational single-centre cohort study to evaluate the effectiveness of treating lupus nephritis with rituximab and mycophenolate mofetil but no oral steroids. Ann Rheum Dis. 2013;72(8):1280-6.
- Simard JF, Rossides M, Gunnarsson I, Svenungsson E, Arkema EV. Infection hospitalisation in systemic lupus in Sweden. Lupus Sci Med. 2021;8(1).
- Oelzner P, Abendroth K, Hein G, Stein G. Predictors of flares and long-term outcome of systemic lupus erythematosus during combined treatment with azathioprine and low-dose prednisolone. Rheumatol Int1996;16(4):133-9.
- Griffiths B, Emery P, Ryan V, Isenberg D, Akil M, Thompson R, et al. The BILAG multi-centre open randomized controlled trial comparing ciclosporin vs azathioprine in patients with severe SLE. Rheumatology. 2010;49(4):723-32.
- Cheng Y, Ma J, Niu J. Post-marketing safety signals of anifrolumab in systemic lupus erythematosus: a pharmacovigilance study based on FAERS. BMC Rheumatol. 2025;9(1):90.
- Furie RA, Morand EF, Bruce IN, Manzi S, Kalunian KC, Vital EM, et al. Type I interferon inhibitor anifrolumab in active systemic lupus erythematosus (TULIP-1): a randomised, controlled, phase 3 trial. Lancet Rheumatol2019;1(4):e208-e19.
- Kalunian KC, Furie R, Morand EF, Bruce IN, Manzi S, Tanaka Y, et al. A Randomized, Placebo-Controlled Phase III Extension Trial of the Long-Term Safety and Tolerability of Anifrolumab in Active Systemic Lupus Erythematosus. Arthritis Rheumatol. 2023;75(2):253-65.
- Riggs JM, Hanna RN, Rajan B, Zerrouki K, Karnell JL, Sagar D, et al. Characterisation of anifrolumab, a fully human anti-interferon receptor antagonist antibody for the treatment of systemic lupus erythematosus. Lupus science & medicine. 2018;5(1):e000261.
- Ronnblom L, Leonard D. Interferon pathway in SLE: one key to unlocking the mystery of the disease. Lupus Sci Med. 2019;6(1):e000270.
- Furie R, Khamashta M, Merrill JT, Werth VP, Kalunian K, Brohawn P, et al. Anifrolumab, an Anti-Interferon-alpha Receptor Monoclonal Antibody, in Moderate-to-Severe Systemic Lupus Erythematosus. Arthritis Rheumatol. 2017;69(2):376-86.
- Bruce IN, van Vollenhoven RF, Morand EF, Furie RA, Manzi S, White WB, et al. Sustained glucocorticoid tapering in the phase 3 trials of anifrolumab: a post hoc analysis of the TULIP-1 and TULIP-2 trials. Rheumatology. 2023;62(4):1526-34.
- Troldborg A, Remkus L, Eek D, Deleuran B. Anifrolumab treatment improves patient-reported quality of life and decreases disease activity and corticosteroid use in patients with systemic lupus erythematosus: A qualitative study in Denmark. Lupus. 2024;33(9):962-973.
- Tani C, Cardelli C, Zen M, Moroni L, Piga M, Ceccarelli F, et al. Anifrolumab in Refractory Systemic Lupus Erythematosus: A Real-World, Multicenter Study. J Rheumatol. 2024;51(11):1096-101.
- Touma Z, Bruce IN, Furie R, Morand E, Tummala R, Chandran S, et al. Reduced organ damage accumulation in adult patients with SLE on anifrolumab plus standard of care compared to real-world external controls. Ann Rheum Dis. 2025;84(5):767-76.
- Jayne D, Rovin B, Mysler EF, Furie RA, Houssiau FA, Trasieva T, et al. Phase II randomised trial of type I interferon inhibitor anifrolumab in patients with active lupus nephritis. Ann Rheum Dis. 2022;81(4):496-506.
- Navarra SV, Guzman RM, Gallacher AE, Hall S, Levy RA, Jimenez RE, et al. Efficacy and safety of belimumab in patients with active systemic lupus erythematosus: a randomised, placebo-controlled, phase 3 trial. Lancet. 2011;377(9767):721-31.
- Blumenfeld Z, Mischari O, Schultz N, Boulman N, Balbir-Gurman A. Gonadotropin releasing hormone agonists may minimize cyclophosphamide associated gonadotoxicity in SLE and autoimmune diseases. Seminars Arthrit Rheum. 2011;41(3):346-52.
- Zahr N, Arnaud L, Marquet P, Haroche J, Costedoat-Chalumeau N, Hulot JS, et al. Mycophenolic acid area under the curve correlates with disease activity in lupus patients treated with mycophenolate mofetil. Arthritis Rheum. 2010;62(7):2047-54.
- Ginzler EM, Dooley MA, Aranow C, Kim MY, Buyon J, Merrill JT, et al. Mycophenolate mofetil or intravenous cyclophosphamide for lupus nephritis. N Engl J Med 2005;353(21):2219-28.
- Ginzler EM, Wofsy D, Isenberg D, Gordon C, Lisk L, Dooley MA, et al. Nonrenal disease activity following mycophenolate mofetil or intravenous cyclophosphamide as induction treatment for lupus nephritis: findings in a multicenter, prospective, randomized, open-label, parallel-group clinical trial. Arthrit Rheum. 2010;62(1):211-21.
- Dooley MA, Jayne D, Ginzler EM, Isenberg D, Olsen NJ, Wofsy D, et al. Mycophenolate versus azathioprine as maintenance therapy for lupus nephritis. N Engl J Med. 2011;365(20):1886-95.
- Ordi-Ros J, Saez-Comet L, Perez-Conesa M, Vidal X, Mitjavila F, Castro Salomo A, et al. Enteric-coated mycophenolate sodium versus azathioprine in patients with active systemic lupus erythematosus: a randomised clinical trial. Ann Rheum Dis. 2017;76(9):1575-82.
- Olivieri G, Ceccarelli F, Natalucci F, Pirone C, Orefice V, Pacucci VA, et al. Five-years drug survival of mycophenolate mofetil therapy in patients with systemic lupus erythematosus: Comparison between renal and non-renal involvement. Joint Bone Spine. 2021;88(6):105246.
- Manger K, Kalden JR, Manger B. Cyclosporin A in the treatment of systemic lupus erythematosus: results of an open clinical study. Br J Rheumatol. 1996;35:669-75.
- Griffiths B, Emery P, Ryan V, Isenberg D, Akil M, Thompson R, et al. The BILAG multi-centre open randomized controlled trial comparing ciclosporin vs azathioprine in patients with severe SLE. Rheumatology (Oxford). 2010;49(4):723-32.
- Paziana K, Del Monaco M, Cardonick E, Moritz M, Keller M, Smith B, et al. Ciclosporin use during pregnancy. Drug Saf. 2013;36(5):279-94.
- Yoon KH. Efficacy and cytokine modulating effects of tacrolimus in systemic lupus erythematosus: a review. J Biomed Biotechnol 2010;2010:686480.
- Kamanamool N, Ingsathit A, Rattanasiri S, Ngamjanyaporn P, Kasitanont N, Chawanasuntorapoj R, et al. Comparison of disease activity between tacrolimus and mycophenolate mofetil in lupus nephritis: a randomized controlled trial. Lupus. 2017:961203317739131.
- Mössner E, Brünker P, Moser S, Püntener U, Schmidt C, Herter S, et al. Increasing the efficacy of CD20 antibody therapy through the engineering of a new type II anti-CD20 antibody with enhanced direct and immune effector cell-mediated B-cell cytotoxicity. Blood. 2010; 115(22):4393-402.
- Parodis I, Soder F, Faustini F, Kasza Z, Samuelsson I, Zickert A, et al. Rituximab-mediated late-onset neutropenia in systemic lupus erythematosus – distinct roles of BAFF and APRIL. Lupus. 2018;27(9):1470-8.
- Wincup C, Menon M, Smith E, Schwartz A, Isenberg D, Jury EC, et al. Presence of anti-rituximab antibodies predicts infusion-related reactions in patients with systemic lupus erythematosus. Ann Rheum Dis. 2019;78(8):1140-2.
- Faustini F, Dunn N, Kharlamova N, Ryner M, Bruchfeld A, Malmstrom V, et al. First exposure to rituximab is associated to high rate of anti-drug antibodies in systemic lupus erythematosus but not in ANCA-associated vasculitis. Arthrit Res Ther. 2021;23(1):211.
- Merrill JT, Neuwelt CM, Wallace DJ, Shanahan JC, Latinis KM, Oates JC, et al. Efficacy and safety of rituximab in moderately-to-severely active systemic lupus erythematosus: the randomized, double-blind, phase II/III systemic lupus erythematosus evaluation of rituximab trial. Arthritis Rheum. 2010 Jan;62(1):222-33.
- Terrier B, Amoura Z, Ravaud P, Hachulla E, Jouenne R, Combe B, et al. Safety and efficacy of rituximab in systemic lupus erythematosus: results from 136 patients from the French AutoImmunity and Rituximab registry. Arthritis Rheum. 2010;62(8):2458-66.
- Ramos-Casals M, Garcia-Hernandez FJ, de Ramon E, Callejas JL, Martinez-Berriotxoa A, Pallares L, et al. Off-label use of rituximab in 196 patients with severe, refractory systemic autoimmune diseases. Clin Exp Rheumatol. 2010;28(4):468-76.
- Gunnarsson I, Jonsdottir T. Rituximab treatment in lupus nephritis–where do we stand? Lupus. 2013;22(4):381-9.
- Ma L, Peng L, Zhao J, Bai W, Jiang N, Zhang S, et al. Efficacy and safety of Janus kinase inhibitors in systemic and cutaneous lupus erythematosus: A systematic review and meta-analysis. Autoimmun Rev. 2023;22(12):103440.
- Aringer M, Houssiau F, Gordon C, Graninger WB, Voll RE, Rath E, et al. Adverse events and efficacy of TNF-alpha blockade with infliximab in patients with systemic lupus erythematosus: long-term follow-up of 13 patients. Rheumatology. 2009;48(11):1451-4.
- van Vollenhoven RF, Hahn BH, Tsokos GC, Wagner CL, Lipsky P, Touma Z, et al. Efficacy and safety of ustekinumab, an IL-12 and IL-23 inhibitor, in patients with active systemic lupus erythematosus: results of a multicentre, double-blind, phase 2, randomised, controlled study. Lancet. 2018;392(10155):1330-9.
- Morand E, Pike M, Merrill JT, van Vollenhoven R, Werth VP, Hobar C, et al. Deucravacitinib, a Tyrosine Kinase 2 Inhibitor, in Systemic Lupus Erythematosus: A Phase II, Randomized, Double-Blind, Placebo-Controlled Trial. Arthritis Rheumatol. 2023;75(2):242-52.
- Schwab I, Nimmerjahn F. Intravenous immunoglobulin therapy: how does IgG modulate the immune system? Nat Rev Immunol. 2013;13(3):176-89.
- Seite JF, Goutsmedt C, Youinou P, Pers JO, Hillion S. Intravenous immunoglobulin induces a functional silencing program similar to anergy in human B cells. J Allergy Clin Immunol. 2014; 133(1):181-8 e1-9.
- Zandman-Goddard G, Levy Y, Shoenfeld Y. Intravenous immunoglobulin therapy and systemic lupus erythematosus. Clin Rev Allergy Immunol. 2005;29(3):219-28.
- Legault K, Schunemann H, Hillis C, Yeung C, Akl EA, Carrier M, et al. Mcmaster RARE-bestpractices clinical practice guideline on diagnosis and management of the catastrophic antiphospholipid syndrome. J Thromb Haemostasis (2018) 16(8):1656–64.
- Alexander T, Thiel A, Rosen O, Massenkeil G, Sattler A, Kohler S, et al. Depletion of autoreactive immunologic memory followed by autologous hematopoietic stem cell transplantation in patients with refractory SLE induces long-term remission through de novo generation of a juvenile and tolerant immune system. Blood. 2009;113(1):214-23.
- Illei GG, Cervera R, Burt RK, Doria A, Hiepe F, Jayne D, et al. Current state and future directions of autologous hematopoietic stem cell transplantation in systemic lupus erythematosus. Ann Rheum Dis. 2011;70(12):2071-4.
- Rodriguez SC, Olguin AM, Miralles CP, Viladrich PF. Characteristics of meningitis caused by Ibuprofen: report of 2 cases with recurrent episodes and review of the literature. Medicine. 2006;85(4):214-20. Nephritis Trial. Arthritis Rheum. 2004;50(12):3934-40.
- Müller F, Taubmann J, Bucci L, Wilhelm A, Bergmann C, Völkl S, et al. CD19 CAR T-Cell Therapy in Autoimmune Disease – A Case Series with Follow-up. N Engl J Med. 2024 Feb 22;390(8):687-700.

