Riktlinjer för läkemedelsbehandling vid reumatoid artrit
Inledning
Arbetsgrupp:
Cathrine Ersmarker, Inger Gjertsson, Alf Kastbom, Heidi Kokkonen, Jon Lampa, Hanna Lindberg, Carl Turesson (sammankallande)
Sammanfattning
Behandling av patienter med RA syftar till att dämpa sjukdomsaktivitet – om möjligt till klinisk remission – samt förebygga leddestruktion och en allvarlig sjukdomsutveckling på längre sikt. Det är viktigt att tidigt identifiera patienter med hög risk för persisterande, allvarlig sjukdom. Prognostiska faktorer har stor betydelse för valet av behandling. Viktiga principer i behandlingsstrategier vid tidig RA är tidig insättning av sjukdomsmodifierande läkemedel (disease modifying anti-rheumatic drugs; DMARDs), som t ex behandling med metotrexat i adekvata doser, täta kontroller och snabba förändringar av dos och läkemedel vid otillfredställande effekt. Behandling med biologiska DMARDs (bDMARDs) har en framträdande roll, och strukturerad uppföljning av effekt och säkerhet i register är viktig. JAK-hämmare utgör ett värdefullt komplement till behandlingsarsenalen, men kräver särskilt beaktande av säkerhetsaspekter hos de äldre patienterna. Strukturerade försök till nedtrappning av bDMARDs och JAK-hämmare kan framför allt övervägas vid tidigt insatt behandling och god, persisterande effekt.
Särskilda överväganden kan behövas vid behandling av extraartikulära manifestationer, t.ex. bör man välja annan behandling än TNF-hämmare vid aktiv interstitiell lungsjukdom.
Riktlinjerna sammanfattas schematiskt i två flödesscheman: dels avseende behandlingsstrategier vid tidig RA och rekommendationer vid ofullständig terapieffekt (Flödesschema 1), och dels avseende specifika rekommendationer vid intolerans för metotrexat (Flödesschema 2).
Åtgärder som inte rekommenderas beskrivs i en lista över Kloka Kliniska Val för att optimera patientnytta (Appendix 2).
Innehåll
Bakgrund
Avsikten är att sammanfatta aktuella principer för läkemedelsbehandling vid reumatoid artrit (RA) baserat på den evidens som finns i litteraturen eller, i de fall sådan saknas, baserat på konsensus. Grad av evidens anges enligt GRADE som hög, måttlig, låg eller mycket låg evidensstyrka, där hög evidensstyrka är den högsta graden av evidens (se Appendix 1). I de fall där ett påstående inte leder till en tydlig rekommendation, eller rekommendationer bygger enbart på konsensus eller expertsynpunkter, anges ingen evidensgradering. Dubbelblinda, kontrollerade studier har störst betydelse för behandlingsrekommendationerna. Registerbaserade observationsstudier utgör ett viktigt komplement främst när det gäller säkerhet och effekt över längre tid. Referenslistan innefattar nyckelreferenser som stöder evidensgraderingen, och utgör inte någon fullständig sammanställning av den relevanta litteraturen. Ren smärtstillande behandling (t.ex. paracetamol, NSAID-preparat och opioider) diskuteras inte i detta dokument.
Rekommendationerna ansluter i tillämpliga delar till internationella rekommendationer, framför allt den Europeiska reumatologorganisationen EULARs riktlinjer för läkemedelsbehandling av RA från 2022 (1) och den amerikanska reumatologorganisationen ACRs riktlinjer för läkemedelsbehandling av RA från 2021(2), och till Socialstyrelsens nationella riktlinjer för rörelseorganens sjukdomar från 2021 (3). Evidensgraderingen utgår i stor utsträckning från det arbete som utförts inom ramen för framtagandet av det vetenskapliga underlaget för Socialstyrelsens riktlinjer. I dessa fall finns närmare information om sammanställd evidens och dess gradering i Socialstyrelsens underlag (3, 4). Rekommendationerna är en vidareutveckling av den senaste uppdateringen av de nationella terapiriktlinjerna från Svensk Reumatologisk Förening (SRF) 2025. Riktlinjedokumentet uppdateras årligen. Processen för uppdatering börjar med att arbetsgruppen tar fram ett utkast, som går på remiss till SRFs Professorskollegium. Efter synpunkter därifrån revideras utkastet, och den nya versionen tas upp till diskussion på SRFs Riktlinjedag i januari. Efter denna diskussion tar arbetsgruppen fram ett nytt underlag till SRFs styrelse, som beslutar om de nya riktlinjerna.
Rekommendationerna har utformats för att vara ett stöd vid handläggningen av patienter med RA. Varje reumatolog ansvarar som alltid för utformningen av behandlingen av sina patienter baserat på sin egen kunskap och erfarenhet. Den individuella variationen mellan patienter är betydande, och det finns ofta stora svårigheter med att extrapolera från kliniska studier till enskilda patienter.
Riktlinjerna utgår från överväganden om behandling vid tidig RA samt vid terapisvikt eller intolerans för ordinerad behandling, och gäller i dessa delar även patienter med etablerad RA. Särskilda aspekter kan behöva vägas in hos patienter med etablerad RA, såsom stigande ålder, olika komplikationer av sjukdomen (t.ex. extraartikulära manifestationer och komorbiditet) och patientens erfarenhet av tidigare givna behandlingar.
De viktigaste nyheterna i 2026 års version
Det finns en lång rad mindre ändringar i flertalet stycken i riktlinjedokumentet, men de viktigaste enskilda förändringarna är:
- Ett avsnitt om läkemedelsbehandling av äldre patienter med RA har lagts till. Viktiga aspekter som man behöver ta hänsyn till i denna patientgrupp lyfts fram, tillsammans med en kortfattad beskrivning av relevant evidens. Avsnittet kan modifieras och byggas ut i framtida uppdateringar.
- Flödesschemat har uppdaterats och harmoniserats med texten i riktlinjedokumentet, där det tydligt framgår att biologiska läkemedel (med TNF-hämmare listade först) är huvudalternativet vid otillräcklig effekt av metotrexat. Som tidigare gäller att tillägg av andra konventionella syntetiska DMARDs kan övervägas vid avsaknad av ogynnsamma prognostiska faktorer.
- Avsnittet om säkerhetsaspekter på behandling med JAK-hämmare har uppdaterats med redogörelse för det aktuella kunskapsläget utifrån observationsstudier med längre uppföljningstid. Rekommendationerna är oförändrade, och i linje med ställningstaganden från den europeiska läkemedelsmyndigheten.
- Avsnittet om biosimilarer har uppdaterats och kortats, och det tidigare Appendix 7, där alla tillgängliga biosimilarer i Sverige beskrevs, har tagits bort.
- Rekommendationerna om nedtrappning av DMARDs har uppdaterats och harmoniserats med EULARs rekommendationer. Vid stabil remission kan dosreduktion övervägas för alla typer av DMARDs, men fullständig utsättning medför hög risk för försämring.
- Avsnittet om behandling av extraartikulära manifestationer har kompletterats med aktuella referenser om immunmodulerande och fibroshämmande behandling mot interstitiell lungsjukdom.
- Informationen om säkerhetsaspekter på behandling med bDMARDs har kompletterats med aktuella referenser till studier av risken för malignitet.
- Avsnittet om immunogenicitet har uppdaterats med ytterligare information om betydelsen av samtidig metotrexatbehandling för att minska risken för utveckling av anti-läkemedelsantikroppar mot TNF-hämmare.
Definitioner
Diagnos
Svårigheten att tidigt ställa diagnosen RA skall inte underskattas. ACR/EULARs klassifikationskriterier för RA från 2010 (5) kan användas som ett stöd i tidig diagnostik. En översättning till svenska av dessa kriterier finns i Appendix 3.
ACR/EULAR kriterierna fokuserar på faktorer hos patienter med tidig artrit som är associerade med persisterande och erosiv sjukdom, och har tagits fram för att underlätta korrekt och konsekvent identifiering av RA i tidigt skede av sjukdomen. Syftet är att underlätta tidigt insättande av effektiv terapi för att i möjligaste mån förhindra eller minimera utvecklingen av erosiv sjukdom.
Det finns även en EULAR-definition av erosiv sjukdom (för definition se Appendix 3), som är förenlig med klassificering som RA, även hos patienter som inte uppfyller 2010 års kriterier (6). Denna definition av erosiv sjukdom har i en studie validerats hos patienter med tidig RA, och där uppvisat jämförbar sensitivitet och specificitet med 1987 års kriterier(7).
I 2010 års kriterier anges antikroppar mot citrullinerade proteiner (ACPA), som är ett samlingsbegrepp innefattande antikroppar mot flera olika citrullinerade proteiner/peptider, t. ex. vimentin och fibrinogen. I klinisk rutin analyseras ACPA såsom antikroppar mot cykliska citrullinerade peptider (CCP) med antigenet CCP2. Då olika ACPA har potentiellt olika karaktäristika anges den specifika analysmetoden (anti-CCP) genomgående i detta dokument.
Underlaget för behandlingsrekommendationer för de patienter som uppfyller 2010 års kriterier, men inte 1987 års kriterier(8), är fortfarande begränsat, framför allt för äldre behandlingar. I en placebokontrollerad studie visades en singeldos rituximab försena, men inte förhindra, artritutveckling hos patienter med artralgier och hög risk för framtida RA (9). Effekten av Abatacept på progressionen från anti-CCP positiv artralgi till RA har utvärderats i två olika studier med olika behandlingslängd, 6 respektive 12 månader där behandlingsgruppen i lägre grad utvecklade RA jämfört med placebogruppen under observationstiden men med signaler om att skillnaderna minskar över tiden efter avslutad behandling, varför längre uppföljningstid krävs (10, 11). En studie på hydroxyklorokin stoppades i förtid då man vid interimsanalys inte kunde visa någon effekt av hydroxyklorokin jämfört placebo på utvecklingen av RA(12) . Även metotrexate har studerats som behandling för att förhindra utvecklingen av artrit hos indivder med artralgi men utan någon påvisad effekt(13). Behandling med sjukdomsmodifierande läkemedel till patienter med ökad risk för framtida RA men utan klinisk artrit rekommenderas i nuläget inte.
Sjukdomsaktivitet och svårighetsgrad
För begreppen låg/medelhög/hög aktivitet, förutsätts i detta dokument att begreppen definieras av varje enskild reumatolog genom en sammanvägning av kliniska fynd och biokemiska variabler . Det är viktigt att ställningstagande till behandling och byte av behandling görs genom en sammanvägning av all tillgänglig information. Aktivitetsindex skall således ses som stöd för klinikern i beslutsprocessen. Det är också viktigt att väga in andra faktorer som påverkar sjukdomens svårighetsgrad, såsom förekomst av extraartikulära manifestationer, progredierande funktionsnedsättning och progress av ledskador konstaterade vid röntgenundersökning (14). Allvarliga extraartikulära manifestationer (15, 16) och hög persisterande sjukdomsaktivitet (17) ökar risken för kardiovaskulär komorbiditet och förtida död.
Nivån av RF och, i mindre utsträckning, anti-CCP antikroppar, påverkas av behandling och sjunker vid minskande sjukdomsaktivitet (18), men det finns inte tillräckligt vetenskapligt stöd för att använda RF och/eller anti-CCP som aktivitets- eller destruktionsmarkörer över tid.
Disease Activity Score (DAS) är ett aktivitetsindex i vilket antalet svullna och ömma leder, SR eller CRP samt patientens globala värdering av hälsotillståndet (VAS-skala) ingår. Den mest använda varianten baseras på bedömning av 28 fördefinierade leder (DAS28), med strikta gränser avseende sjukdomsaktivitet (19, 20) (Appendix 4). Den kliniska verkligheten är dock alltför komplex för att terapibeslut skall kunna styras strikt utifrån ett DAS28-värde. Relationen mellan DAS28 och inflammation varierar för olika individer, och flera studier har rapporterat högre DAS28 på gruppnivå hos kvinnor än hos män i förhållande till inflammationsgrad (21, 22).
Som alternativ till DAS28 kan andra indices användas såsom Simple Disease Activity Index (SDAI) (23) (Appendix 4). SDAI är validerat, är enkelt att räkna ut och korrelerar starkt med DAS28. Clinical Disease Activity Index (CDAI), som också är ett validerat instrument är en förenkling av SDAI, där CRP är exkluderat. CDAI innehåller således inga akuta fasreaktanter, och en fördel kan bland annat vara att det går att räkna ut omgående utan blodprovstagning (24) (Appendix 4).
Prognosiska faktorer
Prognostiska faktorer för progredierande leddestruktion är förekomst av RF och/eller anti-CCP antikroppar, hög SR, högt CRP, tidig förekomst av erosioner och antal svullna leder (25). Ju fler ogynnsamma prognostiska faktorer som uppvisas av patienten desto sämre bedöms prognosen vara, men svårigheten att bedöma prognos hos en enskild patient är fortfarande betydande.
Bilddiagnostik
Magnetkameraundersökning (Magnet Resonans Imaging, MRI) för att detektera benödem, synoviter och erosioner kan ge information som är användbar för att prediktera utveckling av lederosioner på röntgen (Måttlig evidensstyrka) (26, 27) varför detta kan användas som en komplettering när prognosen är svårvärderad.
Muskuloskeletalt ultraljud (MSUS) med gråskaleultraljud (GSUS) och power doppler (PDUS) ger möjlighet att detektera synoviter, tenosynoviter, utgjutningar och erosioner. Vid tidig RA är synovit detekterad med PDUS starkast associerad med framtida radiografisk progress, medan någon lika tydlig koppling inte ses för GSUS (28-31). Erosioner detekterade med ultraljud är inte lika väl studerat, men har i en mindre studie visat sig korrelera signifikant till progress av radiografiska erosioner, hos patienter med odifferentierad artrit och tidig RA (29).
Såväl MRI som ultraljudsfynd har visats vara associerade med radiografisk progress även när man tar hänsyn till andra relevanta prediktorer (26-30). I en studie som genomfördes inom ramen för tight control-uppföljning tillförde dock inte MRI eller ultraljud något utöver en klinisk prediktionsmodell, inkluderande ålder, kön, CRP, anti-CCP, DAS28-CRP och röntgenerosioner, för prediktion av radiografisk progress (32).
Sammantaget bedöms underlaget vara otillräckligt för att kunna definiera exakt vilken roll MRI och ultraljud bör ha som prognostiskt verktyg i klinisk vardag (33).
En sammanfattning över hur de olika bilddiagnostiska metoderna kan användas finns i Appendix 6.
HAQ som prognostisk faktor
För framtida funktionsförmåga, men även för komorbiditet och mortalitet, har funktionsnivån mätt med HAQ (Health Assessment Questionnaire) prognostisk betydelse (34, 35).
Livsstilsfaktorer
Vid bedömning av patienter med RA bör även livsstilsfaktorer som kan påverka prognosen beaktas. Screening för riskfaktorer för kardiovaskulär sjukdom och intervention mot dessa bör genomföras enligt separata rekommendationer från SRF. Likaledes bör livsstilsfaktorer sammanhängande med den ökade risken för osteoporos och osteoporosrelaterade frakturer beaktas. Rökning medför en ökad risk för erosiv sjukdom (36) och för komorbiditet. Rökning kan även minska effekten av anti-reumatisk behandling, vilket är visat för metotrexat och TNF-hämmare (37-39). Det finns även begränsat underlag som talar för en negativ påverkan av rökning på effekten av rituximab (40).
Övervikt/fetma förefaller vara associerat med aspekter på sjukdomens prognos via flera olika mekanismer. Å ena sidan har övervikt hos patienter med tidig RA, och framförallt fetma med BMI >30, associerats till lägre förekomst av erosioner vid 2-3 års uppföljning (41-44), men å andra sidan till högre sjukdomsaktivitet efter 2 år (45, 46).
Sammanfattning: prognostiska faktorer
Förekomst av RF och/eller anti-CCP antikroppar, hög SR, högt CRP, tidig förekomst av erosioner och antal svullna leder är starkt kopplade till en sämre prognos. MRI och ultraljud kan ge viss prognostisk information, men underlaget bedöms vara otillräckligt för att definiera exakt vilken roll de bör ha som prognostiska verktyg i klinisk vardag. Funktionsnivå och livsstilsfaktorer bör beaktas.
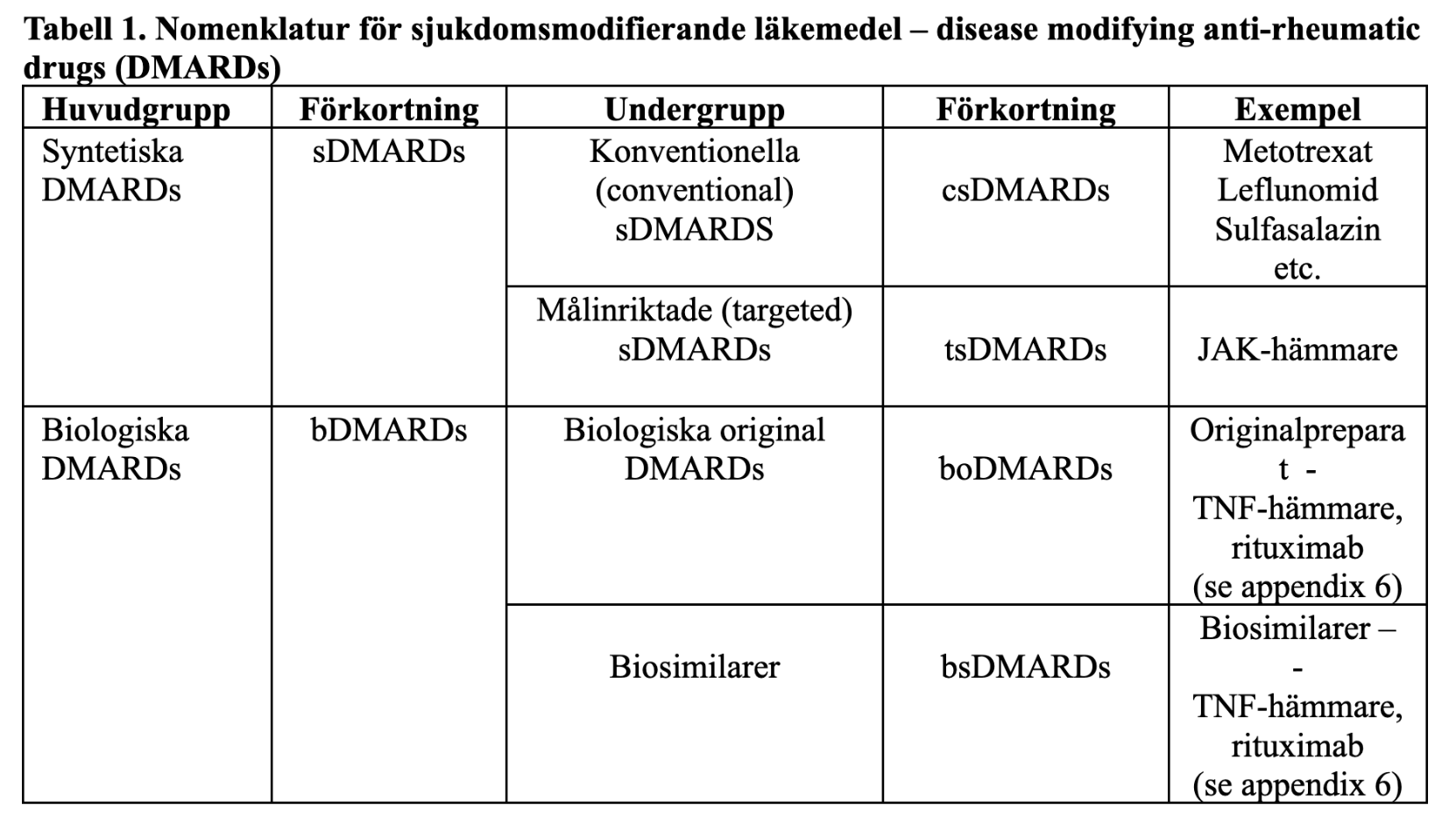
Nomenklatur för anti-reumatiska läkemedel
I riktlinjerna används konsekvent den internationella beteckningen på sjukdomsmodifierande/långverkande anti-reumatiska läkemedel – DMARDs (Disease Modifying Anti-Rheumatic Drugs), med internationellt accepterad nomenklatur (47) (Tabell 1).
Övergripande behandlingsstrategi
Terapimål
Målsättningen vid behandling av patienter med RA, speciellt i tidigt skede, bör vara att uppnå remission, då det är förknippat med mindre destruktionsprogress, bättre funktionsförmåga och minskad risk för extraartikulära manifestationer, komorbiditeter och för tidig död.
I de fall behandlingsmålet remission inte kan uppnås, på grund av svårbehandlad sjukdom eller andra patientrelaterade faktorer, kan låg sjukdomaktivitet (Appendix 4) vara ett rimligt behandlingsmål.
Definitioner för begreppet remission finns (Appendix 5)(19, 48), men de är behäftade med vissa svagheter. Hos metotrexatbehandlade patienter med RA som uppnått klinisk remission definierat som DAS28<2.6 kan kvarstående oöm ledsvullnad vara förenad med fortsatt röntgenologisk destruktion(49). Mer stringenta uppsättningar av remissionskriterier, gemensamma för ACR och EULAR, uppdaterades 2022(50)(Appendix 5).
Studier av patienter i klinisk remission, definierat utifrån DAS28, SDAI eller CDAI, har påvisat kvarstående subklinisk synovit med MRI eller med muskuloskeletalt ultraljud (MSUS) (51, 52)).
Täta kontroller och aktiv uppföljning – ”tight control”
Förutom preparatval har uppföljning, utvärdering och ställningstagande till terapiändringar betydelse för utfallet. Täta kontroller och aktiv behandling som styrs av kvarstående sjukdomsaktivitet har visats bidra till bättre utfall för patienter med medelhög till hög sjukdomsaktivitet (Låg evidensstyrka) (53-55). Det finns utbredd konsensus kring denna behandlingsprincip (56). Inom ramen för organisationen för kunskapsstyrning inom hälso- och sjukvård har ett Personcentrerat och Sammanhållet Vårdförlopp (PSV) för Reumatoid Artrit utarbetats. Del 1 beskriver hur tidig diagnostik och monitorering under första året efter diagnos bör bedrivas för att minska risken för funktionsnedsättning och komplikationer av RA. Del 2 beskriver uppföljning under resten av livet och båda delarna refererar till dessa riktlinjer vad gäller läkemedelsbehandling.
Två randomiserade kontrollerade studier (RCT) har visat att så kallad ”tight control” strategi (täta kontroller och aktiv behandling som styrs av kvarstående sjukdomsaktivitet) som styrs med hjälp av MSUS vid tidig RA gav upphov till ökad läkemedelsbehandling men utan att ge bättre resultat med avseende på klinisk remission samt radiologiska erosioner jämfört med motsvarande program utan MSUS (57, 58), varför en sådan strategi inte rekommenderas.
Vid utebliven terapieffekt bör man göra en ny värdering av underlaget för aktivitetsbedömningen, då relationen mellan sammansatta sjukdomsaktivitetsmått och inflammation varierar (se Sjukdomsaktivitet och Svårighetsgrad, ovan). I vissa fall kan utökad behandling behöva inriktas mot kvarstående smärta snarare än ytterligare antireumatisk terapi.
Kvarstående smärta
Fibromyalgi och generaliserad smärta (i senare litteratur benämnd nociplastisk smärta) har högre prevalens vid RA jämfört med den övriga populationen (59). Vid uttalad smärta (definieras som VAS > 40 mm (60)) och samtidigt tecken på låg inflammationsaktivitet (lågt antal svullna leder, låga inflammationsparametrar) rekommenderas utvärdering och bedömning om det föreligger entesiter eller annan behandlingsbar orsak till det kroniska smärttillståndet. Även ställningstagande till smärtdämpande rehabiliteringsåtgärder rekommenderas (61). Om tecken finns på generaliserad smärta (smärta i kroppens fyra kvadranter med eller utan allodyni, dvs smärtupplevelse vid beröring) föreligger låg sannolikhet för förbättrad sjukdomsaktivitet med optimerad antireumatisk behandling. I detta läge rekommenderas smärtanalys och rehabiliteringsplan. Överväg bedömning av smärtspecialist. Vid generaliserad smärta är sällan enbart farmakologisk behandling framgångsrik. Här rekommenderas i första hand individuellt anpassade program med rörelse- och konditionsträning. Vid otillräcklig effekt av icke-farmakologisk behandling kan farmakologisk behandling prövas, i första hand lågdos tricykliska antidepressiva, t ex amitryptilin, alternativt serotonin- och noradrenalin återupptagshämmare (SNRI-preparat, exempelvis venlafaxin) och i andra hand antikonvulsiva som gabapentin och pregabalin. För dosering och behandlingsinstruktioner, se FASS. Nämnas bör att selektiva serotonin återupptagshämmare (SSRI-preparat) såsom citalopram och sertralin i stort sett inte har någon analgetisk effekt och inte ska användas vid smärtbehandling.
För ytterligare fördjupning inom detta område rekommenderas den mest aktuella svenska läroboken om Smärta och Inflammation (62).
Uppföljning och utveckling
Terapin vid RA är under snabb utveckling, och osäkerheten är betydande både kring vilka terapier som är bäst för olika patienter, vilka biverkningar som riskeras och kring långtidseffekterna (positiva och negativa) av olika terapier. Svenska reumatologer har stora möjligheter att bidra till kunskap inom alla dessa områden genom det kvalitetsregister, svensk reumatologis kvalitetsregister (SRQ) som drivs av SRF. Medverkan i detta register rekommenderas därför kraftfullt, och resultat från studier som bygger på uppföljningssystemen är viktiga för utformningen av behandlingsrekommendationerna.
Strategier för behandling med sjukdomsmodifierande antireumatiska läkemedel (DMARDs)
En översikt över behandlingsstrategier vid tidig RA och rekommendationer vid ofullständig terapieffekt, samt rekommendationer för behandling vid intolerans för metotrexat finns i två separata flödesscheman.
Låg sjukdomsaktivitet
Då tillgängliga prognostiska indikatorer är otillräckliga speciellt för att identifiera patienter med god prognos rekommenderas behandling med DMARDs till alla patienter, även de med lågaktiv sjukdom. Det saknas studier specifikt inriktade på patienter med lågaktiv sjukdom. Metotrexat är en väl dokumenterad och beprövad behandling mot RA (63), framförallt hos patienter med faktorer som indikerar dålig prognos. Alternativ för patienter med lågaktiv sjukdom är hydroxyklorokin eller sulfasalazin. För denna patientgrupp bör diagnosen fortlöpande omvärderas. Intraartikulära steroidinjektioner är en viktig kompletterande behandling.
Medelhög sjukdomsaktivitet
Primär behandling:
Metotrexat i stigande dos upp till 20-30 mg/vecka inom 4-8 veckor har vistats ha mycket god effekt vid behandling av RA (Hög evidensstyrka) (64-66). Olika startdoser (från 5-25 mg) och upptrappningsstrategier har studerats (65). Högre startdos och snabbare upptrappning ger snabbare effekt, men är i vissa, dock inte alla, studier kopplade till ökade risk för biverkningar (särskilt gastrointestinala). Individuella aspekter som ålder, njurfunktion och komorbiditet behöver vägas in vid val av start- och måldos.
Peroral behandling är i de flesta fall ett förstahandsval och den beredningsform som är mest välstuderad (66). Parenteral administration av metotrexat ger något bättre klinisk effekt än peroral behandling vid direkt jämförelse (67, 68), och kan övervägas vid otillräcklig effekt av peroral behandling, men det vetenskapliga underlaget för ett sådant förfarande är begränsat (Mycket låg evidensstyrka) (68-70). En lägre frekvens av vissa, men inte alla, biverkningar vid parenteral behandling jämfört med peroral är visad i en metaanalys (71). En retrospektiv, okontrollerad uppföljningsstudie visade att en hög andel av patienter med tidigare otillräcklig effekt eller intolerans för peroralt metotrexat kvarstod under lång tid på parenteral metotrexatbehandling (70). Det saknas dock kontrollerade studier specifikt inriktade på patienter som inte tolererat peroralt metotrexat.
Folsyrasubstitution minskar risken för biverkningar (Måttlig evidensstyrka) (72-74). Vanliga och väldokumenterade behandlingsregimer är Folsyra 5 mg, 1-2 tabletter per vecka, ej samma dag som metotrexat.
Utvärdering bör ske efter 3 månader med tolerabel maxdos metotrexat. Om inte särskilda skäl talar emot, bör behandlingen till en början kombineras med lågdos kortikosteroider (5-7.5 mg dagligen)(Måttlig till låg evidensstyrka, se särskilt avsnitt om Kortisonbehandling vid tidig RA nedan). Intraartikulär steroidbehandling är en viktig kompletterande behandling.
Vid otillräcklig effekt av metotrexat; bDMARDs och tsDMARDs:
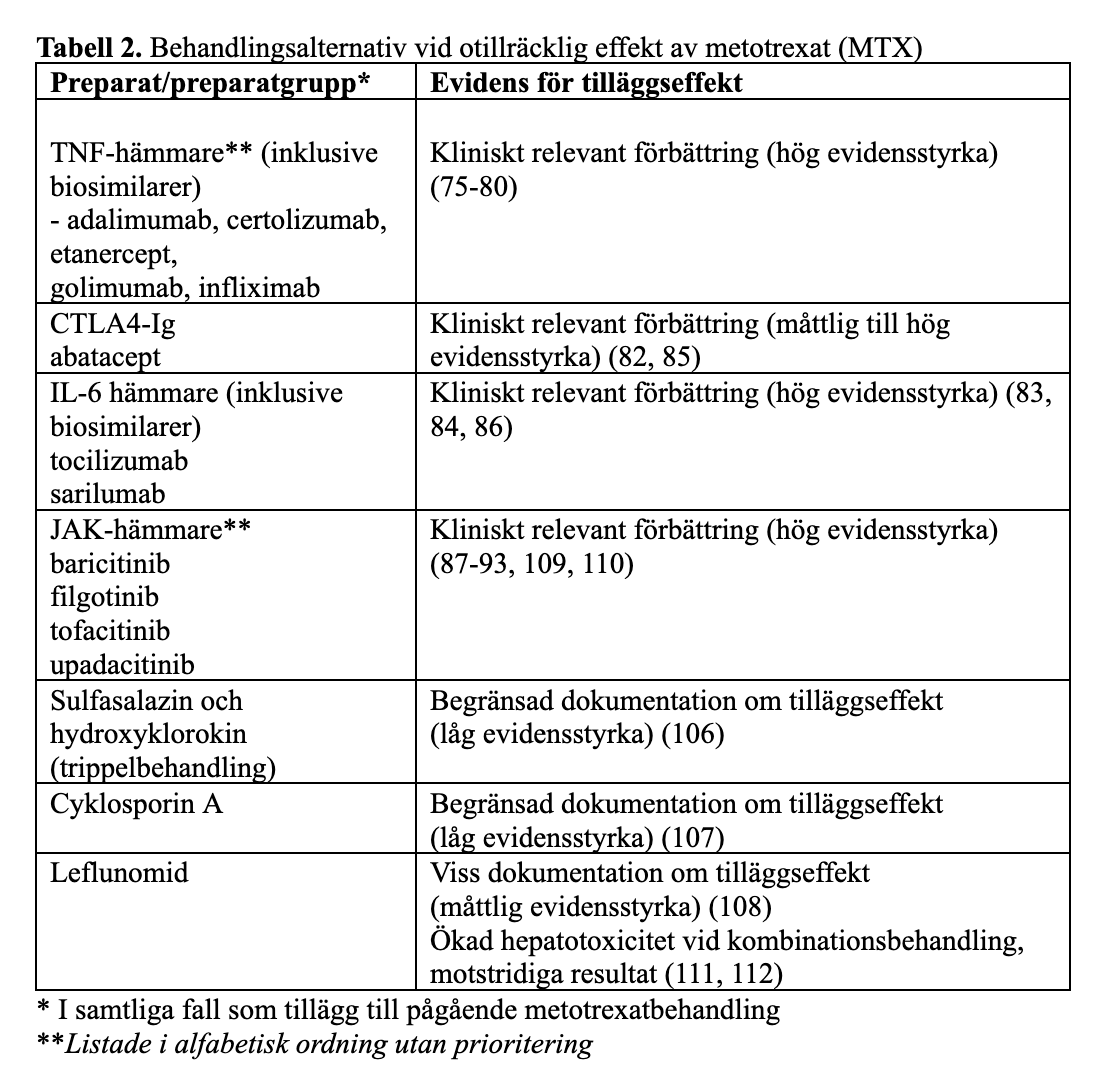
Tillägg av TNF-hämmare (Tabell 2) (Hög evidensstyrka) (75-80).
Tillägg av abatacept, tocilizumab eller sarilumab till metotrexatbehandling är alternativ till TNF-hämmare (Hög evidensstyrka) (81-86). Även tillägg av JAK-hämmare är alternativ (Hög evidensstyrka) (87-93), (Tabell 2, Tabell 3).
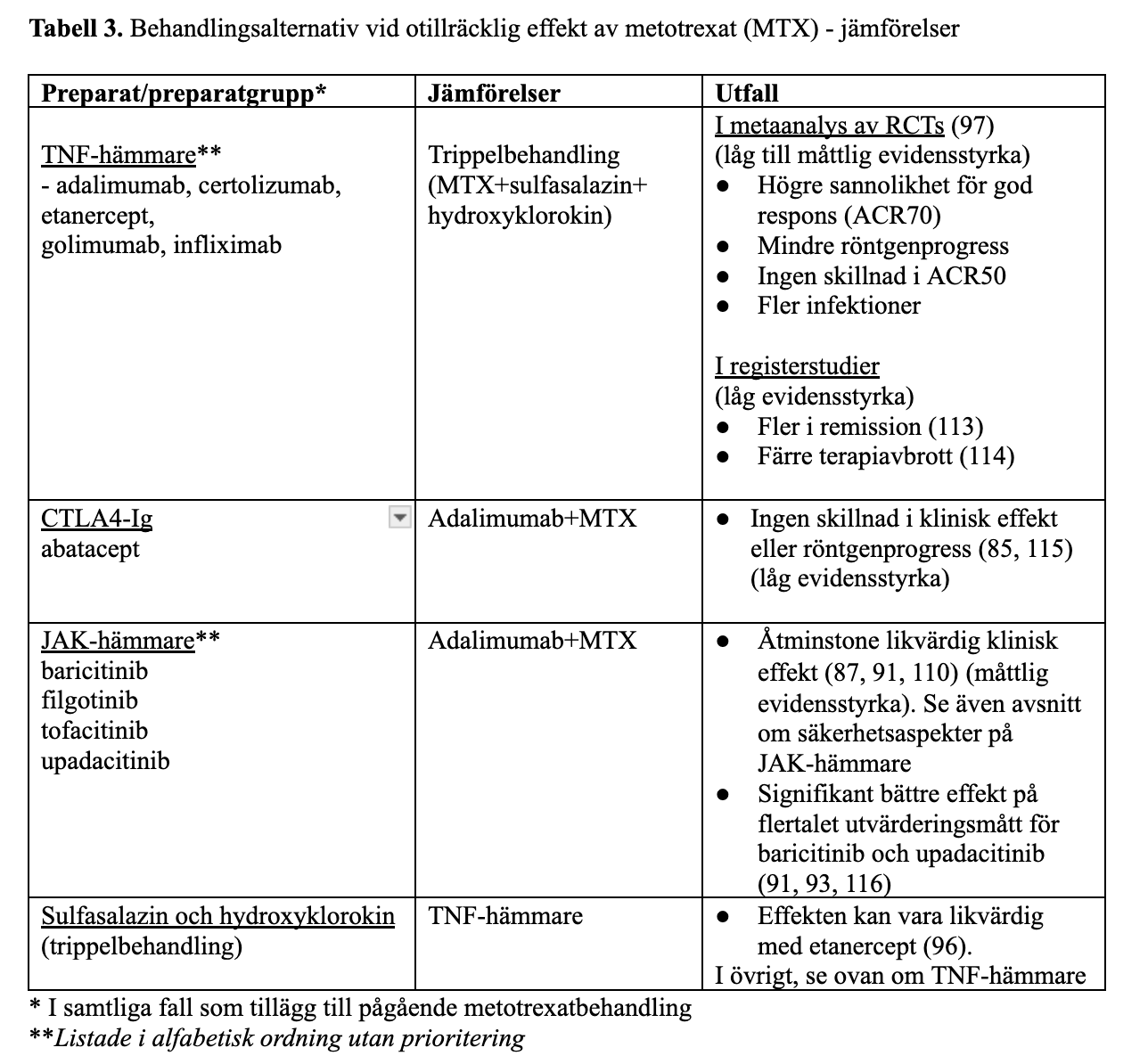
Dokumentationen är mer omfattande och visar på större effekt för bDMARDs än för kombinationer av csDMARDs i denna situation (Tabell 2). En systematisk metaanalys inkluderade tre randomiserade studier (94-96) avseende effekten av tillägg av sulfasalazin och hydroxyklorokin (så kallad trippelterapi) respektive TNF-hämmare vid otillräcklig effekt av metotrexat (97) (Tabell 3).
Hos patienter med otillräcklig effekt av metotrexat har tillägg av TNF-hämmare också dokumenterat bättre effekt mot progress av strukturella ledskador än enbart metotrexat (Måttlig evidensstyrka)(76, 98), medan motsvarande dokumentation saknas för kombinationsbehandlingar med flera olika csDMARDs.
Den samlade bedömningen utifrån studierna som ingår i metaanalysen (97) och övrig tillgänglig evidens, inklusive registerstudier (Tabell 3) blir att tillägg av TNF-hämmare till metotrexat tycks ge något bättre effekt än tillägg av sulfasalazin och hydroxyklorokin i denna situation (Låg till måttlig evidensstyrka) (81-84).
Den kliniska erfarenheten av behandling med abatacept eller tocilizumab, och den senare registrerade IL-6 receptorblockaren sarilumab, som första bDMARD vid RA i Sverige är i nuläget mindre än för TNF-hämmare, och säkerhetsdokumentationen är sammantaget mindre omfattande. (86).
JAK-hämmarna baricitinib, filgotinib, tofacitinib och upadacitinib (listade i alfabetisk ordning utan prioritering) registrerades i Sverige för behandling av RA 2017 (baricitinib och tofacitinib) respektive 2020 (upadacitinib) och 2021 (filgotinib). Den kliniska erfarenheten av långtidsbehandling med JAK-hämmare vid RA i Sverige är således ännu relativt begränsad. Det finns dock omfattande data från kliniska prövningar, och även omfattande långtidsuppföljning från dessa, framför allt för tofacitinib (99). För tofacitinib finns även flerårig klinisk erfarenhet från behandling i andra länder, t.ex. USA (100, 101). Angående säkerhetsaspekter på behandling med JAK-hämmare, se särskilt avsnitt (sidan 30).
Behandling med abatacept eller tocilizumab (listade i alfabetisk ordning utan prioritering), och även rituximab, rekommenderas hos patienter med indikation för bDMARD-behandling men absoluta eller relativa kontraindikationer för TNF-hämmare, till exempel patienter med måttlig hjärtsvikt (NYHA grad III), demyeliniserande nervsjukdom eller överlappssyndrom med drag av SLE, och vid svår hjärtsvikt (NYHA grad IV, här är dock rituximab kontraindicerat). Sarilumab är också ett alternativ hos denna patientgrupp.
Vid otillräcklig effekt av metotrexat; csDMARDs:
Vid få eller inga ogynnsamma prognostiska faktorer kan kombination av metotrexat med andra csDMARDs övervägas (102), såsom antingen sulfasalazin enbart (103) eller hydroxyklorokin enbart (104, 105). Kombinationsbehandling med metotrexat, sulfasalazin och hydroxyklorokin (så kallad trippelbehandling) dämpar sjukdomsaktivitet effektivare än behandling med ett eller två av dessa csDMARDs, men den dokumenterade erfarenheten av tilläggsbehandling till patienter med otillräcklig effekt av metotrexat är begränsad (Låg evidensstyrka) (106). (Tabell 2) (96).
Det finns även stöd för att tillägg av cyklosporin A (Låg evidensstyrka) (107) eller leflunomid (Måttlig till låg evidensstyrka) (108) har effekt i denna situation. Dokumentationen om långtidsbehandling med dessa kombinationer är dock mycket begränsad.
Vid intolerans för metotrexat:
Överväg leflunomid alternativt sulfasalazin, eventuellt kombinerat med anti-malariamedel (i första hand hydroxyklorokin, som är bäst dokumenterat). Studier av patienter med intolerans för metotrexat saknas, och dessa rekommendationer bygger på studier av sulfasalazin (117) respektive leflunomid (118) hos metotrexatnaiva patienter.
Vid intolerans, kontraindikationer för eller otillräcklig effekt av dessa preparat bör annan DMARD behandling övervägas (se Alternativa preparat, sid 15).
Vid intolerans för metotrexat och ogynnsamma prognostiska faktorer: Överväg i första hand tocilizumab, alternativt sarilumab. Resultat från en direkt jämförande studie av tocilizumab i monoterapi och adalimumab i monoterapi hos patienter med aktiv sjukdom som inte tolererade metotrexat eller där metotrexatbehandling ansågs olämplig visar bättre klinisk effekt av tocilizumab (119). Underlaget angående tocilizumab i monoterapi i denna situation bygger även på extrapolering från en studie av tocilizumab i monoterapi hos metotrexatnaiva patienter (120) och en studie av tocilizumab i monoterapi hos patienter med tidigare otillräcklig effekt av metotrexat eller annat DMARD (121). Även sarilumab har i en randomiserad studie visats vara mer effektiv än adalimumab i monoterapi (122).
JAK-hämmare (baricitinib, filgotinib, tofacitinib eller upadacitinib, listade i alfabetisk ordning utan prioritering) är alternativ. Detta baseras på extrapolering från studier där tofacitinib har använts i monoterapi vid behandling av patienter med tidigare otillräcklig effekt av eller intolerans för ≥ 1 DMARD (huvudsakligen (123) eller helt och hållet (124, 125) metotrexat), på en motsvarande studie av filgotinib i monoterapi till patienter med tidigare otillräcklig effekt av metotrexat (126), och på studier av tofacitinib eller upadacitinib (127, 128) respektive baricitinib i monoterapi hos patienter med ingen eller begränsad tidigare exposition för metotrexat (129). En systematisk översikt över studier av patienter som inte tidigare behandlats med metotrexat visar att tsDMARDs (i detta fall tofacitinib och baricitinib) i monoterapi är effektivare än enbart metotrexat, men samtidigt att kombinationsterapi med metotrexat för dessa preparat ger bättre klinisk effekt än monoterapi och bör eftersträvas (130).
Även behandling med TNF-hämmare som är registrerade för monoterapi (adalimumab, certolizumab eller etanercept, listade i alfabetisk ordning utan prioritering) kan övervägas vid intolerans för metotrexat och ogynnsamma prognostiska faktorer. Dokumentation av klinisk effekt och minskad leddestruktion på röntgen hos patienter behandlade med certolizumab finns i en studie av japanska patienter som avbrutit behandling med metotrexat på grund av biverkningar, oro för biverkningar eller otillräcklig effekt (131). Därutöver bygger rekommendationen på en studie av certolizumab i monoterapi för patienter som avbrutit tidigare DMARD behandling (i flertalet fall inkluderande metotrexat) pga otillräcklig effekt eller intolerans (132), samt studier av etanercept (133) respektive adalimumab (134) hos metotrexatnaiva patienter. Dessa data stöds även av en systematisk översikt (130), som samtidigt konstaterar att kombinationsterapi med metotrexat för dessa TNF-hämmare ger bättre klinisk effekt än monoterapi.
Vid behandling med adalimumab, certolizumab eller etanercept utan samtidigt metotrexat bör kombination med annan DMARD behandling eftersträvas, då sannolikheten för bestående effekt av TNF-hämmare tycks vara större vid sådan kombinationsbehandling (Låg evidensstyrka) (135).
Vid otillräcklig effekt av eller intolerans för förändrad/kompletterad behandling:
Vid otillräcklig effekt av behandling med TNF-hämmare: Överväg behandling med abatacept, rituximab eller tocilizumab (listade i alfabetisk ordning utan prioritering), se nedan under avsnittet bDMARDs (Måttlig evidensstyrka) (136-138). Sarilumab har också visats ge signifikant klinisk effekt hos patienter med otillräcklig effekt eller intolerans för behandling med TNF-hämmare (139).
Behandling med JAK-hämmare (baricitinib, filgotinib, tofacitinib, eller upadacitinib, (listade i alfabetisk ordning utan prioritering) (måttlig evidensstyrka) (140, 141) eller byte till en andra TNF-hämmare (Låg evidensstyrka) (142-144) är alternativ. Beakta säkerhetdata vid behandling av riskpopulationer med JAK-hämmare (se sid 31)!
Vid intolerans för behandling med TNF-hämmare rekommenderas byte till annan TNF-hämmare (se nedan), alternativt behandling med abatacept, rituximab, sarilumab eller tocilizumab (listade i alfabetisk ordning utan prioritering) eller JAK-hämmare.
Hos patienter som har otillräcklig effekt av kombinationsbehandling med csDMARDs, eller intolerans för sådan behandling, bör bDMARDs (TNF-hämmare alternativt abatacept eller tocilizumab (listade i alfabetisk ordning utan prioritering)) övervägas vid högaktiv sjukdom eller tecken på progredierande leddestruktion. I annat fall kan ytterligare behandlingsförsök med andra csDMARDs i kombination eller monoterapi övervägas.
Hög sjukdomsaktivitet
Rekommendationerna överensstämmer i stora drag med dem vid medelhög sjukdomsaktivitet, med undantag av val av första DMARD-behandling, där kombinationsbehandling med metotrexat och TNF-hämmare (eller andra bDMARDs, se nedan) eller med sulfasalazin och hydroxyklorokin kan övervägas. SRFs riktlinjer skiljer sig härvidlag från EULARs och ACRs, som rekommenderar metotrexat i monoterapi som startbehandling för alla patienter med RA (som inte har kontraindikationer). SRFs tolkning baseras på evidens som indikerar att subgrupper av RA patienter kan ha god nytta av kombinationsbehandling, framför allt bDMARDs och metotrexat vid högaktiv tidig sjukdom med dålig prognos.
Kombinationsbehandling med metotrexat, sulfasalazin, hydroxyklorokin och lågdos kortison har bättre effekt än sekventiell monoterapi med sulfasalazin följt av andra csDMARDs på sjukdomsaktivitet och leddestruktion (Låg evidensstyrka) (145, 146), med bibehållen god effekt vid långtidsuppföljning under upp till 11 år (147), varför det är ett alternativ för denna patientgrupp. Direkta jämförelser mellan denna kombinationsbehandling och behandling med metotrexat plus lågdos kortison saknas.
I en öppen, randomiserad studie av patienter med tidig RA och måttlig till hög sjukdomsaktivitet (huvudsakligen genomförd i de nordiska länderna, NORD-STAR studien) (148) gav konventionell behandling (metotrexat tillsammans med något av intial prednisolonbehandling, sulfasalazin+hydroxyklorokin eller frekventa intraartikulära steroidinjektioner enligt särskilt protokoll) klinisk remission efter 1 år i lägre utsträckning än metotrexat i kombination med abatacept eller certolizumab, medan skillnaden gentemot tocilizumab + metotrexat inte var statistiskt säkerställd(149).
TNF-hämmare
TNF-hämmare i kombination med metotrexat, eventuellt initialt kombinerat med lågdos kortikosteroidbehandling enligt ovan (sid 9), rekommenderas för patienter med flera faktorer som indikerar ogynnsam prognos (Hög till måttlig evidensstyrka) (134, 150-152), till exempel för patienter med tidigt påvisade erosioner på röntgen tillsammans med positiv RF eller anti-CCP eller kraftigt förhöjd CRP/SR. Det bör understrykas att detta avser en liten grupp bland alla patienter med nydebuterad RA.
TNF-hämmarna adalimumab, certolizumab, etanercept, golimumab och infliximab (listade i alfabetisk ordning utan prioritering) har dokumenterad effekt vid hög sjukdomsaktivitet och ogynnsam prognos och är registrerade för motsvarande indikation.
Den potentiella fördelen med tidig behandling med TNF-hämmare är störst hos patienter med snabbt progredierande leddestruerande sjukdom. Direkta jämförelser vid tidig RA har visat att kombination av TNF-hämmare och metotrexat har en bättre sjukdomsdämpande effekt än metotrexat enbart för patienter med hög sjukdomsaktivitet (Hög till måttlig evidensstyrka) (134, 150-153).
Det saknas direkta jämförelser mellan omedelbart initierad behandling med TNF-hämmare och metotrexat och behandling som inleds med metotrexat och kompletteras med TNF-hämmare efter kort tid (< 6 månader). I en randomiserad, kontrollerad studie som hade detta grundupplägg ingick också utsättning av TNF-hämmare vid låg sjukdomsaktivitet (tidigast redan efter 12 veckors behandling) och nedtrappning av metotrexat vid klinisk remission (154). Man fann inte några skillnader mellan behandlingsstrategierna efter 1 år (154), men dessa resultat har tveksam relevans för klinisk praxis, där behandlingen ofta fortsättes under längre tid efter uppnådd låg sjukdomsaktivitet/remission.
I en post-hoc analys från en studie av patienter med tidig RA, hög sjukdomsaktivitet och ogynnsam prognos som inte svarat tillfredställande på metotrexat gav tillägg av öppen behandling med adalimumab förbättring av samma storleksordning som initial, dubbelblind behandling med adalimumab och metotrexat (155).
Andra bDMARDs:
Abatacept och tocilizumab har båda godkända indikationer enligt FASS som innefattar aktiv och progressiv RA som inte har behandlats med metotrexat tidigare. Det finns stöd för att abatacept kan ge god klinisk effekt (Måttlig till Hög evidensstyrka) och minskad progress av leddestruktion (Måttlig evidensstyrka) i kombination med metotrexat som första linjens behandling hos patienter med hög sjukdomsaktivitet och ogynnsam prognos (156, 157). Det finns även stöd för att tocilizumab kan ge god klinisk effekt i monoterapi eller i kombination med metotrexat (Måttlig till Hög evidensstyrka), och minskad progress av leddestruktion i kombination med metotrexat (Måttlig evidensstyrka) som första linjens behandling hos patienter med hög sjukdomsaktivitet och ogynnsam prognos(158, 159). Baserat på denna evidens och NORD-STAR studien (se ovan) kan abatacept och tocilizumab vara alternativ för behandling av denna patientgrupp.
Det saknas i dagsläget data om behandling med sarilumab i denna situation, och preparatet är inte registrerat för användning som första linjens behandling utan tidigare DMARD-behandling.
Vid tidig insättning av biologiskt läkemedel är det av särskilt stor vikt att behandlingseffekt och biverkningar följs upp på ett strukturerat sätt i SRQ och att dosminskning, och möjligen utsättning, övervägs vid långtidsremission (se särskilda avsnitt nedan).
Vid otillräcklig effekt eller intolerans för behandling enligt ovan följer rekommendationerna väsentligen dem vid medelhög initial sjukdomsaktivitet (se även flödesschema i separata illustrationer). Även här är abatacept och tocilizumab/sarilumab samt JAK-hämmare alternativ till TNF-hämmare för patienter som börjat med metotrexat utan bDMARD.
Kombination av csDMARDs
En studie visade att kombinationsbehandling med metotrexat, sulfasalazin, hydroxyklorokin och högdos steroider (initialt 60 mg prednisolon, snabb nedtrappning) kan ha en effekt på sjukdomsaktivitet och leddestruktion vid tidig RA som liknar den för kombinationen av metotrexat och TNF-hämmare (Låg evidensstyrka) (160). En dubbelblind, direkt jämförande studie visade likartad klinisk effekt efter 6 månader av etanercept i kombination med metotrexat och behandling med metotrexat, sulfasalazin och hydroxyklorokin (95).
Kombinationsbehandling med metotrexat, sulfasalazin, hydroxyklorokin, eventuellt tillsammans med lågdos kortison (≤7.5 mg, ej högre), är således ett alternativ för denna patientgrupp.
Alternativa preparat
Utöver de preparat som angetts ovan, finns ett antal som kan komma till användning som alternativ. Cyklosporin A är registrerat för behandling av RA och har dokumenterad effekt på progress av ledskador vid röntgenundersökning (Hög evidensstyrka) (161), men användningen har begränsats av bristande långtidstolerabilitet (162). För azatioprin finns en hel del erfarenhet som talar för en viss men begränsad klinisk effekt, och preparatet har indikationen ”svår aktiv reumatoid artrit som inte kan kontrolleras med mindre toxiska substanser (DMARDs)”. Behandling med mycofenolatmofetil förekommer vid RA, men preparatet är inte registrerat för denna indikation. Anakinra diskuteras i ett separat stycke nedan (sid 21).
TNF-hämmare
Val av TNF-hämmare
Fem originalpreparat som specifikt hämmar tumör nekros faktorn (TNF) är registrerade för behandling av RA – adalimumab (registrerat 2003), certolizumab (registrerat 2010), etanercept (registrerat 2000), golimumab (registrerat 2010) och infliximab (registrerat 1999) (listade i alfabetisk ordning utan prioritering). För adalimumab, etanercept och infliximab (listade i alfabetisk ordning utan prioritering) finns dessutom biosimilarer (se särskilt avsnitt).
Tillgängliga data från kliniska prövningar ger inte stöd för att någon TNF-hämmare är mer effektiv än någon annan (78, 163). I EXXELERATE-studien jämfördes certolizumab (n= 457) och adalimumab (n=458) som tillägg till metotrexat vid behandling av RA (164). Vid utvärdering av det primära utfallsmåttet (efter 12 veckor) fanns ingen skillnad i respons avseende ACR 20/50/70 mellan de båda behandlingsgrupperna. Effekt var likartad vid uppföljning efter 2 år. Vid otillräcklig effekt av den första TNF-hämmaren (efter 12 veckor; oavsett om det var certolizumab eller adalimumab) uppnådde 58% respektive 62% låg sjukdomsaktivitet vid byte till den andra. Inga skillnader mellan de båda preparaten noterades avseende svårighetsgraden av biverkningar eller biverkningsmönstret (164).
En metaanalys av 44 randomiserade kontrollerade studier av TNF-hämmare vid RA visade dock en signifikant lägre risk att avbryta behandling med etanercept jämfört med placebo eller csDMARDs på grund av ogynnsamma händelser, medan denna risk var ökad jämfört med placebo/csDMARDs för adalimumab, certolizumab och infliximab (165). Två observationella registerstudier från Skandinavien (utgående från det danska registret DANBIO (166) respektive ARTIS i Sverige (167)) med uppföljningstid upp till 5 år, har liksom flera andra europeiska registerstudier (168-173), visat att en större andel av RA-patienter utan tidigare bDMARD-behandling som behandlas med etanercept än patienter som behandlas med infliximab kvarstår på behandlingen vid uppföljningstidens slut. Man har funnit ett likartat mönster i analys av patienter utan samtidig behandling med csDMARDs, med sämre behandlingsöverlevnad för infliximab än för etanercept, och intermediär behandlingsöverlevnad för adalimumab (173).
Två registerstudier från USA visar delvis avvikande resultat (174, 175). I RADIUS studien (174) fann man ingen skillnad i behandlingsöverlevnad mellan infliximab/etanercept/adalimumab efter 48 månader, men signifikant färre etanercept-behandlade avbröt pga biverkningar. En enda studie visade högre andel avbrott i behandlingen för adalimumab och etanercept jämfört med infliximab (175). Slutligen visade en metaanalys av publicerade observationsstudier en signifikant lägre risk att avbryta behandling med etanercept jämfört med infliximab respektive adalimumab vid uppföljning under 3-4 år (176).
Skillnader i behandlingstraditioner och ersättningssystem för behandling mellan olika länder kan tänkas påverka resultaten. Studierna är inte randomiserade, och möjligheten att justera för relevanta confounders varierar mellan studierna. Sammantaget tycks patienter kvarstå längre på behandling med etanercept än med infliximab vid insättning av en första TNF-hämmare vid RA (Låg evidensstyrka). Två stora nordiska studier har visat en intermediär behandlingsduration för adalimumab i förhållande till etanercept och infliximab (166, 167) vilket även var konklusionen i metaanalysen som nämns ovan (Låg evidensstyrka) (176). När det gäller jämförelser mellan TNF-hämmarna i observationsstudier av kliniska effektparametrar är det vetenskapliga underlaget otillräckligt för att dra slutsatser (Mycket låg evidensstyrka).
Det finns begränsat med data från studier av TNF-hämmarna certolizumab och golimumab i kliniska register (176) och i förskrivningsdatabaser (177, 178). I en registerstudie från Finland var sannolikheten att avbryta behandling vid RA med golimumab lägre än för certolizumab och infliximab, och jämförbar med adalimumab och etanercept (179).
Tillgängliga studier ger ett otillräckligt underlag för slutsatser om skillnader i effekt för certolizumab och golimumab jämfört med andra TNF-hämmare (Mycket låg evidensstyrka).
Sammanfattningsvis finns begränsat med data om jämförelse mellan TNF-hämmare vid RA. I de flesta observationsstudier är det fler patienter som avbryter behandling med infliximab jämfört med etanercept.
I valet mellan preparaten bör även tillgänglig erfarenhet av enskilda preparat samt kostnader och lokala resurser vägas in.
Att enbart på grund av kostnadsskäl genomföra byte från ett originalpreparat till en biosimilar tillhörande ett annat originalpreparat rekommenderas ej.
Kombination med csDMARDs
Kombination av TNF-hämmare och metotrexat har i flera studier av patienter med tidig, högaktiv RA visat sig vara effektivare än monoterapi med metotrexat (Hög evidensstyrka) (134, 150-152). Adalimumab och etanercept (listade i alfabetisk ordning utan prioritering) kan ges som monoterapi, men effekten för dessa TNF-hämmare är bättre i kombinationsterapi med metotrexat både vad avser inflammationsdämpning och destruktionshämning (Måttlig evidensstyrka) (77, 78, 133). Även certolizumab är, baserat på kliniska studier (132), registrerat för monoterapibehandling.
TNF-hämmare har använts i kombination med andra DMARDs än metotrexat, inklusive sulfasalazin, leflunomid och azatioprin. Registerstudier visar att långtidseffekt och tolerabilitet är bättre vid dessa kombinationer än vid monoterapi med TNF-hämmare (135) (Låg evidensstyrka). Visst stöd finns för att leflunomid i kombination med TNF-hämmare kan ha likvärdig effekt och tolerabilitet som kombinationen metotrexat och TNF-hämmare (180, 181) (Låg evidensstyrka) (För information om godkända indikationer i monoterapi, se Appendix 7).
Patienter med otillräcklig effekt eller intolerans för TNF-hämmare
Vid behandling med TNF-hämmare bör man vara uppmärksam på att en del patienter uppnår partiell respons vid 3 månader och definitiv utvärdering kan ibland anstå till 6 månader efter insatt behandling. Randomiserade placebokontrollerade studier har visat att behandling med abatacept (Måttlig evidensstyrka), rituximab (Måttlig evidensstyrka) och tocilizumab (Måttlig evidensstyrka) (136-138) (listade i alfabetisk ordning utan prioritering) har effekt hos patienter med inadekvat respons på TNF-hämmare. Motsvarande evidens finns även för sarilumab (139) och för JAK-hämmarna baricitinib (141), filgotinib (109), tofacitinib (140) och upadacitinib (182) (listade i alfabetisk ordning utan prioritering).
Observationsstudier och klinisk erfarenhet talar för att behandling med en andra TNF-hämmare också kan vara effektiv (Låg evidensstyrka) (142, 143), kanske framför allt hos patienter med sekundär svikt (försämring efter en initial förbättring) på infliximab (Mycket låg evidensstyrka) (183). Detta stöds även av en randomiserad kontrollerad studie som visade att golimumab hade bättre effekt än placebo hos patienter som tidigare behandlats med någon annan TNF-hämmare (144) (Låg till måttlig evidensstyrka), och av explorerande analyser i en studie av patienter som, efter att inte uppnått signifikant klinisk förbättring efter 12 veckor i en randomiserad, dubbelblind studie, bytte från initialbehandlingen med adalimumab eller certolizumab till den andra TNF-hämmaren (164).
Det vetenskapliga underlaget för att öka dosen av infliximab eller för att korta ner behandlingsintervallet vid otillräcklig effekt är begränsat (184-189). Det finns även begränsat vetenskapligt stöd för nyttan av nedkortat behandlingsintervall till varje vecka för behandling med adalimumab i monoterapi för patienter med etablerad RA (134, 190). Med tanke på den svaga evidensen (191), och bättre underlag för byte till annan bDMARD, rekommenderas inte dosökning av TNF-hämmare eller nedkortat behandlingsintervall i denna situation.
Visst stöd finns för att effekten av rituximab kan vara bättre än den som uppnås av byte av TNF-hämmare (192, 193), i synnerhet för seropositiva patienter med bristande effekt av den första TNF-hämmaren (194). En randomiserad öppen studie visade att vid ofullständig effekt av en första TNF-hämmare, där majoriteten av patienterna upplevt sekundär svikt efter i genomsnitt två år, var byte av verkningsmekanism (till abatacept, rituximab eller tocilizumab) mer effektivt för att uppnå EULAR respons jämfört med en andra TNF-hämmare (69% versus 52% efter 24 veckor) (195). Liknande resultat ses i en svensk registerstudie där byte från första TNF-hämmare till rituximab eller tocilizumab gav god EULAR respons efter ett år, vilket inte sågs vid byte till annan TNF-hämmare eller abatacept (196). En kanadensisk registerstudie visar på att abatacept som andra biologisk behandling hade signifikant bättre läkemedelsöverlevnad efter nio år jämfört med en andra TNF-hämmare (medelbehandlingstid (SD) för abatacept:4.80 (0.45) år jämfört med för anti-TNF: 2.82 (0.24) år, p<0.001)(197).
Sammantaget finns visst vetenskapligt stöd för att rekommendera byte av verkningsmekanism vid otillräcklig effekt av en första TNF-hämmare, varför det rekommenderas enligt ovan. Dosökning av infliximab vid otillräcklig effekt rekommenderas inte.
Vid intolerans för någon TNF-hämmare kan man i de flesta fall byta till någon av de övriga (Låg evidensstyrka) (142-144). Registerdata talar för att effekten i detta fall kan vara bättre än vid byte till annan TNF-hämmare efter terapisvikt (143).
Icke anti-TNF biologiska DMARDs (bDMARDs)
Abatacept
Abatacept, ett humant fusionsprotein som modifierar kostimulering vid antigenpresentation och därmed hämmar T-cellsaktivering, registrerades 2007 (med ändrad indikation 2010 samt 2016) ” i kombination med metotrexat för behandling av måttlig till svår aktiv RA hos vuxna patienter som svarat otillräckligt på tidigare behandling med en eller flera sjukdomsmodifierande läkemedel (DMARDs), inklusive metotrexat eller en TNF-hämmare”, och för ”behandling av högaktiv och progressiv sjukdom hos vuxna patienter med reumatoid artrit som inte tidigare behandlats med metotrexat”. Abatacept är registrerat för såväl intravenös som subkutan behandling. Enligt registreringstexten kan subkutan behandling föregås av en inledande intravenös bolusdos, men det finns dokumentation om klinisk effekt som är likvärdig med annan biologisk behandling i frånvaro av en sådan bolusdos (85).
Abataceptbehandling i förhållande till andra bDMARDs
Abatacept får inte kombineras med andra biologiska preparat eftersom risken för allvarliga biverkningar, främst infektioner, då visats vara ökad (198). Kunskap om behandling med abatacept efter rituximab-behandling är begränsad (199). Visst stöd finns för att behandling med annat biologiskt preparat kan starta innan B-cellsnivåerna normaliserats utan ökad risk för allvarlig infektion (200) (Mycket låg evidensstyrka).
Abataceptbehandling i förhållande till andra bDMARDs
Abatacept får inte kombineras med andra biologiska preparat eftersom risken för allvarliga biverkningar, främst infektioner, då visats vara ökad (198). Kunskap om behandling med abatacept efter rituximab-behandling är begränsad (199). Visst stöd finns för att behandling med annat biologiskt preparat kan starta innan B-cellsnivåerna normaliserats utan ökad risk för allvarlig infektion (200) (Mycket låg evidensstyrka).
Abataceptbehandling – Jämförelser med andra bDMARDs
I en randomiserad studie av patienter med inadekvat respons på metotrexat, men ingen tidigare biologisk behandling, var effekten av både abatacept och infliximab bättre än placebo (201). Studien var inte primärt upplagd för att jämföra abatacept och infliximab, men efter 12 månaders uppföljning var förbättringen i sjukdomsaktivitet signifikant större i abatacept-gruppen än i den grupp som behandlades med infliximab.
I en direkt jämförande randomiserad kontrollerad studie av abatacept som subkutan injektion och adalimumab, båda i kombination med metotrexat, fann man ingen skillnad i klinisk effekt eller effekt på progress av ledskador på röntgen efter ett års uppföljning (Låg evidensstyrka) (85). Det fanns inga betydande skillnader i tid till effekt eller förekomst av allvarliga biverkningar mellan preparaten (85). Vid tvåårsuppföljning i studien var det alltjämt ingen skillnad i klinisk eller radiografisk effekt, men färre patienter i abatacept-gruppen avbröt behandlingen på grund av biverkningar (115).
Rituximab
Rituximab, en kimär monoklonal antikropp mot CD20 antigen på B-celler, är sedan 2006 registrerat för behandling ”i kombination med metotrexat av vuxna patienter med svår aktiv RA som har haft ett otillräckligt svar eller är intoleranta mot andra sjukdoms-modifierande antireumatiska läkemedel inklusive behandling med en eller flera TNF-hämmare” (202). Det finns långvarig erfarenhet av rituximab från behandling av B-cellslymfom.
Det finns också en jämförande studie där rituximab använts som första bDMARD (dvs utanför registrerad indikation) för RA. I denna öppna, randomiserade studie med non-inferiority design jämfördes TNF-hämmare (adalimumab eller etanercept) och rituximab som första bDMARD till RA patienter med otillräcklig effekt av csDMARDs. Rituximab gavs som startdos 2×1000 mg samt efter 26 veckor vid persisterande sjukdomsaktivitet. Inga skillnader i kliniskt utfall sågs mellan grupperna efter 1 år (203).
Dosering av rituximab
Flera studier har försökt fastställa optimal dosering med rituximab. Dosen 2×500 mg har studerats som alternativ till den rekommenderade 2×1000 mg hos patienter som tidigare behandlats med DMARD eller TNF-hämmare (204-207). För några kliniska effektmått, men inte för andra, utfaller dosen 2×1000 mg signifikant bättre i en av de relevanta studierna (204), men inte i den andra (205), men numeriskt uppnår fler patienter god respons med 2×1000 mg än med 2×500 mg i bägge studierna. Utanför registrerad indikation har bionaiva patienter som sviktat på metotrexat uppvisat likartad klinisk effekt av rituximab i doserna 2×1000 mg och 2×500 mg vid uppföljning efter 6-12 månader (208, 209).
När det gäller destruktionsutveckling finns det dock indikationer på att rituximab, i kombination med metotrexat, i dosen 2×1000 mg på kort sikt (upp till ett år) hindrar röntgenprogress bättre än dosen 2×500 mg, baserat på en studie av en population med tidig, aktiv RA utan tidigare metotrexat behandling (210). Hos tidigare TNF-hämmarbehandlade patienter som svarat på en första behandling med rituximab 2×1000 mg kan återbehandling med dosen 1×1000 mg ge likartad klinisk respons som 2×1000 mg. Röntgenologiska data saknas (211).
Intervall mellan rituximab-behandlingar
Tiden för kvarstående terapieffekt varierar mellan olika patienter. I FASS texten anges att behovet av ny behandlingsomgång bör utvärderas efter 24 veckor och att behandling upprepas vid detta tillfälle om patienten svarat på behandlingen men har kvarstående sjukdomsaktivitet. I annat fall följs patienten och återbehandling ges vid tecken på återkommande sjukdomsaktivitet. För patienter som inte svarat på behandlingen inom 24 veckor ska i första hand alternativ behandling övervägas. Visst stöd finns för att seropositiva patienter som inte svarat på en första behandlingsomgång kan få effekt av en andra kur, troligen på grund av en mer komplett B-cellsdepletion (204, 208, 212).
Tillgängliga resultat tyder på att fast återbehandling vid 24 veckor kan medföra bättre sjukdomskontroll än symtomstyrd återbehandling (204, 205, 213). Inga uppgifter finns om utfallet av andra (t.ex individualiserade) fasta intervall mellan återbehandlingarna. Observationsdata tyder på att symptomstyrd återbehandling leder till att rituximabinfusioner efter hand kan ges med längre intervall (214).
Sammanfattningsvis kan en rimlig strategi vara initialbehandling med rituximab 2×1000 mg var 6:e månad till remission eller önskat behandlingsmål och därefter kan en mer individualiserad regim avseende dos och doseringsintervall övervägas, varvid man bör sträva efter lägsta effektiva dos vid långtidsbehandling (se även avsnitt om Säkerhetsapekter).
Kombinationsbehandling vid rituximab
Dokumentation om kombinationsbehandling med annat DMARD än metotrexat är begränsad. Stöd finns för att leflunomid fungerar i denna situation (215).
Visst stöd finns för att behandling med annat biologiskt preparat kan starta innan B-cellsnivåerna normaliserats utan ökad risk för allvarlig infektion (200) (Mycket låg evidensstyrka).
IL-6 hämning (tocilizumab och sarilumab)
Två IL-6 (interleukin 6) hämmande preparat finns nu registrerade av EMA, tocilizumab och sarilumab. Tocilizumab är en humaniserad monoklonal antikropp som binder till IL-6 receptorn, och mest välstuderat av de båda IL-6 hämmarna. Tocilizumab registrerades 2009 för intravenös behandling och
2014 även för subkutan administrering (dosering en gång/vecka). Tocilizumab är indicerat för ”behandling av svår, aktiv och progressiv reumatoid artrit (RA) hos vuxna som inte har behandlats med metotrexat tidigare” och för ”behandling av måttlig till svår aktiv reumatoid artrit (RA) hos vuxna patienter som antingen inte har haft tillräcklig effekt av eller som inte tolererat tidigare behandling med en eller flera sjukdomsmodifierande antireumatiska läkemedel (DMARDs) eller tumörnekrosfaktor-(TNF)-hämmare”. Klinisk effekt och säkerhet har visat sig vara jämförbara mellan den intravenösa och den subkutana behandlingen hos patienter med samtidig behandling med metotrexat (216).
Sarilumab är en human monoklonal antikropp mot IL-6 receptorn, som godkändes 2017 för ”behandling av måttlig till svår aktiv reumatoid artrit (RA) hos vuxna patienter som antingen inte har haft tillräcklig effekt av eller som inte tolererat tidigare behandling med en eller flera sjukdomsmodifierande antireumatiska läkemedel (DMARDs)”. Sarilumab har längre halveringstid än tocilizumab och ges subkutant varannan vecka. Flera studier har påvisat god effekt hos såväl metotrexat-nonresponders som anti-TNF-nonresponders (86, 139, 217, 218), biverkningsprofilen har visat sig vara jämförbar med tocilizumab (86) och långtidsuppföljning har inte indikerat nya biverkningssignaler (219).
Monoterapi och kombinationsbehandling – tocilizumab/sarilumab
Tocilizumab kan enligt registreringstexten ges som monoterapi vid intolerans mot metotrexat eller när fortsatt behandling med metotrexat är olämplig, och rekommenderas i denna situation som ett alternativ för patienter som debuterar med hög sjukdomsaktivitet eller medelhög sjukdomsaktivitet med ogynnsamma prognostiska faktorer (158, 159). På kort sikt förefaller effekten vara likartad för flertalet kliniska utfallsmått för tocilizumab i monoterapi jämfört med i kombination med metotrexat (220, 221), vilket även är visat i ett par observationsstudier (222, 223) och i en systematisk översikt (130). En studie från 2016 har dock visat snabbare inflammationsdämpning och bättre prevention av leddestruktion med tocilizumab i kombination med metotrexat jämfört med tocilizumab i monoterapi (224). I en observationsstudie som innefattade data från 8 olika nationella register var det färre som kvarstod under lång tid på behandling med tocilizumab i monoterapi jämfört med tocilizumabbehandling i kombination med något csDMARD(225).
Sarilumab är mindre studerat än tocilizumab, men i en jämförande studie hade monoterapi med sarulimab bättre klinisk effekt än adalimumab (122). Liksom tocilizumab är sarilumab registrerat för monoterapi vid intolerans mot metotrexat (Appendix 7). Till skillnad från tocilizumab är sarilumab ej registrerat för behandling av DMARD-naiva patienter.
Särskilda aspekter på IL-6 hämning
Långtidserfarenheten av behandling med tocilizumab är mer begränsad än för TNF-hämmare. En prospektiv observationell multicenterstudie jämförde utfallet efter ett års behandling med TNF-hämmare eller tocilizumab hos patienter med otillräcklig effekt av csDMARDs (226). Patienterna som behandlades med tocilizumab med eller utan metotrexat hade kortare sjukdomsduration och högre sjukdomsaktivitet, jämfört med patienter behandlade med TNF-hämmare med eller utan metotrexat. En större förbättring i flertalet kliniska utfallsmått observerades i tocilizumabgruppen (226). I en europeisk registerstudie sågs ingen skillnad i effekt mellan tocilizumab vs TNF-hämmare, vare sig i monoterapi eller i kombination med metotrexat (227). Svenska registerdata visade dock på bättre 1-årsutfall för tocilizumab jämfört med TNF-hämmare(196).
Det finns begränsad erfarenhet av behandling med tocilizumab efter behandling med abatacept eller rituximab. En explorerande studie av ett begränsat antal patienter med aktiv sjukdom trots kvarstående B-cellsdepletering i blodet ett år efter rituximab-behandling visade dock en signifikant klinisk förbättring efter behandling med tocilizumab, men inte med abatacept (228). Det finns inga publicerade data angående behandling med sarilumab efter behandling med abatacept eller rituximab.
Det saknas kunskap om kombinationsbehandling med tocilizumab eller sarilumab och andra biologiska läkemedel.
Genom tocilizumabs förmåga att hämma IL-6 medierad aktivering reduceras snabbt och effektivt akuta fasreaktanter av behandlingen. Remission, definierat som DAS28<2.6, uppnås därför av relativt fler patienter jämfört med andelen av patienter som uppnår remission vid mätning av sjukdomsaktivitetsmått där akuta fasreaktanter har mindre (SDAI) eller ingen betydelse (CDAI). Vid jämförelse av påverkan på sjukdomsaktiviteten mellan olika biologiska läkemedel där inte alla har lika uttalad effekt på akuta fasreaktanter får man ha detta i åtanke (229). Dessa aspekter är tillämpliga även för det senare introducerade sarilumab.
Anakinra
Anakinra är en interleukin-1 receptorantagonist, och är registrerad 2002 för ”användning i kombination med metotrexat för behandling av symtom hos patienter med reumatoid artrit som svarat otillräckligt på behandling med enbart metotrexat”. Kliniska studier har dokumenterat inflammationsdämpande och destruktionshämmande effekter (Måttlig till Hög evidensstyrka) (230). Indirekta jämförelser talar för att sannolikheten för klinisk respons hos patienter med otillräcklig effekt av metotrexat är lägre vid behandling med anakinra och metotrexat än vid behandling med TNF-hämmare och metotrexat (Låg evidensstyrka) (78). Anakinra kan vara ett alternativ när andra biologiska läkemedel inte har avsedd effekt, inte tolereras eller är kontraindicerade, men det saknas studier med preparatet inriktade på denna patientpopulation, varför andra, bättre dokumenterade strategier rekommenderas i första hand (se ovan).
”Targeted” syntetiska DMARDS (tsDMARDs)
Baricitinib, filgotinib, tofacitinib och upadacitinib är tsDMARDs för oralt bruk av klassen januskinas (JAK)-hämmare, som blev tillgängliga i Sverige under 2017 respektive 2020 (upadacitinib) och 2021 (filgotinib). Baricitinib hämmar huvudsakligen JAK1 och JAK2, medan tofacitinib har sin huvudsakliga effekt på JAK1 och JAK3 och filgotinib och upadacitinib huvudsakligen hämmar JAK1.
Barictinib, filgotinib och upadacitinib är indicerade för ”behandling av måttlig till svår aktiv reumatoid artrit hos vuxna patienter med otillräckligt behandlingssvar på eller intolerans mot ett eller flera sjukdomsmodifierande antireumatiska läkemedel (DMARDs).” De kan enligt registreringstexterna ”användas som monoterapi eller i kombination med metotrexat”.
Registreringstexten anger att tofacitinib ”i kombination med metotrexat är indicerat för behandling av måttlig till svår aktiv reumatoid artrit hos vuxna patienter när ett eller flera sjukdomsmodifierande antireumatika (DMARDs) inte haft tillräcklig effekt eller gett biverkningar.” Tofacitinib kan enligt registreringstexten ges ”som monoterapi vid intolerans mot metotrexat eller om fortsatt behandling med metotrexat är olämplig”.
Enligt beslut av Tandvårds- och Läkemedelsförmånsverket subventioneras JAK-hämmarna endast när behandling med TNF-hämmare gett otillräcklig effekt eller inte är lämplig.
Effekten av JAK-hämmare finns dokumenterad såväl hos patienter med aktiv sjukdom trots tidigare behandling med bDMARDs (140, 141, 182) som hos bDMARD-naiva patienter med otillräcklig effekt av csDMARDs (87-93, 109, 110). Det finns begränsad dokumentation i kliniska prövningar av behandling av patienter som behandlats med andra bDMARDs än TNF-hämmare (141, 182, 231).
I en dubbelblind jämförelse av upadacitinib och abatacept (intravenös behandling) till patienter med otillräcklig effekt av ≥ 1 bDMARD var förbättringen av DAS28-CRP och andelen med DAS28-CRP < 2.6 större efter 12 veckor bland dem som behandlades med upadacitinib (231). Den största skillnaden för delkomponenterna i DAS28-CRP observerades för CRP. Skillnaderna mellan grupperna var mindre efter 24 veckor än efter 12 veckor. Fler patienter drabbades av allvarlig händelse, trombos eller leverpåverkan bland dem som behandlats med upadacitinib (231).
I en nationell svensk observationsstudie var förbättringen i patientrapporterad smärta, justerad för sjukdomskaraktäristika, komorbiditeter och aktuell och tidigare behandling, något större vid start av JAK-hämmare jämfört med TNF-hämmare (232). Skillnaden var tydligast bland dem som tidigare behandlats med flera bDMARDs.
Evidens finns även för effekt av tofacitinib i monoterapi hos patienter med otillräcklig effekt eller intolerans för ≥ 1 csDMARD (i majoriteten av fallen metotrexat) eller bDMARD (123, 124) och för filgotinib eller upadacitinib hos patienter med otillräcklig effekt av metotrexat (125, 126). En systematisk översikt (130) visar att både tofacitinib och baricitinib i monoterapi är effektivare än metotrexat, men samtidigt att kombinationsterapi med metotrexat ger bättre klinisk effekt än monoterapi och bör eftersträvas. (Appendix 7)
Det finns även dokumentation avseende effekt av behandling med JAK-hämmare hos patienter med ingen eller begränsad tidigare DMARD-behandling (127-129).
Det saknas direkta jämförelser mellan JAK-hämmarna, och även jämförande observationsstudier. I valet mellan preparaten bör tillgänglig lokal erfarenhet samt aktuell kostnadsbild vägas in.
Biosimilarer, switch och immunogenicitet
Biosimilarer och switch
- Biosimilarer (bsDMARDs) är biologiska DMARDs (bDMARDs) som är alternativ till originalpreparat och som har jämförbar biokemi, farmakokinetik och -dynamik, klinisk effekt, immunogencititet och biverkningsprofil.
- Ordet switch används när man byter från ett originalpreparat till dess biosimilar eller vice versa, eller från en biosimilar till en annan som har samma originalpreparat.
- Multipel switch innebär att man mer än en gång byter mellan originalpreparat och biosimilar eller mellan biosimilar och biosimilar.
Biosimilarerna är mycket lika, men inte helt identiska med originalpreparatet. Inom reumatologin finns idag biosimilarer för adalimumab, etanercept, infliximab, rituximab, tociluzmab och ustekinumab (listade i alfabetisk ordning utan prioritering). Den medicinska indikationen skall styra valet av läkemedelsbehandling inklusive val av biologiskt preparat, det vill säga behandlande läkare skall ha möjlighet att använda det läkemedel som medicinskt sett har störst sannolikhet att fungera effektivt och säkert för varje individ med kronisk reumatisk sjukdom.
Läkemedelverket gav under hösten 2023 ut en delrapport avseende multipel switch av biologiska läkemedel (233). Vare sig i denna rapport, eller i en systematisk översikt med metaanalys (234) avseende biosimilarer för infliximab, etanercept, och adalimumab vid behandling av RA fann man inga signifikanta skillnader i effekt, säkerhet eller immunogenicitet. I en omfattande analys baserad på EudraVigilance granskades 75 327 rapporter (566 249 läkemedel–händelsepar) av misstänkta biverkningar för originalpreparaten adalimumab, etanercept, infliximab och rituximab jämfört med deras biosimilarer (235). Resultaten visade inga nya säkerhets- eller effektsignaler. Samtidigt framhålls behovet av fortsatt noggrann farmakovigilans, eftersom evidensen för byte mellan original och biosimilar, och särskilt för multipla byten och långtidseffekter, fortfarande är begränsad.
Noceboeffekten. Effekter av switch kan vara svårbedömd pga noceboeffekten, dvs att patientens negativa förväntningar kan förvärra biverkningar och/eller sjukdomssymptom vilka kan vara betydande vid switch. I en nyligen publicerad studie av switch från infliximab till biosimilar bytte 13 % av patienterna tillbaka till originalpreparatet pga noceboeffekten (236). För att minska noceboeffekten vid byte från originalpreparat till biosimilar är det viktigt att kommunikationen med patient (och anhöriga) är god. Multidisciplinärt teamarbete har i detta sammanhang visat sig vara mycket gynnsamt (237, 238).
Sammantaget har man hittills inte funnit några negativa signaler avseende effekt och säkerhet vid vare sig enkel eller multipel switch vid behandling av RA, men den vetenskapliga evidensen är begränsad. Med utgångspunkt från detta kan byte från behandling med originalpreparat övervägas hos patienter som är i stabil remission eller har stabilt låg sjukdomsaktivitet. Patienterna skall vara välinformerade om alla relevanta aspekter på behandlingen, strukturerad uppföljning skall ske och beredskap skall finnas för att sätta in annan adekvat behandling om bytet inte faller väl ut.
SRF betonar att det är av största vikt att följa upp klinisk effekt och säkerhet för både bDMARDs och bsDMARDs inom ramen för kvalitetsregistret SRQ. Spårbarhet med batchnummer är viktigt för att kunna följa upp eventuella skillnader mellan originalprodukt och biosimilar.
Immunogenicitet vid behandling med biologiska läkemedel
Behandling med bDMARDs kan ge upphov till immunogenicitet, dvs utveckling av läkemedels-neutraliserande ADA (anti-drug antibodies). Förekomst av ADA har visat sig vara associerat med lägre serumkoncentration av TNF-hämmare, sämre effekt och mer biverkningar (239). En retrospektiv studie har visat att upprepad analys av ADA samt läkemedels-koncentration kan vara av värde för att tidigt kunna konstatera terapisvikt på TNF-blockad (240). Förekomst av ADA ökar över tid och tycks inte nå en platåfas (241). Jämförelsen mellan olika studier försvåras av att olika metoder används för att mäta ADA och att tidpunkten för provtagning varierar, vilket har betydelse för resultatet (242-249). I det material som finns tillgängligt tycks uppkomst och frekvens av ADA hos patienter med RA som behandlas med biosimilarer i stort sett vara likartad, eller åtminstone inte ökad, jämfört med original-läkemedlet (250-257). Om en patient har utvecklat ADA mot original-läkemedlet kommer dessa med allra största sannolikhet att korsreagera mot biosimilaren (258). Erfarenheten från de switchstudier vid RA där man bytt från original-läkemedel till en biosimilar talar för att frekvensen av ADA inte ökar vid byte. De data som finns angående upprepade byten mellan original-läkemedel och biosimilarer talar inte för att immunogeniciteten ökar, men endast ett fåtal studier har undersökt detta(233).
Samtidig behandling med metotrexat tycks minska problem med immunogenicitet (239) och också öka serumnivån av vissa TNF-hämmare, möjligen på grund av minskad utveckling av antiläkemedelsantikroppar (ADA) (259, 260). Flera studier visar att tillägg av metotrexat i doser över 10 mg/vecka ökar serumkoncentrationen av adalimumab, minskar risken för ADA och förbättrar behandlingssvar (260-265). I en stor prospektiv RA-kohort sågs lägre risk för ADA och bättre kliniskt utfall hos patienter som fick metotrexat i kombination med biologiskt läkemedel (264). Nyligen bekräftades detta även i en analys av data från en randomiserad fas III-studie, där högre adalimumab-nivåer (≥ 4–6 mg/L) var kopplade till bättre respons och lägre risk för ADA (265). Patienter som är eller tidigare varit rökare tycks ha ökad risk att utveckla ADA (241).
Om rutinanalyser av läkmedelskoncentrationer och ADA, dvs therapeutic drug monitoring (TDM) t ex vid insättning och med standardiserade intervall under behandlingen, är av värde är fortfarande oklart. I dagsläget rekommenderar EULAR inte TDM vid behandling av reumatisk sjukdom med biologiska läkemedel(266). Systematiska översikter har dock visat att TDM kan förbättra behandlingseffekt och kostnadseffektivitet, men evidensen är fortfarande begränsad och heterogen (267, 268). I NOR-DRUM B studien visades dock att TDM – i jämförelse med standard-hantering av infliximab behandling hos patienter med RA, AS, psoriasisartrit, ulcerös colit, Mb Crohn och psoriasis – ledde till att en större andel av patienter i TDM-gruppen undvek försämring (i sjukdomsspecifika mått) jämfört med kontrollerna(269). Detta gällde enbart patienter med etablerad infliximab-behandling (minst 30 veckors behandling med infliximab) och effekten utvärderades efter 48 veckor. TDM hade ingen effekt på uppnående av remission från insättandet av infliximab och upp till 30 veckor (270).
Immunofarmakologiska analyser bör ske inom ramen för en strukturerad uppföljning eftersom kinetiken och betydelsen av ADA i många fall är oklar (271). Mätning av läkemedelskoncentration (så nära nästa administrationstillfälle som möjligt) samt nivå av ADA kan vara av värde vid klinisk misstanke om sviktande effekt av TNF-blockad. Låg koncentration av läkemedel tillsammans med hög titer av ADA (enligt pre-definierat tröskelvärde) talar för utveckling av immunogenicitet, och att läkemedlet inte längre har avsedd biologisk effekt. Om läkemedelsnivåerna är höga, men patienten inte har effekt av läkemedlet kan detta tala för att det är rationellt att byta till ett läkemedel med annan verkningsmekanism.
Tänk på att:
- Om behandling med originalpreparat avbrutits på grund av biverkan eller bristande effekt, rekommenderas inte behandling med dess biosimilarer. Evidensen för switch mellan biosimilarer och multipel switch är begränsad, och sådana bör endast utföras inom ramen för strukturerad uppföljning. Registrera alltid switch i SRQ. På det sättet får svensk reumatologi data från klinisk praxis som kan besvara frågorna kring ev risker med biologiska läkemedel inkluderande originalpreparat, biosimilarer och switch.
- TDM rekommenderas inte som rutinåtgärd vid behandling av RA med biologiska läkemedel.
Destruktionshämning, serologisk prediktion, nedtrappning/utsättning
bDMARDs, tsDMARDs och destruktionshämning
Kliniska studier visar att TNF-hämmare bromsar utveckling av leddestruktion, särskilt om TNF-hämmaren kombineras med metotrexat (Hög evidensstyrka) (76-78, 133). Även för abatacept, rituximab, tocilizumab och sarilumab finns data som visar en destruktionshämmande effekt (Måttlig evidensstyrka) (121, 218, 272-275). För rituximab har påvisats destruktionshämmande effekt hos patienter med tidigare inadekvat respons på TNF-hämmare (273), medan data som visar destruktionshämmande effekt av abatacept, tocilizumab och sarilumab kommer från studier av bDMARD- naiva patienter (115, 121, 218, 272, 274).
Det finns också data som visar att biologiska läkemedel i kombination med metotrexat kan minska röntgendestruktion även hos patienter som är fortsatt inflammatoriskt aktiva. Denna dissociation mellan klinisk effekt och effekt på röntgendestruktion har undersökts och påvisats för infliximab (276), etanercept (277), adalimumab (278), tocilizumab (279) och rituximab (280) i uppföljning upp till 1 år, för rituximab (280) och adalimumab (278) hos patienter med tidig RA och för övriga hos patienter med etablerad RA (276, 277, 279).
I en metaanalys av röntgenprogress i kliniska prövningar omfattande olika csDMARDs, steroider och bDMARDs rapporterades mindre röntgenprogress hos patienter behandlade med csDMARD kombinationer, csDMARD i kombination med kortison eller csDMARD i kombination med bDMARD jämfört med behandling med ett csDMARD preparat (281). Resultaten visar att en mer omfattande behandling överlag leder till mindre röntgenprogress, men säkra slutsatser om jämförelser mellan olika preparat och kombinationer kan inte dras med tanke på den betydande heterogeniteten mellan olika studier.
Det finns även studier som visar att JAK-hämmare bromsar leddestruktion jämfört med behandling med csDMARDs hos patienter med aktiv sjukdom. (93, 110, 127, 128, 282). Detta är visat hos patienter med ingen eller begränsad tidigare behandling med csDMARDs för såväl tofacitinib (127) som baricitinib (283) och upadacitinib (128), och för baricitinib och upadacitinib även hos patienter med otillräcklig effekt av tidigare csDMARD behandling (93, 282, 283).
Effekt på radiografisk leddestruktion utgör ett viktigt underlag för beslut om terapi, men bör inte ensamt styra det kliniska ställningstagandet beträffande insättning av preparat eller fortsatt behandling.
Serologiska prediktorer för behandlingsutfall för olika bDMARDs
Effekten av rituximab är bäst dokumenterad hos RF- positiva RA patienter (284). Data tyder på att effekten av rituximab på gruppnivå är bättre hos RF och/eller anti-CCP antikroppspositiva RA patienter än hos antikroppsnegativa, med liknande mönster för abatacept (Tabell 4). En metaanalys som innefattade både randomiserade, kontrollerade kliniska prövningar och observationsstudier visade ett tydligare samband mellan RF-positivitet och klinisk respons vid behandling med rituximab än vid abatacept (285).
Motsvarande mönster har inte observerats vid behandling med TNF-hämmare. Data när det gäller IL-6 hämmare är motstridiga (Tabell 4).
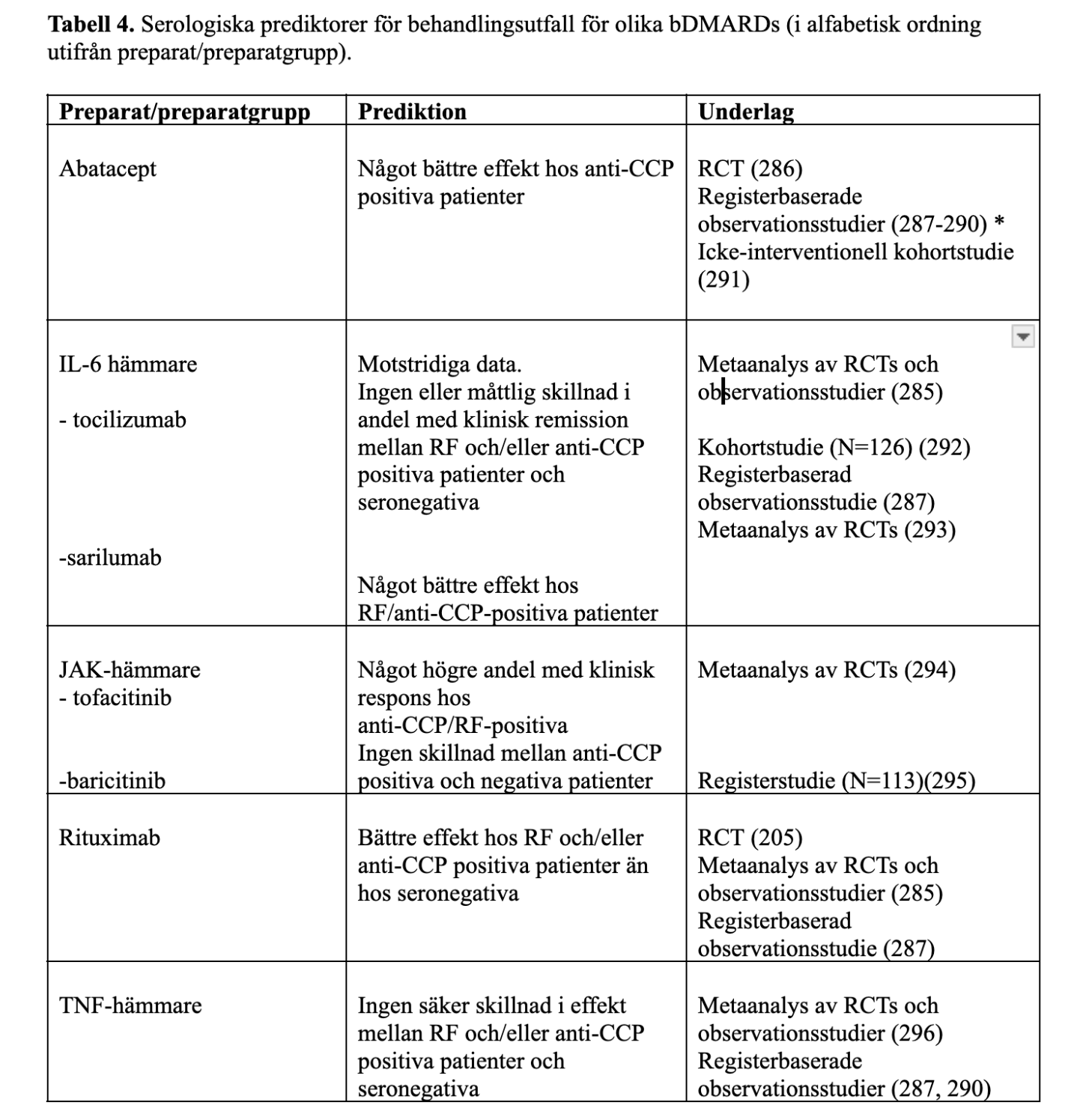
*Även lägre risk att avsluta abatacept och högre sannolikhet för klinisk förbättring hos RF positiva jämfört med RF negativa.
I en post hoc analys av EXXELERATE-studien noterades att patienter med hög nivå av RF (högsta kvartilen, >204 IU/ml) hade bättre respons på certolizumab pegol än på adalimumab (297). Man såg även lägre koncentration av adalimumab i denna grupp, och föreslog att högre omsättning av fullständiga antikroppar än av pegylerat antikroppsfragment utan Fc-del skulle kunna förklara resultaten.
Sammanfattning: prediktorer för behandlingsutfall för olika bDMARDs
Effekten av rituximab på gruppnivå är bättre hos RF och/eller anti-CCP antikroppspositiva RA patienter än hos antikroppsnegativa. Effekten av abatacept är något större på gruppnivå hos RF och/eller anti-CCP antikroppspositiva patienter jämfört med seronegativa patienter.
För IL-6 hämmare är data motstridiga, och för TNF-hämmare har man inte sett något samband mellan anti-CCP eller RF och effekt.
Utifrån nuvarande kunskapsläge om samband mellan antikroppspositivitet och behandlingsrespons, kan val av bDMARDs dock inte enbart styras av dessa serologiska fynd.
Nedtrappning eller utsättning av DMARDs
Mycket talar för att en stor andel av patienter som svarat väl på behandling med TNF-hämmare kan minska dosen med bibehållen god effekt medan utsättning medför en större risk för ökad sjukdomsaktivitet. Data för andra bDMARDs och tsDMARDs är sparsamma men pekar i samma riktning (298-304).
TNF-hämmare
Nedtrappad dos av TNF-hämmare hos patienter med RA som haft låg sjukdomsaktivitet i 3-12 månader är enligt en Cochranerapport från 2019 jämförbart med fortsatt full dos med avseende på sjukdomsaktivitet, andel som bibehåller låg sjukdomsaktivitet och funktionsförmåga enligt HAQ, men möjligen förknippat med lätt ökning av röntgenprogress (300). I de ingående studierna hade man trappat ned enligt ett förutbestämt schema, eller utifrån sjukdomsaktivitet. Majoriteten av studier har undersökt adalimumab eller etanercept, men dosreduktion finns även studerat hos patienter behandlade med metotrexat i kombination med certolizumab, där ingen klinisk relevant skillnad sågs mellan bibehållen respektive halverad dos certolizumab (305).
Utsättning av TNF-hämmare hos patienter som haft låg sjukdomsaktivitet i 1-12 månader medförde enligt nämnda Cochranerapport ökad sjukdomsaktivitet, lägre andel med bibehållen låg sjukdomaktivitet och sämre funktionsförmåga enligt HAQ, jämfört med patienter som fortsatte med TNF-hämmare (300). Utsättning ledde i en studie med 84 patienter till att 63% fick ett skov under uppföljningtiden på ett år, jämfört med 5% hos dem med bibehållen behandling, men flertalet uppnådde åter remission efter återinsatt TNF-hämmare(306).
I en RCT-studie från Norge där patienterna efter att ha uppnått stabil remission randomiserades till att antingen behålla oförändrad medicinering eller under några månader dosreducera TNF-hämmare innan utsättning, förblev endast 25 % av patienterna som satt ut behandlingen i remission efter tre år, trots fortsatt behandling med csDMARD (307).
En 10 års uppföljning av DRESS-studien visade att aktivitetsstyrd dosreducering av TNF-hämmare ger bibehållen remission hos stor andel av patienterna, men vid utsättning av TNF-hämmare var det bara 21% som bibehöll remission. Man såg också tendenser till ökad radiologisk progress hos dem som återfick hög sjukdomsaktivitet (308).
Flertalet studier visar att sannolikheten att bibehålla låg sjukdomaktivitet efter utsättning var större om TNF-hämmare startats tidigt i sjukdomsförloppet och haft god och stabil effekt som kvarstått i flera månader innan preparaten utsatts (Låg evidensstyrka) (154, 309-313).
Vad gäller ledskador på röntgen har man sett en lätt ökad risk för minimal radiografisk progress (modifierat Sharp-van der Heijde-score >0.5) efter 52 veckor (RR 1.22) (måttlig evidensstyrka) och en högre risk vid utsättning (RR 1.69) (hög evidensstyrka). Det saknas långtidsuppföljning av radiografiskt utfall vid både nedtrappning och utsättning (300).
Andra bDMARDs
Enstaka randomiserade, kontrollerade studier rapporterar om försök till nedtrappning eller utsättning av andra bDMARDs.
Abatacept gavs i en randomiserad, dubbelblind studie till patienter med tidig, metotrexatnaiv RA med ogynnsam prognos, som uppnått remission under behandling med metotrexat + abatacept, i halverad eller oförändrad dos. Man såg ingen skillnad i risk för försämring mellan grupperna under den 1 år långa uppföljningstiden (314). I AVERT-studien av patienter med tidig RA, som behandlades med abatacept + metotrexat vs abatacept vs metotrexat, sattes all RA-behandling ut efter uppnådd remission, och sex månader senare var 25%, 28% vs 17% i remission (157). I AVERT-2 randomiserades patienter i remission till (1) fortsatt behandling med abatacept + metotrexat, (2) halverad dos abatacept under 24 veckor följt av utsättning, i kombination med metotrexat, eller (3) monoterapi abatacept i full dos. Andelen patienter i remission var efter 48 veckor 74%, 48% respektive 57%, men utan statistiskt signifikanta skillnader(315).
Tocilizumab gavs till patienter med RA under 1 år och hos de 350 patienter som uppnått låg sjukdomsaktivit jämfördes bibehållen dos med dosminskning (i genomsnitt 66% av full dos) i en registerstudie. I båda grupperna hade 85% bibehållen låg sjukdomsaktivitet enligt CDAI efter ett års uppföljning (316).
I en studie av patienter med aktiv etablerad RA, som uppnått remission efter tillägg av tocilizumab till metotrexat, fick 84 % uppblossande sjukdomsaktivitet efter utsättning av tocilizumab, men svarade bra på återinsättning (317).
Hos patienter med RA där låg sjukdomsaktivitet uppnåddes efter minst 6 månaders behandling med abatacept eller tocilizumab jämfördes bibehållen dos med successiv dosreduktion med mål att helt sätta ut preparatet(318). Under uppföljningstiden ökade sjukdomsaktiviteten signifikant mer i dosreduktionsgrupperna.
tsDMARDs
Endast ett mycket litet antal studier rapporterar utsättningsförsök för tsDMARDs. En långtidsuppföljning avseende baricitinib, där patienter med etablerad RA som ingått i tidigare Fas 3-studier med baricitinib (90, 91, 129, 141), och uppnått låg eller ingen sjukdomsaktivitet, randomiserades till fortsatt dos på 4 mg/dag eller halverad dos på 2 mg/dag(319). Patienter som fick kvarstå på den högre dosen hade i högre grad bibehållen låg sjukdomsaktivitet (80% för 4 mg vs 67% för 2 mg) eller remission (40% för 4 mg vs 33% för 2 mg). För flertalet patienter gav en återgång till den högre dosen ånyo gott svar på behandlingen.
Tofacitinib har studerats i en RCT (n=122) där patienter med LDA randomiserades till fortsatt full dos, halverad dos eller utsättning(320). Låg sjukdomsaktivitet bibehölls efter 6 månader hos 95%, 64% vs 20%. Liknande fynd, med lägre risk för skov vid dosreduktion än vid direkt utsättning, har rapporterats i en observationsstudie (321), där man även fann god effekt i fleratalet fall vid återinsättning.
Andra aspekter på utsättning/nedtrappning av b/tsDMARDs
Den tid som patienter varit kliniskt lågaktiva/i remission före utsättning/dosminskning har varierat mellan olika studier, vanligen 3-12 månader. Ännu är det inte möjligt att ange ett optimalt tidsintervall för hur lång remission som krävs före dosminskning eller utsättning, men att remissionen bör vara stabil får anses väl belagt (1, 322, 323).
Flera observationella studier rapporterar faktorer av betydelse för en framgångsrik nedtrappning av bDMARDs (324-328). I dessa påvisas framför allt tidigt insatt behandling med bDMARD, fortsatt behandling med csDMARD, inget behov av kortison eller tidig uttrappning av kortison, att vara i remission enligt DAS28 samt ha lägre HAQ som associerade med framgångrisk nedtrappning av bDMARD. Det föreslogs även att kortare sjukdomsduration, hög ålder, manligt kön och avsaknad av antikroppar kan vara mer vanligt hos dem med framgångrik nedtrappning av bDMARD.
Utsättning/nedtrappning av csDMARDs
Avseende dosreduktion och/eller utsättande av csDMARD rekommenderar EULAR tydligt en försiktighet med utsättning. När steroider har avslutats och patienten befinner sig i stabil remission kan dosreduktion/utglesning av DMARDs, oavsett typ (bDMARD, tsDMARD eller csDMARD), övervägas. EULAR-rekommendationen från 2022 betonar att det inte finns någon föredragen ordning för nedtrappning mellan bDMARDs eller csDMARDs eftersom de kliniska effekterna inte skiljer sig mellan de olika nedtrappningsstrategierna(1) Studier med en uppföljningstid på 1-3 år visar att ökad sjukdomsaktivitet är vanligare bland de patienter som, efter att uppnått klinisk remission, dosminskat eller satt ut csDMARD (329-331). Effekterna av återinsättning var i dessa studier varierande, och klinsk remission kunde inte alltid uppnås ånyo.
Utsättning av MTX men bibehållen b/tsDMARD har studerats i en systematisk översiktsartikel (332). Patienter i remission på kombinationsbehandling med MTX och TNFi, tocilizumab, abatacept eller tofacitinib randomiserades till att behålla eller sätta ut MTX. I grupperna som avlutade MTX var det i genomsnitt 10% färre som bibehöll remission under uppföljningstiden, som var 6-18 månader.
Sammanfattning: nedtrappning eller utsättning av DMARDs
Nedtrappning av DMARDs bör övervägas hos patienter med ett bestående terapisvar, framför allt hos patienter med tidig RA som uppnått remission, förutsatt att en noggrann uppföljning görs och beredskap finns för återinsättning av preparatet (Måttlig evidensstyrka). Att helt sätta ut TNF-hämmare och andra DMARDs innebär en högre risk för ökad sjukdomsaktivitet. Att vid försämring återgå till tidigare effektiv dos av preparatet ter sig säkert och effektivt. Ingen säker tidsperiod kan anges där patienten ska ha varit i remission eller haft låg sjukdomsaktivitet, men i de studier som är gjorda har patienterna haft stabil sjukdom i 3-12 månader. EULAR rekommenderar minst 6 månaders remission innan försök till nedtrappning (1).
Säkerhetsaspekter på bDMARDs och tsDMARDs
Säkerhetsaspekter på behandling med bDMARDs
De kontraindikationer som gäller för preparaten skall givetvis beaktas. Dessa innefattar för samtliga biologiska medel överkänslighet mot ingående substanser och aktiva, allvarliga infektioner. För TNF-hämmarna adalimumab, certolizumab, golimumab och infliximab utgör måttlig-svår hjärtsvikt (NYHA grad III-IV) kontraindikation, medan försiktighet rekommenderas för etanercept i dessa fall. Svår hjärtsvikt (NYHA grad IV) är kontraindikation för rituximab, och för anakinra är svårt nedsatt njurfunktion och neutropeni (antal neutrofila granulocyter < 1,5 x 109/l) kontraindikationer.
Försiktighet vid behandling med TNF-hämmare rekommenderas även vid demyeliniserande nervsjukdom och överlappssyndrom med drag av systemisk lupus erythematosus. För ytterligare information om kontraindikationer och rekommenderad försiktighet hänvisas till respektive preparatmonografi.
Uppföljning i register av patienter med RA som erhåller bDMARDs är av stor betydelse för utvärdering av såväl dessa komorbiditeter som ovanliga biverkningar och för långtidsuppföljningar av t.ex. malignitetsrisker.
För särskilda aspekter på behandling inför och under graviditet och i samband med amning, se separata riktlinjer från SRF.
Infektioner
Behandling med TNF-hämmare är associerad med en ökad risk för aktivering av latent tuberkulos (TB). För övriga bDMARDs finns inte säkerställt att de ökar risken för reaktivering av latent TB, men fall av TB finns rapporterat i anslutning till behandling med samtliga bDMARDs (333). Därför bör patienten utvärderas på ett strukturerat sätt avseende tuberkulosexposition inför start av behandling med bDMARD, och vaksamhet avseende ny tuberkulosexposition under pågående behandling rekommenderas (se SRFs separata rekommendationer).
Det finns rapporter om reaktivering av hepatit B i samband med flera biologiska behandlingar (334) och i vissa fall har patienter utvecklat fulminant leversvikt under behandling med TNF-hämmare, och även under behandling med rituximab (särskilt mot lymfom), varför screening i syfte att upptäcka kronisk aktiv hepatit B rekommenderas före behandlingsstart med bDMARD (se SRFs separata rekommendationer).
En metaanalys visade ökad risk för allvarliga infektioner hos patienter som behandlats med TNF-hämmare i kliniska prövningar (335). Även en omfattande genomgång av observationella studier pekar på en förhöjd infektionsrisk med TNF-hämmare liksom för andra bDMARDs (336) . Det finns inga tydliga skillnader mellan TNF-hämmare och övriga bDMARDs avseende risken för allvarliga infektioner (336).
I samband med rituximab-behandling har låga IgG-nivåer före behandlingsstart (337) eller under pågående behandling (338) kopplats till ökad risk för allvarlig infektion, varför mätning av IgG före initierande av rituximab rekommenderas. Vidare har sjunkande nivåer av IgG och IgM observerats under behandling, varför monitorering av Ig-nivåer inför upprepad rituximab-behandling kan övervägas och skärpt uppmärksamhet rekommenderas särskilt vid initialt låga Ig-nivåer eller vid samtidig hög infektionskänslighet (339). En senare observationell retrospektiv studie av 83 patienter (uppföljningstid 13 år) tyder inte på ökad förekomst av allvarliga infektioner hos patienter som utvecklade hypogammaglobulinemi under rituximab-behandling (340).
Så kallad ”late-onset neutropenia” (neutrofiler <1.5 x109 /l mer än 4 veckor efter infusion) finns rapporterat i samband med rituximabbehandling vid bland annat RA, men förefaller inte vara ett större säkerhetsproblem. Tillståndet har hittills inte rapporterats kopplat till ökad infektionsförekomst och andelen som återfår neutropeni vid återbehandling med rituximab har varit låg (341).
Malignitet
Metaanalyser av kliniska prövningar (342) och observationsstudier (343-345), och en färsk sammanställning av observationsstudier (346) tyder inte på någon ökad risk för malignitet överlag hos RA patienter som behandlats med TNF-hämmare. Däremot kan man i nuläget inte helt utesluta mycket små riskökningar för icke-melanom hud cancer (347), melanom (348, 349) och cervixcancer (350). Råd angående solvanor, solskydd och kontroll av hudförändringar samt följsamhet till screeningprogram för cervixcancer är därför relevant för denna patientgrupp. Dokumentationen gällande malignitetsrisker är mest omfattande för TNF-hämmare. Även för abatacept finns data talande för en riskökning för icke-melanom hudcancer vid jämförelse med csDMARDs eller TNF-hämmare (351, 352). Ytterligare en stor observationell studie indikerar en riskökning för melanom, men dock inte allmän cancer-risk, med abatacept jämfört med andra bDMARDs (353), men denna riskökning har inte bekräftats i några andra publicerade observationella studier. En nyligen publicerad observationell studie där icke-melanom hudcancer var exkluderad fann ingen generellt ökad cancer-risk för abatacept (354). Avseende risker för malignitet med andra biologiska preparat har data från metaanalys av kliniska prövningar (355) samt från nationella svenska registerstudier (356, 357) inte talat för någon ökad risk för malignitet överlag för övriga bDMARDs som används vid RA.
Underlaget för att ge rekommendationer om bDMARD behandling hos patienter med tidigare diagnostiserad malignitet är begränsat. Situationen är komplex då immunsystemets komponenter kan ha omväxlande pro- och antitumöreffekter i olika stadier av malignitets- och metastasutveckling. Observationella studier av RA patienter som startat behandling med TNF-hämmare eller andra bDMARDs (i denna studie enbart rituximab och anakinra) efter malignitet har inte visat någon säker ökning av recidivförekomst jämfört med RA patienter utan bDMARD behandling, dvs hittillsvarande selektion av patienter till terapi efter malignitet förefaller inte medföra ökad recidivrisk (344, 358-363). Patienter med aktuell eller tidigare malignitet har exkluderats ur kliniska prövningar av bDMARDs.
Sammanfattningsvis rekommenderas tills vidare försiktighet och individuell bedömning där man får väga in tid sedan cancerdiagnos, genomförd behandling och resultat, risk för återfall och behovet av RA-behandling. Utöver att välja rituximab till patienter med tidigare B-cellsmalignitet (i samråd med onkolog) finns inte underlag för att rekommendera något specifikt bDMARD i denna situation.
Övriga säkerhetsaspekter
Flera oberoende observationsstudier rapporterar ökad incidens av tarmperforation under tocilizumab-behandling jämfört med andra bDMARDs(346). I en stor observationsstudie konstaterades att tarmperforation vid RA är ovanligt, men att det förelåg en ökad frekvens under tocilizumab-behandling (4.5 / 1000 personår) jämfört med TNF-blockad (1.8 / 1000 personår) och denna riskökning var inte associerad till tidigare anamnes på divertikulit (364). Riskökning för tocilizumab jämfört med andra bDMARDs bekräftas även i andra studier(365). En studie pekar även på ökad förekomst av divertikulit vid tocilizumab (366), medan det finns begränsat med data avseende divertikulit och tarmperforation i samband med andra IL-6 blockande preparat.
Ökad risk för tarmperforation vid IL-6 blockad skall beaktas, och IL-6 hämmande läkemedel bör användas med stor försiktighet hos patienter med tidigare anamnes på divertikulit eller sår i tarm.
Säkerhetsaspekter på behandling med JAK-hämmare
Kunskapsläget kring säkerhet vid behandling med JAK-hämmare är föränderligt och är generellt sett sämre jämfört med flertalet bDMARDs. Därför bör varje förskrivande läkare vara observant på ny information och rekommendationer från myndigheter, samt medverka till kunskapsutveckling via biverkningsrapportering och noggrann uppföljning inom ramen för kvalitetsregister. Generellt för JAK-hämmarna gäller att säkerhetsdata från register och långtidsuppföljningar av kliniska prövningar finns i störst omfattning för tofacitinib och baricitinib, och minst för filgotinib och upadacitinib. I jämförbara delar framträder dock inga avgörande skillnader mellan de olika JAK-hämmarnas säkerhetsprofiler (367).
Läkemedelsmyndigheterna i både Europa (EMA) (368) och USA (FDA) (369) har utfärdat rekommendationer angående försiktighet vid förskrivning av JAK-hämmare vid RA. Dessa rekommendationer baseras framför allt på ORAL Surveillance studien, en randomiserad säkerhetsstudie med RA-patienter över 50 år (n=4362) med minst en kardiovaskulär riskfaktor och som haft otillräcklig effekt av metotrexat. Tofacitinib förknippades med ökad risk för VTE, malignitet, hjärtinfarkt och totalmortalitet jämfört med patienter behandlade med TNF-hämmare (adalimumab eller etanercept) efter i genomsnitt 4 års uppföljning (370). Studiedata indikerar att det beräknade antalet patienter i gruppen beskriven ovan som skulle behöva behandlas med tofacitinib 5 mg x 2 istället för med adalimumab eller etanercept i ett år för att en kardiovaskulär händelse (major adverse cardiovascular event, MACE) skulle inträffa (number needed to harm) var 567, och motsvarande antal för malignitet var 275 (370). Posthoc-analyser av ORAL Surveillance har identifierat att riskökningen för JAK-hämmare återfinns hos patienter med ålder >65 år, pågående eller tidigare rökning, eller tidigare känd aterosklerotisk hjärt-kärlsjukdom (371, 372).
Säkerhetssignalen avseende kardiovaskulär sjukdom från ORAL Surveillance studien återfinns inte i registerstudier och kliniska prövningars långtidsuppföljningar av tofacitinib och övriga JAK-hämmare (99, 303, 373-385). Registerstudierna har dock i flertalet fall kortare uppföljningstid än ORAL Surveillance (386, 387). Vad gäller gäller VTE har flera registerstudier och en meta-analys av observationella data funnit en signifikant ökad risk, i synnerhet för lungemboli, vid behandling med JAK-hämmare (framförallt baricitinib) i jämförelse med anti-TNF (388-390).
Vad gäller malignitet (undantaget icke-melanom hudcancer) har meta-analyser påvisat signifikant ökad risk vid behandling med JAK-hämmare jämfört med anti-TNF (391, 392), men dataunderlaget i dessa studier utgörs framförallt av ORAL Surveillance. Dock visade en oberoende registerstudie från Tyskland, som jämförde JAK-hämmare (framförallt baricitinib och tofacitinib) mot samtliga bDMARDs, även den en ökad malignitetsrisk(393). Överrisken sågs enbart efter 16 månaders uppföljning, dvs efter liknande tidsspann som i ORAL Surveillance. Den relativa risken för malignitet hos patienter över 60 år med JAK-hämmare jämfört var 1,93 (95% KI 1,43-2,60) jämfört med samtliga bDMARDs, och number needed to harm beräknades till 135 patientår, dvs lägre än i ORAL Surveillance. För patienter under 60 år vid behandlingsstart sågs ingen risksignal för malignitet(393). I motsats till den tyska studien visade en stor amerikansk studie baserad på försäkringsdata från patienter ≥65 år inte någon generellt ökad risk för malignitet vid JAK-hämning jämfört med bDMARDS, men medianbehandlingstiden i studien var endast 1,8 år (394). En annan observationsstudie, med längre uppföljningstid (median ≥3,5 år), påvisade inte heller någon signfikant ökad malignitetsrisk med JAK-hämmare jämfört med anti-TNF (395).Slutligen påvisade en nyligen publicerad meta-analys av observationsstudier (utan den tyska registerstudien) inte någon ökad malignitetsrisk vid JAK-hämning jämfört med anti-TNF (390).
Avseende icke-melanom hudcancer har både svenska registerdata och en meta-analys av kliniska prövningar påvisat en signifikant ökad risk med JAK-hämmare jämfört med anti-TNF med en incidensratkvot på 1,9 (95% KI 1,2-3,1) (357, 392).
Sammantaget har risksignalerna från ORAL Surveillance vad gäller VTE och malignitet bekräftats i flera, men inte i alla, uppföljande studier. Vad gäller kardiovaskulär sjukdom har ingen uppföljande studie hittills bekräftat en statistiskt signifikant riskökning med JAK-hämmare. En genomlysning utförd av EMAs expertgrupp 2022 ledde till följande försiktighetsåtgärder, att appliceras på samtliga JAK-hämmare:
JAK-hämmare bör enbart användas när inga andra alternativ är lämpliga till patienter med:
- Ålder ≥65 år
- Pågående eller tidigare rökning
- Andra kardiovaskulära riskfaktorer
- Andra riskfaktorer för malignitet
Oberoende av ovanstående skall JAK-hämmare användas med försiktighet hos patienter med riskfaktorer för VTE utöver RA (hög ålder, tidigare VTE, ärftlig koagulationsstörning, malignitet, immobilisering).
Om JAK-hämmare bedöms nödvändigt till patienter med ovanstående riskfaktorer rekommenderar EMA att man överväger användning av en lägre dos. EMA rekommenderar också att patienter under behandling med JAK-hämmare regelbundet undersöks avseende hudcancer.
I brist på långtidsdata avseende säkerhetsskillnader mellan olika JAK-hämmare (396, 397), samt beaktande försiktighetsprincipen och evidensvärdet av randomiserad klinisk prövning designad för att studera säkerhetsutfall (dvs ORAL Surveillance) anser SRF, i likhet med EMA och FDA, att ovanstående försiktighet bör appliceras på samtliga JAK-hämmare. Vidare är det av stor vikt, såsom för alla RA patienter, att se över och vid behov intervenera mot modifierbara riskfaktorer för komorbiditeter hos patienter med pågående behandling med JAK-hämmare.
Graviditet och överkänslighet mot ingående substanser utgör kontraindikationer för de fyra godkända JAK-hämmarna. För filgotinib, tofacitinib och upadacitinib är även allvarlig infektion kontraindikation enligt FASS, samt för de två sistnämnda grav leversvikt. Laboratoriemässiga avvikelser associerade med JAK-hämmare är minskning av leukocyter samt ökning av transaminaser och lipider. Dessa är dock inte frekventa skäl till avbruten behandling (128, 141, 378, 398, 399).
Incidensen för allvarliga infektioner i kliniska prövningar och öppna förlängningsstudier av JAK-hämmare har, bortsett från ORAL Surveillance studien varit jämförbar med motsvarande data för övriga bDMARDs (336). Några tydliga skillnader gentemot bDMARDs avseende infektionstyper har hittills inte framkommit, undantaget en ökad risk för Herpes Zoster. Hög ålder och asiatiskt urspung är kopplat till ökad risk för Herpes Zoster vid behandling med JAK-hämmare (400). Ett icke-levande vaccin mot Herpes Zoster (Shingrix®) finns numera tillgängligt i Sverige.
En färsk meta-analys av RCTs fann ingen ökad risk för gastrointestinal perforation med JAK-hämmare jämfört med konventionella DMARDs (401).
Kortisonbehandling vid tidig och etablerad RA
Då effekten av DMARDs inte är direkt insättande finns ofta behov av en snabbare inflammationsdämpning hos patienter med tidig RA och medelhög till hög sjukdomsaktivitet. Vid medelhög till hög sjukdomsaktivitet finns evidens för att peroralt prednisolon har positiva effekter. Som överbryggande behandling vid medelhög till hög sjukdomsaktivitet rekommenderas Prednisolon i dosen 5-7.5 mg/dag (lågdos), om inte särskilda skäl talar emot (Måttlig till låg evidensstyrka) (402-405). Snabb inflammations-dämpning uppnås ofta (Låg evidensstyrka). Det finns även evidens för destruktionshämning i studier avseende tidig RA löpande över två år (Hög evidensstyrka) (404, 406, 407). En RCT av lågdos kortisonbehandling (5 mg dagligen vs placebo under 2 år) till äldre patienter med etablerad RA visar också att kortisonbehandling ger destruktionshämning och lägre sjukdomsaktivitet än placebo (408).
Kortisonbehandling under lång tid är behäftat med kända risker för toxicitet, vilket bör beaktas vid initiering av behandling. Nyligen publicerade data konfirmerar tidigare studier som talar för att patienter med långvarig kortisonbehandling har en tydligt ökad risk för att utveckla diabetes mellitus (409) och andra studier indikerar riskökning för cerebrovaskulär sjukdom (410) samt ökad frekvens infektioner (408). En litteraturgenomgång publicerad 2016 konstaterade att prednisolondoser upp till 5 mg per dag vid tidig RA var associerade med låg total toxicitet, och doser över 10 mg med hög toxicitet, medan risken med doser mellan 5 och 10 mg var relaterade till förekomst av samtidiga riskfaktorer för bl a osteoporos, infektioner och hjärt-kärlsjukdom(411). En observationell studie visade att doser >5 mg vid etablerad RA ger signifikant ökad risk för kardiovaskulär sjukdom (412). En översikt från 2018 fann ingen skillnad avseende förändring i bentäthet över tid hos patienter med tidig RA och behandlade respektive inte behandlade med prednisolon i upp till 24 månader (413). En 7-årsuppföljning från en prospektiv studie av 602 patienter med tidig RA visade ingen tydlig skillnad avseende långtids-toxicitet mellan patienter med vs utan kortisonbehandling(414).
Vad gäller uttrappningstiden av kortison finns ingen evidens avseende optimal tid. Här behöver göras en avvägning mellan å ena sidan destruktionshämning vid långtidsbehandling och å andra sidan känd risk för biverkningar, samt risken att patienter kan kvarstå längre på kortison än vad som är kliniskt motiverat, där terapibyte snarare är att föredra.
Rekommendationen, som också går i linje med EULARs uppdaterade riktlinjer (415), är därför att trappa ut kortisonet så snart som möjligt efter uppnått behandlingsmål (låg sjukdomsaktivitet/remission).
Återkomst av sjukdomsaktivitet efter nedtrappning/uttrappning av kortison bör bedömas som behandlingssvikt på aktuell behandling, och föranleder fortsatt behandlingsstrategiska överväganden, se tidigare avsnitt om otillräcklig effekt av metotrexat samt flödesschema.
Det bör även noteras att det finns otillräckligt underlag för att bedöma den övergripande nyttan av lågdos kortison vid kombinationsbehandling med TNF-hämmare och andra bDMARDs.
Sammanfattning: Patienter med tidig RA som medicinerar med monoterapi csDMARD och saknar kända riskfaktorer (t ex diabetes, osteoporos eller känd hjärt-kärlsjukdom) för ogynnsamma kortisonrelaterade händelser bör behandlas med lågdos kortison som överbryggande behandling. Kortison bör trappas ut så snart som möjligt efter uppnått behandlingsmål (låg sjukdomsaktivitet/remission).
Ytterligare aspekter på kortisonbehandling vid tidig RA
Det finns också dokumentation som stöder att prednison i dosen 10 mg/dag ger snabbare förbättring, mindre leddestruktion, och mindre behov av tilläggsterapi med ytterligare csDMARD/bDMARD än om kortisonbehandling inte ges (416). Detta baseras på en tvåårig, placebokontrollerad studie med tät kontroll i kombination med metotrexat vid tidig RA. Biverkningarna på kort sikt (2 år) var inte fler bland de som behandlades med prednison. Att notera är att bentäthetsmätning gjordes vid inklusion, att osteoporos utgjorde exklusionskriterium och att alla patienter behandlades med calcium, D-vitamin och bisfosfonat (416).
En högre initial kortisondos, som sedan minskas till lågdos, kan ge bättre dämpning av sjukdomsaktiviteten under själva högdosbehandlingen (417), men betydelsen för sjukdomsutvecklingen på längre sikt är oklar. Nyligen visade en post-hoc analys av två randomiserade studier (BeSt och IMPROVED) med denna regim, tillsammans med csDMARDs, att snabb nedtrappning från högdos kortison resulterade i återkomst av sjukdomsaktivitet hos upp till 40 % av patienterna (418). Värdet av kortisonbehandling måste vägas mot de risker som är förknippade med behandlingen. Osteoporosprofylax är obligat och behandling skall ges enligt särskilda behandlingsriktlinjer (se hänvisning nedan).
Ett möjligt alternativ eller komplement till peroral lågdosbehandling med prednisolon/prednison är intraartikulära kortisoninjektioner, där biverkningar på lång sikt och uttrappningsproblem sannolikt är mindre än vid peroral behandling. Systematisk behandling med intraartikulära steroidinjektioner i inflammerade leder har ingått i behandlingsprogram som har lett till betydande förbättring hos patienter med tidig RA (53, 54, 156, 419), och flera översikter har också pekat i denna riktning(420, 421). Dock saknas direkta jämförelser med behandling utan intraartikulära kortisoninjektioner. Information om effekten på röntgenologisk leddestruktion av intraartikulära kortisoninjektioner saknas, men visst stöd finns för att sådan behandling kortsiktigt kan minska graden av erosionsutveckling undersökt med magnetkamera hos patienter med tidig RA (Mycket låg evidensstyrka) (422).
Behandling av extraartikulära manifestationer
Vid allvarliga extraartikulära manifestationer som systemisk vaskulit med och utan allvarliga ögonkomplikationer (sklerit eller retinal vaskulit) eller vaskulitassocierad perifer neuropati rekommenderas behandling med cyklofosfamid och högdos kortikosteroider enligt samma principer som för primär systemisk småkärlsvaskulit (Låg evidensstyrka) (423, 424). Sådan behandling bör även övervägas vid interstitiell lungsjukdom med snabbt progredierande symptom (Mycket låg evidensstyrka) (425, 426). Behandling med chlorambucil (Låg evidensstyrka) (427) eller cyklofosfamid (Mycket låg evidensstyrka) (427) kan övervägas vid systemisk amyloidos med allvarlig organpåverkan. Visst stöd finns även för att behandling med TNF-hämmare (Mycket låg evidensstyrka) (428) kan vara effektiva i detta sammanhang.
Det finns också visst stöd för att TNF-hämmare (Mycket låg evidensstyrka) (429) eller rituximab (Mycket låg evidensstyrka) (430) kan ha effekt hos patienter med terapirefraktär reumatoid vaskulit. Därutöver finns enstaka fallrapporter om framgångsrik behandling av systemisk RA relaterad vaskulit med abatacept (431) och tocilizumab (432).
Det finns rapporter om behandling av ILD med abatacept (433, 434), rituximab (435), och tocilizumab (436) med stabilisering av lungsjukdomen, men inga kontrollerade studier. Jämförelser av mortalitet i observationsstudier av sådana patienter som behandlats med rituximab eller abatacept har gett motstridiga resultat (437, 438). I en systematisk översikt konstaterades att man i flera observationsstudier funnit lägre risk för progress av ILD under behandling med abatacept jämfört med TNF-hämmare (439). Systematisk uppföljning med kvantifiering av ILD-förändringar detekterade med high-resolution CT indikerar också förbättring hos abataceptbehandlade RA-patienter (440).
I en observationsstudie från 5 centra i USA av patienter med RA som började med mykofenolat mofetil, azatioprin eller rituximab pga ILD konstaterades bättre uveckling av lungfunktionen jämfört med den förväntade utifrån deras tidigare progress (441). Även cyklosporin kan övervägas för patienter med RA-associerad ILD (Mycket låg evidensstyrka) (442, 443).
Det finns rapporter om att TNF-hämmare kan ha en negativ effekt på ILD, och även motsvarande data för andra läkemedel som leflunomid, rituximab och tocilizumab(444). Eventuella kausalsamband bakom dessa associationer är mycket svårbedömda.
I en systematisk litteraturöversikt konstaterades att det inte finns några tydliga skillnader mellan olika DMARD preparat när det gäller risken för ILD i kliniska prövningar. Observationsstudier indikerade däremot en lägre risk i förhållande till TNF-hämmare för metotrexat, och möjligen även för tofacitinib(445).
Nintedanib och pirfenidon är två perorala läkemedel som hämmar fibrotisk vävnadsmodellering. Medan nintedanib blockerar flera tyrosinkinaser och därmed profibrotiska intracellulära signalvägar är mekanismen för pirfenidon inte helt klarlagd. Antifibrotisk behandling med nintedanib bromsade försämring av lungsjukdomen bland RA-patienter i en subgruppsanalys av en randomiserad kontrollerad studie av behandling av patienter med ILD (446, 447).
En studie specifikt inriktad på patienter med RA och ILD, där antifibrotisk behandling med pirfenidon utvärderades, avbröts i förtid på grund av långsam inklusion av patienter under pandemin med COVID-19 (448). Studien innehöll betydligt färre patienter än planerat, och uppnådde inte det primära utfallsmåttet. Däremot såg man ett signifikant bättre utfall än för placebo i sekundära utfallsmått, framför allt hos patienter med lungförändringar talande för ”usual interstitial pneumonitis”, UIP.
I linje med detta har man i observationsstudier av patienter med RA och ILD som behandlats med nintedanib eller pirfenidone i klinisk praxis observerat en stabilisering av lungfunktionen, vilket kontrasterade mot en progredierande försämring under det föregående året (449, 450). En metaanalys av publicerade randomiserade kontrollerade studier och observationsstudier av nintendanib eller pirfenidon mot RA associead ILD indikerade en stabilisering av forcerad vitalkapacitet, med mindre robusta data om diffusionskapacitet (451).
I studierna av nintedanib och pirfenidon inkluderades enbart patienter med utbredd fibros, >10 % av lungparenkymet. Man såg inte någon interaktion mellan antifibrotisk och antiinflammatorisk behandling, och inte någon ökad risk för allvarliga biverkningar hos dem som erhållit båda typerna av terapier.
Sammantaget bör antifibrotisk behandling övervägas som tillägg till DMARD-behandling hos patienter med RA och UIP med utbredd lungfibros (>10%) med aktuell progress. SRF rekommenderar att kombinationsbehandling hanteras i ett nära samarbete mellan reumatolog och lungmedicinare. Ett sådant samarbete kan även innefatta ställningstagande till lungtransplantation hos patienter med allvarlig, progredierande sjukdom.
Metotrexat kan ge upphov till en toxisk pneumonit, som kliniskt och histopatologiskt skiljer sig från kronisk interstitiell lungsjukdom (interstitial lung disease, ILD) som associeras med RA (452, 453). I en stor observationsstudie med långtidsuppföljning av patienter med tidig RA fann man en lägre risk för utveckling av ILD hos patienter som behandlades med metotrexat, och en längre genomsnittlig tid till ILD-diagnos hos metotrexatbehandlade (454). I likhet med detta har en negativ association mellan metotrexatbehandling och ILD hos patienter med RA även konstaterats i fall-kontrollanalyser av patientpopulationer från flera olika länder (455). I en systematisk litteraturgenomgång konstaterades att de flesta välgjorda studier som undersökt om det finns något samband mellan metotrexat och ILD-utveckling vid RA indikerar att det inte finns något sådant samband (456).
Sammantaget bedöms utifrån detta metotrexat kunna ha positiva effekter på RA associerad inflammation även i lungorna, och ILD utgör inte någon kontraindikation för metotrexat.
Högdos kortikosteroidbehandling kan vara effektiv vid allvarliga extraartikulära manifestationer även i situationer där man avstår från annan immunsuppression (457). Som långsiktig strategi rekommenderas aktiv DMARD behandling till patienter med extraartikulära manifestationer, dels för att minska risken för ytterligare extraartikulära komplikationer, dels för att förebygga en allvarlig sjukdomsutveckling i övrigt (457). Till exempel förbättras ofta leukocytnivåer hos neutropena patienter med Feltys syndrom i samband med behandling med metotrexat (Mycket låg evidensstyrka)(458).
Behandling med abatacept tycks kunna minska sjukdomsaktiviteten och ge ökad tårproduktion och salivproduktion vid sekundärt Sjögrens syndrom hos patienter med RA (Låg evidensstyrka)(459).
Sammantaget bör intensifierad immunsupprimerande behandling övervägas till patienter med allvarliga extraartikulära manifestationer av RA, såsom systemisk vaskulit eller ILD. Vid aktiv ILD finns skäl att välja annan behandling än TNF-hämmare, och vid UIP-mönster i samråd med lungmedicinare överväga antifibrotisk behandling.
Läkemedelsbehandling av äldre patienter med RA
I EULARs rekommendationer för RA framgår att riktlinjerna inte är åldersspecifika men att hänsyn måste tas till ålder (1). Generellt gäller att även äldre patienter bör behandlas enligt treat-to-target-principen, men särskild hänsyn behöver tas till komorbiditet, polyfarmaci och njurfunktion, och dosjusteringar kan behövas.
Utöver kronologisk ålder bör även biologiska faktorer vägas in. Ett centralt begrepp i detta sammanhang är frailty (skörhet), som beskriver nedsatt fysiologisk reserv och ökad sårbarhet för stressfaktorer. Frailty är relaterat till, men inte detsamma som, hög ålder och bör beaktas vid val och uppföljning av behandling för att optimera nytta och minska risk. Vid RA är frailty vanligt (cirka en tredjedel av patienterna) och främst kopplat till hög sjukdomsaktivitet snarare än kronologisk ålder (460).
När det gäller läkemedelsval och säkerhet hos äldre RA-patienter visade en japansk metaanalys från 2024 att mtx och bDMARDs är effektiva även hos patienter >65 år, men att risken för biverkningar ökar, vilket påverkar risk-/nyttaförhållandet (461).
Methotrexate: Vid behandling med mtx krävs särskild vaksamhet vid nedsatt njurfunktion och vid interaktioner med till exempel diuretika, annan än hydroklortiazid, samt protonpumpshämmare (462). Allvarlig MTX-toxicitet, framför allt benmärgstoxicitet ses nästan uteslutande hos patienter >70 år och är kopplad till nedsatt njurfunktion och interaktionsgivande läkemedel. Behandling med MTX när eGFR är < 30 är inte tillrådligt.
Glukokortikoider: I GLORIA-studien, en RCT där patienter ≥65 år med aktiv RA randomiserades till 5 mg prednisolon dagligen eller placebo under två år som tillägg till standardbehandling, sågs signifikant lägre sjukdomsaktivitet och mindre ledförstörelse, men fler (oftast milda–måttliga) biverkningar och infektioner (463). Glukokortikoider har en tydligt dosberoende påverkan på infektionsrisken, och denna är högre än för csDMARDs och vid högre doser i nivå med eller högre än för b/tsDMARDs. Högre ålder förstärker risken ytterligare (464).
bDMARDs och tsDMARDs. I en metaanalys av 32 studier (post-hoc RCTs och observationsstudier) med över 95 000 patienter (varav cirka 24 % ≥60 år) ingick TNFi (22 studier), tocilizumab (4), abatacept (2), tofacitinib (2), rituximab (1) och en studie med blandade biologiska läkemedel. TNFi hade god effekt hos äldre även om behandlingssvaret var något lägre hos äldre jämfört med yngre, dessutom sågs hos äldre en högre biverkningsrisk (framför allt infektioner). Abatacept hade likvärdig behandlingseffekt men det fanns signaler om ökad risk för allvarliga infektioner jämfört med yngre patienter. Tocilizumab och rituximab visade lägre behandlingseffekt och högre infektionsrisk hos äldre (465). En senare översikt visar att IL-6-hämmarna tocilizumab och sarilumab generellt har god tolerabilitet hos äldre. (466).
Avseende tsDMARDs: Var god se även avsnittet ”Säkerhetsaspekter på behandling med JAK-hämmare” (sid 29-31).
Sammanfattning. Treat-to-target-principen gäller även för äldre patienter, men behandlingen bör individualiseras med hänsyn till biologisk ålder och andra aspekter. Särskild uppmärksamhet krävs avseende njurfunktion, läkemedelsinteraktioner och infektionsrisk. Alla DMARDs kan användas med god effekt hos äldre, men med ökad risk för biverkningar, särskilt infektioner. Avseende behandling med glukokortikoider bör lägsta möjliga dos under kortast möjliga tid eftersträvas.
Uppföljningssystem och principer för utvärdering av farmakologisk behandling
Det är väsentligt att individuella effektmål uppsättes och att behandlingen utvärderas kontinuerligt. I den kliniska utvärderingen ingår t.ex. HAQ, VAS-skalor för global hälsa och smärta, ledömhet /ledsvullnad och biokemiska inflammationsvariabler. I klinisk praxis kan DAS-nivåer, CDAI-nivåer eller SDAI-nivåer med fördel användas vid evaluering. ACR responskriterier och EULAR responskriterier är komplement i den kliniska utvärderingen av enskilda patienter, men det bör påpekas att dessa mått främst är utvecklade för att användas i kliniska prövningar. Kriterier för remission enligt ACR eller EULAR bör också beaktas (se Appendix 4). Studier kring optimal monitorering av leddestruktion med röntgen saknas, men i enlighet med EULAR riktlinjer (1, 63) och Personcentrerat och Sammanhållet Vårdförlopp (PSV) för Reumatoid Artrit rekommenderas att röntgen av händer och fötter genomförs vid diagnos samt övervägs i samband med 1-årsuppföljning. Även senare kan röntgen behövas som beslutsunderlag för upp- eller nedtrappning av terapi. Sammanfattningsvis bör understrykas att inget enskilt effektmått kan ersätta reumatologens samlade bedömning av terapisvar.
Om behandlingen ger en kliniskt signifikant förbättring efter sammanvägning av tillgänglig information enligt ovan, fortsättes den, om inte skall behandlingen avbrytas. Vid tveksamhet beträffande effekt rekommenderas strukturerat utsättningsförsök, dvs utvärdering av sjukdomsaktivitet efter utsättning enligt samma modell som skisserats för utvärdering av behandlingseffekt. Se även avsnittet Nedtrappning eller avslutning av DMARDs.
Uppföljning av patienter som behandlas med nya eller etablerade behandlingsformer skall ske på ett strukturerat sätt för att verifiera terapieffekter som visats i kliniska studier, men även för att följa utvecklingen av eventuella biverkningar. Här bör poängteras att alla oväntade händelser under behandling med nya preparat skall registreras och rapporteras oberoende av om man bedömer att ett samband med behandlingen föreligger eller ej. Alla som behandlar patienter med RA rekommenderas att följa upp effekter och biverkningar av behandling med hjälp av SRQ, som drivs av SRF, där en elektronisk biverkningsrapporterings-modul finns för direkt rapportering av biverkningar.
Indikatorer och målnivåer från Socialstyrelsen
Socialstyrelsens nationella riktlinjer för rörelseorganens sjukdomar uppdaterades 2021 (3). I dessa ingår en rad indikatorer avsedda för användning i strukturerad uppföljning av riktlinjernas användning. https://www.socialstyrelsen.se/kunskapsstod-och-regler/regler-och-riktlinjer/nationella-riktlinjer/riktlinjer-och-utvarderingar/rorelseorganens-sjukdomar/
Därutöver har Socialstyrelsen fastställt målnivåer för flera av dessa indikatorer, bland annat några som är direkt kopplade till läkemedelsbehandling vid RA:
- Andelen patienter med nyinsatt behandling med DMARD mot RA som har uppföljande registrering i SRQ inom 2-6- månader. Målnivå: ≥ 90 %
- Andelen patienter med RA som behandlas med bDMARDs eller tsDMARDs. Målnivå: Riksgenomsnittet ± 25 %.
- Andelen patienter med RA som får bDMARD utan tidigare behandling med csDMARD. Målnivå: Riksgenomsnittet ± 25 %.
Övriga rekommendationer av relevans för läkemedelsbehandling vid RA
Säkerhetsaspekter på behandling med DMARDs
- Vaccination hos patienter med inflammatoriska reumatiska sjukdomar.
- Läkemedelsbehandling i samband med graviditet och amning hos patienter med reumatisk sjukdom.
- Screening för tuberkulos hos patienter med reumatisk sjukdom inför start av bDMARDbehandling.
- Screening för hepatit B inför behandling med bDMARD
- Antibiotikaprofylax vid tandvård
- Provtagning och kontroller vid antireumatisk behandling
- Ögonkontroller vid behandling med klorokinpreparat
Rekommendationerna finns på SRFs hemsida (http://www.svenskreumatologi.se/index2.htm).
Primärprevention avseende kardiovaskulära riskfaktorer vid inflammatorisk reumatisk sjukdom
Patienter med RA, som grupp betraktade, löper ökad risk att insjukna i hjärt-kärlsjukdom. Särskilt gäller det patienter som har extraartikulära manifestationer och/eller persisterande hög SR/CRP. Dessa grupper har en riskökning jämförbar med den man ser vid diabetes mellitus. Det är därför angeläget att vi reumatologer screenar för kardiovaskulära riskfaktorer och ser till att behandling av dessa initieras. Beroende på lokala traditioner bör dock behandlingen i flertalet fall skötas av eller i nära samarbete med primärvården. Det ankommer dock på oss att sprida kunskapen om den ökade risken för kardiovaskulär sjukdom hos reumatiker till primärvården. Var god se rekommendationer på hemsidan (http://www.svenskreumatologi.se/index2.htm).
Som ett komplement till dessa rekommendationer finns bakgrundsdokumentation om kunskapsläget om inverkan på kardiovaskulär risk för olika antireumatiska läkemedel.
Osteoporos
Förutom den lednära nedsättningen av bentätheten har patienter med RA också en ökad risk för generaliserad osteoporos och för osteoporosrelaterade frakturer. Låg bentäthet är associerat till erosivitetsgrad och minskning av bentätheten sammanhänger bland annat med sjukdomsaktiviteten (467, 468). Utöver behandling med DMARDs bör även ställningstagande till utredning av, profylax mot och behandling av osteoporos göras vid RA. Var god se även Läkemedelverkets behandlingsrekommendation för osteoporos (Läkemedel vid osteoporos för att förhindra benskörhetsfrakturer – behandlingsrekommendation | Läkemedelsverket (lakemedelsverket.se)), Socialstyrelsens nationella riktlinjer för diagnostik och behandling av osteoporos, Nationella riktlinjer för rörelseorganens sjukdomar – stöd för styrning och ledning (Nationella riktlinjer för rörelseorganens sjukdomar – Socialstyrelsen) EULARs rekommendationer för prevention och handläggning av osteoporotiska frakturer från 2016 (469) samt , ACRs rekommendationer för prevention och behandling av kortisoninducerad osteoporos från 2017 (470).
Med hjälp av FRAX (WHO fracture risk assessement tool) kan frakturrisk uppskattas. FRAX resultatet utgör ett hjälpmedel för att ta ställning till om bentäthetsmätning bör göras och om specifik behandling bör sättas in. Att ha behandlats med 5 mg prednisolon per dag i minst tre månader och att ha RA utgör två av flera oberoende riskfaktorer i FRAX (http://www.shef.ac.uk/FRAX/?lang=se). Det finns dock indikationer på att FRAX underestimerar risken för fraktur vid RA (471).
Flödesscheman
Flödesschema 1 - Behandlingsstrategier vid tidig RA och rekommendationer vid ofullständig terapieffekt
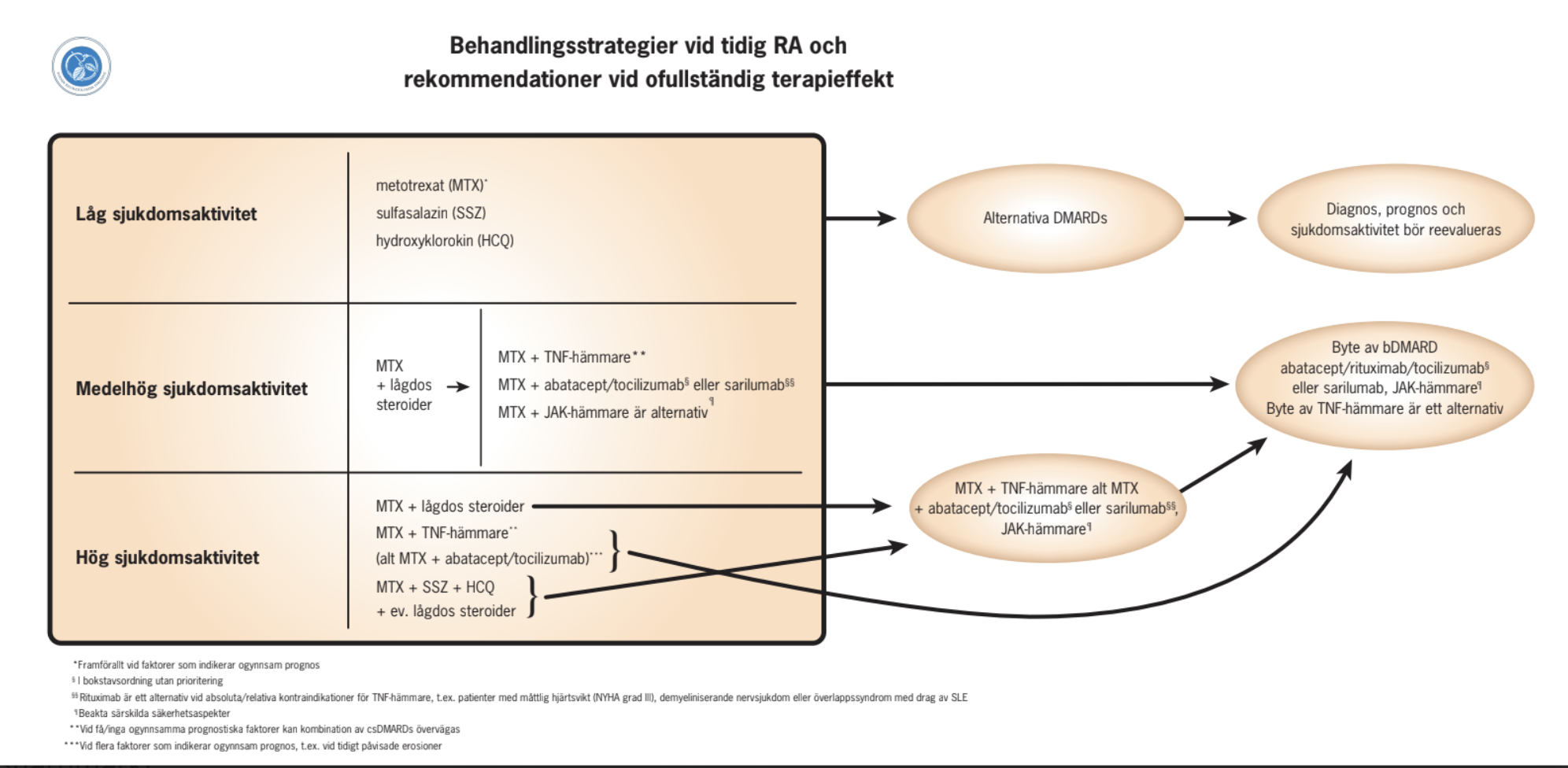
Flödesscham 2 - Läkemedelsbehandling vid RA: Rekommendationer vid intolerans för metotrexat, och strategier vid ofullständig terapieffekt
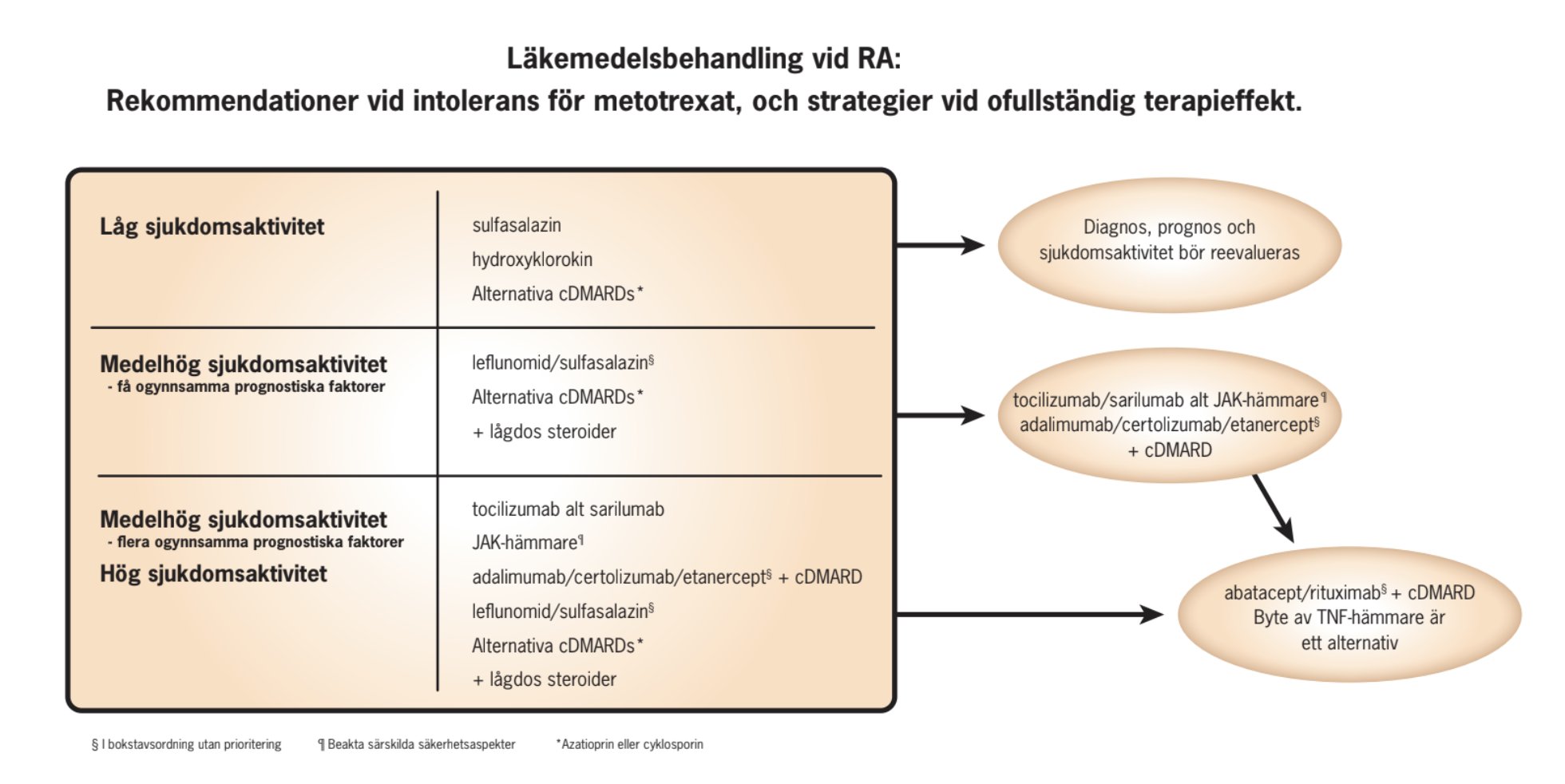
Dokument
Riktlinjer för läkemedelsbehandling vid RA
Flödesschema Behandlingsstrategier vid tidig RA och rekommendationer vid ofullständig terapieffekt
Flödesschema Rekommendationer vid intolerans för metotrexat, och strategier vid ofullständig terapieffekt
Appendix
1. Evidensgradering
2. Kloka kliniska val
3 klassifikationskriterier
4. Gradering av sjukdomsaktivitet
5. Remissionskriterier
6. Bilddiagnostik faktaruta
7. Bdmards och tsdmards
Referenser
Referenser
- Smolen JS, Landewé RBM, Bergstra SA, Kerschbaumer A, Sepriano A, Aletaha D, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2022 update. Ann Rheum Dis. 2023;82(1):3-18.
- Fraenkel L, Bathon J, England BR, St Clair EW, Arayssi T, Carandang K, et al. 2021 American College of Rheumatology Guideline for the Treatment of Rheumatoid Arthritis. Arthritis Rheumatol. 2021;73(7):1108-23.
- Socialstyrelsen. Nationella riktlinjer för rörelseorganens sjukdomar. Reumatoid artrit, axial spondylartrit, psoriasisartrit, artros och osteoporos. 2021. Stöd för styrning och ledning. Artikelnummer 2021-1-7137. ISBN 978-91-7555-551-5 2021.
- Socialstyrelsen. Nationella riktlinjer för rörelseorganens sjukdomar. Osteoporos,artros, inflammatorisk ryggsjukdom och ankyloserande spondylit, psoriasisartrit och reumatoid artrit. Stöd för styrning och ledning. 2012-5-1. 2012.
- Aletaha D, Neogi T, Silman AJ, Funovits J, Felson DT, Bingham CO, 3rd, et al. 2010 Rheumatoid arthritis classification criteria: an American College of Rheumatology/European League Against Rheumatism collaborative initiative. Arthritis Rheum. 2010;62(9):2569-81.
- van der Heijde D, van der Helm-van Mil AH, Aletaha D, Bingham CO, Burmester GR, Dougados M, et al. EULAR definition of erosive disease in light of the 2010 ACR/EULAR rheumatoid arthritis classification criteria. Ann Rheum Dis. 2013;72(4):479-81.
- Le Loet X, Nicolau J, Boumier P, Daragon A, Mejjad O, Pouplin S, et al. Validation of the 2010-ACR/EULAR -classification criteria using newly EULAR-defined erosion for rheumatoid arthritis on the very early arthritis community-based (VErA) cohort. Joint Bone Spine. 2015;82(1):38-41.
- Arnett FC, Edworthy SM, Bloch DA, McShane DJ, Fries JF, Cooper NS, et al. The American Rheumatism Association 1987 revised criteria for the classification of rheumatoid arthritis. Arthritis Rheum. 1988;31(3):315-24.
- Gerlag DM, Safy M, Maijer KI, Tang MW. Effects of B-cell directed therapy on the preclinical stage of rheumatoid arthritis: the PRAIRI study. 2019;78(2):179-85.
- Rech J, Tascilar K, Hagen M, Kleyer A, Manger B, Schoenau V, et al. Abatacept inhibits inflammation and onset of rheumatoid arthritis in individuals at high risk (ARIAA): a randomised, international, multicentre, double-blind, placebo-controlled trial. Lancet. 2024;403(10429):850-9.
- Cope AP, Jasenecova M, Vasconcelos JC, Filer A, Raza K, Qureshi S, et al. Abatacept in individuals at high risk of rheumatoid arthritis (APIPPRA): a randomised, double-blind, multicentre, parallel, placebo-controlled, phase 2b clinical trial. Lancet. 2024;403(10429):838-49.
- Deane KD, Striebich CC, Feser ML, O’Dell JR, James JA, Sparks JA, et al. A phase 2 trial of hydroxychloroquine in individuals at risk for rheumatoid arthritis. Arthritis Rheumatol. 2025.
- Krijbolder DI, Verstappen M, van Dijk BT, Dakkak YJ, Burgers LE, Boer AC, et al. Intervention with methotrexate in patients with arthralgia at risk of rheumatoid arthritis to reduce the development of persistent arthritis and its disease burden (TREAT EARLIER): a randomised, double-blind, placebo-controlled, proof-of-concept trial. Lancet. 2022;400(10348):283-94.
- Aletaha D, Smolen JS. The definition and measurement of disease modification in inflammatory rheumatic diseases. Rheum Dis Clin North Am. 2006;32(1):9-44, vii.
- Turesson C, O’Fallon WM, Crowson CS, Gabriel SE, Matteson EL. Occurrence of extraarticular disease manifestations is associated with excess mortality in a community based cohort of patients with rheumatoid arthritis. J Rheumatol. 2002;29(1):62-7.
- Turesson C, McClelland RL, Christianson TJ, Matteson EL. Severe extra-articular disease manifestations are associated with an increased risk of first ever cardiovascular events in patients with rheumatoid arthritis. Ann Rheum Dis. 2007;66(1):70-5.
- Wallberg-Jonsson S, Johansson H, Ohman ML, Rantapaa-Dahlqvist S. Extent of inflammation predicts cardiovascular disease and overall mortality in seropositive rheumatoid arthritis. A retrospective cohort study from disease onset. J Rheumatol. 1999;26(12):2562-71.
- Bohler C, Radner H, Smolen JS, Aletaha D. Serological changes in the course of traditional and biological disease modifying therapy of rheumatoid arthritis. Ann Rheum Dis. 2013;72(2):241-4.
- Prevoo ML, van ’t Hof MA, Kuper HH, van Leeuwen MA, van de Putte LB, van Riel PL. Modified disease activity scores that include twenty-eight-joint counts. Development and validation in a prospective longitudinal study of patients with rheumatoid arthritis. Arthritis Rheum. 1995;38(1):44-8.
- Fleischmann Rea. Disease activity score 28-joint count: are erythrocyte sedimentation and C-reactive protein versions comparable? Arthritis Rheum. 2012;64:S1128-S9.
- Sokka T, Toloza S, Cutolo M, Kautiainen H, Makinen H, Gogus F, et al. Women, men, and rheumatoid arthritis: analyses of disease activity, disease characteristics, and treatments in the QUEST-RA study. Arthritis Res Ther. 2009;11(1):R7.
- Ahlmén M, Svensson B, Albertsson K, Forslind K, Hafström I. Influence of gender on assessments of disease activity and function in early rheumatoid arthritis in relation to radiographic joint damage. Ann Rheum Dis. 2010;69(1):230-3.
- Smolen JS, Breedveld FC, Schiff MH, Kalden JR, Emery P, Eberl G, et al. A simplified disease activity index for rheumatoid arthritis for use in clinical practice. Rheumatology (Oxford). 2003;42(2):244-57.
- Aletaha D, Nell VP, Stamm T, Uffmann M, Pflugbeil S, Machold K, et al. Acute phase reactants add little to composite disease activity indices for rheumatoid arthritis: validation of a clinical activity score. Arthritis Res Ther. 2005;7(4):R796-806.
- Combe B, Landewe R, Daien CI, Hua C, Aletaha D, Alvaro-Gracia JM, et al. 2016 update of the EULAR recommendations for the management of early arthritis. 2017;76(6):948-59.
- Krabben A, Stomp W, van Nies JA, Huizinga TW, van der Heijde D, Bloem JL, et al. MRI-detected subclinical joint inflammation is associated with radiographic progression. Ann Rheum Dis. 2014;73(11):2034-7.
- Hetland ML, Ostergaard M, Stengaard-Pedersen K, Junker P, Ejbjerg B, Jacobsen S, et al. Anti-cyclic citrullinated peptide antibodies, 28-joint Disease Activity Score, and magnetic resonance imaging bone oedema at baseline predict 11 years’ functional and radiographic outcome in early rheumatoid arthritis. Scand J Rheumatol. 2019;48(1):1-8.
- Naredo E, Collado P, Cruz A, Palop MJ, Cabero F, Richi P, et al. Longitudinal power Doppler ultrasonographic assessment of joint inflammatory activity in early rheumatoid arthritis: predictive value in disease activity and radiologic progression. Arthritis Rheum. 2007;57(1):116-24.
- Funck-Brentano T, Gandjbakhch F, Etchepare F, Jousse-Joulin S, Miquel A, Cyteval C, et al. Prediction of radiographic damage in early arthritis by sonographic erosions and power Doppler signal: a longitudinal observational study. Arthritis Care Res (Hoboken). 2013;65(6):896-902.
- Boyesen P, Haavardsholm EA, van der Heijde D, Ostergaard M, Hammer HB, Sesseng S, et al. Prediction of MRI erosive progression: a comparison of modern imaging modalities in early rheumatoid arthritis patients. Ann Rheum Dis. 2011;70(1):176-9.
- Macchioni P, Magnani M, Mule R, Galletti S, Catanoso M, Pignotti E, et al. Ultrasonographic predictors for the development of joint damage in rheumatoid arthritis patients: a single joint prospective study. Clin Exp Rheumatol. 2013;31(1):8-17.
- Sundin U, Sundlisater NP, Aga AB, Sexton J, Nordberg LB, Hammer HB, et al. Value of MRI and ultrasound for prediction of therapeutic response and erosive progression in patients with early rheumatoid arthritis managed by an aggressive treat-to-target strategy. RMD Open. 2021;7(1).
- Carstensen SMD, Terslev L, Jensen MP, Østergaard M. Future use of musculoskeletal ultrasonography and magnetic resonance imaging in rheumatoid arthritis. Curr Opin Rheumatol. 2020;32(3):264-72.
- Sokka T, Kautiainen H, Hannonen P, Pincus T. Changes in Health Assessment Questionnaire disability scores over five years in patients with rheumatoid arthritis compared with the general population. Arthritis Rheum. 2006;54(10):3113-8.
- Young A, Koduri G, Batley M, Kulinskaya E, Gough A, Norton S, et al. Mortality in rheumatoid arthritis. Increased in the early course of disease, in ischaemic heart disease and in pulmonary fibrosis. Rheumatology (Oxford). 2007;46(2):350-7.
- Saevarsdottir S, Rezaei H, Geborek P, Petersson I, Ernestam S, Albertsson K, et al. Current smoking status is a strong predictor of radiographic progression in early rheumatoid arthritis: results from the SWEFOT trial. Ann Rheum Dis. 2015;74(8):1509-14.
- Mattey DL, Brownfield A, Dawes PT. Relationship between pack-year history of smoking and response to tumor necrosis factor antagonists in patients with rheumatoid arthritis. J Rheumatol. 2009;36(6):1180-7.
- Saevarsdottir S, Wedren S, Seddighzadeh M, Bengtsson C, Wesley A, Lindblad S, et al. Patients with early rheumatoid arthritis who smoke are less likely to respond to treatment with methotrexate and tumor necrosis factor inhibitors: observations from the Epidemiological Investigation of Rheumatoid Arthritis and the Swedish Rheumatology Register cohorts. Arthritis Rheum. 2011;63(1):26-36.
- Soderlin MK, Petersson IF, Geborek P. The effect of smoking on response and drug survival in rheumatoid arthritis patients treated with their first anti-TNF drug. Scand J Rheumatol. 2012;41(1):1-9.
- Khan A, Scott DL, Batley M. Smoking, rheumatoid factor status and responses to rituximab. Ann Rheum Dis. 2012;71(9):1587-8.
- Westhoff G, Rau R, Zink A. Radiographic joint damage in early rheumatoid arthritis is highly dependent on body mass index. Arthritis Rheum. 2007;56(11):3575-82.
- van der Helm-van Mil AH, van der Kooij SM, Allaart CF, Toes RE, Huizinga TW. A high body mass index has a protective effect on the amount of joint destruction in small joints in early rheumatoid arthritis. Ann Rheum Dis. 2008;67(6):769-74.
- de Rooy DP, van der Linden MP, Knevel R, Huizinga TW, van der Helm-van Mil AH. Predicting arthritis outcomes–what can be learned from the Leiden Early Arthritis Clinic? Rheumatology (Oxford). 2011;50(1):93-100.
- Baker JF, Ostergaard M, George M, Shults J, Emery P, Baker DG, et al. Greater body mass independently predicts less radiographic progression on X-ray and MRI over 1-2 years. Ann Rheum Dis. 2014;73(11):1923-8.
- Lupoli R, Pizzicato P, Scalera A, Ambrosino P, Amato M, Peluso R, et al. Impact of body weight on the achievement of minimal disease activity in patients with rheumatic diseases: a systematic review and meta-analysis. Arthritis Res Ther. 2016;18(1):297.
- Levitsky A, Brismar K, Hafstrom I, Hambardzumyan K, Lourdudoss C, van Vollenhoven RF, et al. Obesity is a strong predictor of worse clinical outcomes and treatment responses in early rheumatoid arthritis: results from the SWEFOT trial. RMD Open. 2017;3(2):e000458.
- Smolen JS, van der Heijde D, Machold KP, Aletaha D, Landewe R. Proposal for a new nomenclature of disease-modifying antirheumatic drugs. Ann Rheum Dis. 2014;73(1):3-5.
- Pinals RS, Masi AT, Larsen RA. Preliminary criteria for clinical remission in rheumatoid arthritis. Arthritis Rheum. 1981;24(10):1308-15.
- Aletaha D, Smolen JS. Joint damage in rheumatoid arthritis progresses in remission according to the Disease Activity Score in 28 joints and is driven by residual swollen joints. Arthritis Rheum. 2011;63(12):3702-11.
- Studenic P, Aletaha D, de Wit M, Stamm T, Alasti F, Lacaille D, et al. American College of Rheumatology/EULAR remission criteria for rheumatoid arthritis: 2022 revision. Ann Rheum Dis. 2023;82(1):74-80.
- Gandjbakhch F, Conaghan PG, Ejbjerg B, Haavardsholm EA, Foltz V, Brown AK, et al. Synovitis and osteitis are very frequent in rheumatoid arthritis clinical remission: results from an MRI study of 294 patients in clinical remission or low disease activity state. J Rheumatol. 2011;38(9):2039-44.
- Nguyen H, Ruyssen-Witrand A, Gandjbakhch F, Constantin A, Foltz V, Cantagrel A. Prevalence of ultrasound-detected residual synovitis and risk of relapse and structural progression in rheumatoid arthritis patients in clinical remission: a systematic review and meta-analysis. Rheumatology (Oxford). 2014;53(11):2110-8.
- Grigor C, Capell H, Stirling A, McMahon AD, Lock P, Vallance R, et al. Effect of a treatment strategy of tight control for rheumatoid arthritis (the TICORA study): a single-blind randomised controlled trial. Lancet. 2004;364(9430):263-9.
- Hetland ML, Stengaard-Pedersen K, Junker P, Lottenburger T, Ellingsen T, Andersen LS, et al. Combination treatment with methotrexate, cyclosporine, and intraarticular betamethasone compared with methotrexate and intraarticular betamethasone in early active rheumatoid arthritis: an investigator-initiated, multicenter, randomized, double-blind, parallel-group, placebo-controlled study. Arthritis Rheum. 2006;54(5):1401-9.
- Verstappen SM, Jacobs JW, van der Veen MJ, Heurkens AH, Schenk Y, ter Borg EJ, et al. Intensive treatment with methotrexate in early rheumatoid arthritis: aiming for remission. Computer Assisted Management in Early Rheumatoid Arthritis (CAMERA, an open-label strategy trial). Ann Rheum Dis. 2007;66(11):1443-9.
- Smolen JS, Breedveld FC, Burmester GR, Bykerk V, Dougados M, Emery P, et al. Treating rheumatoid arthritis to target: 2014 update of the recommendations of an international task force. 2016;75(1):3-15.
- Haavardsholm EA, Aga AB, Olsen IC, Lillegraven S, Hammer HB, Uhlig T, et al. Ultrasound in management of rheumatoid arthritis: ARCTIC randomised controlled strategy trial. Bmj. 2016;354:i4205.
- Dale J, Stirling A, Zhang R, Purves D, Foley J, Sambrook M, et al. Targeting ultrasound remission in early rheumatoid arthritis: the results of the TaSER study, a randomised clinical trial. Ann Rheum Dis. 2016;75(6):1043-50.
- Wolfe F, Michaud K. Severe rheumatoid arthritis (RA), worse outcomes, comorbid illness, and sociodemographic disadvantage characterize ra patients with fibromyalgia. J Rheumatol. 2004;31(4):695-700.
- Tubach F, Ravaud P, Martin-Mola E, Awada H, Bellamy N, Bombardier C, et al. Minimum clinically important improvement and patient acceptable symptom state in pain and function in rheumatoid arthritis, ankylosing spondylitis, chronic back pain, hand osteoarthritis, and hip and knee osteoarthritis: Results from a prospective multinational study. Arthritis Care Res (Hoboken). 2012;64(11):1699-707.
- Geenen R, Overman CL, Christensen R, Åsenlöf P, Capela S, Huisinga KL, et al. EULAR recommendations for the health professional’s approach to pain management in inflammatory arthritis and osteoarthritis. Ann Rheum Dis. 2018;77(6):797-807.
- Kosek E, Lampa J, Nisell R. Smärta och Inflammation vid reumatiska sjukdomar och vanliga smärttillstånd i rörelseapparaten. Lund: Studentlitteratur; 2019.
- Combe B, Landewe R, Lukas C, Bolosiu HD, Breedveld F, Dougados M, et al. EULAR recommendations for the management of early arthritis: report of a task force of the European Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT). Ann Rheum Dis. 2007;66(1):34-45.
- Visser K, Katchamart W, Loza E, Martinez-Lopez JA, Salliot C, Trudeau J, et al. Multinational evidence-based recommendations for the use of methotrexate in rheumatic disorders with a focus on rheumatoid arthritis: integrating systematic literature research and expert opinion of a broad international panel of rheumatologists in the 3E Initiative. Ann Rheum Dis. 2009;68(7):1086-93.
- Visser K, van der Heijde D. Optimal dosage and route of administration of methotrexate in rheumatoid arthritis: a systematic review of the literature. Ann Rheum Dis. 2009;68(7):1094-9.
- Lopez-Olivo MA, Siddhanamatha HR, Shea B, Tugwell P, Wells GA, Suarez-Almazor ME. Methotrexate for treating rheumatoid arthritis. Cochrane Database Syst Rev. 2014(6):Cd000957.
- Braun J, Kastner P, Flaxenberg P, Wahrisch J, Hanke P, Demary W, et al. Comparison of the clinical efficacy and safety of subcutaneous versus oral administration of methotrexate in patients with active rheumatoid arthritis: results of a six-month, multicenter, randomized, double-blind, controlled, phase IV trial. Arthritis Rheum. 2008;58(1):73-81.
- Bujor AM, Janjua S, LaValley MP, Duran J, Braun J, Felson DT. Comparison of oral versus parenteral methotrexate in the treatment of rheumatoid arthritis: A meta-analysis. PLoS One. 2019;14(9):e0221823.
- Lambert CM, Sandhu S, Lochhead A, Hurst NP, McRorie E, Dhillon V. Dose escalation of parenteral methotrexate in active rheumatoid arthritis that has been unresponsive to conventional doses of methotrexate: a randomized, controlled trial. Arthritis Rheum. 2004;50(2):364-71.
- Scott DG, Claydon P, Ellis C. Retrospective evaluation of continuation rates following a switch to subcutaneous methotrexate in rheumatoid arthritis patients failing to respond to or tolerate oral methotrexate: the MENTOR study. Scand J Rheumatol. 2014;43(6):470-6.
- Li D, Yang Z, Kang P, Xie X. Subcutaneous administration of methotrexate at high doses makes a better performance in the treatment of rheumatoid arthritis compared with oral administration of methotrexate: A systematic review and meta-analysis. Semin Arthritis Rheum. 2016;45(6):656-62.
- Ortiz Z, Shea B, Suarez Almazor M, Moher D, Wells G, Tugwell P. Folic acid and folinic acid for reducing side effects in patients receiving methotrexate for rheumatoid arthritis. Cochrane Database Syst Rev. 2000(2):Cd000951.
- Prey S, Paul C. Effect of folic or folinic acid supplementation on methotrexate-associated safety and efficacy in inflammatory disease: a systematic review. Br J Dermatol. 2009;160(3):622-8.
- Liu L, Liu S, Wang C, Guan W, Zhang Y, Hu W, et al. Folate Supplementation for Methotrexate Therapy in Patients With Rheumatoid Arthritis: A Systematic Review. J Clin Rheumatol. 2019;25:197-202.
- Moreland LW, Schiff MH, Baumgartner SW, Tindall EA, Fleischmann RM, Bulpitt KJ, et al. Etanercept therapy in rheumatoid arthritis. A randomized, controlled trial. Ann Intern Med. 1999;130(6):478-86.
- Lipsky PE, van der Heijde DM, St Clair EW, Furst DE, Breedveld FC, Kalden JR, et al. Infliximab and methotrexate in the treatment of rheumatoid arthritis. Anti-Tumor Necrosis Factor Trial in Rheumatoid Arthritis with Concomitant Therapy Study Group. N Engl J Med. 2000;343(22):1594-602.
- Weinblatt ME, Keystone EC, Furst DE, Moreland LW, Weisman MH, Birbara CA, et al. Adalimumab, a fully human anti-tumor necrosis factor alpha monoclonal antibody, for the treatment of rheumatoid arthritis in patients taking concomitant methotrexate: the ARMADA trial. Arthritis Rheum. 2003;48(1):35-45.
- Gartlehner G, Hansen RA, Jonas BL, Thieda P, Lohr KN. The comparative efficacy and safety of biologics for the treatment of rheumatoid arthritis: a systematic review and metaanalysis. J Rheumatol. 2006;33(12):2398-408.
- Smolen J, Landewe RB, Mease P, Brzezicki J, Mason D, Luijtens K, et al. Efficacy and safety of certolizumab pegol plus methotrexate in active rheumatoid arthritis: the RAPID 2 study. A randomised controlled trial. Ann Rheum Dis. 2009;68(6):797-804.
- Keystone EC, Genovese MC, Klareskog L, Hsia EC, Hall ST, Miranda PC, et al. Golimumab, a human antibody to tumour necrosis factor {alpha} given by monthly subcutaneous injections, in active rheumatoid arthritis despite methotrexate therapy: the GO-FORWARD Study. Ann Rheum Dis. 2009;68(6):789-96.
- Kremer JM, Westhovens R, Leon M, Di Giorgio E, Alten R, Steinfeld S, et al. Treatment of rheumatoid arthritis by selective inhibition of T-cell activation with fusion protein CTLA4Ig. N Engl J Med. 2003;349(20):1907-15.
- Kremer JM, Dougados M, Emery P, Durez P, Sibilia J, Shergy W, et al. Treatment of rheumatoid arthritis with the selective costimulation modulator abatacept: twelve-month results of a phase iib, double-blind, randomized, placebo-controlled trial. Arthritis Rheum. 2005;52(8):2263-71.
- Smolen JS, Beaulieu A, Rubbert-Roth A, Ramos-Remus C, Rovensky J, Alecock E, et al. Effect of interleukin-6 receptor inhibition with tocilizumab in patients with rheumatoid arthritis (OPTION study): a double-blind, placebo-controlled, randomised trial. Lancet. 2008;371(9617):987-97.
- Genovese MC, McKay JD, Nasonov EL, Mysler EF, da Silva NA, Alecock E, et al. Interleukin-6 receptor inhibition with tocilizumab reduces disease activity in rheumatoid arthritis with inadequate response to disease-modifying antirheumatic drugs: the tocilizumab in combination with traditional disease-modifying antirheumatic drug therapy study. Arthritis Rheum. 2008;58(10):2968-80.
- Weinblatt ME, Schiff M, Valente R, van der Heijde D, Citera G, Zhao C, et al. Head-to-head comparison of subcutaneous abatacept versus adalimumab for rheumatoid arthritis: findings of a phase IIIb, multinational, prospective, randomized study. Arthritis Rheum. 2013;65(1):28-38.
- Genovese MC, Fleischmann R, Kivitz AJ, Rell-Bakalarska M, Martincova R, Fiore S, et al. Sarilumab Plus Methotrexate in Patients With Active Rheumatoid Arthritis and Inadequate Response to Methotrexate: Results of a Phase III Study. Arthritis Rheumatol. 2015;67(6):1424-37.
- van Vollenhoven RF, Fleischmann R, Cohen S, Lee EB, Garcia Meijide JA, Wagner S, et al. Tofacitinib or adalimumab versus placebo in rheumatoid arthritis. N Engl J Med. 2012;367(6):508-19.
- Kremer J, Li ZG, Hall S, Fleischmann R, Genovese M, Martin-Mola E, et al. Tofacitinib in combination with nonbiologic disease-modifying antirheumatic drugs in patients with active rheumatoid arthritis: a randomized trial. Ann Intern Med. 2013;159(4):253-61.
- van der Heijde D, Tanaka Y, Fleischmann R, Keystone E, Kremer J, Zerbini C, et al. Tofacitinib (CP-690,550) in patients with rheumatoid arthritis receiving methotrexate: twelve-month data from a twenty-four-month phase III randomized radiographic study. Arthritis Rheum. 2013;65(3):559-70.
- Dougados M, van der Heijde D. Baricitinib in patients with inadequate response or intolerance to conventional synthetic DMARDs: results from the RA-BUILD study. 2017;76(1):88-95.
- Taylor PC, Keystone EC, van der Heijde D, Weinblatt ME, Del Carmen Morales L, Reyes Gonzaga J, et al. Baricitinib versus Placebo or Adalimumab in Rheumatoid Arthritis. N Engl J Med. 2017;376(7):652-62.
- Burmester GR, Kremer JM, Van den Bosch F, Kivitz A, Bessette L, Li Y, et al. Safety and efficacy of upadacitinib in patients with rheumatoid arthritis and inadequate response to conventional synthetic disease-modifying anti-rheumatic drugs (SELECT-NEXT): a randomised, double-blind, placebo-controlled phase 3 trial. Arthritis Rheumatol. 2018;391(10139):2503-12.
- Fleischmann R, Pangan AL, Song IH, Mysler E, Bessette L, Peterfy C, et al. Upadacitinib Versus Placebo or Adalimumab in Patients With Rheumatoid Arthritis and an Inadequate Response to Methotrexate: Results of a Phase III, Double-Blind, Randomized Controlled Trial. 2019;71(11):1788-800.
- van Vollenhoven RF, Ernestam S, Geborek P, Petersson IF, Coster L, Waltbrand E, et al. Addition of infliximab compared with addition of sulfasalazine and hydroxychloroquine to methotrexate in patients with early rheumatoid arthritis (Swefot trial): 1-year results of a randomised trial. Lancet. 2009;374(9688):459-66.
- Moreland LW, O’Dell JR, Paulus HE, Curtis JR, Bathon JM, St Clair EW, et al. A randomized comparative effectiveness study of oral triple therapy versus etanercept plus methotrexate in early aggressive rheumatoid arthritis: the treatment of Early Aggressive Rheumatoid Arthritis Trial. Arthritis Rheum. 2012;64(9):2824-35.
- O’Dell JR, Mikuls TR, Taylor TH, Ahluwalia V, Brophy M, Warren SR, et al. Therapies for active rheumatoid arthritis after methotrexate failure. N Engl J Med. 2013;369(4):307-18.
- Bae SC, Lee YH. Comparative efficacy and safety of TNF-inhibitor plus methotrexate versus oral triple therapy in patients with active rheumatoid arthritis inadequately responding to methotrexate: A meta-analysis of randomized controlled trials. Int J Clin Pharmacol Ther. 2018;56(6):263-9.
- Keystone EC, Kavanaugh AF, Sharp JT, Tannenbaum H, Hua Y, Teoh LS, et al. Radiographic, clinical, and functional outcomes of treatment with adalimumab (a human anti-tumor necrosis factor monoclonal antibody) in patients with active rheumatoid arthritis receiving concomitant methotrexate therapy: a randomized, placebo-controlled, 52-week trial. Arthritis Rheum. 2004;50(5):1400-11.
- Cohen SB, Tanaka Y, Mariette X, Curtis JR, Lee EB, Nash P, et al. Long-term safety of tofacitinib up to 9.5 years: a comprehensive integrated analysis of the rheumatoid arthritis clinical development programme. RMD Open. 2020;6(3):6:e001395
- Reed GW, Gerber RA, Shan Y, Takiya L, Dandreo KJ, Gruben D, et al. Real-World Comparative Effectiveness of Tofacitinib and Tumor Necrosis Factor Inhibitors as Monotherapy and Combination Therapy for Treatment of Rheumatoid Arthritis. Rheumatol Ther. 2019;6(4):573-86.
- Kremer JM, Bingham CO, 3rd, Cappelli LC, Greenberg JD, Madsen AM, Geier J, et al. Postapproval Comparative Safety Study of Tofacitinib and Biological Disease-Modifying Antirheumatic Drugs: 5-Year Results from a United States-Based Rheumatoid Arthritis Registry. ACR Open Rheumatol. 2021;3(3):173-84.
- Choy EH, Smith C, Dore CJ, Scott DL. A meta-analysis of the efficacy and toxicity of combining disease-modifying anti-rheumatic drugs in rheumatoid arthritis based on patient withdrawal. Rheumatology (Oxford). 2005;44(11):1414-21.
- Capell HA, Madhok R, Porter DR, Munro RA, McInnes IB, Hunter JA, et al. Combination therapy with sulfasalazine and methotrexate is more effective than either drug alone in patients with rheumatoid arthritis with a suboptimal response to sulfasalazine: results from the double-blind placebo-controlled MASCOT study. Ann Rheum Dis. 2007;66(2):235-41.
- Trnavsky K, Gatterova J, Linduskova M, Peliskova Z. Combination therapy with hydroxychloroquine and methotrexate in rheumatoid arthritis. Z Rheumatol. 1993;52(5):292-6.
- Rempenault C, Combe B, Barnetche T, Gaujoux-Viala C, Lukas C, Morel J, et al. Clinical and Structural Efficacy of Hydroxychloroquine in Rheumatoid Arthritis: A Systematic Review. Arthritis Care Res (Hoboken). 2019.
- O’Dell JR, Leff R, Paulsen G, Haire C, Mallek J, Eckhoff PJ, et al. Treatment of rheumatoid arthritis with methotrexate and hydroxychloroquine, methotrexate and sulfasalazine, or a combination of the three medications: results of a two-year, randomized, double-blind, placebo-controlled trial. Arthritis Rheum. 2002;46(5):1164-70.
- Tugwell P, Pincus T, Yocum D, Stein M, Gluck O, Kraag G, et al. Combination therapy with cyclosporine and methotrexate in severe rheumatoid arthritis. The Methotrexate-Cyclosporine Combination Study Group. N Engl J Med. 1995;333(3):137-41.
- Kremer JM, Genovese MC, Cannon GW, Caldwell JR, Cush JJ, Furst DE, et al. Concomitant leflunomide therapy in patients with active rheumatoid arthritis despite stable doses of methotrexate. A randomized, double-blind, placebo-controlled trial. Ann Intern Med. 2002;137(9):726-33.
- Genovese MC, Kalunian K, Gottenberg JE, Mozaffarian N, Bartok B, Matzkies F, et al. Effect of Filgotinib vs Placebo on Clinical Response in Patients With Moderate to Severe Rheumatoid Arthritis Refractory to Disease-Modifying Antirheumatic Drug Therapy: The FINCH 2 Randomized Clinical Trial. Jama. 2019;322(4):315-25.
- Combe B, Kivitz A, Tanaka Y, van der Heijde D, Simon J, Baraf H, et al. Filgotinib versus placebo or adalimumab in patients with rheumatoid arthritis and inadequate response to methotrexate: a phase III randomised clinical trial. Ann Rheum Dis. 2021;80(7):848-58.
- Curtis JR, Beukelman T, Onofrei A, Cassell S, Greenberg JD, Kavanaugh A, et al. Elevated liver enzyme tests among patients with rheumatoid arthritis or psoriatic arthritis treated with methotrexate and/or leflunomide. Ann Rheum Dis. 2010;69(1):43-7.
- Bird P, Griffiths H, Tymms K, Nicholls D, Roberts L, Arnold M, et al. The SMILE study — safety of methotrexate in combination with leflunomide in rheumatoid arthritis. J Rheumatol. 2013;40(3):228-35.
- Sung YK, Cho SK, Kim D, Choi CB, Won S, Bang SY, et al. Comparative effectiveness of treatment options after conventional DMARDs failure in rheumatoid arthritis. Rheumatol Int. 2017;37(6):975-82.
- Erhardt DP, Cannon GW, Teng CC, Mikuls TR, Curtis JR. Low Persistence Rates in Rheumatoid Arthritis Patients Treated with Triple Therapy are Attributed to Adverse Drug Events Associated with Sulfasalazine. Arthritis Care Res (Hoboken). 2019;71(10):1326-35.
- Schiff M, Weinblatt ME, Valente R, van der Heijde D, Citera G, Elegbe A, et al. Head-to-head comparison of subcutaneous abatacept versus adalimumab for rheumatoid arthritis: two-year efficacy and safety findings from AMPLE trial. Ann Rheum Dis. 2014;73(1):86-94.
- Keystone EC, Taylor PC, Tanaka Y, Gaich C, DeLozier AM, Dudek A, et al. Patient-reported outcomes from a phase 3 study of baricitinib versus placebo or adalimumab in rheumatoid arthritis: secondary analyses from the RA-BEAM study. N Engl J Med. 2017;76(11):1853-61.
- Hannonen P, Mottonen T, Hakola M, Oka M. Sulfasalazine in early rheumatoid arthritis. A 48-week double-blind, prospective, placebo-controlled study. Arthritis Rheum. 1993;36(11):1501-9.
- Strand V, Cohen S, Schiff M, Weaver A, Fleischmann R, Cannon G, et al. Treatment of active rheumatoid arthritis with leflunomide compared with placebo and methotrexate. Leflunomide Rheumatoid Arthritis Investigators Group. Arch Intern Med. 1999;159(21):2542-50.
- Gabay C, Emery P, van Vollenhoven R, Dikranian A, Alten R, Pavelka K, et al. Tocilizumab monotherapy versus adalimumab monotherapy for treatment of rheumatoid arthritis (ADACTA): a randomised, double-blind, controlled phase 4 trial. Lancet. 2013;381(9877):1541-50.
- Jones G, Sebba A, Gu J, Lowenstein MB, Calvo A, Gomez-Reino JJ, et al. Comparison of tocilizumab monotherapy versus methotrexate monotherapy in patients with moderate to severe rheumatoid arthritis: the AMBITION study. Ann Rheum Dis. 2010;69(1):88-96.
- Nishimoto N, Hashimoto J, Miyasaka N, Yamamoto K, Kawai S, Takeuchi T, et al. Study of active controlled monotherapy used for rheumatoid arthritis, an IL-6 inhibitor (SAMURAI): evidence of clinical and radiographic benefit from an x ray reader-blinded randomised controlled trial of tocilizumab. Ann Rheum Dis. 2007;66(9):1162-7.
- Burmester GR, Lin Y, Patel R, van Adelsberg J, Mangan EK, Graham NM, et al. Efficacy and safety of sarilumab monotherapy versus adalimumab monotherapy for the treatment of patients with active rheumatoid arthritis (MONARCH): a randomised, double-blind, parallel-group phase III trial. Ann Rheum Dis. 2017;76(5):840-7.
- Fleischmann R, Kremer J, Cush J, Schulze-Koops H, Connell CA, Bradley JD, et al. Placebo-controlled trial of tofacitinib monotherapy in rheumatoid arthritis. N Engl J Med. 2012;367(6):495-507.
- Fleischmann R, Mysler E, Hall S, Kivitz AJ, Moots RJ, Luo Z, et al. Efficacy and safety of tofacitinib monotherapy, tofacitinib with methotrexate, and adalimumab with methotrexate in patients with rheumatoid arthritis (ORAL Strategy): a phase 3b/4, double-blind, head-to-head, randomised controlled trial. Lancet. 2017;390(10093):457-68.
- Smolen JS, Pangan AL, Emery P, Rigby W, Tanaka Y, Vargas JI, et al. Upadacitinib as monotherapy in patients with active rheumatoid arthritis and inadequate response to methotrexate (SELECT-MONOTHERAPY): a randomised, placebo-controlled, double-blind phase 3 study. Lancet. 2019;393(10188):2303-11.
- Kavanaugh A, Kremer J, Ponce L, Cseuz R, Reshetko OV, Stanislavchuk M, et al. Filgotinib (GLPG0634/GS-6034), an oral selective JAK1 inhibitor, is effective as monotherapy in patients with active rheumatoid arthritis: results from a randomised, dose-finding study (DARWIN 2). Ann Rheum Dis. 2017;76(6):1009-19.
- Lee EB, Fleischmann R, Hall S, Wilkinson B, Bradley JD, Gruben D, et al. Tofacitinib versus methotrexate in rheumatoid arthritis. N Engl J Med. 2014;370(25):2377-86.
- van Vollenhoven R, Takeuchi T, Pangan AL, Friedman A, Mohamed MF, Chen S, et al. Efficacy and Safety of Upadacitinib Monotherapy in Methotrexate-naïve Patients with Moderately to Severely Active Rheumatoid Arthritis (SELECT-EARLY): Multi-center, Multi-country, Randomized, Double-blind, Active-comparator Trial. Arthritis Rheumatol. 2020;72(10):1607-20.
- Fleischmann R, Schiff M, van der Heijde D, Ramos-Remus C, Spindler A, Stanislav M, et al. Baricitinib, Methotrexate, or Combination in Patients With Rheumatoid Arthritis and No or Limited Prior Disease-Modifying Antirheumatic Drug Treatment. Arthritis Rheumatol. 2017;69(3):506-17.
- Emery P, Pope JE, Kruger K, Lippe R, DeMasi R, Lula S, et al. Efficacy of Monotherapy with Biologics and JAK Inhibitors for the Treatment of Rheumatoid Arthritis: A Systematic Review. Adv Ther. 2018;35(10):1535-63.
- Tanaka Y, Yamamoto K, Takeuchi T, Yamanaka H, Ishiguro N, Eguchi K, et al. Long-term efficacy and safety of certolizumab pegol in Japanese rheumatoid arthritis patients who could not receive methotrexate: 52-week results from an open-label extension of the HIKARI study. Mod Rheumatol. 2014;24(5):725-33.
- Fleischmann R, Vencovsky J, van Vollenhoven RF, Borenstein D, Box J, Coteur G, et al. Efficacy and safety of certolizumab pegol monotherapy every 4 weeks in patients with rheumatoid arthritis failing previous disease-modifying antirheumatic therapy: the FAST4WARD study. Ann Rheum Dis. 2009;68(6):805-11.
- Klareskog L, van der Heijde D, de Jager JP, Gough A, Kalden J, Malaise M, et al. Therapeutic effect of the combination of etanercept and methotrexate compared with each treatment alone in patients with rheumatoid arthritis: double-blind randomised controlled trial. Lancet. 2004;363(9410):675-81.
- Breedveld FC, Weisman MH, Kavanaugh AF, Cohen SB, Pavelka K, van Vollenhoven R, et al. The PREMIER study: A multicenter, randomized, double-blind clinical trial of combination therapy with adalimumab plus methotrexate versus methotrexate alone or adalimumab alone in patients with early, aggressive rheumatoid arthritis who had not had previous methotrexate treatment. Arthritis Rheum. 2006;54(1):26-37.
- Kristensen LE, Saxne T, Nilsson JA, Geborek P. Impact of concomitant DMARD therapy on adherence to treatment with etanercept and infliximab in rheumatoid arthritis. Results from a six-year observational study in southern Sweden. Arthritis Res Ther. 2006;8(6):R174.
- Genovese MC, Becker JC, Schiff M, Luggen M, Sherrer Y, Kremer J, et al. Abatacept for rheumatoid arthritis refractory to tumor necrosis factor alpha inhibition. N Engl J Med. 2005;353(11):1114-23.
- Cohen SB, Emery P, Greenwald MW, Dougados M, Furie RA, Genovese MC, et al. Rituximab for rheumatoid arthritis refractory to anti-tumor necrosis factor therapy: Results of a multicenter, randomized, double-blind, placebo-controlled, phase III trial evaluating primary efficacy and safety at twenty-four weeks. Arthritis Rheum. 2006;54(9):2793-806.
- Emery P, Keystone E, Tony HP, Cantagrel A, van Vollenhoven R, Sanchez A, et al. IL-6 receptor inhibition with tocilizumab improves treatment outcomes in patients with rheumatoid arthritis refractory to anti-tumour necrosis factor biologicals: results from a 24-week multicentre randomised placebo-controlled trial. Ann Rheum Dis. 2008;67(11):1516-23.
- Fleischmann R, van Adelsberg J, Lin Y, Castelar-Pinheiro GD, Brzezicki J, Hrycaj P, et al. Sarilumab and Nonbiologic Disease-Modifying Antirheumatic Drugs in Patients With Active Rheumatoid Arthritis and Inadequate Response or Intolerance to Tumor Necrosis Factor Inhibitors. Arthritis Rheumatol. 2017;69(2):277-90.
- Burmester GR, Blanco R, Charles-Schoeman C, Wollenhaupt J, Zerbini C, Benda B, et al. Tofacitinib (CP-690,550) in combination with methotrexate in patients with active rheumatoid arthritis with an inadequate response to tumour necrosis factor inhibitors: a randomised phase 3 trial. Lancet. 2013;381(9865):451-60.
- Genovese MC, Kremer J, Zamani O, Ludivico C, Krogulec M, Xie L, et al. Baricitinib in Patients with Refractory Rheumatoid Arthritis. N Engl J Med. 2016;374(13):1243-52.
- Hyrich KL, Lunt M, Watson KD, Symmons DP, Silman AJ. Outcomes after switching from one anti-tumor necrosis factor alpha agent to a second anti-tumor necrosis factor alpha agent in patients with rheumatoid arthritis: results from a large UK national cohort study. Arthritis Rheum. 2007;56(1):13-20.
- Karlsson JA, Kristensen LE, Kapetanovic MC, Gulfe A, Saxne T, Geborek P. Treatment response to a second or third TNF-inhibitor in RA: results from the South Swedish Arthritis Treatment Group Register. Rheumatology (Oxford). 2008;47(4):507-13.
- Smolen JS, Kay J, Doyle MK, Landewe R, Matteson EL, Wollenhaupt J, et al. Golimumab in patients with active rheumatoid arthritis after treatment with tumour necrosis factor alpha inhibitors (GO-AFTER study): a multicentre, randomised, double-blind, placebo-controlled, phase III trial. Lancet. 2009;374(9685):210-21.
- Mottonen T, Hannonen P, Leirisalo-Repo M, Nissila M, Kautiainen H, Korpela M, et al. Comparison of combination therapy with single-drug therapy in early rheumatoid arthritis: a randomised trial. FIN-RACo trial group. Lancet. 1999;353(9164):1568-73.
- Korpela M, Laasonen L, Hannonen P, Kautiainen H, Leirisalo-Repo M, Hakala M, et al. Retardation of joint damage in patients with early rheumatoid arthritis by initial aggressive treatment with disease-modifying antirheumatic drugs: five-year experience from the FIN-RACo study. Arthritis Rheum. 2004;50(7):2072-81.
- Rantalaiho V, Korpela M, Laasonen L, Kautiainen H, Jarvenpaa S, Hannonen P, et al. Early combination disease-modifying antirheumatic drug therapy and tight disease control improve long-term radiologic outcome in patients with early rheumatoid arthritis: the 11-year results of the Finnish Rheumatoid Arthritis Combination Therapy trial. Arthritis Res Ther. 2010;12(3):R122.
- Glinatsi D, Heiberg MS, Rudin A, Nordström D, Haavardsholm EA, Gudbjornsson B, et al. Head-to-head comparison of aggressive conventional therapy and three biological treatments and comparison of two de-escalation strategies in patients who respond to treatment: study protocol for a multicenter, randomized, open-label, blinded-assessor, phase 4 study. Trials. 2017;18(1):161.
- Østergaard M, van Vollenhoven R, Rudin A, Hetland ML, Heiberg MS, Nordström DC, et al. Certolizumab pegol, abatacept, tocilizumab or active conventional treatment in early rheumatoid arthritis: 48-week clinical and radiographic results of the investigator-initiated randomised controlled NORD-STAR trial. Ann Rheum Dis. 2023;82(10):1286-95.
- St Clair EW, van der Heijde DM, Smolen JS, Maini RN, Bathon JM, Emery P, et al. Combination of infliximab and methotrexate therapy for early rheumatoid arthritis: a randomized, controlled trial. Arthritis Rheum. 2004;50(11):3432-43.
- Emery P, Breedveld FC, Hall S, Durez P, Chang DJ, Robertson D, et al. Comparison of methotrexate monotherapy with a combination of methotrexate and etanercept in active, early, moderate to severe rheumatoid arthritis (COMET): a randomised, double-blind, parallel treatment trial. Lancet. 2008;372(9636):375-82.
- Kavanaugh A, Fleischmann RM, Emery P, Kupper H, Redden L, Guerette B, et al. Clinical, functional and radiographic consequences of achieving stable low disease activity and remission with adalimumab plus methotrexate or methotrexate alone in early rheumatoid arthritis: 26-week results from the randomised, controlled OPTIMA study. Ann Rheum Dis. 2013;72(1):64-71.
- Emery P, Bingham C, Burmester G, Bykerk V, Furst D, Mariette X, et al. Improvements in Patient-Reported outcomes Following 52 Weeks of Treatment with Certolizumab Pegol in Combination with Methotrexate in Dmard-Naive Patients with Severe, Active and Progressive Rheumatoid Arthritis: Results from the C-Early Randomized, Double-Blind, Controlled Phase 3 Study. Value Health. 2015;18(7):A707-8.
- Soubrier M, Puechal X, Sibilia J, Mariette X, Meyer O, Combe B, et al. Evaluation of two strategies (initial methotrexate monotherapy vs its combination with adalimumab) in management of early active rheumatoid arthritis: data from the GUEPARD trial. Rheumatology (Oxford). 2009;48(11):1429-34.
- Smolen JS, Emery P, Fleischmann R, van Vollenhoven RF, Pavelka K, Durez P, et al. Adjustment of therapy in rheumatoid arthritis on the basis of achievement of stable low disease activity with adalimumab plus methotrexate or methotrexate alone: the randomised controlled OPTIMA trial. Lancet. 2014;383(9914):321-32.
- Westhovens R, Robles M, Ximenes AC, Nayiager S, Wollenhaupt J, Durez P, et al. Clinical efficacy and safety of abatacept in methotrexate-naive patients with early rheumatoid arthritis and poor prognostic factors. Ann Rheum Dis. 2009;68(12):1870-7.
- Emery P, Burmester GR, Bykerk VP, Combe BG, Furst DE, Barre E, et al. Evaluating drug-free remission with abatacept in early rheumatoid arthritis: results from the phase 3b, multicentre, randomised, active-controlled AVERT study of 24 months, with a 12-month, double-blind treatment period. Ann Rheum Dis. 2015;74(1):19-26.
- Burmester GR, Rigby WF, van Vollenhoven RF, Kay J. Tocilizumab in early progressive rheumatoid arthritis: FUNCTION, a randomised controlled trial. 2016;75(6):1081-91.
- Bijlsma JW, Welsing PM, Woodworth TG, Middelink LM, Petho-Schramm A, Bernasconi C, et al. Early rheumatoid arthritis treated with tocilizumab, methotrexate, or their combination (U-Act-Early): a multicentre, randomised, double-blind, double-dummy, strategy trial. Lancet. 2016;388(10042):343-55.
- Goekoop-Ruiterman YP, de Vries-Bouwstra JK, Allaart CF, van Zeben D, Kerstens PJ, Hazes JM, et al. Clinical and radiographic outcomes of four different treatment strategies in patients with early rheumatoid arthritis (the BeSt study): A randomized, controlled trial. Arthritis Rheum. 2008;58(2 Suppl):S126-35.
- Jones G, Halbert J, Crotty M, Shanahan EM, Batterham M, Ahern M. The effect of treatment on radiological progression in rheumatoid arthritis: a systematic review of randomized placebo-controlled trials. Rheumatology (Oxford). 2003;42(1):6-13.
- Kvien TK, Zeidler HK, Hannonen P, Wollheim FA, Forre O, Hafstrom I, et al. Long term efficacy and safety of cyclosporin versus parenteral gold in early rheumatoid arthritis: a three year study of radiographic progression, renal function, and arterial hypertension. Ann Rheum Dis. 2002;61(6):511-6.
- Nam JL, Winthrop KL, van Vollenhoven RF, Pavelka K, Valesini G, Hensor EM, et al. Current evidence for the management of rheumatoid arthritis with biological disease-modifying antirheumatic drugs: a systematic literature review informing the EULAR recommendations for the management of RA. Ann Rheum Dis. 2010;69(6):976-86.
- Smolen JS, Burmester GR, Combe B, Curtis JR, Hall S, Haraoui B, et al. Head-to-head comparison of certolizumab pegol versus adalimumab in rheumatoid arthritis: 2-year efficacy and safety results from the randomised EXXELERATE study. Lancet. 2016;388(10061):2763-74.
- Michaud TL, Rho YH, Shamliyan T, Kuntz KM, Choi HK. The Comparative Safety of Tumor Necrosis Factor Inhibitors in Rheumatoid Arthritis: A Meta-analysis Update of 44 Trials. Am J Med. 2014;127(12):1208-32.
- Hetland ML, Christensen IJ, Tarp U, Dreyer L, Hansen A, Hansen IT, et al. Direct comparison of treatment responses, remission rates, and drug adherence in patients with rheumatoid arthritis treated with adalimumab, etanercept, or infliximab: results from eight years of surveillance of clinical practice in the nationwide Danish DANBIO registry. Arthritis Rheum. 2010;62(1):22-32.
- Neovius M, Arkema EV, Olsson H, Eriksson JK, Kristensen LE, Simard JF, et al. Drug survival on TNF inhibitors in patients with rheumatoid arthritis comparison of adalimumab, etanercept and infliximab. Ann Rheum Dis. 2015;74(2):354-60.
- Kristensen LE, Saxne T, Geborek P. The LUNDEX, a new index of drug efficacy in clinical practice: results of a five-year observational study of treatment with infliximab and etanercept among rheumatoid arthritis patients in southern Sweden. Arthritis Rheum. 2006;54(2):600-6.
- Kievit W, Adang EM, Fransen J, Kuper HH, van de Laar MA, Jansen TL, et al. The effectiveness and medication costs of three anti-tumour necrosis factor alpha agents in the treatment of rheumatoid arthritis from prospective clinical practice data. Ann Rheum Dis. 2008;67(9):1229-34.
- Du Pan SM, Dehler S, Ciurea A, Ziswiler HR, Gabay C, Finckh A. Comparison of drug retention rates and causes of drug discontinuation between anti-tumor necrosis factor agents in rheumatoid arthritis. Arthritis Rheum. 2009;61(5):560-8.
- Scire CA, Caporali R, Sarzi-Puttini P, Frediani B, Di Franco M, Tincani A, et al. Drug survival of the first course of anti-TNF agents in patients with rheumatoid arthritis and seronegative spondyloarthritis: analysis from the MonitorNet database. Clin Exp Rheumatol. 2013;31(6):857-63.
- Flouri I, Markatseli TE, Voulgari PV, Boki KA, Papadopoulos I, Settas L, et al. Comparative effectiveness and survival of infliximab, adalimumab, and etanercept for rheumatoid arthritis patients in the Hellenic Registry of Biologics: Low rates of remission and 5-year drug survival. Semin Arthritis Rheum. 2014;43(4):447-57.
- Silvagni E, Bortoluzzi A, Carrara G, Zanetti A, Govoni M, Scire CA. Comparative effectiveness of first-line biological monotherapy use in rheumatoid arthritis: a retrospective analysis of the RECord-linkage On Rheumatic Diseases study on health care administrative databases. BMJ Open. 2018;8(9):e021447.
- Markenson JA, Gibofsky A, Palmer WR, Keystone EC, Schiff MH, Feng J, et al. Persistence with anti-tumor necrosis factor therapies in patients with rheumatoid arthritis: observations from the RADIUS registry. J Rheumatol. 2011;38(7):1273-81.
- Greenberg JD, Reed G, Decktor D, Harrold L, Furst D, Gibofsky A, et al. A comparative effectiveness study of adalimumab, etanercept and infliximab in biologically naive and switched rheumatoid arthritis patients: results from the US CORRONA registry. Ann Rheum Dis. 2012;71(7):1134-42.
- Souto A, Maneiro JR, Gomez-Reino JJ. Rate of discontinuation and drug survival of biologic therapies in rheumatoid arthritis: a systematic review and meta-analysis of drug registries and health care databases. Rheumatology (Oxford). 2016;55(3):523-34.
- Dalen J, Svedbom A, Black CM, Lyu R, Ding Q, Sajjan S, et al. Treatment persistence among patients with immune-mediated rheumatic disease newly treated with subcutaneous TNF-alpha inhibitors and costs associated with non-persistence. Rheumatol Int. 2016;36(7):987-95.
- Dalen J, Svedbom A, Black CM, Kachroo S. Second-line treatment persistence and costs among patients with immune-mediated rheumatic diseases treated with subcutaneous TNF-alpha inhibitors. Rheumatol Int. 2017;37(12):2049-58.
- Aaltonen KJ, Joensuu JT, Pirila L, Kauppi M, Uutela T, Varjolahti-Lehtinen T, et al. Drug survival on tumour necrosis factor inhibitors in patients with rheumatoid arthritis in Finland. Scand J Rheumatol. 2017;46(5):359-63.
- Finckh A, Dehler S, Gabay C. The effectiveness of leflunomide as a co-therapy of tumour necrosis factor inhibitors in rheumatoid arthritis: a population-based study. Ann Rheum Dis. 2009;68(1):33-9.
- De Stefano R, Frati E, Nargi F, Baldi C, Menza L, Hammoud M, et al. Comparison of combination therapies in the treatment of rheumatoid arthritis: leflunomide-anti-TNF-alpha versus methotrexate-anti-TNF-alpha. Clin Rheumatol. 2010;29(5):517-24.
- Genovese MC, Fleischmann R, Combe B, Hall S, Rubbert-Roth A, Zhang Y, et al. Safety and efficacy of upadacitinib in patients with active rheumatoid arthritis refractory to biologic disease-modifying anti-rheumatic drugs (SELECT-BEYOND): a double-blind, randomised controlled phase 3 trial. Lancet. 2018;391(10139):2513-24.
- Virkki LM, Valleala H, Takakubo Y, Vuotila J, Relas H, Komulainen R, et al. Outcomes of switching anti-TNF drugs in rheumatoid arthritis–a study based on observational data from the Finnish Register of Biological Treatment (ROB-FIN). Clin Rheumatol. 2011;30(11):1447-54.
- Blom M, Kievit W, Kuper HH, Jansen TL, Visser H, den Broeder AA, et al. Frequency and effectiveness of dose increase of adalimumab, etanercept, and infliximab in daily clinical practice. Arthritis Care Res (Hoboken). 2010;62(9):1335-41.
- Rahman MU, Strusberg I, Geusens P, Berman A, Yocum D, Baker D, et al. Double-blinded infliximab dose escalation in patients with rheumatoid arthritis. Ann Rheum Dis. 2007;66(9):1233-8.
- Durez P, Van den Bosch F, Corluy L, Veys EM, De Clerck L, Peretz A, et al. A dose adjustment in patients with rheumatoid arthritis not optimally responding to a standard dose of infliximab of 3 mg/kg every 8 weeks can be effective: a Belgian prospective study. Rheumatology (Oxford). 2005;44(4):465-8.
- Ariza-Ariza R, Navarro-Sarabia F, Hernandez-Cruz B, Rodriguez-Arboleya L, Navarro-Compan V, Toyos J. Dose escalation of the anti-TNF-alpha agents in patients with rheumatoid arthritis. A systematic review. Rheumatology (Oxford). 2007;46(3):529-32.
- Pavelka K, Jarosova K, Suchy D, Senolt L, Chroust K, Dusek L, et al. Increasing the infliximab dose in rheumatoid arthritis patients: a randomised, double blind study failed to confirm its efficacy. Ann Rheum Dis. 2009;68(8):1285-9.
- Cohen SB, Kremer JM, Dandreo KJ, Reed GW, Magner R, Shan Y, et al. Outcomes of infliximab dose escalation in patients with rheumatoid arthritis. Clin Rheumatol. 2019;38(9):2501-8.
- van de Putte LB, Rau R, Breedveld FC, Kalden JR, Malaise MG, van Riel PL, et al. Efficacy and safety of the fully human anti-tumour necrosis factor alpha monoclonal antibody adalimumab (D2E7) in DMARD refractory patients with rheumatoid arthritis: a 12 week, phase II study. Ann Rheum Dis. 2003;62(12):1168-77.
- Eng G, Stoltenberg MB, Szkudlarek M, Bouchelouche PN, Christensen R, Bliddal H, et al. Efficacy of treatment intensification with adalimumab, etanercept and infliximab in rheumatoid arthritis: a systematic review of cohort studies with focus on dose. Semin Arthritis Rheum. 2013;43(2):144-51.
- Finckh A, Ciurea A, Brulhart L, Moller B, Walker UA, Courvoisier D, et al. Which subgroup of patients with rheumatoid arthritis benefits from switching to rituximab versus alternative anti-tumour necrosis factor (TNF) agents after previous failure of an anti-TNF agent? Ann Rheum Dis. 2010;69(2):387-93.
- Chatzidionysiou K, van Vollenhoven RF. Rituximab versus anti-TNF in patients who previously failed one TNF inhibitor in an observational cohort. Scand J Rheumatol. 2013;42(3):190-5.
- Emery P, Gottenberg JE, Rubbert-Roth A, Sarzi-Puttini P, Choquette D, Taboada VM, et al. Rituximab versus an alternative TNF inhibitor in patients with rheumatoid arthritis who failed to respond to a single previous TNF inhibitor: SWITCH-RA, a global, observational, comparative effectiveness study. Ann Rheum Dis. 2015;74(6):979-84.
- Gottenberg JE, Brocq O, Perdriger A, Lassoued S, Berthelot JM, Wendling D, et al. Non-TNF-Targeted Biologic vs a Second Anti-TNF Drug to Treat Rheumatoid Arthritis in Patients With Insufficient Response to a First Anti-TNF Drug: A Randomized Clinical Trial. Jama. 2016;316(11):1172-80.
- Frisell T, Dehlin M, Di Giuseppe D, Feltelius N, Turesson C, Askling J. Comparative effectiveness of abatacept, rituximab, tocilizumab and TNFi biologics in RA: results from the nationwide Swedish register. Rheumatology (Oxford). 2019.
- Choquette D, Bessette L, Alemao E, Haraoui B, Postema R, Raynauld JP, et al. Persistence rates of abatacept and TNF inhibitors used as first or second biologic DMARDs in the treatment of rheumatoid arthritis: 9 years of experience from the Rhumadata(R) clinical database and registry. Arthritis Res Ther. 2019;21(1):138.
- Weinblatt M, Combe B, Covucci A, Aranda R, Becker JC, Keystone E. Safety of the selective costimulation modulator abatacept in rheumatoid arthritis patients receiving background biologic and nonbiologic disease-modifying antirheumatic drugs: A one-year randomized, placebo-controlled study. Arthritis Rheum. 2006;54(9):2807-16.
- Mishra R, Singh V, Pritchard CH. Safety of biologic agents after rituximab therapy in patients with rheumatoid arthritis. Rheumatol Int. 2011;31(4):481-4.
- Genovese MC, Breedveld FC, Emery P, Cohen S, Keystone E, Matteson EL, et al. Safety of biological therapies following rituximab treatment in rheumatoid arthritis patients. Ann Rheum Dis. 2009;68(12):1894-7.
- Schiff M, Keiserman M, Codding C, Songcharoen S, Berman A, Nayiager S, et al. Efficacy and safety of abatacept or infliximab vs placebo in ATTEST: a phase III, multi-centre, randomised, double-blind, placebo-controlled study in patients with rheumatoid arthritis and an inadequate response to methotrexate. Ann Rheum Dis. 2008;67(8):1096-103.
- Lopez-Olivo MA, Amezaga Urruela M, McGahan L, Pollono EN, Suarez-Almazor ME. Rituximab for rheumatoid arthritis. Cochrane Database Syst Rev. 2015;1:Cd007356.
- Porter D, van Melckebeke J, Dale J, Messow CM, McConnachie A, Walker A, et al. Tumour necrosis factor inhibition versus rituximab for patients with rheumatoid arthritis who require biological treatment (ORBIT): an open-label, randomised controlled, non-inferiority, trial. Lancet. 2016;388(10041):239-47.
- Rubbert-Roth A, Tak PP, Zerbini C, Tremblay JL, Carreno L, Armstrong G, et al. Efficacy and safety of various repeat treatment dosing regimens of rituximab in patients with active rheumatoid arthritis: results of a Phase III randomized study (MIRROR). Rheumatology (Oxford). 2010;49(9):1683-93.
- Emery P, Fleischmann R, Filipowicz-Sosnowska A, Schechtman J, Szczepanski L, Kavanaugh A, et al. The efficacy and safety of rituximab in patients with active rheumatoid arthritis despite methotrexate treatment: results of a phase IIB randomized, double-blind, placebo-controlled, dose-ranging trial. Arthritis Rheum. 2006;54(5):1390-400.
- Bredemeier M, de Oliveira FK, Rocha CM. Low- versus high-dose rituximab for rheumatoid arthritis: A systematic review and meta-analysis. Arthritis Care Res (Hoboken). 2014;66:228-35.
- Bredemeier M, Campos GG, de Oliveira FK. Updated systematic review and meta-analysis of randomized controlled trials comparing low- versus high-dose rituximab for rheumatoid arthritis. Clin Rheumatol. 2015;34(10):1801-5.
- Emery P, Deodhar A, Rigby WF, Isaacs JD, Combe B, Racewicz AJ, et al. Efficacy and safety of different doses and retreatment of rituximab: a randomised, placebo-controlled trial in patients who are biological naive with active rheumatoid arthritis and an inadequate response to methotrexate (Study Evaluating Rituximab’s Efficacy in MTX iNadequate rEsponders (SERENE)). Ann Rheum Dis. 2010;69(9):1629-35.
- Chatzidionysiou K, Lie E, Nasonov E, Lukina G, Hetland ML, Tarp U, et al. Effectiveness of two different doses of rituximab for the treatment of rheumatoid arthritis in an international cohort: data from the CERERRA collaboration. Arthritis Res Ther. 2016;18:50.
- Tak PP, Rigby W, Rubbert-Roth A, Peterfy C, van Vollenhoven RF, Stohl W, et al. Sustained inhibition of progressive joint damage with rituximab plus methotrexate in early active rheumatoid arthritis: 2-year results from the randomised controlled trial IMAGE. Ann Rheum Dis. 2012;71(3):351-7.
- Mariette X, Rouanet S, Sibilia J, Combe B, Le Loet X, Tebib J, et al. Evaluation of low-dose rituximab for the retreatment of patients with active rheumatoid arthritis: a non-inferiority randomised controlled trial. Ann Rheum Dis. 2014;73(8):1508-14.
- Vital EM, Dass S, Rawstron AC, Buch MH, Goeb V, Henshaw K, et al. Management of nonresponse to rituximab in rheumatoid arthritis: predictors and outcome of re-treatment. Arthritis Rheum. 2010;62(5):1273-9.
- Emery P, Mease PJ, Rubbert-Roth A, Curtis JR, Muller-Ladner U, Gaylis NB, et al. Retreatment with rituximab based on a treatment-to-target approach provides better disease control than treatment as needed in patients with rheumatoid arthritis: a retrospective pooled analysis. Rheumatology (Oxford). 2011;50(12):2223-32.
- van Herwaarden N, van der Maas A, Jansen TL, Dutmer EA, Hartkamp A, van Riel PL, et al. Can response duration after the first rituximab treatment be used in timing of rituximab retreatment? Scand J Rheumatol. 2013;42(3):251-2.
- Chatzidionysiou K, Lie E, Nasonov E, Lukina G, Hetland ML, Tarp U, et al. Effectiveness of disease-modifying antirheumatic drug co-therapy with methotrexate and leflunomide in rituximab-treated rheumatoid arthritis patients: results of a 1-year follow-up study from the CERERRA collaboration. Ann Rheum Dis. 2012;71(3):374-7.
- Burmester GR, Rubbert-Roth A, Cantagrel A, Hall S, Leszczynski P, Feldman D, et al. A randomised, double-blind, parallel-group study of the safety and efficacy of subcutaneous tocilizumab versus intravenous tocilizumab in combination with traditional disease-modifying antirheumatic drugs in patients with moderate to severe rheumatoid arthritis (SUMMACTA study). Ann Rheum Dis. 2014;73(1):69-74.
- Huizinga TW, Fleischmann RM, Jasson M, Radin AR, van Adelsberg J, Fiore S, et al. Sarilumab, a fully human monoclonal antibody against IL-6Ralpha in patients with rheumatoid arthritis and an inadequate response to methotrexate: efficacy and safety results from the randomised SARIL-RA-MOBILITY Part A trial. Ann Rheum Dis. 2014;73(9):1626-34.
- Genovese MC, van Adelsberg J, Fan C, Graham NMH, van Hoogstraten H, Parrino J, et al. Two years of sarilumab in patients with rheumatoid arthritis and an inadequate response to MTX: safety, efficacy and radiographic outcomes. Rheumatology (Oxford). 2018;57(8):1423-31.
- Genovese MC. Long-term safety and efficacy of sarilumab plus methotrexate on disease activity, physical function and radiographic progression: 5 years of sarilumab plus methotrexate treatment. Arthritis Rheumatol. 2019;5(2):e000887.
- Dougados M, Kissel K, Sheeran T, Tak PP, Conaghan PG, Mola EM, et al. Adding tocilizumab or switching to tocilizumab monotherapy in methotrexate inadequate responders: 24-week symptomatic and structural results of a 2-year randomised controlled strategy trial in rheumatoid arthritis (ACT-RAY). Ann Rheum Dis. 2013;72(1):43-50.
- Teitsma XM, Marijnissen AK, Bijlsma JW, Lafeber FP, Jacobs JW. Tocilizumab as monotherapy or combination therapy for treating active rheumatoid arthritis: a meta-analysis of efficacy and safety reported in randomized controlled trials. Arthritis Res Ther. 2016;18(1):211.
- Forsblad-d’Elia H, Bengtsson K, Kristensen LE, Jacobsson LT. Drug adherence, response and predictors thereof for tocilizumab in patients with rheumatoid arthritis: results from the Swedish biologics register. Rheumatology (Oxford). 2015;54(7):1186-93.
- Pers YM, Fortunet C, Constant E, Lambert J, Godfrin-Valnet M, De Jong A, et al. Predictors of response and remission in a large cohort of rheumatoid arthritis patients treated with tocilizumab in clinical practice. Rheumatology (Oxford). 2014;53(1):76-84.
- Kaneko Y, Atsumi T, Tanaka Y, Inoo M, Kobayashi-Haraoka H, Amano K, et al. Comparison of adding tocilizumab to methotrexate with switching to tocilizumab in patients with rheumatoid arthritis with inadequate response to methotrexate: 52-week results from a prospective, randomised, controlled study (SURPRISE study). Ann Rheum Dis. 2016;75(11):1917-23.
- Gabay C, Riek M, Hetland ML, Hauge EM, Pavelka K, Tomsic M, et al. Effectiveness of tocilizumab with and without synthetic disease-modifying antirheumatic drugs in rheumatoid arthritis: results from a European collaborative study. Ann Rheum Dis. 2016;75(7):1336-42.
- Choy EH, Bernasconi C, Aassi M, Molina JF, Epis OM. Treatment of Rheumatoid Arthritis With Anti-Tumor Necrosis Factor or Tocilizumab Therapy as First Biologic Agent in a Global Comparative Observational Study. Arthritis Care Res (Hoboken). 2017;69(10):1484-94.
- Lauper K, Nordstrom DC, Pavelka K, Hernandez MV, Kvien TK, Kristianslund EK, et al. Comparative effectiveness of tocilizumab versus TNF inhibitors as monotherapy or in combination with conventional synthetic disease-modifying antirheumatic drugs in patients with rheumatoid arthritis after the use of at least one biologic disease-modifying antirheumatic drug: analyses from the pan-European TOCERRA register collaboration. Ann Rheum Dis. 2018;77(9):1276-82.
- Das S, Vital EM, Horton S, Bryer D, El-Sherbiny Y, Rawstron AC, et al. Abatacept or tocilizumab after rituximab in rheumatoid arthritis? An exploratory study suggests non-response to rituximab is associated with persistently high IL-6 and better clinical response to IL-6 blocking therapy. Ann Rheum Dis. 2014;73(5):909-12.
- Smolen JS, Aletaha D. Interleukin-6 receptor inhibition with tocilizumab and attainment of disease remission in rheumatoid arthritis: the role of acute-phase reactants. Arthritis Rheum. 2011;63(1):43-52.
- Bresnihan B, Alvaro-Gracia JM, Cobby M, Doherty M, Domljan Z, Emery P, et al. Treatment of rheumatoid arthritis with recombinant human interleukin-1 receptor antagonist. Arthritis Rheum. 1998;41(12):2196-204.
- Rubbert-Roth A, Enejosa J, Pangan AL, Haraoui B, Rischmueller M, Khan N, et al. Trial of Upadacitinib or Abatacept in Rheumatoid Arthritis. N Engl J Med. 2020;383(16):1511-21.
- Eberhard A, Di Giuseppe D, Askling J, Bergman S, Bower H, Chatzidionysiou K, et al. Effectiveness of JAK Inhibitors Compared With Biologic Disease-Modifying Antirheumatic Drugs on Pain Reduction in Rheumatoid Arthritis: Results From a Nationwide Swedish Cohort Study. Arthritis Rheumatol. 2025;77(3):253-62.
- Läkemedelsverket uppdaterar rekommendationer om biosimilarer. 19 september 2023. https://www.lakemedelsverket.se/sv/nyheter/lakemedelsverket-uppdaterar-rekommendation-om-biosimilarer. 2023.
- de Oliveira Ascef B, Almeida MO, de Medeiros-Ribeiro AC, de Oliveira Andrade DC, de Oliveira Junior HA, de Soárez PC. Impact of switching between reference biologics and biosimilars of tumour necrosis factor inhibitors for rheumatoid arthritis: a systematic review and network meta-analysis. Sci Rep. 2023;13(1):13699.
- Nikitina V, Laurini GS, Montanaro N, Motola D. Comparative Safety Profiles of Biosimilars vs. Originators Used in Rheumatology: A Pharmacovigilance Analysis of the EudraVigilance Database. J Clin Med. 2025;14(5).
- Boone NW, Liu L, Romberg-Camps MJ, Duijsens L, Houwen C, van der Kuy PHM, et al. The nocebo effect challenges the non-medical infliximab switch in practice. Eur J Clin Pharmacol. 2018;74(5):655-61.
- Petit J, Antignac M, Poilverd RM, Baratto R, Darthout S, Desouches S, et al. Multidisciplinary team intervention to reduce the nocebo effect when switching from the originator infliximab to a biosimilar. RMD Open. 2021;7(1).
- Smolen JS, Caporali R, Doerner T, Fautrel B, Benedetti F, Pieper B, et al. Treatment journey in rheumatoid arthritis with biosimilars: from better access to good disease control through cost savings and prevention of nocebo effects. RMD Open. 2021;7(2).
- Thomas SS, Borazan N, Barroso N, Duan L, Taroumian S, Kretzmann B, et al. Comparative Immunogenicity of TNF Inhibitors: Impact on Clinical Efficacy and Tolerability in the Management of Autoimmune Diseases. A Systematic Review and Meta-Analysis. BioDrugs. 2015;29(4):241-58.
- Garces S, Antunes M, Benito-Garcia E, da Silva JC, Aarden L, Demengeot J. A preliminary algorithm introducing immunogenicity assessment in the management of patients with RA receiving tumour necrosis factor inhibitor therapies. Ann Rheum Dis. 2014;73(6):1138-43.
- Quistrebert J, Hassler S, Bachelet D, Mbogning C, Musters A, Tak PP, et al. Incidence and risk factors for adalimumab and infliximab anti-drug antibodies in rheumatoid arthritis: A European retrospective multicohort analysis. Semin Arthritis Rheum. 2019;48(6):967-75.
- Bendtzen K, Geborek P, Svenson M, Larsson L, Kapetanovic MC, Saxne T. Individualized monitoring of drug bioavailability and immunogenicity in rheumatoid arthritis patients treated with the tumor necrosis factor alpha inhibitor infliximab. Arthritis Rheum. 2006;54(12):3782-9.
- Krieckaert CL, Bartelds GM, Lems WF, Wolbink GJ. The effect of immunomodulators on the immunogenicity of TNF-blocking therapeutic monoclonal antibodies: a review. Arthritis Res Ther. 2010;12(5):217.
- Bartelds GM, Krieckaert CL, Nurmohamed MT, van Schouwenburg PA, Lems WF, Twisk JW, et al. Development of antidrug antibodies against adalimumab and association with disease activity and treatment failure during long-term follow-up. Jama. 2011;305(14):1460-8.
- Jamnitski A, Bartelds GM, Nurmohamed MT, van Schouwenburg PA, van Schaardenburg D, Stapel SO, et al. The presence or absence of antibodies to infliximab or adalimumab determines the outcome of switching to etanercept. Ann Rheum Dis. 2011;70(2):284-8.
- Maneiro JR, Salgado E, Gomez-Reino JJ. Immunogenicity of monoclonal antibodies against tumor necrosis factor used in chronic immune-mediated Inflammatory conditions: systematic review and meta-analysis. JAMA Intern Med. 2013;173(15):1416-28.
- Garces S, Demengeot J, Benito-Garcia E. The immunogenicity of anti-TNF therapy in immune-mediated inflammatory diseases: a systematic review of the literature with a meta-analysis. Ann Rheum Dis. 2013;72(12):1947-55.
- van Schouwenburg PA, Rispens T, Wolbink GJ. Immunogenicity of anti-TNF biologic therapies for rheumatoid arthritis. Nat Rev Rheumatol. 2013;9(3):164-72.
- Bloem K, van Leeuwen A, Verbeek G, Nurmohamed MT, Wolbink GJ, van der Kleij D, et al. Systematic comparison of drug-tolerant assays for anti-drug antibodies in a cohort of adalimumab-treated rheumatoid arthritis patients. J Immunol Methods. 2015;418:29-38.
- Yoo DH, Racewicz A, Brzezicki J, Yatsyshyn R, Arteaga ET, Baranauskaite A, et al. A phase III randomized study to evaluate the efficacy and safety of CT-P13 compared with reference infliximab in patients with active rheumatoid arthritis: 54-week results from the PLANETRA study. Arthritis Res Ther. 2016;18:82.
- Yoo DH, Prodanovic N, Jaworski J, Miranda P, Ramiterre E, Lanzon A, et al. Efficacy and safety of CT-P13 (biosimilar infliximab) in patients with rheumatoid arthritis: comparison between switching from reference infliximab to CT-P13 and continuing CT-P13 in the PLANETRA extension study. Ann Rheum Dis. 2017;76(2):355-63.
- Park W, Yoo DH, Miranda P, Brzosko M, Wiland P, Gutierrez-Urena S, et al. Efficacy and safety of switching from reference infliximab to CT-P13 compared with maintenance of CT-P13 in ankylosing spondylitis: 102-week data from the PLANETAS extension study. Ann Rheum Dis. 2017;76(2):346-54.
- Emery P, Vencovsky J, Sylwestrzak A, Leszczynski P, Porawska W, Baranauskaite A, et al. 52-week results of the phase 3 randomized study comparing SB4 with reference etanercept in patients with active rheumatoid arthritis. Rheumatology (Oxford). 2017;56(12):2093-101.
- Emery P, Suh CH, Weinblatt ME, Smolen JS, Keystone EC, Genovese M, et al. Impact of immunogenicity on efficacy and tolerability of tumour necrosis factor inhibitors: pooled analysis of biosimilar studies in rheumatoid arthritis. Scand J Rheumatol. 2020;49(5):361-70.
- Huizinga TWJ, Toori Y, Muniz R. Adalimumab Biosimilars in the Treatment of Rheumatoid Arthritis: A Systematic Review of the Evidence for Biosimilarity. Rheumatol Ther. 2021;8(1):41-61.
- Lu X, Hu R, Peng L, Liu M, Sun Z. Efficacy and Safety of Adalimumab Biosimilars: Current Critical Clinical Data in Rheumatoid Arthritis. Front Immunol. 2021;12:638444.
- Strand V, Gonçalves J, Hickling TP, Jones HE, Marshall L, Isaacs JD. Immunogenicity of Biosimilars for Rheumatic Diseases, Plaque Psoriasis, and Inflammatory Bowel Disease: A Review from Clinical Trials and Regulatory Documents. BioDrugs. 2020;34(1):27-37.
- Takeuchi T, Yamanaka H, Tanaka Y, Sakurai T, Saito K, Ohtsubo H, et al. Evaluation of the pharmacokinetic equivalence and 54-week efficacy and safety of CT-P13 and innovator infliximab in Japanese patients with rheumatoid arthritis. Mod Rheumatol. 2015;25(6):817-24.
- Krieckaert CL, Nurmohamed MT, Wolbink GJ. Methotrexate reduces immunogenicity in adalimumab treated rheumatoid arthritis patients in a dose dependent manner. Ann Rheum Dis. 2012;71(11):1914-5.
- Pouw MF, Krieckaert CL, Nurmohamed MT, van der Kleij D, Aarden L, Rispens T, et al. Key findings towards optimising adalimumab treatment: the concentration-effect curve. Ann Rheum Dis. 2015;74(3):513-8.
- Burmester GR, Kivitz AJ, Kupper H, Arulmani U, Florentinus S, Goss SL, et al. Efficacy and safety of ascending methotrexate dose in combination with adalimumab: the randomised CONCERTO trial. Ann Rheum Dis. 2015;74(6):1037-44.
- Vogelzang EH, Pouw MF, Nurmohamed M, Kneepkens EL, Rispens T, Wolbink GJ, et al. Adalimumab trough concentrations in patients with rheumatoid arthritis and psoriatic arthritis treated with concomitant disease-modifying antirheumatic drugs. Ann Rheum Dis. 2015;74(2):474-5.
- Martínez-Feito A, Plasencia-Rodríguez C, Navarro-Compán V, Hernández-Breijo B, González M, Monjo I, et al. The effect of methotrexate versus other disease-modifying anti-rheumatic drugs on serum drug levels and clinical response in patients with rheumatoid arthritis treated with tumor necrosis factor inhibitors. Clin Rheumatol. 2019;38(3):949-54.
- Bitoun S, Hässler S, Ternant D, Szely N, Gleizes A, Richez C, et al. Response to Biologic Drugs in Patients With Rheumatoid Arthritis and Antidrug Antibodies. JAMA Netw Open. 2023;6(7):e2323098.
- Gehin JE, Klaasen RA, Klami Kristianslund E, Jyssum I, Sexton J, Warren DJ, et al. Therapeutic serum level for adalimumab in rheumatoid arthritis: explorative analyses of data from a randomised phase III trial. RMD Open. 2024;10(4).
- Krieckaert CL, van Tubergen A, Gehin JE, Hernandez-Breijo B, Le Mélédo G, Balsa A, et al. EULAR points to consider for therapeutic drug monitoring of biopharmaceuticals in inflammatory rheumatic and musculoskeletal diseases. Ann Rheum Dis. 2023;82(1):65-73.
- Krieckaert C, Hernández-Breijo B, Gehin JE, le Mélédo G, Balsa A, Jani M, et al. Therapeutic drug monitoring of biopharmaceuticals in inflammatory rheumatic and musculoskeletal disease: a systematic literature review informing EULAR points to consider. RMD Open. 2022;8(2).
- Dong W, Hu X, Wu C, Wang G, Fang Y, Shi L, et al. Efficacy, safety, and cost-effectiveness of therapeutic drug monitoring (TDM) for TNF inhibitor therapy in rheumatic disease: A systematic review and meta-analysis. Semin Arthritis Rheum. 2023;63:152302.
- Syversen SW, Jørgensen KK, Goll GL, Brun MK, Sandanger Ø, Bjørlykke KH, et al. Effect of Therapeutic Drug Monitoring vs Standard Therapy During Maintenance Infliximab Therapy on Disease Control in Patients With Immune-Mediated Inflammatory Diseases: A Randomized Clinical Trial. JAMA 2021;326(23):2375-84.
- Syversen SW, Goll GL, Jørgensen KK, Sandanger Ø, Sexton J, Olsen IC, et al. Effect of Therapeutic Drug Monitoring vs Standard Therapy During Infliximab Induction on Disease Remission in Patients With Chronic Immune-Mediated Inflammatory Diseases: A Randomized Clinical Trial. Jama. 2021;325(17):1744-54.
- Kharlamova N, Hermanrud C, Dunn N, Ryner M, Hambardzumyan K, Vivar Pomiano N, et al. Drug Tolerant Anti-drug Antibody Assay for Infliximab Treatment in Clinical Practice Identifies Positive Cases Earlier. Front Immunol. 2020;11:1365.
- Genant HK, Peterfy CG, Westhovens R, Becker JC, Aranda R, Vratsanos G, et al. Abatacept inhibits progression of structural damage in rheumatoid arthritis: results from the long-term extension of the AIM trial. Ann Rheum Dis. 2008;67(8):1084-9.
- Keystone E, Emery P, Peterfy CG, Tak PP, Cohen S, Genovese MC, et al. Rituximab inhibits structural joint damage in patients with rheumatoid arthritis with an inadequate response to tumour necrosis factor inhibitor therapies. Ann Rheum Dis. 2009;68(2):216-21.
- Kremer JM, Blanco R, Brzosko M, Burgos-Vargas R, Halland AM, Vernon E, et al. Tocilizumab inhibits structural joint damage in rheumatoid arthritis patients with inadequate responses to methotrexate: results from the double-blind treatment phase of a randomized placebo-controlled trial of tocilizumab safety and prevention of structural joint damage at one year. Arthritis Rheum. 2011;63(3):609-21.
- Kivitz A, Olech E, Borofsky M, Zazueta BM, Navarro-Sarabia F, Radominski SC, et al. Subcutaneous tocilizumab versus placebo in combination with disease-modifying antirheumatic drugs in patients with rheumatoid arthritis. Arthritis Care Res (Hoboken). 2014;66(11):1653-61.
- Smolen JS, Han C, Bala M, Maini RN, Kalden JR, van der Heijde D, et al. Evidence of radiographic benefit of treatment with infliximab plus methotrexate in rheumatoid arthritis patients who had no clinical improvement: a detailed subanalysis of data from the anti-tumor necrosis factor trial in rheumatoid arthritis with concomitant therapy study. Arthritis Rheum. 2005;52(4):1020-30.
- Landewe R, van der Heijde D, Klareskog L, van Vollenhoven R, Fatenejad S. Disconnect between inflammation and joint destruction after treatment with etanercept plus methotrexate: results from the trial of etanercept and methotrexate with radiographic and patient outcomes. Arthritis Rheum. 2006;54(10):3119-25.
- Smolen JS, van der Heijde DM, Keystone EC, van Vollenhoven RF, Goldring MB, Guerette B, et al. Association of joint space narrowing with impairment of physical function and work ability in patients with early rheumatoid arthritis: protection beyond disease control by adalimumab plus methotrexate. Ann Rheum Dis. 2013;72(7):1156-62.
- Smolen JS, Avila JC, Aletaha D. Tocilizumab inhibits progression of joint damage in rheumatoid arthritis irrespective of its anti-inflammatory effects: disassociation of the link between inflammation and destruction. Ann Rheum Dis. 2012;71(5):687-93.
- Aletaha D, Alasti F, Smolen JS. Rituximab dissociates the tight link between disease activity and joint damage in rheumatoid arthritis patients. Ann Rheum Dis. 2013;72(1):7-12.
- Graudal N, Jurgens G. Similar effects of disease-modifying antirheumatic drugs, glucocorticoids, and biologic agents on radiographic progression in rheumatoid arthritis: meta-analysis of 70 randomized placebo-controlled or drug-controlled studies, including 112 comparisons. Arthritis Rheum. 2010;62(10):2852-63.
- van der Heijde D, Dougados M, Chen YC, Greenwald M. Effects of baricitinib on radiographic progression of structural joint damage at 1 year in patients with rheumatoid arthritis and an inadequate response to conventional synthetic disease-modifying antirheumatic drugs. RMD Open. 2018;4(1):e000662.
- van der Heijde D, Schiff M, Tanaka Y. Low rates of radiographic progression of structural joint damage over 2 years of baricitinib treatment in patients with rheumatoid arthritis. RMD Open. 2019;5(1):e000898.
- Higashida J, Wun T, Schmidt S, Naguwa SM, Tuscano JM. Safety and efficacy of rituximab in patients with rheumatoid arthritis refractory to disease modifying antirheumatic drugs and anti-tumor necrosis factor-alpha treatment. J Rheumatol. 2005;32(11):2109-15.
- Maneiro RJ, Salgado E, Carmona L, Gomez-Reino JJ. Rheumatoid factor as predictor of response to abatacept, rituximab and tocilizumab in rheumatoid arthritis: Systematic review and meta-analysis. Semin Arthritis Rheum. 2013;43(1):9-17.
- Sokolove J, Schiff M, Fleischmann R, Weinblatt ME, Connolly SE, Johnsen A, et al. Impact of baseline anti-cyclic citrullinated peptide-2 antibody concentration on efficacy outcomes following treatment with subcutaneous abatacept or adalimumab: 2-year results from the AMPLE trial. Ann Rheum Dis. 2016;75(4):709-14.
- Courvoisier DS, Chatzidionysiou K, Mongin D, Lauper K, Mariette X, Morel J, et al. The impact of seropositivity on the effectiveness of biologic anti-rheumatic agents: results from a collaboration of 16 registries. Rheumatology (Oxford). 2021;60(2):820-8.
- Gottenberg JE, Ravaud P, Cantagrel A, Combe B, Flipo RM, Schaeverbeke T, et al. Positivity for anti-cyclic citrullinated peptide is associated with a better response to abatacept: data from the ’Orencia and Rheumatoid Arthritis’ registry. Ann Rheum Dis. 2012;71(11):1815-9.
- Gottenberg JE, Courvoisier DS, Hernandez MV. Brief Report: Association of Rheumatoid Factor and Anti-Citrullinated Protein Antibody Positivity With Better Effectiveness of Abatacept: Results From the Pan-European Registry Analysis. Arthritis Rheumatol. 2016;68(6):1346-52.
- Tymms K, Butcher B, Smith T, Littlejohn G. Impact of anti-citrullinated protein antibody on tumor necrosis factor inhibitor or abatacept response in patients with rheumatoid arthritis. Eur J Rheumatol. 2021;8(2):62-72.
- Nusslein HG, Alten R, Galeazzi M, Lorenz HM, Nurmohamed MT, Bensen WG, et al. Prognostic factors for abatacept retention in patients who received at least one prior biologic agent: an interim analysis from the observational, prospective ACTION study. BMC Musculoskelet Disord. 2015;16:176.
- Narvaez J, Magallares B, Diaz Torne C, Hernandez MV, Reina D, Corominas H, et al. Predictive factors for induction of remission in patients with active rheumatoid arthritis treated with tocilizumab in clinical practice. Semin Arthritis Rheum. 2015.
- Genovese MC, Fleischmann R, Kivitz A, Lee EB, van Hoogstraten H, Kimura T, et al. Efficacy and safety of sarilumab in combination with csDMARDs or as monotherapy in subpopulations of patients with moderately to severely active rheumatoid arthritis in three phase III randomized, controlled studies. Arthritis Res Ther. 2020;22(1):139.
- Bird P, Bensen W, El-Zorkany B, Kaine J, Manapat-Reyes BH, Pascual-Ramos V, et al. Tofacitinib 5 mg Twice Daily in Patients with Rheumatoid Arthritis and Inadequate Response to Disease-Modifying Antirheumatic Drugs: A Comprehensive Review of Phase 3 Efficacy and Safety. J Clin Rheumatol. 2019;25(3):115-26.
- Takahashi N, Asai S, Kobayakawa T, Kaneko A, Watanabe T, Kato T, et al. Predictors for clinical effectiveness of baricitinib in rheumatoid arthritis patients in routine clinical practice: data from a Japanese multicenter registry. Sci Rep. 2020;10(1):21907.
- Lv Q, Yin Y, Li X, Shan G, Wu X, Liang D, et al. The status of rheumatoid factor and anti-cyclic citrullinated peptide antibody are not associated with the effect of anti-TNFalpha agent treatment in patients with rheumatoid arthritis: a meta-analysis. PLoS One. 2014;9(2):e89442.
- Smolen JS, Taylor PC, Tanaka Y, Takeuchi T, Hashimoto M, Cara C, et al. Impact of high rheumatoid factor levels on treatment outcomes with certolizumab pegol and adalimumab in patients with rheumatoid arthritis. Rheumatology (Oxford). 2024;63(11):3015-24.
- Nam JL, Takase-Minegishi K, Ramiro S. Efficacy of biological disease-modifying antirheumatic drugs: a systematic literature review informing the 2016 update of the EULAR recommendations for the management of rheumatoid arthritis. 2017;76(6):1113-36.
- Henaux S, Ruyssen-Witrand A, Cantagrel A, Barnetche T, Fautrel B, Filippi N, et al. Risk of losing remission, low disease activity or radiographic progression in case of bDMARD discontinuation or tapering in rheumatoid arthritis: systematic analysis of the literature and meta-analysis. Ann Rheum Dis. 2018;77(4):515-22.
- Verhoef LM, van den Bemt BJ, van der Maas A, Vriezekolk JE, Hulscher ME, van den Hoogen FH, et al. Down-titration and discontinuation strategies of tumour necrosis factor-blocking agents for rheumatoid arthritis in patients with low disease activity. Cochrane Database Syst Rev. 2019;5:Cd010455.
- Vasconcelos LB, Silva MT, Galvao TF. Reduction of biologics in rheumatoid arthritis: a systematic review and meta-analysis. Rheumatol Int. 2020;40(12):1949-59.
- Uhrenholt L, Christensen R, Dinesen WKH, Liboriussen CH, Andersen SS, Dreyer L, et al. Risk of flare after tapering or withdrawal of biologic/targeted synthetic disease-modifying anti-rheumatic drugs in patients with rheumatoid arthritis or axial spondyloarthritis: a systematic review and meta-analysis. Rheumatology (Oxford). 2022;61(8):3107-22.
- Fleischmann R, Mysler E, Bessette L, Peterfy CG, Durez P, Tanaka Y, et al. Long-term safety and efficacy of upadacitinib or adalimumab in patients with rheumatoid arthritis: results through 3 years from the SELECT-COMPARE study. RMD Open. 2022;8(1):e002012.
- Uhrenholt L, Christensen R, Dreyer L, Hauge EM, Schlemmer A, Loft AG, et al. Disease activity-guided tapering of biologics in patients with inflammatory arthritis: a pragmatic, randomized, open-label, equivalence trial. Scand J Rheumatol. 2023;52(5):481-92.
- Weinblatt ME, Bingham CO, 3rd, Burmester GR, Bykerk VP, Furst DE, Mariette X, et al. A Phase III Study Evaluating Continuation, Tapering, and Withdrawal of Certolizumab Pegol After One Year of Therapy in Patients With Early Rheumatoid Arthritis. Arthritis Rheumatol. 2017;69(10):1937-48.
- Lillegraven S, Paulshus Sundlisæter N, Sexton J, Olsen IC, Lexberg Å S, Madland TM, et al. Effect of tapered versus stable treatment with tumour necrosis factor inhibitors on disease flares in patients with rheumatoid arthritis in remission: a randomised, open label, non-inferiority trial. Ann Rheum Dis. 2023;82(11):1394-403.
- Kjørholt KE, Sundlisæter NP, Aga AB, Sexton J, Olsen IC, Lexberg Å S, et al. Three-Year Results of Tapering Tumor Necrosis Factor Inhibitor to Withdrawal Compared to Stable Tumor Necrosis Factor Inhibitor Among Patients With Rheumatoid Arthritis in Sustained Remission: A Multicenter Randomized Trial. Arthritis Rheumatol. 2025;77(10):1327-36.
- van der Togt CJT, den Broeder N, Boonstra MS, van der Maas A, den Broeder AA, van Herwaarden N. Disease activity-guided dose optimization including discontinuation of TNF inhibitors in rheumatoid arthritis is effective for up to 10 years: an observational follow-up of the DRESS study. Rheumatology (Oxford). 2025;64(2):533-40.
- Quinn MA, Conaghan PG, O’Connor PJ, Karim Z, Greenstein A, Brown A, et al. Very early treatment with infliximab in addition to methotrexate in early, poor-prognosis rheumatoid arthritis reduces magnetic resonance imaging evidence of synovitis and damage, with sustained benefit after infliximab withdrawal: results from a twelve-month randomized, double-blind, placebo-controlled trial. Arthritis Rheum. 2005;52(1):27-35.
- Goekoop-Ruiterman YP, de Vries-Bouwstra JK, Allaart CF, van Zeben D, Kerstens PJ, Hazes JM, et al. Comparison of treatment strategies in early rheumatoid arthritis: a randomized trial. Ann Intern Med. 2007;146(6):406-15.
- Tanaka Y, Takeuchi T, Mimori T, Saito K, Nawata M, Kameda H, et al. Discontinuation of infliximab after attaining low disease activity in patients with rheumatoid arthritis: RRR (remission induction by Remicade in RA) study. Ann Rheum Dis. 2010;69(7):1286-91.
- Emamikia S, Arkema EV, Gyori N, Detert J, Chatzidionysiou K, Dougados M, et al. Induction maintenance with tumour necrosis factor-inhibitor combination therapy with discontinuation versus methotrexate monotherapy in early rheumatoid arthritis: a systematic review and meta-analysis of efficacy in randomised controlled trials. RMD Open. 2016;2(2):e000323.
- Tanaka Y, Smolen JS, Jones H, Szumski A, Marshall L, Emery P. The effect of deep or sustained remission on maintenance of remission after dose reduction or withdrawal of etanercept in patients with rheumatoid arthritis. Arthritis Res Ther. 2019;21(1):164.
- Westhovens R, Robles M, Ximenes AC, Wollenhaupt J, Durez P, Gomez-Reino J, et al. Maintenance of remission following 2 years of standard treatment then dose reduction with abatacept in patients with early rheumatoid arthritis and poor prognosis. Ann Rheum Dis. 2015;74(3):564-8.
- Emery P, Tanaka Y, Bykerk V, Huizinga T, Citera G, Bingham C, et al. Sustained Remission and Outcomes with Abatacept plus Methotrexate Following Stepwise Dose De-escalation in Patients with Early Rheumatoid Arthritis. Rheumatol Ther. 2023;10(3):707-27.
- Park JW, Kim MJ, Kim HA, Kim JH, Lee EB, Shin K. The Aftermath of Tapering Tocilizumab After Achieving Treatment Target in Patients With Rheumatoid Arthritis: A Nationwide Cohort Study. Front Med (Lausanne). 2022;9:839206.
- Huizinga TW, Conaghan PG, Martin-Mola E, Schett G, Amital H, Xavier RM, et al. Clinical and radiographic outcomes at 2 years and the effect of tocilizumab discontinuation following sustained remission in the second and third year of the ACT-RAY study. Ann Rheum Dis. 2015;74(1):35-43.
- Bouman CAM, Tweehuysen L, Haverkort D, van den Ende CH, van der Maas A, den Broeder AA. Abatacept and tocilizumab tapering in rheumatoid arthritis patients: results of SONATA-a retrospective, exploratory cohort study. Rheumatol Adv Pract. 2018;2(1):rky008.
- Takeuchi T, Genovese MC, Haraoui B, Li Z, Xie L, Klar R, et al. Dose reduction of baricitinib in patients with rheumatoid arthritis achieving sustained disease control: results of a prospective study. Ann Rheum Dis. 2019;78(2):171-8.
- Wang M, Xue Y, Du F, Ma L, Lu LJ, Jiang L, et al. Continuation, reduction, or withdrawal of tofacitinib in patients with rheumatoid arthritis achieving sustained disease control: a multicenter, open-label, randomized controlled trial. Chin Med J (Engl). 2023;136(3):331-40.
- Mori S, Ueki Y. Outcomes of dose reduction, withdrawal, and restart of tofacitinib in patients with rheumatoid arthritis: a prospective observational study. Clin Rheumatol. 2019;38(12):3391-400.
- van Mulligen E, de Jong PHP, Kuijper TM, van der Ven M, Appels C, Bijkerk C, et al. Gradual tapering TNF inhibitors versus conventional synthetic DMARDs after achieving controlled disease in patients with rheumatoid arthritis: first-year results of the randomised controlled TARA study. Rheumatology (Oxford). 2019;78(6):746-53.
- Smolen JS, Pedersen R, Jones H, Mahgoub E, Marshall L. Impact of flare on radiographic progression after etanercept continuation, tapering or withdrawal in patients with rheumatoid arthritis. Ann Rheum Dis. 2020;59(1):153-64.
- Krause D, Krause C, Rudolf H, Baraliakos X, Braun J, Schmitz E. Dose tapering of biologic agents in patients with rheumatoid arthritis-results from a cohort study in Germany. Clin Rheumatol. 2021;40(3):887-93.
- Dierckx S, Sokolova T, Lauwerys BR, Avramovska A, de Bellefon LM, Toukap AN, et al. Tapering of biological antirheumatic drugs in rheumatoid arthritis patients is achievable and cost-effective in daily clinical practice: data from the Brussels UCLouvain RA Cohort. Arthritis Res Ther. 2020;22(1):96.
- Arnold S, Jaeger VK, Scherer A, Ciurea A, Walker UA, Kyburz D. Discontinuation of biologic DMARDs in a real-world population of patients with rheumatoid arthritis in remission: outcome and risk factors. Rheumatology (Oxford). 2021;61(1):131-8.
- Kameda H, Hirata A, Katagiri T, Takakura Y, Inoue Y, Takenaka S, et al. Prediction of disease flare by biomarkers after discontinuing biologics in patients with rheumatoid arthritis achieving stringent remission. Sci Rep. 2021;11(1):6865.
- Ochiai M, Tanaka E, Sato E, Inoue E, Abe M, Saka K, et al. Successful discontinuation of biological disease-modifying antirheumatic drugs in patients with rheumatoid arthritis in real-world settings. Mod Rheumatol. 2021;31(4):790-5.
- Klarenbeek NB, van der Kooij SM, Güler-Yüksel M, van Groenendael JH, Han KH, Kerstens PJ, et al. Discontinuing treatment in patients with rheumatoid arthritis in sustained clinical remission: exploratory analyses from the BeSt study. Ann Rheum Dis. 2011;70(2):315-9.
- Lillegraven S, Paulshus Sundlisæter N, Aga AB, Sexton J, Olsen IC, Fremstad H, et al. Effect of Half-Dose vs Stable-Dose Conventional Synthetic Disease-Modifying Antirheumatic Drugs on Disease Flares in Patients With Rheumatoid Arthritis in Remission: The ARCTIC REWIND Randomized Clinical Trial. Jama. 2021;325(17):1755-64.
- Kjørholt KE, Sundlisæter NP, Aga AB, Sexton J, Olsen IC, Fremstad H, et al. Effects of tapering conventional synthetic disease-modifying antirheumatic drugs to drug-free remission versus stable treatment in rheumatoid arthritis (ARCTIC REWIND): 3-year results from an open-label, randomised controlled, non-inferiority trial. Lancet Rheumatol. 2024;6(5):e268-e78.
- Meng CF, Rajesh DA, Jannat-Khah DP, Jivanelli B, Bykerk V. Can Patients With Controlled Rheumatoid Arthritis Taper Methotrexate From Targeted Therapy and Sustain Remission? A Systematic Review and Metaanalysis. J Rheumatol. 2023;50(1):36-47.
- Dobler CC. Biologic Agents and Tuberculosis. Microbiol Spectr. 2016;4(6).
- Loomba R, Liang TJ. Hepatitis B Reactivation Associated With Immune Suppressive and Biological Modifier Therapies: Current Concepts, Management Strategies, and Future Directions. Gastroenterology. 2017;152(6):1297-309.
- Bongartz T, Sutton AJ, Sweeting MJ, Buchan I, Matteson EL, Montori V. Anti-TNF antibody therapy in rheumatoid arthritis and the risk of serious infections and malignancies: systematic review and meta-analysis of rare harmful effects in randomized controlled trials. Jama. 2006;295(19):2275-85.
- Sepriano A, Kerschbaumer A, Bergstra SA, Smolen JS, van der Heijde D, Caporali R, et al. Safety of synthetic and biological DMARDs: a systematic literature review informing the 2022 update of the EULAR recommendations for the management of rheumatoid arthritis. Ann Rheum Dis. 2023;82(1):107-18.
- Gottenberg JE, Ravaud P, Bardin T, Cacoub P, Cantagrel A, Combe B, et al. Risk factors for severe infections in patients with rheumatoid arthritis treated with rituximab in the autoimmunity and rituximab registry. Arthritis Rheum. 2010;62(9):2625-32.
- van Vollenhoven RF, Fleischmann RM, Furst DE, Lacey S, Lehane PB. Longterm Safety of Rituximab: Final Report of the Rheumatoid Arthritis Global Clinical Trial Program over 11 Years. J Rheumatol. 2015;42(10):1761-6.
- Buch MH, Smolen JS, Betteridge N, Breedveld FC, Burmester G, Dorner T, et al. Updated consensus statement on the use of rituximab in patients with rheumatoid arthritis. Ann Rheum Dis. 2011;70(6):909-20.
- Evangelatos G, Fragoulis GE, Klavdianou K, Moschopoulou M, Vassilopoulos D, Iliopoulos A. Hypogammaglobulinemia after rituximab for rheumatoid arthritis is not rare and is related with good response: 13 years real-life experience. Rheumatology (Oxford). 2021;60(5):2375-82.
- Monaco WE, Jones JD, Rigby WF. Rituximab associated late-onset neutropenia-a rheumatology case series and review of the literature. Clin Rheumatol. 2016;35(10):2457-62.
- Askling J, Fahrbach K, Nordstrom B, Ross S, Schmid CH, Symmons D. Cancer risk with tumor necrosis factor alpha (TNF) inhibitors: meta-analysis of randomized controlled trials of adalimumab, etanercept, and infliximab using patient level data. Pharmacoepidemiol Drug Saf. 2011;20(2):119-30.
- Mariette X, Matucci-Cerinic M, Pavelka K, Taylor P, van Vollenhoven R, Heatley R, et al. Malignancies associated with tumour necrosis factor inhibitors in registries and prospective observational studies: a systematic review and meta-analysis. Ann Rheum Dis. 2011;70(11):1895-904.
- Waljee AK, Higgins PDR, Jensen CB, Villumsen M, Cohen-Mekelburg SA, Wallace BI, et al. Anti-tumour necrosis factor-α therapy and recurrent or new primary cancers in patients with inflammatory bowel disease, rheumatoid arthritis, or psoriasis and previous cancer in Denmark: a nationwide, population-based cohort study. Rheumatology (Oxford). 2020;5(3):276-84.
- Simon TA, Suissa S, Boers M, Hochberg MC, Skovron ML, Askling J, et al. Malignancy outcomes in patients with rheumatoid arthritis treated with abatacept and other disease-modifying antirheumatic drugs: Results from a 10-year international post-marketing study. Semin Arthritis Rheum. 2024;64:152240.
- Sepriano A, Kerschbaumer A, Bergstra SA, Smolen J, van der Heijde D, Caporali R, et al. Safety of synthetic and biological DMARDs: a systematic literature review informing the 2022 update of the EULAR recommendations for the management of rheumatoid arthritis. Ann Rheum Dis. 2023;82(1):107-18.
- Raaschou P, Simard JF, Asker Hagelberg C, Askling J. Rheumatoid arthritis, anti-tumour necrosis factor treatment, and risk of squamous cell and basal cell skin cancer: cohort study based on nationwide prospectively recorded data from Sweden. Bmj. 2016;352:i262.
- Raaschou P, Simard JF, Holmqvist M, Askling J. Rheumatoid arthritis, anti-tumour necrosis factor therapy, and risk of malignant melanoma: nationwide population based prospective cohort study from Sweden. Bmj. 2013;346:f1939.
- Mercer LK, Askling J, Raaschou P, Dixon WG, Dreyer L, Hetland ML, et al. Risk of invasive melanoma in patients with rheumatoid arthritis treated with biologics: results from a collaborative project of 11 European biologic registers. Ann Rheum Dis. 2017;76:386-91.
- Wadstrom H, Frisell T. Do RA or TNF inhibitors increase the risk of cervical neoplasia or of recurrence of previous neoplasia? A nationwide study from Sweden. 2016;75(7):1272-8.
- Xie W, Yang X, Huang H, Gao D, Ji L, Zhang Z. Risk of malignancy with non-TNFi biologic or tofacitinib therapy in rheumatoid arthritis: A meta-analysis of observational studies. Semin Arthritis Rheum. 2020;50(5):930-7.
- Simon TA, Dong L, Suissa S, Michaud K, Pedro S, Hochberg M, et al. Abatacept and non-melanoma skin cancer in patients with rheumatoid arthritis: a comprehensive evaluation of randomised controlled trials and observational studies. Ann Rheum Dis. 2024;83(2):177-83.
- de Germay S, Bagheri H, Despas F, Rousseau V, Montastruc F. Abatacept in rheumatoid arthritis and the risk of cancer: a world observational post-marketing study. Rheumatology (Oxford). 2020;59(9):2360-7.
- Westermann R, Cordtz RL, Duch K, Mellemkjaer L, Hetland ML, Magnussen B, et al. Cancer risk with tocilizumab/sarilumab, abatacept and rituximab treatment in patients with rheumatoid arthritis: a Danish cohort study. Rheumatology (Oxford). 2025;64(3):1019-28.
- Lopez-Olivo MA, Tayar JH, Martinez-Lopez JA, Pollono EN, Cueto JP, Gonzales-Crespo MR, et al. Risk of malignancies in patients with rheumatoid arthritis treated with biologic therapy: a meta-analysis. Jama. 2012;308(9):898-908.
- Wadstrom H, Frisell T, Askling J. Malignant Neoplasms in Patients With Rheumatoid Arthritis Treated With Tumor Necrosis Factor Inhibitors, Tocilizumab, Abatacept, or Rituximab in Clinical Practice: A Nationwide Cohort Study From Sweden. JAMA Intern Med. 2017;177(11):1605-12.
- Huss V, Bower H, Hellgren K, Frisell T, Askling J. Cancer risks with JAKi and biological disease-modifying antirheumatic drugs in patients with rheumatoid arthritis or psoriatic arthritis: a national real-world cohort study. Ann Rheum Dis. 2023;82(7):911-9.
- Strangfeld A, Hierse F, Rau R, Burmester GR, Krummel-Lorenz B, Demary W, et al. Risk of incident or recurrent malignancies among patients with rheumatoid arthritis exposed to biologic therapy in the German biologics register RABBIT. Arthritis Res Ther. 2010;12(1):R5.
- Raaschou P, Frisell T, Askling J. TNF inhibitor therapy and risk of breast cancer recurrence in patients with rheumatoid arthritis: a nationwide cohort study. Ann Rheum Dis. 2015;74(12):2137-43.
- Silva-Fernandez L, Lunt M, Kearsley-Fleet L, Watson KD, Dixon WG, Symmons DP, et al. The incidence of cancer in patients with rheumatoid arthritis and a prior malignancy who receive TNF inhibitors or rituximab: results from the British Society for Rheumatology Biologics Register-Rheumatoid Arthritis. Rheumatology (Oxford). 2016;55(11):2033-9.
- Raaschou P, Soderling J, Turesson C, Askling J. Tumor Necrosis Factor Inhibitors and Cancer Recurrence in Swedish Patients With Rheumatoid Arthritis: A Nationwide Population-Based Cohort Study. Ann Intern Med. 2018;169(5):291-9.
362. Xie W, Xiao S, Huang Y, Sun X, Gao D, Ji L, et al. A meta-analysis of biologic therapies on risk of new or recurrent cancer in patients with rheumatoid arthritis and a prior malignancy. Rheumatology (Oxford). 2020;59(5):930-9.
- Westermann R, Cordtz R, Duch K, Mellemkjaer L, Hetland ML, Rasmussen LA, et al. Cancer recurrence risk with bDMARD treatment in patients with rheumatoid arthritis and a history of cancer: a nationwide Danish register-based cohort study. RMD Open. 2025;11(2).
- Barbulescu A, Delcoigne B, Askling J, Frisell T. Gastrointestinal perforations in patients with rheumatoid arthritis treated with biological disease-modifying antirheumatic drugs in Sweden: a nationwide cohort study. RMD Open. 2020;6(2).
- Xie F, Yun H, Bernatsky S, Curtis JR. Brief Report: Risk of Gastrointestinal Perforation Among Rheumatoid Arthritis Patients Receiving Tofacitinib, Tocilizumab, or Other Biologic Treatments. Arthritis Rheumatol 2016;68(11):2612-7.
- Rempenault C, Lukas C, Combe B, Herrero A, Pane I, Schaeverbeke T, et al. Risk of diverticulitis and gastrointestinal perforation in rheumatoid arthritis treated with tocilizumab compared to rituximab or abatacept. Rheumatology (Oxford) 2022;61(3):953-62.
- Kerschbaumer A, Smolen JS, Nash P, Doerner T, Dougados M, Fleischmann R, et al. Points to consider for the treatment of immune-mediated inflammatory diseases with Janus kinase inhibitors: a systematic literature research. RMD Open. 2020;6(3):e001374.
- European Medical Agency. https://www.ema.europa.eu/en/medicines/human/referrals/janus-kinase-inhibitors-jaki.
- Food and Drug Administration. https://www.fda.gov/drugs/drug-safety-and-availability/fda-requires-warnings-about-increased-risk-serious-heart-related-events-cancer-blood-clots-and-death.
- Ytterberg SR, Bhatt DL, Mikuls TR, Koch GG, Fleischmann R, Rivas JL, et al. Cardiovascular and Cancer Risk with Tofacitinib in Rheumatoid Arthritis. N Engl J Med. 2022;386(4):316-26.
- Charles-Schoeman C, Buch MH, Dougados M, Bhatt DL, Giles JT, Ytterberg SR, et al. Risk of major adverse cardiovascular events with tofacitinib versus tumour necrosis factor inhibitors in patients with rheumatoid arthritis with or without a history of atherosclerotic cardiovascular disease: a post hoc analysis from ORAL Surveillance. Ann Rheum Dis. 2023;82(1):119-29.
- Kristensen LE, Danese S, Yndestad A, Wang C, Nagy E, Modesto I, et al. Identification of two tofacitinib subpopulations with different relative risk versus TNF inhibitors: an analysis of the open label, randomised controlled study ORAL Surveillance. Ann Rheum Dis. 2023;82(7):901-10.
- Cohen SB, van Vollenhoven RF, Winthrop KL, Zerbini CAF, Tanaka Y, Bessette L, et al. Safety profile of upadacitinib in rheumatoid arthritis: integrated analysis from the SELECT phase III clinical programme. Ann Rheum Dis. 2020;80(3):304-11.
- Kavanaugh A, Westhovens RR, Winthrop KL, Lee SJ, Tan Y, An D, et al. Safety and Efficacy of Filgotinib: Up to 4-year Results From an Open-label Extension Study of Phase II Rheumatoid Arthritis Programs. J Rheumatol. 2021;48(8):1230-8.
- Winthrop KL, Citera G, Gold D, Henrohn D, Connell CA, Shapiro AB, et al. Age-based (<65 vs ≥65 years) incidence of infections and serious infections with tofacitinib versus biological DMARDs in rheumatoid arthritis clinical trials and the US Corrona RA registry. Ann Rheum Dis. 2021;80(1):134-6.
- Hoisnard L, Pina Vegas L, Dray-Spira R, Weill A, Zureik M, Sbidian E. Risk of major adverse cardiovascular and venous thromboembolism events in patients with rheumatoid arthritis exposed to JAK inhibitors versus adalimumab: a nationwide cohort study. Ann Rheum Dis. 2023;82(2):182-8.
- Khosrow-Khavar F, Desai RJ, Lee H, Lee SB, Kim SC. Tofacitinib and Risk of Malignancy: Results From the Safety of Tofacitinib in Routine Care Patients With Rheumatoid Arthritis (STAR-RA) Study. Arthritis Rheumatol. 2022;74(10):1648-59.
- Taylor PC, Takeuchi T, Burmester G, Durez P, Smolen J, Deberdt W, et al. Safety of baricitinib for the treatment of rheumatoid arthritis over a median of 4.6 and up to 9.3 years of treatment: final results from long-term extension study and integrated database. Ann Rheum Dis. 2022;81(3):335-43.
- Burmester GR, Cohen SB, Winthrop K, Nash P, Irvine AD, Deodhar A, et al. Safety profile of upadacitinib over 15 000 patient-years across rheumatoid arthritis, psoriatic arthritis, ankylosing spondylitis and atopic dermatitis. RMD Open. 2023;9(1).
- Tong X, Shen CY, Jeon HL, Li Y, Shin JY, Chan SC, et al. Cardiovascular risk in rheumatoid arthritis patients treated with targeted synthetic and biological disease-modifying antirheumatic drugs: A multi-centre cohort study. J Intern Med. 2023;294(3):314-25.
- Fleischmann R, Curtis JR, Charles-Schoeman C, Mysler E, Yamaoka K, Richez C, et al. Safety profile of upadacitinib in patients at risk of cardiovascular disease: integrated post hoc analysis of the SELECT phase III rheumatoid arthritis clinical programme. Ann Rheum Dis. 2023;82(9):1130-41.
- Fleischmann R, Swierkot J, Penn SK, Durez P, Bessette L, Bu X, et al. Long-term safety and efficacy of upadacitinib versus adalimumab in patients with rheumatoid arthritis: 5-year data from the phase 3, randomised SELECT-COMPARE study. RMD Open. 2024;10(2).
- Burmester GR, Gottenberg JE, Caporali R, Winthrop KL, Tanaka Y, Ekoka Omoruyi EV, et al. Integrated safety analysis of filgotinib in patients with moderate-to-severe rheumatoid arthritis over a treatment duration of up to 8.3 years. Ann Rheum Dis. 2024;83(9):1110-7.
- Westhovens R, Winthrop KL, Kavanaugh A, Greenwald M, Dagna L, Cseuz R, et al. Safety and efficacy of filgotinib in patients with rheumatoid arthritis: final results of the DARWIN 3 long-term extension study. RMD Open. 2025;11(1).
- Silvagni E, Bortoluzzi A, Occhino G, Bellelli G, Garaffoni C, Delvino P, et al. Frailty and cardiovascular safety of JAK inhibitors versus TNF inhibitors in rheumatoid arthritis: a real-world comparative study of drug effects and patient profiles. Front Pharmacol. 2025;16:1565909.
- Bower H, Frisell T, di Giuseppe D, Delcoigne B, Askling J. Comparative cardiovascular safety with janus kinase inhibitors and biological disease-modifying antirheumatic drugs as used in clinical practice: an observational cohort study from Sweden in patients with rheumatoid arthritis. RMD Open. 2023;9(4).
- Aymon R, Mongin D, Guemara R, Salis Z, Askling J, Choquette D, et al. Incidence of Major Adverse Cardiovascular Events in Patients With Rheumatoid Arthritis Treated With JAK Inhibitors Compared With Biologic Disease-Modifying Antirheumatic Drugs: Data From an International Collaboration of Registries. Arthritis Rheumatol. 2025;77(9):1194-204.
- Molander V, Bower H, Frisell T, Delcoigne B, Di Giuseppe D, Askling J. Venous thromboembolism with JAK inhibitors and other immune-modulatory drugs: a Swedish comparative safety study among patients with rheumatoid arthritis. Ann Rheum Dis. 2023;82(2):189-97.
- Salinas CA, Louder A, Polinski J, Zhang TC, Bower H, Phillips S, et al. Evaluation of VTE, MACE, and Serious Infections Among Patients with RA Treated with Baricitinib Compared to TNFi: A Multi-Database Study of Patients in Routine Care Using Disease Registries and Claims Databases. Rheumatol Ther. 2022:1-23.
- Solitano V, Ahuja D, Lee HH, Gaikwad R, Yeh KH, Facciorusso A, et al. Comparative Safety of JAK Inhibitors vs TNF Antagonists in Immune-Mediated Inflammatory Diseases: A Systematic Review and Meta-Analysis. JAMA Netw Open. 2025;8(9):e2531204.
- Bezzio C, Vernero M, Ribaldone DG, Alimenti E, Manes G, Saibeni S. Cancer Risk in Patients Treated with the JAK Inhibitor Tofacitinib: Systematic Review and Meta-Analysis. Cancers (Basel). 2023;15(8):2197.
- Russell MD, Stovin C, Alveyn E, Adeyemi O, Chan CKD, Patel V, et al. JAK inhibitors and the risk of malignancy: a meta-analysis across disease indications. Ann Rheum Dis. 2023;82(8):1059-67.
- Schaefer M, Purschke A, Zietemann V, Rudi T, Meissner Y, Richter A, et al. Comparative risk of incident malignancies in rheumatoid arthritis patients treated with Janus kinase inhibitors or bDMARDs: observational data from the German RABBIT register. Ann Rheum Dis. 2025;84(11):1779-90.
- Ahmed S, Pfeiffer RM, Jackson SS, Song M, Mariette X, Seror R, et al. Cancer risk of Janus kinase inhibitors and biological disease-modifying antirheumatic drugs among older Americans with rheumatoid arthritis. Rheumatology (Oxford). 2025;64(7):4172-80.
- Xu C, Wang SI, Leung YY, Wei JC. Comparative Cancer Incidence by Organ Site in Rheumatoid Arthritis Treated with Janus Kinase Inhibitors versus Tumor Necrosis Factor Inhibitors: A Retrospective Real-World Cohort Analysis. Biologics. 2025;19:525-38.
- Clarke B, Yates M, Adas M, Bechman K, Galloway J. The safety of JAK-1 inhibitors. J Rheumatol. 2021;60(Suppl 2):ii24-ii30.
- Benucci M, Damiani A, Infantino M, Manfredi M, Lari B, Grossi V, et al. Cardiovascular safety, cancer and Jak-inhibitors: Differences to be highlighted. Pharmacological research. 2022;183:106359.
- Wollenhaupt J, Silverfield J, Lee EB, Curtis JR, Wood SP, Soma K, et al. Safety and efficacy of tofacitinib, an oral janus kinase inhibitor, for the treatment of rheumatoid arthritis in open-label, longterm extension studies. J Rheumatol. 2014;41(5):837-52.
- Smolen JS, Genovese MC, Takeuchi T, Hyslop D, Macias W, Rooney T, et al. Safety Profile of Baricitinib in Patients with Active Rheumatoid Arthritis with over 2 Years Median Time in Treatment. J Rheumatol. 2019;46(1):7-18.
- Winthrop K, Isaacs J, Calabrese L, Mittal D, Desai S, Barry J, et al. Opportunistic infections associated with Janus kinase inhibitor treatment for rheumatoid arthritis: A structured literature review. Semin Arthritis Rheum. 2023;58:152120.
- Sathapanasiri T, Meraz M, Mokri H, S KV, Wijarnpreecha K, Schlesinger N, et al. Gastrointestinal Perforation as a Safety Concern Among Patients With Rheumatoid Arthritis Receiving JAK Inhibitor Therapy: A Systematic Review and Network Meta-Analysis. Arthritis Care Res (Hoboken). 2025;77(10):1222-8.
- Smolen JS, Landewe R, Breedveld FC, Buch M, Burmester G, Dougados M, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2013 update. Ann Rheum Dis. 2014;73:492-509.
- Gotzsche PC, Johansen HK. Short-term low-dose corticosteroids vs placebo and nonsteroidal antiinflammatory drugs in rheumatoid arthritis. Cochrane Database Syst Rev. 2004(3):Cd000189.
- Svensson B, Boonen A, Albertsson K, van der Heijde D, Keller C, Hafstrom I. Low-dose prednisolone in addition to the initial disease-modifying antirheumatic drug in patients with early active rheumatoid arthritis reduces joint destruction and increases the remission rate: a two-year randomized trial. Arthritis Rheum. 2005;52(11):3360-70.
- Da Silva JA, Jacobs JW, Kirwan JR, Boers M, Saag KG, Ines LB, et al. Safety of low dose glucocorticoid treatment in rheumatoid arthritis: published evidence and prospective trial data. Ann Rheum Dis. 2006;65(3):285-93.
- Kirwan JR, Bijlsma JW, Boers M, Shea BJ. Effects of glucocorticoids on radiological progression in rheumatoid arthritis. Cochrane Database Syst Rev. 2007(1):Cd006356.
- Wassenberg S, Rau R, Zeidler H. A dose of only 5 mg prednisolone daily retards radiographic progression in early rheumatoid arthritis – the Low-Dose Prednisolone Trial. Clin Exp Rheumatol. 2011;29(5 Suppl 68):S68-72.
- Boers M, Hartman L, Opris-Belinski D, Bos R, Kok MR, Da Silva J, et al. Low dose, add-on prednisolone in patients with rheumatoid arthritis aged 65+: the pragmatic randomised, double-blind placebo-controlled GLORIA trial. Ann Rheum Dis. 2022;81(7):925-36.
- Ozen G, Pedro S, Holmqvist ME, Avery M, Wolfe F, Michaud K. Risk of diabetes mellitus associated with disease-modifying antirheumatic drugs and statins in rheumatoid arthritis. Ann Rheum Dis. 2017;76(5):848-54.
- Ajeganova S, Svensson B, Hafstrom I. Low-dose prednisolone treatment of early rheumatoid arthritis and late cardiovascular outcome and survival: 10-year follow-up of a 2-year randomised trial. BMJ Open. 2014;4(4):e004259.
- Strehl C, Bijlsma JW, de Wit M, Boers M, Caeyers N, Cutolo M, et al. Defining conditions where long-term glucocorticoid treatment has an acceptably low level of harm to facilitate implementation of existing recommendations: viewpoints from an EULAR task force. 2016;75(6):952-7.
- Ocon AJ, Reed G, Pappas DA. Short-term dose and duration-dependent glucocorticoid risk for cardiovascular events in glucocorticoid-naive patients with rheumatoid arthritis. Ann Rheum Dis. 2021;80(12):1522-9.
- Blavnsfeldt AG, de Thurah A, Thomsen MD, Tarp S, Langdahl B, Hauge EM. The effect of glucocorticoids on bone mineral density in patients with rheumatoid arthritis: A systematic review and meta-analysis of randomized, controlled trials. RMD Open. 2018;114:172-80.
- Roubille C, Rincheval N, Dougados M, Flipo RM, Daures JP, Combe B. Seven-year tolerability profile of glucocorticoids use in early rheumatoid arthritis: data from the ESPOIR cohort. Ann Rheum Dis. 2017;76(11):1797-802.
- Smolen JS, Landewé RBM, Bijlsma JWJ, Burmester GR, Dougados M, Kerschbaumer A. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2019 update. Ann Rheum Dis. 2020;79(6):685-99.
- Bakker MF, Jacobs JW, Welsing PM, Verstappen SM, Tekstra J, Ton E, et al. Low-dose prednisone inclusion in a methotrexate-based, tight control strategy for early rheumatoid arthritis: a randomized trial. Ann Intern Med. 2012;156(5):329-39.
- Smolen JS, Landewe R, Bijlsma J, Burmester G, Chatzidionysiou K, Dougados M, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease-modifying antirheumatic drugs: 2016 update. 2017;76(6):960-77.
- Maassen JM, dos Santos Sobrín R, Bergstra SA, Goekoop R, Huizinga T, Allaart CF. Glucocorticoid discontinuation in patients with early rheumatoid and undifferentiated arthritis: a post-hoc analysis of the BeSt and IMPROVED studies. Ann Rheum Dis. 2021;80(9):1124-9.
- Hetland ML, Heiberg MS, Sokka-Isler T, Rudin A, Østergaard M, Haavardsholm E, et al. Treatment with methotrexate plus oral prednisolone versus triple therapy (methotrexate/sulfasalazine/hydroxychloroquine) plus intra-articular glucocorticoids in early rheumatoid arthritis: a prespecified nonrandomised subgroup analysis of clinical and radiographic data at 48 weeks from the NORD-STAR trial’s conventional treatment arm. Ann Rheum Dis. 2025;84(6):937-48.
- Cushman DM, Bruno B, Christiansen J, Schultz A, McCormick ZL. Efficacy of Injected Corticosteroid Type, Dose, and Volume for Pain in Large Joints: A Narrative Review. Pm r. 2018;10(7):748-57.
- Cushman DM, Ofek E, Syed RH, Clements N, Gardner JE, Sams JM, et al. Comparison of Varying Corticosteroid Type, Dose, and Volume for the Treatment of Pain in Small- and Intermediate-Size Joint Injections: A Narrative Review. Pm r. 2019;11(7):758-70.
- Conaghan PG, O’Connor P, McGonagle D, Astin P, Wakefield RJ, Gibbon WW, et al. Elucidation of the relationship between synovitis and bone damage: a randomized magnetic resonance imaging study of individual joints in patients with early rheumatoid arthritis. Arthritis Rheum. 2003;48(1):64-71.
- Scott DG, Bacon PA. Intravenous cyclophosphamide plus methylprednisolone in treatment of systemic rheumatoid vasculitis. Am J Med. 1984;76(3):377-84.
- Foster CS, Forstot SL, Wilson LA. Mortality rate in rheumatoid arthritis patients developing necrotizing scleritis or peripheral ulcerative keratitis. Effects of systemic immunosuppression. Ophthalmology. 1984;91(10):1253-63.
- Kim DS. Interstitial lung disease in rheumatoid arthritis: recent advances. Curr Opin Pulm Med. 2006;12(5):346-53.
- Ota M, Iwasaki Y, Harada H, Sasaki O, Nagafuchi Y, Nakachi S, et al. Efficacy of intensive immunosuppression in exacerbated rheumatoid arthritis-associated interstitial lung disease. Mod Rheumatol. 2016:1-7.
- Berglund K, Keller C, Thysell H. Alkylating cytostatic treatment in renal amyloidosis secondary to rheumatic disease. Ann Rheum Dis. 1987;46(10):757-62.
- Nakamura T, Higashi S, Tomoda K, Tsukano M, Baba S. Efficacy of etanercept in patients with AA amyloidosis secondary to rheumatoid arthritis. Clin Exp Rheumatol. 2007;25(4):518-22.
- Puechal X, Miceli-Richard C, Mejjad O, Lafforgue P, Marcelli C, Solau-Gervais E, et al. Anti-tumour necrosis factor treatment in patients with refractory systemic vasculitis associated with rheumatoid arthritis. Ann Rheum Dis. 2008;67(6):880-4.
- Puechal X, Gottenberg JE, Berthelot JM, Gossec L, Meyer O, Morel J, et al. Rituximab therapy for systemic vasculitis associated with rheumatoid arthritis: Results from the AutoImmunity and Rituximab Registry. Arthritis Care Res (Hoboken). 2012;64(3):331-9.
- Sauer BC, Al Attar L, Shaver T. Abatacept as a Therapeutic Option for Rheumatoid Vasculitis. Arthritis Care Res (Hoboken). 2018;10(4):e2506.
- Iijima T, Suwabe T, Sumida K, Hayami N, Hiramatsu R, Hasegawa E, et al. Tocilizumab improves systemic rheumatoid vasculitis with necrotizing crescentic glomerulonephritis. Mod Rheumatol. 2015;25(1):138-42.
- Nakashita T, Ando K, Takahashi K, Motojima S. Possible effect of abatacept on the progression of interstitial lung disease in rheumatoid arthritis patients. Respir Investig. 2016;54(5):376-9.
- Fernandez-Diaz C, Loricera J, Castaneda S, Lopez-Mejias R, Ojeda-Garcia C, Olive A, et al. Abatacept in patients with rheumatoid arthritis and interstitial lung disease: A national multicenter study of 63 patients. Semin Arthritis Rheum. 2018;48(1):22-7.
- Ines M, Zeineb Z, Selma B, Olfa S, Leila R, Rawdha T, et al. Efficacy and safety of rituximab in rheumatoid arthritis-associated interstitial lung disease: a systematic review and meta-analysis. Expert Opin Biol Ther. 2025;25(10):1087-99.
- Manfredi A, Cassone G, Furini F, Gremese E, Venerito V, Atzeni F, et al. Tocilizumab therapy in rheumatoid arthritis with interstitial lung disease: a multicentre retrospective study. Intern Med J. 2020;50(9):1085-90.
- Shih PC, Wang SI, Wang QW, Wei JCC. Association of Abatacept with Lower Mortality Risk Compared to Rituximab in Rheumatoid Arthritis-Associated Interstitial Lung Disease: An Emulated Target Trial. Arthritis Rheumatol. 2025.
- Frideres H, Wichman CS, Dong J, Roul P, Yang Y, Baker JF, et al. Non-TNFi biologic and targeted synthetic DMARDs in rheumatoid arthritis-associated interstitial lung disease: A propensity score-matched, active-comparator, new-user study. Semin Arthritis Rheum. 2025;73:152735.
- Vicente-Rabaneda EF, Atienza-Mateo B, Blanco R, Cavagna L, Ancochea J, Castañeda S, et al. Efficacy and safety of abatacept in interstitial lung disease of rheumatoid arthritis: A systematic literature review. Eur Respir J. 2021;20(6):102830.
- Shoda T, Kotani T, Koyama M, Yoshikawa A, Wada Y, Makino H, et al. The Therapeutic Efficacy of Abatacept for Rheumatoid Arthritis-Associated Interstitial Lung Disease: Insights from a 12-Month Trial Using Semi-Quantitative Chest High-Resolution Computed Tomography Imaging. J Clin Med. 2024;13(19).
- Matson SM, Baqir M, Moua T, Marll M, Kent J, Iannazzo NS, et al. Treatment Outcomes for Rheumatoid Arthritis-Associated Interstitial Lung Disease: A Real-World, Multisite Study of the Impact of Immunosuppression on Pulmonary Function Trajectory. Chest. 2023;163(4):861-9.
- Puttick MP, Klinkhoff AV, Chalmers A, Ostrow DN. Treatment of progressive rheumatoid interstitial lung disease with cyclosporine. J Rheumatol. 1995;22(11):2163-5.
- Ogawa D, Hashimoto H, Wada J, Ueno A, Yamasaki Y, Yamamura M, et al. Successful use of cyclosporin A for the treatment of acute interstitial pneumonitis associated with rheumatoid arthritis. Rheumatology (Oxford). 2000;39(12):1422-4.
- Roubille C, Haraoui B. Interstitial lung diseases induced or exacerbated by DMARDS and biologic agents in rheumatoid arthritis: a systematic literature review. Semin Arthritis Rheum. 2014;43(5):613-26.
- Zhang Q, McDermott GC, Juge PA, Chang SH, Vanni KM, Qian G, et al. Disease-modifying antirheumatic drugs and risk of incident interstitial lung disease among patients with rheumatoid arthritis: A systematic review and meta-analysis. Semin Arthritis Rheum. 2024;69:152561.
- Wells AU, Flaherty KR, Brown KK, Inoue Y, Devaraj A, Richeldi L, et al. Nintedanib in patients with progressive fibrosing interstitial lung diseases-subgroup analyses by interstitial lung disease diagnosis in the INBUILD trial: a randomised, double-blind, placebo-controlled, parallel-group trial. Lancet Respir Med. 2020;8(5):453-60.
- Matteson EL, Aringer M, Burmester GR, Mueller H, Moros L, Kolb M. Effect of nintedanib in patients with progressive pulmonary fibrosis associated with rheumatoid arthritis: data from the INBUILD trial. Clin Rheumatol. 2023;42(9):2311-9.
- Solomon JJ, Danoff SK, Woodhead FA, Hurwitz S, Maurer R, Glaspole I, et al. Safety, tolerability, and efficacy of pirfenidone in patients with rheumatoid arthritis-associated interstitial lung disease: a randomised, double-blind, placebo-controlled, phase 2 study. Lancet Respir Med. 2022:S2213-600(22)00260-0.
- Juge PA, Hayashi K, McDermott GC, Vanni KMM, Kowalski E, Qian G, et al. Effectiveness and tolerability of antifibrotics in rheumatoid arthritis-associated interstitial lung disease. Semin Arthritis Rheum. 2024;64:152312.
- Atienza-Mateo B, Serrano-Combarro A, Loarce Martos J, Vegas-Revenga N, Martín López M, Castañeda S, et al. Real-world evidence of the antifibrotic nintedanib in rheumatoid arthritis-interstitial lung disease. National multicenter study of 74 patients. Semin Arthritis Rheum. 2025;72:152710.
- Narváez J, Aguilar-Coll M, Roig-Kim M, Palacios-Olid J, Maymó-Paituvi P, de Daniel-Bisbe L, et al. Efficacy, safety, and tolerability of antifibrotic agents in rheumatoid arthritis-associated interstitial lung disease: A systematic review and meta-analysis. Autoimmun Rev. 2025;24(6):103804.
- Kremer JM, Alarcón GS, Weinblatt ME, Kaymakcian MV, Macaluso M, Cannon GW, et al. Clinical, laboratory, radiographic, and histopathologic features of methotrexate-associated lung injury in patients with rheumatoid arthritis: a multicenter study with literature review. Ann Rheum Dis. 1997;40(10):1829-37.
- Fragoulis GE, Nikiphorou E, Larsen J, Korsten P, Conway R. Methotrexate-Associated Pneumonitis and Rheumatoid Arthritis-Interstitial Lung Disease: Current Concepts for the Diagnosis and Treatment. Front Med (Lausanne). 2019;6:238.
- Kiely P, Busby AD, Nikiphorou E, Sullivan K, Walsh DA, Creamer P, et al. Is incident rheumatoid arthritis interstitial lung disease associated with methotrexate treatment? Results from a multivariate analysis in the ERAS and ERAN inception cohorts. BMJ Open. 2019;9(5):e028466.
- Juge PA, Lee JS, Lau J, Kawano-Dourado L. Methotrexate and rheumatoid arthritis associated interstitial lung disease. 2021;57(2).
- Dawson JK, Quah E, Earnshaw B, Amoasii C, Mudawi T, Spencer LG. Does methotrexate cause progressive fibrotic interstitial lung disease? A systematic review. Rheumatol Int. 2021;41(6):1055-64.
- Turesson C, Matteson EL. Management of extra-articular disease manifestations in rheumatoid arthritis. Curr Opin Rheumatol. 2004;16(3):206-11.
- Fiechtner JJ, Miller DR, Starkebaum G. Reversal of neutropenia with methotrexate treatment in patients with Felty’s syndrome. Correlation of response with neutrophil-reactive IgG. Arthritis Rheum. 1989;32(2):194-201.
- Tsuboi H, Matsumoto I, Hagiwara S, Hirota T, Takahashi H, Ebe H, et al. Effectiveness of abatacept for patients with Sjogren’s syndrome associated with rheumatoid arthritis. An open label, multicenter, one-year, prospective study: ROSE (Rheumatoid Arthritis with Orencia Trial toward Sjogren’s syndrome Endocrinopathy) trial. Mod Rheumatol. 2016:1-9.
- Gao RC, Wu ZG, Wu ZZ, Hao M, Wu GC. Frailty in rheumatoid arthritis: A systematic review and meta-analysis. Joint Bone Spine. 2022;89(4):105343.
- Sugihara T, Kawahito Y, Kaneko Y, Tanaka E, Yanai R, Yajima N, et al. Systematic review for the treatment of older rheumatoid arthritis patients informing the 2024 update of the Japan College of Rheumatology clinical practice guidelines for the management of rheumatoid arthritis. Mod Rheumatol. 2024;34(5):867-80.
- Kumar C, Kuhn M, Herrmann K, Leuchten N, Aringer M. Severe methotrexate toxicity in elderly patients under diuretics. RMD Open. 2024;10(1).
- Boers M, Hartman L, Opris-Belinski D, Bos R, Kok MR, Da Silva JA, et al. Low dose, add-on prednisolone in patients with rheumatoid arthritis aged 65+: the pragmatic randomised, double-blind placebo-controlled GLORIA trial. Ann Rheum Dis. 2022;81(7):925-36.
- Riley TR, George MD. Risk for infections with glucocorticoids and DMARDs in patients with rheumatoid arthritis. RMD Open. 2021;7(1).
- Dalal DS, Duran J, Brar T, Alqadi R, Halladay C, Lakhani A, et al. Efficacy and safety of biological agents in the older rheumatoid arthritis patients compared to Young: A systematic review and meta-analysis. Semin Arthritis Rheum. 2019;48(5):799-807.
- Kameda H, Maezawa R, Minegishi Y, Imaizumi C, Katagiri T, Ogura T. Targeting IL-6 Signaling: Safety and Effectiveness in Older Patients with Rheumatoid Arthritis. Drugs Aging. 2025;42(10):945-51.
- Forsblad D’Elia H, Larsen A, Waltbrand E, Kvist G, Mellstrom D, Saxne T, et al. Radiographic joint destruction in postmenopausal rheumatoid arthritis is strongly associated with generalised osteoporosis. Ann Rheum Dis. 2003;62(7):617-23.
- Gough AK, Lilley J, Eyre S, Holder RL, Emery P. Generalised bone loss in patients with early rheumatoid arthritis. Lancet. 1994;344(8914):23-7.
- Lems WF, Dreinhöfer KE, Bischoff-Ferrari H, Blauth M, Czerwinski E, da Silva J. EULAR/EFORT recommendations for management of patients older than 50 years with a fragility fracture and prevention of subsequent fractures. Ann Rheum Dis. 2017;76(5):802-10.
- Buckley L, Guyatt G, Fink HA, Cannon M, Grossman J, Hansen KE, et al. 2017 American College of Rheumatology Guideline for the Prevention and Treatment of Glucocorticoid-Induced Osteoporosis. Arthritis Care Res (Hoboken). 2017;69(8):1095-110.
- Broy SB, Tanner SB. Official Positions for FRAX(R) clinical regarding rheumatoid arthritis from Joint Official Positions Development Conference of the International Society for Clinical Densitometry and International Osteoporosis Foundation on FRAX(R). J Clin Densitom. 2011;14(3):184-9.
- Aletaha D, Smolen JS. The Simplified Disease Activity Index (SDAI) and Clinical Disease Activity Index (CDAI) to monitor patients in standard clinical care. Best Pract Res Clin Rheumatol. 2007;21(4):663-75.
- Felson DT, Smolen JS, Wells G, Zhang B, van Tuyl LH, Funovits J, et al. American College of Rheumatology/European League Against Rheumatism provisional definition of remission in rheumatoid arthritis for clinical trials. Arthritis Rheum. 2011;63(3):573-86.

