Riktlinjer för utredning, behandling och uppföljning av jättecellsarterit (GCA)
Sammanfattning
Arbetsgrupp på uppdrag av SRF: Carl Turesson (sammankallande), Erik Hellbacher, Karolina Larsson och Karin Wadström.
Ann Knight, Ola Börjesson och Aladdin Mohammad har deltagit i framtagande av dokumentet, men inte vid den senaste revideringen
Sammanfattning
- Diagnosen bör alltid bekräftas med en objektiv metod såsom biopsi av a temporalis och/eller bilddiagnostik, t. ex. ultraljud.
- Kortison är förstahandsbehandling vid GCA.
- Behandlingsstart får inte fördröjas, t. ex. i väntan på temporalartärbiopsi eller bilddiagnostik.
- Rekommenderad initial dos av prednisolon är 40–60 mg i 4 veckor, därefter successiv nedtrappning.
- Vid synpåverkan eller andra tecken till allvarligt kärlengagemang kan iv metylprednisolon (Solu-Medrol) 500–1000 mg x1xIII övervägas, följt av peroral behandling enligt ovan.
- Rationalen för behandling med tocilizumab eller upadacitinib vid GCA är framför allt deras steroidsparande effekt över tid.
- Tocilizumab rekommenderas som tillägg till prednisolon till patienter med återfall eller aktiv sjukdom under pågående kortisonbehandling, och som uppfyller i riktlinjerna angivna kriterier.
- Upadacitinib är också ett alternativ för denna grupp av patienter. Särskilda säkerhetsaspekter behöver beaktas.
- Tocilizumab och upadacitinib kan även övervägas vid omständigheter som innebär stor risk för allvarliga framtida biverkningar av kortison.
- Det sistnämnda gäller även patienter med nydiagnostiserad GCA med objektivt säkerställd diagnos och uttalad inflammation.
Innehåll
Bakgrund
Vaskulitsjukdomen jättecellsarterit (giant cell arteritis, GCA) drabbar stora och medelstora artärer. Arteria temporalis är den vanligast engagerade artären, därav det tidigare namnet temporalisarterit.
GCA är mycket ovanlig före 50 års ålder och flertalet som insjuknar är mellan 71-80 år. Kvinnor drabbas 2-4 ggr oftare än män. Sjukdomen har högst incidens i Skandinavien (1). Vanliga symtom är nytillkommen huvudvärk, tuggclaudicatio, synpåverkan och ömhet över temporalartärer. Blindhet är den vanligaste allvarliga organmanifestationen vid GCA (2). En betydande andel av patienterna har storkärls-engagemang, dvs. inflammation i aorta med avgångar (3, 4), och även neurologiska symtom förekommer (5). Symtom på polymyalgia reumatika (PMR), feber samt sjukdomskänsla är vanligt förekommande. Behandlingsriktlinjer för isolerad PMR omfattas inte av detta dokument.
Avsikten med dessa riktlinjer är att kortfattat sammanfatta aktuella principer för läkemedelsbehandling vid GCA baserat på den evidens som finns i litteraturen eller, i de fall sådan saknas, baserat på konsensus. För utvalda rekommendationer anges grad av evidens enligt GRADE som hög, måttlig, låg eller mycket låg evidensstyrka, där hög evidensstyrka är den högsta graden av evidens (se Appendix 1)
Riktlinjerna överensstämmer i stora drag med internationella rekommendationer, framför allt med den europeiska reumatologiorganisationen EULARs rekommendationer för handläggning av storkärlsvaskulit (6) och den brittiska reumatologiorganisationen BSRs riktlinje för diagnos och behandling av GCA (7).
Diagnostik
Diagnostiken av GCA baseras på anamnes och kliniska fynd understödda av laboratorieparametrar indikerande inflammation samt en positiv biopsi från a temporalis och/eller bilddiagnostik, t.ex. ultraljudsfynd överensstämmande med vaskulit. Vid stark klinisk misstanke får behandling inte fördröjas, utan ska initieras parallellt med utredning.
American College of Rheumatology (ACR)s klassifikationskriterier från 1990 (8) har använts för klassifikation huvudsakligen i forskningssammanhang, och är inte diagnoskriterier, men kan vara ett stöd vid diagnostik. Reviderade klassifikationskriterier har inkluderat nyare diagnostiska möjligheter t. ex. inom bilddiagnostik (9). Detta synsätt har återspeglats i senare års kliniska prövningar av behandling mot GCA.
Tabell I. ACRs klassifikationskriterier för jättecellsarterit från 1990

ACR och EULAR har gemensamt publicerat nya klassifikationskritierier för GCA (10). Dessa bygger på ett datadrivet och validerat poängsystem där olika symptom, tecken och utredningsfynd viktats. Gemensamt för de nya varianterna av kriterier är att objektiv verifiering med biopsi eller bilddiagnostik antingen är obligat (9) eller har så höga vikter att de i de flesta fall blir avgörande för klassificeringen (10). ACR/EULAR kriterierna har även klinisk vaskulitdiagnos och ålder över 50 år som obligata krav för GCA-klassifikation (10).
Tabell II. ACR/EULARs klassifikationskriterier för jättecellsarterit från 2022

Utredning av misstänkt GCA
För utredning av kraniell GCA (tidigare temporalarterit) finns nu ett accepterat nationellt vårdförlopp (VF-GCA). Här betonas vikten av initial kontakt med reumatolog för planering av utredning och behandling samt att verifikation av diagnos ska ske med biopsi av a temporalis och/eller ultraljud av a temporalis och a axillaris. Omsorgsfull och korrekt initial diagnostisk utredning besparar patienten felaktig kortisonbehandling med dess biverkningsrisker alternativt komplikationer till obehandlad vaskulitsjukdom, såsom blindhet.
För utredning vid misstanke om GCA med enbart engagemang av extra-kraniella kärl finns inte något motsvarande nationellt vårdförlopp. Även här torde tidig involvering av reumatolog och annan relevant specialistkompetens vara av stor betydelse. Enligt EULARs rekommendationer bör alla patienter med misstänkt storkärlsvaskulit remitteras till ett specialiserat team med tillgång till adekvata utredningsverktyg, inklusive bilddiagnostik (6).
Bilddiagnostik vid misstänkt GCA
Kraniell GCA
Ultraljud med doppler är ett komplement till temporalisbiopsi och kan vid typiska ultraljudsfynd i kombination med övertygande klinisk bild och inflammatoriska lab-prover ersätta biopsi (11, 12). Ultraljud av både temporalartärer och axillar-artärer rekommenderas, även om undersökning av axillära artärer bara ökar sensitiviteten något (13). Ödem i kärlväggen (icke komprimerbart halofenomen) är den typiska ultraljudsbilden vid GCA (14, 15). Falskt positiva halotecken kan uppkomma vid andra former av vaskulit, vid infektiösa tillstånd samt hos patienter med svår ateroskleros (16). Ultraljud är en icke-invasiv och ofta lättillgänglig metod, men den kräver adekvat kompetens och erfarenhet hos utövaren för att vara tillförlitlig.
Magnetresonans tomografi (MRT) av temporalisartär är ytterligare en bra metod och vid jämförelse med ultraljud har man funnit likvärdig sensitivitet (69% respektive 67%) och specificitet (båda 91%) (14). MRT ger möjlighet att samtidigt kartlägga strukturella förändringar såsom väggförtjockning och luminal stenos/ocklusion. Vid säkra fynd vid MRT kan man i vissa situationer avstå från biopsi (17). Växande erfarenhet finns nu gällande både MRT och PET-CT (baserat på teknikutveckling) som diagnostiskt verktyg vid frågeställning kraniell GCA (17). Tillgänglighet och kostnad påverkar i nuläget användandets rimlighet i relation till ultraljud. Optimalt utförs undersökning inom 72 timmar efter start glukokortikoider (gäller ultraljud, MR och PET-CT).
Extra-kraniell GCA
PET-CT är framför allt av värde vid diagnostik av storkärlsvaskulit och för differentialdiagnostik avseende malignitet och andra inflammatoriska tillstånd (18). MRT är en annan säker och ofta mer lättillgänglig metod för att diagnosticera aortit. Hittills har MRT och PET-CT visat jämförbar sensitivitet. Ny teknik där man kombinerar MRT och PET kan ge ytterligare information och är mycket lovande för framtiden. Ultraljud kan användas för undersökning av t.ex. carotis- och subclavia artärer och truncus brachiocephalicus (19, 20), men fungerar sämre för diagnostik av isolerad aortit och är en mindre tillförlitlig metod vid storkärls-GCA (21). CT och CT angiografi kan detektera strukturella förändringar förenliga med aortit, men ger inte samma diagnostiska information som PET-CT.
Bilddiagnostisk undersökning av stora kärl i den diagnostiska fasen kan vara av värde för att kartlägga storkärlsengagemang (22) och bör övervägas vid kliniska fynd talande för storkärlsengagemang tex allmänsymptom som feber och viktnedgång, eller mycket höga inflammationsparametrar samt hos patienter där man misstänker jättecellsarterit men utan patologiska fynd vid undersökning av temporalartärer.
Temporalartärsbiopsi
Biopsi är fortfarande ett viktigt alternativ i diagnostiken både som förstahandsalternativ och som komplement då bilddiagnostik ej givit konklusivt svar. Med tanke på att sjukdomen kan vara fokal/segmentell så rekommenderas en biopsilängd på minst 1cm (6, 7, 22).
Den typiska histologiska bilden är en inflammation bestående av CD4 positiva T celler och makrofager i samtliga cellager, dvs en transmural panarterit. Andra karakteristika är en uppsplittring av lamina elastica interna och en myelofibroblastisk proliferation i intiman, det senare leder till en intimaförtjockning som kan orsaka ocklusion av kärlet. I ungefär hälften av de positiva biopsierna ses typiska jätteceller.
I riktlinjerna från ACR och the Vasculitis Foundation från 2021 rekommenderar man att om möjligt ta biopsi inom två veckor efter behandlingsstart med glukokortikoider (22). Det finns dock flera studier som talar för att en biopsi senare än två veckor kan visa fynd förenliga med arterit (23-26). Vid oklar diagnos kan därför en biopsi efter även en längre tids behandling med glukokortikoider användas för att bekräfta men inte utesluta diagnos.
Uppföljning av GCA
Effekt av behandling bör i första hand baseras på klinisk utvärdering; anamnes och klinisk bedömning av eventuella GCA symptom, kombinerat med SR, CRP och blodstatus. Remission definieras som avsaknad av symptom och tecken på GCA förenad med normala laboratorieprover. Recidiv definieras som återkomst av kliniska symptom och inflammatorisk aktivitet i prover. Vid behandling med tocilizumab kan inte CRP användas som effektmått, utan den kliniska utvärderingen, eventuellt kompletterande bilddiagnostik (se nedan) samt i viss mån andra laboratorieavvikelser tydande på inflammation får vägleda, men även SR, Hb och TPK kan påverkas av tocilizumab. Det finns visst stöd för att analys av inflammatoriska biomarkörer som är helt eller delvis oberoende av IL-6, såsom S100-familjen av proteiner, pentraxin-3, serum amyloid A och osteopontin, skulle kunna vara av värde i denna situation, men det saknas i nuläget etablerade cirkulerande biomarkörer för monitorering av inflammation under tocilizumabbehandling (27-29). Även om JAK-hämmare också kan påverka CRP-nivåer via hämning av IL-6-signalering har effekten vid RA visats vara betydligt mindre uttalad än vid direkt IL-6-blockad (30), varför CRP i regel kvarstår som användbar markör för inflammatorisk aktivitet vid behandling med upadacitinib.
De rekommenderade kontrollproverna under behandling med tocilizumab eller upadacitinib vid GCA är desamma som vid behandling av RA (avseende säkerhetsaspekter, se SRFs rekommendationer, http://svenskreumatologi.se/srfs-riktlinjer/ – särskilt Rekommendation för provtagning och kontroller vid antireumatisk behandling).
Rutinmässig användning av bilddiagnostik (UL; MRT; CT och PET) för uppföljning och bedömning av sjukdomsaktivitet efter insatt behandling kan inte generellt rekommenderas, utan bör begränsas till situationer där det är indicerat utifrån den kliniska bilden, t. ex. vid klinisk misstanke om recidiv, och tidigare bilddiagnostiska fynd eller svårbedömda laboratorieparametrar (t.ex. under pågående IL-6 hämning, se ovan) (22, 31). Känd aortavidgning och annan kärlskada orsakad av GCA bör följas, t ex med CT angiografi (17).
Behandling av GCA
Behandling av GCA består i första hand av glukokortikoider, vanligen prednisolon. Därutöver kan kompletterande behandling med sjukdomsmodifierande läkemedel (disease modifying anti-rheumatic drugs, DMARDs) bli aktuell i vissa fall. Detta innefattar i första hand biologiska DMARDs (bDMARDs, i nuläget IL-6 hämmare) och målinriktade syntetiska DMARDs (targeted synthetic DMARDs, tsDMARDs, i nuläget JAK-hämmare).
Glukokortikoider
Tidig insättning av effektiv dos av glukokortikoider kan ha en skyddande effekt mot utveckling av komorbiditeter, fram för allt synpåverkan (32). Det finns inga studier avseende den ideala effektiva dosen av glukokortikoider och alla data vi idag har baseras på tidigare erfarenhet och publicerade behandlingsrekommendationer, i sin tur baserade på expertåsikter och på dessa grundade konsensusuttalanden och rekommendationer (33, 34). Den enda randomiserade studien kring dosering och nedtrappning av glukokortikoider är GiACTA studien, som studerade användning av IL-6 blockeraren tocilizumab vid GCA (35). Det finns ännu ingen långtidsuppföljning av GiACTA som tillåter definitiva slutsatser om optimal dosering.
Kortisonets biverkningar är väl kända t. ex. osteoporos och allvarliga infektioner (36, 37). Balansgången mellan kortisonets biverkningar och risken att underbehandla vaskuliten är svår. I de fall synförlust redan inträffat är denna dock i regel permanent. Det är aldrig är försvarbart att underlåta insättandet av kortison i väntan på temporalartärbiopsi eller ultraljud/MRT.
Perorala glukokortikoider:
Vid okomplicerad GCA (utan tuggklaudikatio eller synpåverkan) ges initial dos motsvarande 40-60 mg prednisolon dagligen.
Det finns inget schema för nedtrappning av glukokortikoider som passar alla patienter och alla kliniska scenarier. Baserat på publicerade data och egna erfarenheter är följande förslag på lämpliga doser av glukokortikoider vid behandling av GCA. Vi vill dock betona att en individuell bedömning ska göras beroende på patientens ålder, befintliga komorbiditeter samt t ex förekomst av synstörning, extra-kraniellt kärlengagemang osv.
Förslag kortisonnedtrappning p.o. behandling:
Före varje dossänkning kontrolleras patientens SR och CRP och återkomst av symtom efterfrågas.
- Startdos 40-60 mg prednisolon/dag i cirka 4 veckor (och normalisering av SR och CRP och förbättring av klinisk bild)
- därefter sänkning av dos med 10 mg varannan vecka till 20 mg per dag
- därefter sänkningar med 2,5 mg med 2–4 veckors mellanrum till 10 mg per dag
- Om inga tecken på recidiv inträffar, kan man därefter reducera med 1 mg var eller varannan månad
Den rekommenderade dagliga dosen av prednisolon vid ett år efter diagnosen är ≤5 mg.
Vid återkommande sjukdomssymtom, ska dosen av prednisolon ökas till senast effektiva dos.
Intravenösa glukokortikoider:
Det finns en mindre randomiserad studie med gynnsam effekt vid användning av intravenösa glukokortikoider (38). Studien som baserades på 27 individer visade att intravenös metylprednisolon i dosen 15 mg/kg i tre dagar initialt, ledde till att fler patienter i denna grupp erhöll ihållande remission (efter utsättning av prednisolon) vid vecka 78. Dessutom var kumulativ mediandos av prednisolon signifikant lägre hos iv gruppen (7860 respektive 5636 mg).
I en retrospektiv observationsstudie från Skåne jämfördes biopsipositiva GCA patienter som fått intravenös behandling (n=111) med metylprednisolon följt av per oral behandling med dem som endast erhållit per oral behandling med glukokortikoider (n=308). Studien visade inte någon signifikant skillnad i förbättring av synskärpa mellan de båda grupperna, men gruppen som fått intravenös behandling hade en signifikant högre risk att insjukna i diabetes inom ett år från diagnos (39).
Vid allvarliga ischemiska manifestationer fram för allt pågående eller hotande synpåverkan (exempelvis dubbelseende, amaurosis fugax, dimsyn, synförlust) rekommenderas insättning av metylprednisolon iv pulsbehandling 500–1000 mg/dag i tre dagar i följd. Optimal dos finns inte studerat men i retrospektiv genomgång avseende effekt på synpåverkan är 1000 mg/dag den mest använda dosen (40). 1000 mg kan därför rekommenderas i första hand, men avsteg göras beroende på klinisk situation/risk för akuta kortisonbiverkningar. Efter iv behandling rekommenderas per orala glukokortikoider i doser enligt ovan.
Om klar indikation för intravenös glukokortikoider föreligger enligt ovan skall den ges snarast möjligt men om en sådan möjlighet dröjer beroende på tillgång till resurser såsom vårdplats eller personal, rekommenderas att man ger peroral behandling i väntan på intravenös.
Tocilizumab vid GCA – evidens
Tocilizumab – en humaniserad monoklonal antikropp som binder till IL-6 receptorn- registrerades 2009 för behandling av reumatoid artrit. Tocilizumab är sedan september 2017 godkänt för behandling av GCA. Den rekommenderade dosen är 162 mg subkutant en gång per vecka i kombination med uttrappande dos av glukokortikoider.
Effekten av behandling med tocilizumab har utvärderats i två randomiserade, placebokontrollerade studier, båda med 52 veckors uppföljning, och med likartad effekt (35, 41). I fas II studien gavs tocilizumab intravenöst (41).
I fas III-studien, som innefattade sammanlagt 251 patienter och ledde fram till godkännande av tocilizumab jämfördes effekten av tocilizumab 162 mg subkutant varje eller varannan vecka med placebo (35, 42). Prednisolon gavs enligt ett nedtrappningsschema under 26 veckor (båda tocilizumab-armarna och en placeboarm) eller 52 veckor (en placeboarm). All studiepersonal var blindad för CRP, men den säkerhetsansvarige utvärderaren var informerad om SR. Andelen med persisterande remission från 12 veckor efter behandlingsstart fram till 1-årsuppföljningen var 56 % (tocilizumab varje vecka) respektive 53 % (tocilizumab varannan vecka) i behandlingsarmarna, och 14 % (prednisolon uttrappningsschema under 26 veckor) respektive 18 % (prednisolon uttrappningsschema under 52 veckor) (35).
Det fanns även signifikanta skillnader i kumulativ prednisolondos till tocilizumabs fördel i båda studierna (35, 41), och en större förbättring i patientrapporterade utfallsmått (hälsorelaterad livskvalitet mätt med SF-36, och patientens globala skattning av sjukdomsaktiviteten) hos dem som behandlats med tocilizumab i fas III-studien (35).
Studierna av tocilizumab vid GCA inkluderade såväl patienter med nydiagnostiserad sjukdom som patienter med återfall (35, 41). Alla patienter hade aktiv sjukdom vid randomiseringen. I en analys begränsad till patienter med återfall observerades signifikanta skillnader jämfört med placebo enbart i gruppen som behandlades med tocilizumab varje vecka (35). För nydiagnostiserade patienter fanns ingen motsvarande skillnad mellan doserna vid uppföljning upp till 1 år. Allvarliga händelser förekom i lägre utsträckning hos patienterna som behandlades med tocilizumab (14 % respektive 15 %) jämfört med placebo (22 % respektive 25 %) i fas III-studien (35) och inte heller vid långtidsuppföljning var allvarliga händelser överrepresenterade (43).
Sammanfattningsvis ger behandling med tocilizumab samtidigt med prednisolon (initialdos prednisolon vid tocilizumab-start i GiACTA studien var 20–60 mg) en högre sannolikhet att uppnå persisterande remission (måttlig evidensstyrka) och en lägre kumulativ prednisolondos (måttlig evidensstyrka). Det finns begränsade data om säkerhet vid behandling med tocilizumab vid GCA. Tillgängliga data från kliniska prövningar tyder inte på någon ökad risk för allvarliga händelser.
Deltagarna i GiACTA-studien hade en GCA-diagnos som bekräftats med biopsi eller bilddiagnostik av stora kärl. Det finns begränsat med data om behandling med tocilizumab av patienter med jättecellsarterit som diagnostiserats enbart på basen av ultraljudsundersökning av kraniala kärl (44), och inga kontrollerade studier av en sådan patientpopulation. Sådan behandling baseras huvudsakligen på klinisk erfarenhet och konsensus.
Det finns begränsat med publicerade data för kombinationsbehandling med metotrexat och tocilizumab vid GCA. I en observationsstudie från Spanien noterades likartad förbättring vid tocilizumab i monoterapi och i kombination med andra DMARDs (huvudsakligen metotrexat), men fler i långtidsremission efter 1 år vid kombinationsbehandling (45). En observationsstudie av patienter med GCA-associerad aortit indikerade fler utan aktiv inflammation enligt bilddiagnostik efter behandling med tocilizumab och metotrexat jämfört med tocilizumab i monoterapi (46).
Även sarilumab har utvärderats för behandling av GCA i en randomiserad kontrollerad fas III studier (47). Studien fick dock avbrytas på grund av långsam rekrytering under pandemin med COVID-19, och inkluderade endast 83 av planerade 360 patienter. Tillgängliga data är förenliga med tidigare erfarenheter av IL-6 hämning vid GCA, men studien är av otillräcklig storlek för säkra slutsatser.
Tocilizumab vid GCA – långtidsuppföljning
Långtidsuppföljning av fas III studien GiACTA i upp till 3 år har rapporterats (43, 48). Mindre än hälften av patienterna kunde bibehålla remission under 2 år efter utsättning av all behandling (43). Återinsättning av tocilizumab vid recidiv gav i flertalet fall ny behandlingsrespons. Det kvarstod en betydande skillnad i kumulativ kortisondos, med lägre doser hos dem som behandlats initialt med tocilizumab, framför allt bland dem som erhållit tocilizumab en gång per vecka (48). Risken för återfall under 3-årsperioden var signifikant lägre jämfört med placebo hos dem som behandlats med tocilizumab varje vecka, men inte i gruppen som fått tocilizumab varannan vecka (48).
Vid långtidsuppföljning av patienter som behandlats med tocilizumab intravenöst i den placebokontrollerade studien fann man att recidiv förekom hos 8/17 patienter som avslutat behandlingen efter 1 år när de var i remission (49). Patienterna som recidiverade var yngre och hade kvarvarande kärlinflammation påvisat med MR (49).
En observationsstudie av 114 patienter med GCA som behandlats med tocilizumab i USA indikerade en kumulativ risk för återfall på över 50% vid uppföljning i minst ett år efter avslutad behandling (50).
Upadacitinib vid GCA - evidens
Upadacitinib är ett tsDMARD för oralt bruk av klassen januskinas (JAK)-hämmare, med huvudsaklig effekt på JAK1. Upadacitinib blev tillgängligt i Sverige under 2020, och godkänt för behandling av jättecellsarterit i april 2025. Den rekommenderade dosen är 15 mg en gång dagligen i kombination med uttrappande dos av glukokortikoider.
JAK-hämmare reglerar många immunologiska processer, inklusive Th1-celler. Det finns även data för andra JAK-hämmare än upadacitinib vid GCA: från djurmodeller (51) samt okontrollerade studier av svårbehandlade patienter (52). En sammanställning av 15 svenska GCA-patienter som behandlats med JAK-hämmare (baricitinib eller tofacitinib) indikerade god kortisonsparande effekt och låg risk för återfall under behandlingen (53).
Till grund för godkännandet av upadacitinib för behandling av GCA låg en placebokontrollerad, randomiserad fas III-studie (SELECT-GCA) (54). Studien innefattade 428 patienter med nydiagnostiserad eller recidiverande aktiv GCA, där diagnosen verifierats med biopsi eller bilddiagnostik (inklusive ultraljud). Man undersökte behandling med upadacitinib i doserna 15 mg eller 7.5 mg dagligen, tillsammans med glukokortikoider som trappades ned under 26 veckor. Detta jämfördes med placebobehandling tillsammans med glukokortikoider med långsammare nedtrappning, under 52 veckor.
En signifikant skillnad jämfört med placebo uppnåddes för gruppen som behandlades med 15 mg upadacitinib, där 46% var i persisterande remission från vecka 12 till vecka 52 efter behandlingsstart, mot 29% i placebogruppen. Det fanns även signifikanta skillnader avseende persisterande komplett remission (inklusive normaliserade CRP och SR), patientrapporterade utfallsmått och kumulativ glukokortikoiddos.
Allvarliga händelser i SELECT-GCA studien rapporterades i högre andel bland patienter i placebogruppen jämfört med dem som behandlats med upadacitinib. Det gällde framför allt allvarliga infektioner (12.7% vid placebo jämfört med 7.9% vid upadacitinib 15 mg), sannolikt pga den större exponeringen för glukokortikoider i placebogruppen. Man noterade dock numeriskt högre förekomst av herpes zoster och venös tromboembolism, men ingen skillnad för allvarliga kardiovaskulära händelser eller maligniteter, bland dem som behandlats med upadacitinib 15 mg.
Preliminära resultat av 2-årsuppföljning i SELECT-GCA studien har rapporterats i abstractform (55). Dessa indikerar persisterande effekt bland patienter som kvarstår på upadacitinib, men recidiv hos mer än 50% av dem som efter att ha uppnått remission randomiserades till utsättning av upadacitinib. Avseende säkerhetsdata var mönstren oförändrade jämfört med det första året, med fortsatt ingen ökad förekomst av allvarliga kardiovaskulära händelser eller maligniteter bland patienter i studien som behandlats med upadacitinib.
Sammanfattningsvis ger behandling med upadacitinib i godkänd dos tillsammans med prednisolon (initialdos prednisolon vid upadacitinib-start i SELECT-GCA-studien var 20–60 mg) en högre sannolikhet att uppnå persisterande remission (måttlig evidensstyrka) och en lägre kumulativ prednisolondos (måttlig evidensstyrka). Förutom de begränsade säkerhetsdata från behandling av patienter med GCA som finns tillgängliga behöver annan säkerhetsinformation om upadacitinib och andra JAK-hämmare beaktas, särskilt från en säkerhetsstudie av äldre patienter med reumatoid artrit (RA) och riskfaktorer för kardiovaskulär sjukdom (56). Den sistnämnda indikerade högre risk för allvarliga kardiovaskulära händelser och malignitet för JAK-hämmaren tofacitinib jämfört med TNF-hämmare. Post hoc analyser påvisade framför allt skillnader bland dem med tidigare dokumenterad kardiovaskulär sjukdom (57), och bland rökare (58, 59). Det finns även en dokumenterat ökad risk för venös tromboembolism för JAK-hämmare jämfört med TNF-hämmare vid behandling av RA (60).
Baserat på detta har den Europeiska läkemedelsmyndigheten EMA i ett utlåtande 2022 rekommenderat att JAK-hämmare enbart bör användas då inga andra alternativ är lämpliga för: a) patienter som är 65 år eller äldre; b) nuvarande eller tidigare rökare; c) andra kardiovaskulära riskfaktorer; d) andra riskfaktorer för malignitet (61). Därutöver skall JAK-hämmare användas med försiktighet hos patienter med riskfaktorer för venös tromboembolism.
Det bör understrykas att antalet godkända alternativ när det gäller behandling med b/tsDMARDs är större vid RA än vid GCA, och att potentiella risker vid behandling med upadacitinib mot GCA även får vägas mot riskerna med långvarig glukokortikoidbehandling.
B/tsDMARD behandling vid GCA - rekommendation
Behandling av GCA med tocilizumab eller upadacitinib ska hanteras av specialist i reumatologi.
Indikationerna för dessa läkemedel innefattar inte någon begränsning av vilka patienter som är aktuella för behandling. Avgränsningen av lämpliga patienter baseras istället på tillgänglig evidens, inklusive säkerhetsdata, samt på konsensus.
Tocilizumab rekommenderas som tillägg till behandling med prednisolon hos patienter som uppfyller samtliga nedanstående kriterier:
- Jättecellsarterit som någon gång verifierats med biopsi eller med bilddiagnostisk undersökning (MRT, CT eller CT-angio av stora kärl, eller ultraljud av temporal/axillarartärer)
- Klinisk försämring under glukokortikoidbehandling eller återfall efter avslutad behandling med glukokortikoider
- Kliniskt aktiv jättecellsarterit
- Aktuell förhöjning av CRP och SR
- Tydliga bieffekter av given glukokortikoidbehandling, eller stor risk för sådana bieffekter vid framtida behandling med glukokortikoider
Upadacitinib är ett alternativ till tocilizumab, särskilt i fall där det är av stor betydelse att kunna använda CRP för monitorering av sjukdomsaktivitet, t.ex. patienter med huvudsakligen storkärlsengagemang och begränsade eller inga lokala symptom eller tecken på inflammation. Baserat på säkerhetsdata från behandling med JAK-hämmare av äldre patienter med reumatoid artrit (56-59) bör annan behandling övervägas före upadacitinib till GCA-patienter med tidigare venös tromboembolism eller aterosklerotisk kardiovaskulär händelse, eller GCA-patienter som är eller har varit rökare.
Tocilizumab eller upadacitinib kan även övervägas som tillägg till behandling med glukokortikoider hos patienter med omständigheter som innebär en stor risk för allvarliga bieffekter vid framtida behandling med glukokortikoider (ex svårinställd diabetes, manifest osteoporos, psykisk sjukdom med försämring vid tidigare behandling med kortison eller svår instabil hjärtsjukdom). Detta gäller även nydiagnostiserade patienter med tydlig klinisk bild, laboratoriemässig inflammation och objektivt verifierad diagnos med biopsi eller bilddiagnostik.
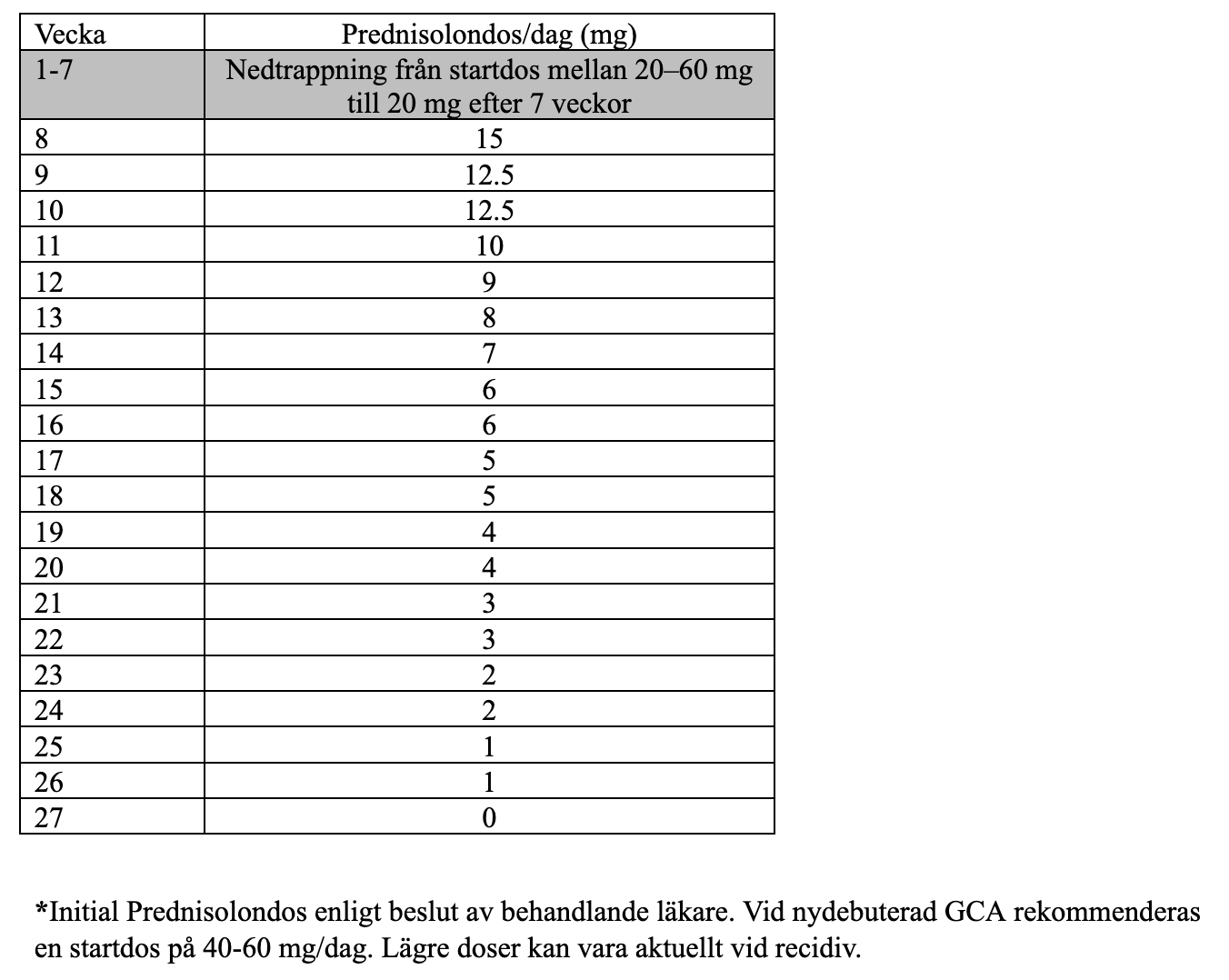
Vid samtidig behandling med tocilizumab eller upadacitinib bör glukokortikoidbehandlingen trappas ned med målet max 15 mg prednisolon dagligen vid vecka 8. Därefter bör man ha som målsättning att trappa ut behandlingen med glukokortikoider helt inom 26 veckor efter behandlingsstart, till exempel enligt det schema som användes i GiACTA-studien (Tabell III).
Det finns god evidens för effekt av tocilizumab (35) och upadacitinib (54) under 1 års behandling. Vid långvarig remission efter mer än 1 års behandling kan utsättningsförsök övervägas. Uppföljningsdata indikerar dock en hög risk för recidiv efter utsättning av tocilizumab (43) och upadacitinib (55) efter 1 års behandling, varför längre behandling ofta kan bli aktuell. Patienterna bör följas upp hos specialist i åtminstone 6 månader efter avslutad behandling.
Successiv nedtrappning före utsättning av tocilizumab har prövats och beskrivits i observationsstudie, men det är fortfarande oklart hur och om gradvis utsättning minskar recidivrisken (62, 63).
Vid återfall bör återinsättning av tocilizumab/upadacitinib övervägas, och även då ges tillsammans med kortikosteroider, där initial steroiddos avgörs av patientens kliniska bild.
För att möjliggöra uppföljning av effekt och säkerhet hos patienter som behandlas med tocilizumab eller upadacitinib i klinisk praxis bör/ska alla patienter som sätts in på dessa läkemedel med indikationen GCA registreras och följas upp i Svensk Reumatologis Kvalitetsregister (SRQ).
Tabell III Schema för Prednisolon-uttrappning i GiACTA-studien* (35).
Andra DMARDs vid GCA
Metotrexat (MTX) har i flera mindre RCT visat viss kortisonsparande effekt; inkluderade patienter fick MTX vid förstagångsinsjuknandet i dosen 7,5–15 mg och krävde på sikt en lägre ackumulerad dos glukokortikoider jämfört med gruppen utan MTX. I en metaanalys (64) av dessa studier fann man en moderat kortisonsparande effekt och en lägre risk för återfall (låg evidensstyrka). I en nyare fall-kontrollstudie medförde tillägg av MTX till kortisonterapi en signifikant lägre risk för recidiv hos de MTX-behandlade patienterna jfr med kontrollerna, möjligen med störst nytta hos patienter med bekräftad recidivbenägenhet (65).
Preliminära data från en öppen, randomiserad jämförelse av subkutant MTX och tocilizumab vid GCA indikerade sämre effekt av MTX på flertalet utfallsmått (66).
Tillägg av MTX i behandling av GCA kan övervägas vid sena återfall utan påtaglig inflammatorisk aktivitet, eller med påtagliga steroidbiverkningar, där patienten inte uppfyller indikationerna för behandling med tocilizumab eller upadacitinib.
TNF-hämmare har studerats (infliximab, adalimumab och etanercept) men sammantaget inte visat någon övertygande effekt (67). Dessa läkemedel rekommenderas inte vid GCA
Cyklofosfamid givet intravenöst i doser 500 mg/m2 kroppsyta, alternativt 500 mg varannan vecka x 6 har vid glukokortikoidberoende och refraktär GCA rapporterats ha en signifikant steroidsparande effekt (68) och drygt 50 % -ig nivå av remissionsinduktion – användandet begränsas dock av biverkningar. Cyklofosfamid bör övervägas vid intracerebralt engagemang av storkärlssjukdom.
Azatioprin gav blygsam glukokortikoid-sparande effekt i dosen 150 mg/dag vid 52 veckor enligt RCT (med ett litet antal studerande patienter) (69) och är därför sällan använt vid GCA.
Abatacept – ett humant fusionsprotein som modifierar ko-stimulering vid antigen-presentation och därmed hämmar T-cellsaktivering. Flera experimentella studier pekar på att aktiverade T celler spelar roll i patogenesen vid GCA, och aktiverade T celler har återfunnits i artärbiopsier från GCA patienter. Abatacept har testats i en fas II studie med 49 patienter med antingen nydebuterad eller recidiverande GCA, där abatacept gavs i kombination med kortison (70). Återfallsfri överlevnad var signifikant bättre och återfallsfrekvensen lägre i abataceptgruppen. Andelen allvarliga biverkningar var densamma i bägge grupperna (70). Sammanfattningsvis tyckes tillägg av abatacept till kortisonbehandling ge lägre risk för återfall (låg evidensstyrka). Behandling med abatacept kan övervägas vid allvarlig biverkan av tocilizumab eller upadacitinib, samt när kontraindikationer för dessa läkemedel föreligger.
Sekukinumab – en monoklonal antikropp riktad mot IL-17A – har testats för behandling av GCA. Detta baseras på att ett centralt patofysiologiskt fynd vid GCA är förekomsten av IL-17 producerande Th1- och Th17-celler i inflammerade kärl. IL-17A blockering skulle därmed kunna vara en terapeutisk möjlighet för behandling av GCA. Detta har undersökts i en dubbelblind randomiserad placebokontrollerad fas II studie som innefattade 52 patienter, med positiva resultat (71). En fas III uppnådde enligt preliminära uppgifter inte sitt primära utfallsmått (72).
Adjuvant behandling vid GCA
Då behandling med glukokortikoider riskerar att orsaka eller försämra osteoporos rekommenderas förebyggande behandling med calcium + D-vitamin till alla och i regel bisfosfonat eller annan anti-resorptiv terapi utifrån övriga riskfaktorer. Var god se även Läkemedelverkets behandlingsrekommendation för osteoporos (Läkemedel vid osteoporos för att förhindra benskörhetsfrakturer – behandlingsrekommendation | Läkemedelsverket (lakemedelsverket.se)), Socialstyrelsens nationella riktlinjer för diagnostik och behandling av osteoporos, Nationella riktlinjer för rörelseorganens sjukdomar – stöd för styrning och ledning (Nationella riktlinjer för rörelseorganens sjukdomar – Socialstyrelsen) EULARs rekommendationer för prevention och handläggning av osteoporotiska frakturer från 2016 (73) samt ACRs rekommendationer för prevention och behandling av kortisoninducerad osteoporos från 2017 (74).
Blodtryck och blodsocker bör monitoreras under behandling med glukokortikoider, speciellt under behandlingens inledande fas.
Trombocythämmare (ASA) eller antikoagulantia ska inte användas rutinmässigt vid GCA. I tidigare riktlinjer rekommenderades ASA under de initiala 3 månaderna, baserat på två retrospektiva observationsstudier (75, 76) som redovisade lägre frekvens synstörningar hos patienter som behandlades med ASA. Nu finns två nyare kohortstudier och en meta-analys (77-79) som inte konfirmerar en skyddande effekt på synen av ASA. Med beaktande av riskerna med denna terapi (t.ex. GI-blödning) avråds nu från dessa terapier om de inte är indicerade av andra skäl (ex ischemisk hjärtsjukdom eller cerebrovaskulär sjukdom).
Appendix
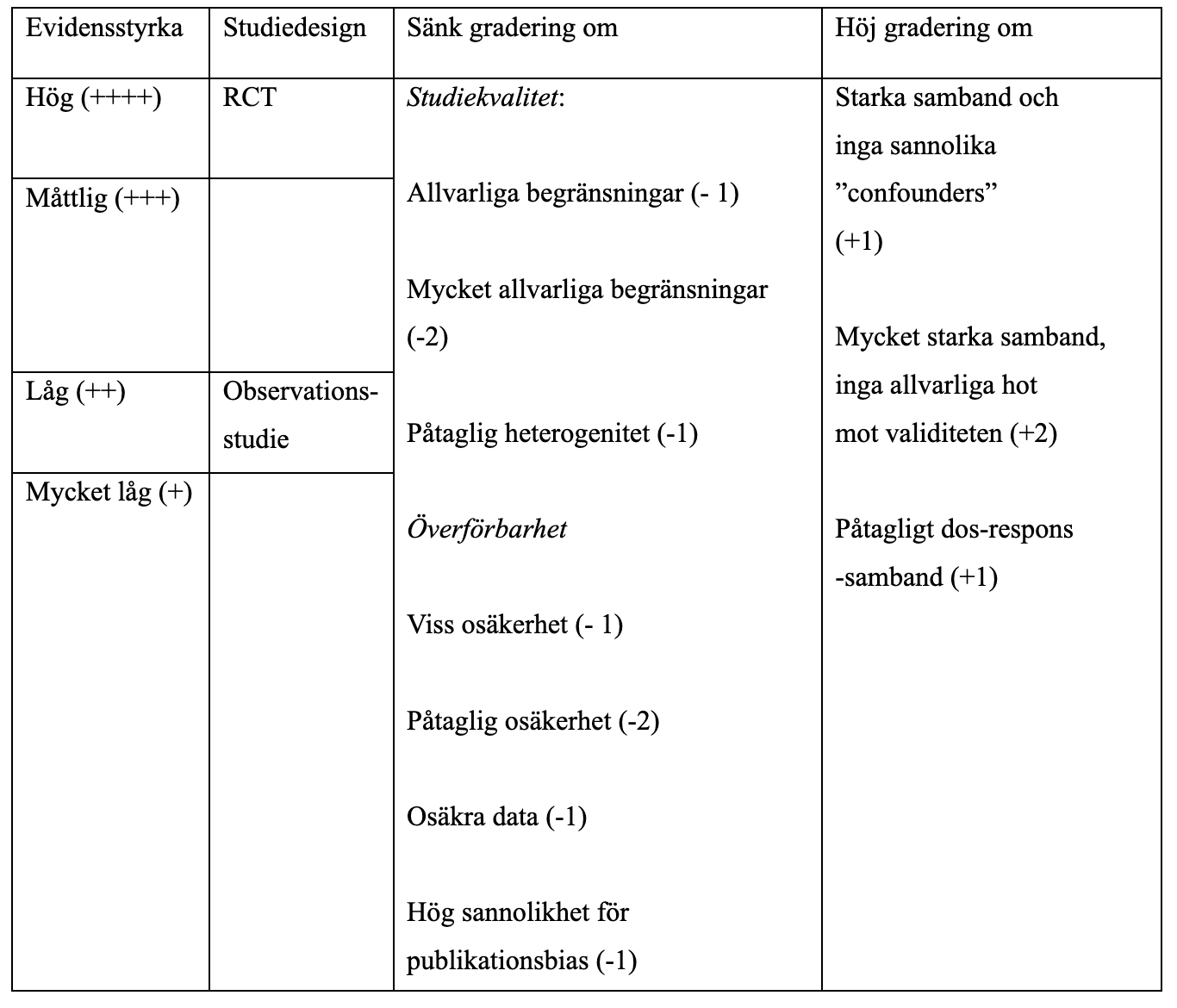
Appendix - Evidensgradering
Kvalitetsgradering av evidens enligt GRADE.
www.gradeworkinggroup.org
Referenser
Hänvisad litteratur
- Sharma A, Mohammad AJ, Turesson C. Incidence and prevalence of giant cell arteritis and polymyalgia rheumatica: A systematic literature review. Semin Arthritis Rheum. 2020;50(5):1040-8.
- Font C, Cid MC, Coll-Vinent B, Lopez-Soto A, Grau JM. Clinical features in patients with permanent visual loss due to biopsy-proven giant cell arteritis. Br J Rheumatol. 1997;36(2):251-4.
- Nuenninghoff DM, Hunder GG, Christianson TJ, McClelland RL, Matteson EL. Incidence and predictors of large-artery complication (aortic aneurysm, aortic dissection, and/or large-artery stenosis) in patients with giant cell arteritis: a population-based study over 50 years. Arthritis Rheum. 2003;48(12):3522-31.
- van der Geest KSM, Sandovici M, Bley TA, Stone JR, Slart R, Brouwer E. Large vessel giant cell arteritis. Lancet Rheumatol. 2024;6(6):e397-e408.
- Caselli RJ, Hunder GG. Neurologic complications of giant cell (temporal) arteritis. Semin Neurol. 1994;14(4):349-53.
- Hellmich B, Agueda A, Monti S, Buttgereit F, de Boysson H, Brouwer E, et al. 2018 Update of the EULAR recommendations for the management of large vessel vasculitis. Ann Rheum Dis. 2020;79(1):19-30.
- Mackie SL, Dejaco C, Appenzeller S, Camellino D, Duftner C, Gonzalez-Chiappe S, et al. British Society for Rheumatology guideline on diagnosis and treatment of giant cell arteritis: executive summary. Rheumatology (Oxford). 2020;59(3):487-94.
- Hunder GG, Bloch DA, Michel BA, Stevens MB, Arend WP, Calabrese LH, et al. The American College of Rheumatology 1990 criteria for the classification of giant cell arteritis. Arthritis Rheum. 1990;33(8):1122-8.
- Dejaco C, Duftner C, Buttgereit F, Matteson EL, Dasgupta B. The spectrum of giant cell arteritis and polymyalgia rheumatica: revisiting the concept of the disease. Rheumatology (Oxford). 2017;56(4):506-15.
- Ponte C, Grayson PC, Robson JC, Suppiah R, Gribbons KB, Judge A, et al. 2022 American College of Rheumatology/EULAR classification criteria for giant cell arteritis. Ann Rheum Dis. 2022;81(12):1647-53.
- Luqmani R, Lee E, Singh S, Gillett M, Schmidt WA, Bradburn M, et al. The Role of Ultrasound Compared to Biopsy of Temporal Arteries in the Diagnosis and Treatment of Giant Cell Arteritis (TABUL): a diagnostic accuracy and cost-effectiveness study. Health Technol Assess. 2016;20(90):1-238.
- Rubenstein E, Maldini C, Gonzalez-Chiappe S, Chevret S, Mahr A. Sensitivity of temporal artery biopsy in the diagnosis of giant cell arteritis: a systematic literature review and meta-analysis. Rheumatology (Oxford). 2020;59(5):1011-20.
- Diamantopoulos AP, Haugeberg G, Hetland H, Soldal DM, Bie R, Myklebust G. Diagnostic value of color Doppler ultrasonography of temporal arteries and large vessels in giant cell arteritis: a consecutive case series. Arthritis Care Res (Hoboken). 2014;66(1):113-9.
- Bley TA, Reinhard M, Hauenstein C, Markl M, Warnatz K, Hetzel A, et al. Comparison of duplex sonography and high-resolution magnetic resonance imaging in the diagnosis of giant cell (temporal) arteritis. Arthritis Rheum. 2008;58(8):2574-8.
- Schmidt WA, Kraft HE, Vorpahl K, Volker L, Gromnica-Ihle EJ. Color duplex ultrasonography in the diagnosis of temporal arteritis. N Engl J Med. 1997;337(19):1336-42.
- Nesher G, Shemesh D, Mates M, Sonnenblick M, Abramowitz HB. The predictive value of the halo sign in color Doppler ultrasonography of the temporal arteries for diagnosing giant cell arteritis. J Rheumatol. 2002;29(6):1224-6.
- Dejaco C, Ramiro S, Bond M, Bosch P, Ponte C, Mackie SL, et al. EULAR recommendations for the use of imaging in large vessel vasculitis in clinical practice: 2023 update. Ann Rheum Dis. 2024;83(6):741-51.
- Soussan M, Nicolas P, Schramm C, Katsahian S, Pop G, Fain O, et al. Management of large-vessel vasculitis with FDG-PET: a systematic literature review and meta-analysis. Medicine (Baltimore). 2015;94(14):e622.
- Bull Haaversen AC, Brekke LK, Kermani TA, Molberg Ø, Diamantopoulos AP. Extended ultrasound examination identifies more large vessel involvement in patients with giant cell arteritis. Rheumatology (Oxford). 2023;62(5):1887-94.
- Skoog J, Svensson C, Eriksson P, Sjöwall C, Zachrisson H. High-frequency ultrasound with superb microvascular imaging: a potential tool for ultrasound assessment in patients with giant cell arteritis. Front Med (Lausanne). 2024;11:1431385.
- Versari A, Pipitone N, Casali M, Jamar F, Pazzola G. Use of imaging techniques in large vessel vasculitis and related conditions. Q J Nucl Med Mol Imaging. 2018;62(1):34-9.
- Maz M, Chung SA, Abril A, Langford CA, Gorelik M, Guyatt G, et al. 2021 American College of Rheumatology/Vasculitis Foundation Guideline for the Management of Giant Cell Arteritis and Takayasu Arteritis. Arthritis Rheum. 2021;73(8):1349-65.
- Achkar AA, Lie JT, Hunder GG, O’Fallon WM, Gabriel SE. How does previous corticosteroid treatment affect the biopsy findings in giant cell (temporal) arteritis? Ann Intern Med. 1994;120(12):987-92.
- Maleszewski JJ, Younge BR, Fritzlen JT, Hunder GG, Goronzy JJ, Warrington KJ, et al. Clinical and pathological evolution of giant cell arteritis: a prospective study of follow-up temporal artery biopsies in 40 treated patients. Mod Pathol. 2017;30(6):788-96.
- Narváez J, Bernad B, Roig-Vilaseca D, García-Gómez C, Gómez-Vaquero C, Juanola X, et al. Influence of previous corticosteroid therapy on temporal artery biopsy yield in giant cell arteritis. Semin Arthritis Rheum. 2007;37(1):13-9.
- Jakobsson K, Jacobsson L, Mohammad AJ, Nilsson J, Warrington K, Matteson EL, et al. The effect of clinical features and glucocorticoids on biopsy findings in giant cell arteritis. BMC Musculoskelet Disord. 2016;17(1):363.
- Tombetti E, Hysa E, Mason JC, Cimmino MA, Camellino D. Blood Biomarkers for Monitoring and Prognosis of Large Vessel Vasculitides. Curr Rheumatol Rep. 2021;23(3):17.
- Farina N, Tomelleri A, Campochiaro C, Dagna L. Giant cell arteritis: Update on clinical manifestations, diagnosis, and management. Eur J Intern Med. 2023;107:17-26.
- Benucci M, Di Girolamo I, Di Girolamo A, Gobbi FL, Damiani A, Guiducci S, et al. Predictive biomarkers of response to tocilizumab in giant cell arteritis (GCA): correlations with imaging activity. Immunol Res. 2024;72(5):1154-60.
- Padula AS, Pappas DA, Fiore S, Blachley TS, Ford K, Emeanuru K, et al. The effect of targeted rheumatoid arthritis therapeutics on systemic inflammation and anemia: analysis of data from the CorEvitas RA registry. Arthritis Res Ther. 2022;24(1):276.
- Quinn KA, Dashora H, Novakovich E, Ahlman MA, Grayson PC. Use of 18F-fluorodeoxyglucose positron emission tomography to monitor tocilizumab effect on vascular inflammation in giant cell arteritis. Rheumatology (Oxford). 2021;60(9):4384-9.
- Ezeonyeji AN, Borg FA, Dasgupta B. Delays in recognition and management of giant cell arteritis: results from a retrospective audit. Clin Rheumatol. 2011;30(2):259-62.
- Bienvenu B, Ly KH, Lambert M, Agard C, Andre M, Benhamou Y, et al. Management of giant cell arteritis: Recommendations of the French Study Group for Large Vessel Vasculitis (GEFA). Rev Med Interne. 2016;37(3):154-65.
- Dasgupta B, Borg FA, Hassan N, Alexander L, Barraclough K, Bourke B, et al. BSR and BHPR guidelines for the management of giant cell arteritis. Rheumatology (Oxford). 2010;49(8):1594-7.
- Stone JH, Tuckwell K, Dimonaco S, Klearman M, Aringer M, Blockmans D, et al. Trial of Tocilizumab in Giant-Cell Arteritis. N Engl J Med. 2017;377(4):317-28.
- Mohammad AJ, Englund M, Turesson C, Tomasson G, Merkel PA. Rate of Comorbidities in Giant Cell Arteritis: A Population-based Study. J Rheumatol. 2017;44(1):84-90.
- Proven A, Gabriel SE, Orces C, O’Fallon WM, Hunder GG. Glucocorticoid therapy in giant cell arteritis: duration and adverse outcomes. Arthritis Rheum. 2003;49(5):703-8.
- Mazlumzadeh M, Hunder GG, Easley KA, Calamia KT, Matteson EL, Griffing WL, et al. Treatment of giant cell arteritis using induction therapy with high-dose glucocorticoids: a double-blind, placebo-controlled, randomized prospective clinical trial. Arthritis Rheum. 2006;54(10):3310-8.
- Henningson H, Hammar B, Mohammad AJ. The use of intravenous methylprednisolone in giant cell arteritis: a population-based study. Rheumatology (Oxford). 2025;64(4):2083-90.
- Chan CC, Paine M, O’Day J. Steroid management in giant cell arteritis. Br J Ophthalmol. 2001;85(9):1061-4.
- Villiger PM, Adler S, Kuchen S, Wermelinger F, Dan D, Fiege V, et al. Tocilizumab for induction and maintenance of remission in giant cell arteritis: a phase 2, randomised, double-blind, placebo-controlled trial. Lancet. 2016;387(10031):1921-7.
- Unizony SH, Dasgupta B, Fisheleva E, Rowell L, Schett G, Spiera R, et al. Design of the tocilizumab in giant cell arteritis trial. Int J Rheumatol. 2013;2013:912562.
- Stone JH, Han J, Aringer M, Blockmans D, Cid MC, Dasgupta B, et al. Long-term effect of tocilizumab in patients with giant cell arteritis: open-label extension phase of the Giant Cell Arteritis Actemra (GiACTA) trial. Lancet Rheumatol. 2021;3(5):E328-E36.
- Sebastian A, Kayani A, Prieto-Pena D, Tomelleri A, Whitlock M, Mo J, et al. Efficacy and safety of tocilizumab in giant cell arteritis: a single centre NHS experience using imaging (ultrasound and PET-CT) as a diagnostic and monitoring tool. RMD Open. 2020;6(3).
- Calderón-Goercke M, Castañeda S, Aldasoro V, Villa I, Moriano C, Romero-Yuste S, et al. Tocilizumab in refractory giant cell arteritis. Monotherapy versus combined therapy with conventional immunosuppressive drugs. Observational multicenter study of 134 patients. Rheumatology (Oxford). 2021;51(2):387-94.
- Martín-Gutiérrez A, Loricera J, Prieto-Peña D, Aldasoro V, Maiz O, de Miguel E, et al. Tocilizumab monotherapy versus combined in aortitis associated with giant cell arteritis: Factors associated with imaging remission in a multicenter open-label study of 196 patients. Semin Arthritis Rheum. 2025;75:152869.
- Schmidt WA, Dasgupta B, Sloane J, Giannelou A, Xu Y, Unizony SH, et al. A phase 3 randomized, double-blind, placebo-controlled study to evaluate the efficacy and safety of sarilumab in patients with giant cell arteritis. Arthritis Res Ther. 2023;25(1):199.
- Stone JH, Spotswood H, Unizony SH, Aringer M, Blockmans D, Brouwer E, et al. New-onset versus relapsing giant cell arteritis treated with tocilizumab: 3-year results from a randomized controlled trial and extension. Rheumatology (Oxford). 2022;61(7):2915-22.
- Adler S, Reichenbach S, Gloor A, Yerly D, Cullmann JL, Villiger PM. Risk of relapse after discontinuation of tocilizumab therapy in giant cell arteritis. Rheumatology (Oxford). 2019;58(9):1639-43.
- Samec MJ, Rakholiya J, Langenfeld H, Crowson CS, Abril A, Wang B, et al. Relapse Risk and Safety of Long-Term Tocilizumab Use Among Patients With Giant Cell Arteritis: A Single-Enterprise Cohort Study. J Rheumatol. 2023;50(10):1310-7.
- Zhang H, Watanabe R, Berry GJ, Tian L, Goronzy JJ, Weyand CM. Inhibition of JAK-STAT Signaling Suppresses Pathogenic Immune Responses in Medium and Large Vessel Vasculitis. Circulation. 2018;137(18):1934-48.
- Koster MJ, Crowson CS, Giblon RE, Jaquith JM, Duarte-García A, Matteson EL, et al. Baricitinib for relapsing giant cell arteritis: a prospective open-label 52-week pilot study. Ann Rheum Dis. 2022;81(6):861-7.
- Eriksson P, Skoglund O, Hemgren C, Sjöwall C. Clinical experience and safety of Janus kinase inhibitors in giant cell arteritis: a retrospective case series from Sweden. Front Immunol. 2023;14:1187584.
- Blockmans D, Penn SK, Setty AR, Schmidt WA, Rubbert-Roth A, Hauge EM, et al. A Phase 3 Trial of Upadacitinib for Giant-Cell Arteritis. N Engl J Med. 2025;392(20):2013-24.
- Schmidt W, Setty A, Dejaco C, Rubbert-Roth A, Cid MC, Ishii T, et al. Efficacy and Safety of Upadacitinib in Giant Cell Arteritis: 2-Year Results From the Re-Randomized, Double-Blind SELECT-GCA Phase 3 Trial (Abstract). Arthritis Rheumatol. 2025;77 https://acrabstracts.org/abstract/efficacy-and-safety-of-upadacitinib-in-giant-cell-arteritis-2-year-results-from-the-re-randomized-double-blind-select-gca-phase-3-trial/. Accessed November 25, 2025.
- Ytterberg SR, Bhatt DL, Mikuls TR, Koch GG, Fleischmann R, Rivas JL, et al. Cardiovascular and Cancer Risk with Tofacitinib in Rheumatoid Arthritis. N Engl J Med. 2022;386(4):316-26.
- Charles-Schoeman C, Buch MH, Dougados M, Bhatt DL, Giles JT, Ytterberg SR, et al. Risk of major adverse cardiovascular events with tofacitinib versus tumour necrosis factor inhibitors in patients with rheumatoid arthritis with or without a history of atherosclerotic cardiovascular disease: a post hoc analysis from ORAL Surveillance. Ann Rheum Dis. 2023;82(1):119-29.
- Curtis JR, Yamaoka K, Chen YH, Bhatt DL, Gunay LM, Sugiyama N, et al. Malignancy risk with tofacitinib versus TNF inhibitors in rheumatoid arthritis: results from the open-label, randomised controlled ORAL Surveillance trial. Ann Rheum Dis. 2023;82(3):331-43.
- Kristensen LE, Danese S, Yndestad A, Wang C, Nagy E, Modesto I, et al. Identification of two tofacitinib subpopulations with different relative risk versus TNF inhibitors: an analysis of the open label, randomised controlled study ORAL Surveillance. Ann Rheum Dis. 2023;82(7):901-10.
- Molander V, Bower H, Frisell T, Delcoigne B, Di Giuseppe D, Askling J. Venous thromboembolism with JAK inhibitors and other immune-modulatory drugs: a Swedish comparative safety study among patients with rheumatoid arthritis. Ann Rheum Dis. 2023;82(2):189-97.
- European Medical Agency. https://www.ema.europa.eu/en/medicines/human/referrals/janus-kinase-inhibitors-jaki.
- Calderón-Goercke M, Loricera J, Moriano C, Castañeda S, Narváez J, Aldasoro V, et al. Optimisation of tocilizumab therapy in giant cell arteritis. A multicentre real-life study of 471 patients. Clin Exp Rheumatol. 2023;41(4):829-36.
- Martín-Gutiérrez A, Loricera J, Aldasoro V, Maiz O, de Miguel E, Galíndez-Agirregoikoa E, et al. Relapses in giant cell arteritis treated with tocilizumab. Retrospective multicenter study of 407 patients in clinical practice. Semin Arthritis Rheum. 2025;71:152640.
- Mahr AD, Jover JA, Spiera RF, Hernandez-Garcia C, Fernandez-Gutierrez B, Lavalley MP, et al. Adjunctive methotrexate for treatment of giant cell arteritis: an individual patient data meta-analysis. Arthritis Rheum. 2007;56(8):2789-97.
- Koster MJ, Yeruva K, Crowson CS, Muratore F, Labarca C, Warrington KJ. Efficacy of Methotrexate in Real-world Management of Giant Cell Arteritis: A Case-control Study. J Rheumatol. 2019;46(5):501-8.
- Samson M, Bourredjem A, Outh R, Grobost V, Lifermann F, Direz G, et al. MEthotrexate versus TOcilizumab for treatment of Giant cell Arteritis (METOGiA trial): a multicenter, randomized, controlled trial. Arthritis Rheumatol. 2025;77:https://acrabstracts.org/abstract/methotrexate-versus-tocilizumab-for-treatment-of-giant-cell-arteritis-metogia-trial-a-multicenter-randomized-controlled-trial/. Accessed November 25, 2025.
- Samson M, Audia S, Janikashvili N, Bonnotte B. Is TNF-alpha really involved in giant cell arteritis pathogenesis? Ann Rheum Dis. 2014;73(1):e1.
- de Boysson H, Boutemy J, Creveuil C, Ollivier Y, Letellier P, Pagnoux C, et al. Is there a place for cyclophosphamide in the treatment of giant-cell arteritis? A case series and systematic review. Semin Arthritis Rheum. 2013;43(1):105-12.
- De Silva M, Hazleman BL. Azathioprine in giant cell arteritis/polymyalgia rheumatica: a double-blind study. Ann Rheum Dis. 1986;45(2):136-8.
- Langford CA, Cuthbertson D, Ytterberg SR, Khalidi N, Monach PA, Carette S, et al. A Randomized, Double-Blind Trial of Abatacept (CTLA-4Ig) for the Treatment of Giant Cell Arteritis. Arthritis Rheumatol. 2017;69(4):837-45.
- Venhoff N, Schmidt WA, Bergner R, Rech J, Unger L, Tony HP, et al. Safety and efficacy of secukinumab in patients with giant cell arteritis (TitAIN): a randomised, double-blind, placebo-controlled, phase 2 trial. Lancet Rheumatol. 2023;5(6):e341-e50.
- https://www.novartis.com/news/media-releases/novartis-provides-update-phase-iii-gcaptain-study-cosentyx-giant-cell-arteritis-gca. 2025.
- Lems WF, Dreinhöfer KE, Bischoff-Ferrari H, Blauth M, Czerwinski E, da Silva J, et al. EULAR/EFORT recommendations for management of patients older than 50 years with a fragility fracture and prevention of subsequent fractures. Ann Rheum Dis. 2017;76(5):802-10.
- Buckley L, Guyatt G, Fink HA, Cannon M, Grossman J, Hansen KE, et al. 2017 American College of Rheumatology Guideline for the Prevention and Treatment of Glucocorticoid-Induced Osteoporosis. Arthritis Care Res (Hoboken). 2017;69(8):1095-110.
- Nesher G, Berkun Y, Mates M, Baras M, Rubinow A, Sonnenblick M. Low-dose aspirin and prevention of cranial ischemic complications in giant cell arteritis. Arthritis Rheum. 2004;50(4):1332-7.
- Lee MS, Smith SD, Galor A, Hoffman GS. Antiplatelet and anticoagulant therapy in patients with giant cell arteritis. Arthritis Rheum. 2006;54(10):3306-9.
- Narvaez J, Bernad B, Gomez-Vaquero C, Garcia-Gomez C, Roig-Vilaseca D, Juanola X, et al. Impact of antiplatelet therapy in the development of severe ischemic complications and in the outcome of patients with giant cell arteritis. Clin Exp Rheumatol. 2008;26(3 Suppl 49):S57-62.
- Berger CT, Wolbers M, Meyer P, Daikeler T, Hess C. High incidence of severe ischaemic complications in patients with giant cell arteritis irrespective of platelet count and size, and platelet inhibition. Rheumatology (Oxford). 2009;48(3):258-61.
- Martinez-Taboada VM, Lopez-Hoyos M, Narvaez J, Munoz-Cacho P. Effect of antiplatelet/anticoagulant therapy on severe ischemic complications in patients with giant cell arteritis: a cumulative meta-analysis. Autoimmun Rev. 2014;13(8):788-94.

