Axial spondylartrit – riktlinjer för läkemedelsbehandling
Sammanfattning
Riktlinjer framtagna på uppdrag av Svensk Reumatologisk Förening 2026:
Helena Forsblad d’Elia, Ulf Lindström, Christos Moulatzikos, Tor Olofsson, Agnes Szentpetery, Johan K Wallman, Sara Wedrén
Sammanfattning av nyheter för 2026
Avseende axial spondylartrit (axSpA) är det enda större tillskottet i behandlingsriktlinjerna att vi avråder från dosökning av sekukinumab från 150 mg till 300 mg vid otillräcklig effekt. Bakgrunden till detta är en nyligen publicerad RCT som visat att sådan dosökning inte ger bättre effekt för patienter med ankyloserande spondylit, vilket står i kontrast med FASS texten. För icke-radiografisk axSpA har sådan dosökning inte heller tidigare rekommenderats.
I bakgrundsdokumentet lyfter vi också att nya klassifikationskriterier för axSpA med högre specificitet har presenterats, dock är dessa ännu inte publicerade.
Avseende psoriasisartrit (PsA) rekommenderas nu IL23-hämmare (guselkumab, risankizumab) respektive ustekinumab på samma nivå som en 2a TNF-hämmare, IL17-hämmare och JAK-hämmare, d.v.s. som alternativ vid behov av andra linjens b/tsDMARD (samt därefter) vid PsA.
Vid indirekta jämförelser av studieresultat har IL23-hämmare vid bio-naiv PsA en effekt på artrit som är ungefär i nivå med vad som ses för TNF-hämmare, även om head-to-head studier ännu saknas. En ny stor (n=1020) RCT har därtill påvisat en klar sjukdomsmodifierande effekt mätt med röntgen för guselkumab i relation till placebo, på ett tydligare vis än vad som varit fallet i tidigare RCTs kring IL23-hämmare vid PsA. Detta, i kombination med en växande klinisk erfarenhet av preparatgruppen utan tydliga säkerhetssignaler, motiverar den förändrade rekommendationen.
För ustekinumab, där head-to-head studier också saknas, framstår effekten vid bio-naiv PsA visserligen som något mindre än för TNF-hämmare vid indirekt jämförelse, men en sjukdomsmodifierande effekt mätt med röntgen har påvisats. Ustekinumab förefaller därtill ha en lägre risk för allvarliga infektioner än exempelvis TNF-hämmare och det finns en mångårig klinisk erfarenhet utan oroande säkerhetssignaler, vilket också vägts in i beslutet kring dess förändrade rekommendation.
Innehåll
Kloka kliniska val
Riktlinjegruppen för axial spondylartrit och psoriasisartrit föreslår följande Kloka Kliniska Val:
- Vid axial spondylartrit är det särskilt angeläget att så långt möjligt försäkra sig om att diagnosen är korrekt innan man inleder behandling med DMARD. Diagnosen skall basera sig på en sammanvägd bedömning av anamnes, kliniska fynd och undersökningsresultat. Enbart benmärgsödem på MR har låg specificitet för axial spondylartrit.
- Vid både axial spondylartrit och psoriasisartrit bör man överväga att omvärdera diagnosen vid uteblivet behandlingssvar.
- För en långsiktigt hållbar läkemedelsanvändning, bör vi i första hand förskriva läkemedel som omfattas av läkemedelsförmånen. I nuläget är sekukinumab den enda IL17-hämmaren som ingår i läkemedelsförmånen vid axial spondylartit. Vid psoriasisartrit ingår IL17-hämmare, IL23-hämmare, JAK-hämmare och IL12/23-hämmare bara i läkemedelsförmånen om TNF-hämmare haft otillräcklig effekt eller inte är lämpliga.
- Vid behandling med sekukinumab vid axial spondylartrit bör man överväga att avstå från följande åtgärder, då de ej tycks bidra till bättre effekt:
- Att vid icke-radiografisk axial spondylartrit ge initial laddningsdos (en dos per vecka under fem veckor
- Att öka dosen från 150 mg till 300 mg var 4:e vecka vid otillräcklig effekt
Bakgrund och syfte
Dessa riktlinjer är framtagna av en arbetsgrupp utsedd av Svensk Reumatologisk Förening (SRF). Avsikten är att sammanfatta aktuella principer för läkemedelsbehandling vid axSpA och PsA baserat på evidens från publicerade studier, internationella rekommendationer och i vissa fall enligt beprövad erfarenhet och konsensus. Riktlinjerna avses att uppdateras årligen. Den individuella variationen mellan patienter är betydande, och det är ofta svårt att extrapolera från kliniska studier till enskilda patienter varför det är viktigt att behandlingsbeslut individanpassas och sker i samråd med patienten. Syftet med rekommendationerna är att:
- skapa en enhetlig strategi vid användandet av främst DMARDs vid spondylartriter (i första hand axSpA och PsA).
- utgöra ett stöd för behandlande läkare och reumaenheter i olika delar av landet.
- bidra till en likartad behandling av dessa patientgrupper i hela landet
- vara underlag vid prioriteringsdiskussioner, såväl internt inom klinikerna som vid diskussioner med sjukhusledningar och regionshuvudmän.
Vid uppdatering av de aktuella riktlinjerna har internationella rekommendationer och riktlinjer beaktats.[1-5] Referenslistan innefattar nyckelreferenser men utgör inte någon fullständig sammanställning av den relevanta litteraturen.
Riktlinjer
Behandlingsriktlinjer för Axial Spondylartrit
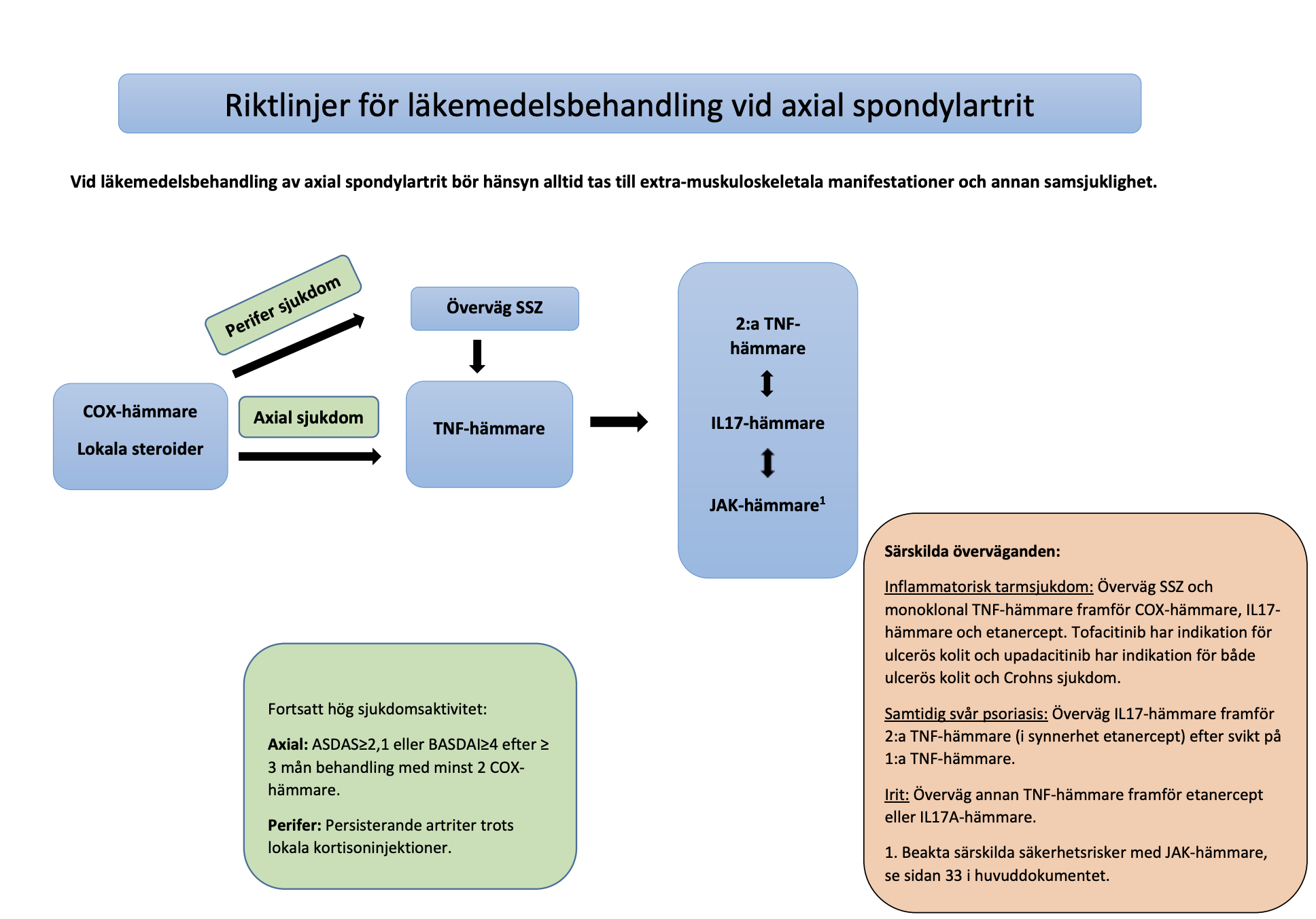
Se även flödesschemat. En mer detaljerad genomgång av bakomliggande evidens inkl. referenser finns i Bakgrundsinformation Axial spondylartrit längre ner i dokumentet.
Vid behandling av axial spondylartrit (axSpA) är det angeläget att försäkra sig om att diagnosen är korrekt. Diagnosen baserar sig på en sammanvägd bedömning av anamnes, kliniska fynd och undersökningsresultat. Enbart benmärgsödem på MR har låg specificitet för axSpA. Vid uteblivet behandlingssvar bör diagnosen omvärderas.
Diagnosen axSpA innefattar icke-radiografisk axSpA (nr-axSpA) och radiografisk axSpA (r-axSpA, även benämnt ankyloserande spondylit, AS).
Vid val av läkemedelsbehandling för axSpA bör man, utöver axial sjukdom, även ta hänsyn till förekomst och grad av perifer sjukdom (artrit, daktylit, entesit), extra-muskuloskeletala manifestationer (irit, inflammatorisk tarmsjukdom [IBD], psoriasis) och annan samsjuklighet. Inför beslut att justera anti-reumatisk terapi p.g.a. otillräcklig behandlingseffekt bör man alltid även överväga alternativa förklaringar, såsom icke-inflammatorisk värk, som ej skulle svara på sådan justering.
COX-hämmare
Första linjens farmakologiska behandling av axSpA är COX-hämmare, vilket majoriteten av patienterna med axSpA har god effekt av. Behandling med COX-hämmare ges vid behov eller kontinuerligt utifrån symtombilden. Det är inte tillräckligt klarlagt om COX-hämmare har en bromsande effekt på radiografisk progress i kotpelaren eller ej. Samma försiktighet och kontraindikationer ska beaktas som vid behandling med COX-hämmare vid andra sjukdomstillstånd.
Kortisoninjektioner
Det finns god klinisk erfarenhet av behandling med lokala kortisoninjektioner vid engagemang av perifera leder och vid sakroiliit. Vid axSpA kan därför lokala kortisoninjektioner provas.
csDMARDs
Vid persisterande/recidiverande perifer artrit kan behandling med sulfasalazin övervägas. Effekten av sulfasalazin på axiala symtom är dock liten. Effekten av metotrexat eller leflunomid vid perifer ledsjukdom vid axSpA är inte adekvat studerad och effekt på axial sjukdom saknas.
b/tsDMARDs
Vid otillräcklig effekt på axiala symptom av minst två COX-hämmare i sammanlagt tre månader eller biverkningar av COX-hämmare, bör bDMARD övervägas. Vid bristande effekt av salazopyrin på perifera artriter bör man också överväga bDMARD.
Beslutet om behandling baseras på klinisk diagnos och hög sjukdomsaktivitet enligt klinisk bedömning, vilken sammanväger förekomst och grad av inflammatoriska sjukdomsuttryck (muskuloskeletala och extramuskuloskeletala), med stöd av validerat sjukdomsaktivitetsmått (i första hand ASDAS-CRP ≥2,1). Faktorer som talar för god klinisk effekt vid behandling med bDMARD är lägre ålder, kortare sjukdomsduration, CRP-stegring, högre grad av inflammatoriska ödem i sakroiliakaleder eller kotpelare på MRT samt HLA-B27-positivitet.
Val av första b/tsDMARD
Bland b/tsDMARDs rekommenderas TNF-hämmare som förstahandspreparat p.g.a. god dokumenterad effekt och lång klinisk erfarenhet. Effekten på axiala symtom bedöms likvärdig mellan de fem TNF-hämmarna, men golimumab och certolizumab ingår endast i läkemedelsförmånen när etanercept eller adalimumab inte är lämpliga.
Det är inte klarlagt om tidig behandling med TNF-hämmare förhindrar utveckling från nr-axSpA till AS, men observationsstudier talar för att behandling med TNF-hämmare kan bromsa utveckling av strukturella förändringar i sakroiliakalederna och kotpelaren.
Vid svikt på första b/tsDMARD
Vid svikt på en första TNF-hämmare kan en annan TNF-hämmare, en IL17-hämmare eller en JAK-hämmare användas. Effekten av dessa tre preparatgrupper är likartad på axiala symptom bland bio-naiva patienter med axSpA, men otillräckligt jämförd bland bio-erfarna patienter. Vid upprepad behandlingssvikt på en preparattyp rekommenderar vi att byta till preparat med annan verkningsmekanism.
Hos patienter med IBD rekommenderas inte behandling med IL17-hämmare eller etanercept, och vid iriter rekommenderas i första hand TNF-hämmare av monoklonal antikroppstyp (d.v.s. ej etanercept).
Vid samtidig svår psoriasis, överväg behandling med IL17-hämmare framför en andra TNF-hämmare (i synnerhet etanercept) efter svikt på en första TNF-hämmare.
Tre IL17-hämmare är godkända för behandling av axSpA, men enbart sekukinumab ingår i läkemedelsförmånen. Radiografisk progress i kotpelaren har visats vara likvärdig vid behandling med TNF-hämmare och IL17A-hämmare. Vid otillräcklig effekt av 150mg sekukinumab ger dosökning till 300mg inte en bättre effekt.
JAK-hämmarna upadacitinib och tofacitinib är godkända för behandling av AS, och upadacitinib även för nr-axSpA. För säkerhetsaspekter med JAK-hämmarbehandling se sidan 33 i huvuddokumentet
Kombination av csDMARD och b/tsDMARD
Det finns inget entydigt stöd för att kombinationsbehandling med csDMARD medför ytterligare behandlingseffekt eller bidrar till förbättrad läkemedelsöverlevnad av b/tsDMARDs vid axSpA.
Behandlingsutvärdering
Utvärdering av behandlingseffekt bör göras efter 3-6 månader och utsättning bör ske om patienten inte svarat på behandlingen. För rekommendation kring utvärderingsinstrument, se sidan 13 samt tabell 4 och 5.
Behandlingslängd/dosreduktion av bDMARD
Flertalet studier har visat att utsättande av bDMARD hos axSpA patienter med inaktiv sjukdom leder till recidiv med hög sjukdomsaktivitet hos en majoritet av patienterna. Dosreduktion/förlängt behandlingsintervall fungerar däremot ofta väl och kan övervägas för patienter som uppnått bestående (minst sex månader) inaktiv sjukdom och där prognosen bedöms som god.
Bakgrundsinformation Axial Spondylartrit
Bakgrundsinformation Axial Spondylartrit
Axial spondylartrit (axSpA) kan ses som ett sjukdomsspektrum som innefattar ankyloserande spondylit (AS), radiografisk axial SpA (r-axSpA) och icke-radiografisk axial SpA (nr-axSpA). Ankyloserande spondylit klassificeras enligt modifierade New York kriterier (Tabell 2),[6] och r-axSpA och nr-axSpA enligt Assessments in SpondyloArthritis International Society´s (ASAS) kriterier (Figur 1).[7] Flertalet patienter med axSpA med radiografisk sakroiliit uppfyller både kriterier för AS och för r-axSpA, vilket medför att begreppen kan betraktas som utbytbara.[8] Nya klassifikationskriterier enligt ASAS och Spondyloarthritis Research and Treatment Network (SPARTAN) med högre specificitet för axSpA har nyligen presenterats men är ännu ej publicerade.
AS har i västvärlden en prevalens på cirka 0,1-0,2 % och cirka 70% är män. Flertalet patienter har symtomdebut före 30 års ålder. I många fall tar det flera år innan diagnos ställs. Epidemiologiska studier tyder på att nr-axSpA kan ha minst lika hög prevalens som AS, men med en mer jämn könsfördelning och är inte sällan förenat med psoriasis eller inflammatorisk tarmsjukdom.[9-11]
Det är viktigt att betona att den kliniska diagnosen inte grundas på klassifikationskriterier eller förekomst av enskilda testresultat, kliniska uppgifter eller fynd, utan bygger på en samlad bedömning av all relevant information. Utförande av t.ex. magnetisk resonanstomografi (MRT) av sakroiliakalederna bör således endast göras när det föreligger klinisk misstanke om axSpA, för att undvika låg specificitet, och datortomografi (DT) (ej röntgen) endast vid längre symptomduration, för att undvika låg sensitivitet.
För utredning av patienter på klinisk misstanke om axSpA rekommenderas i första hand MRT av sakroiliakalederna. Definition på signifikanta ödem i sakroiliakalederna beskrevs tidigare som förekomst av två eller flera separata ödem i samma bildsnitt eller ett ödem som sträckte sig över minst två bildsnitt, lokaliserat subkondralt eller periartikulärt och i hög grad tydande på axSpA.[12] Falskt positiv MRT enligt denna definition har dock påvisats hos 20-40% av friska eller vid ospecifika ryggproblem.[13] I en uppdatering av definitionen för positiv MRT poängterades det kliniska sammanhanget och förekomst av strukturella förändringar såsom erosioner som stöd för en positiv MRT.[14, 15] Ett standardiserat undersökningsprotokoll av sakroiliakaleder med MRT för diagnostisering av sakroiliit har tagits fram för att optimera undersökningen. Minst fyra sekvenser rekommenderas som innefattar inflammationskänsliga, fettkänsliga och erosionskänsliga sådana, för att optimalt visualisera aktiv inflammation, strukturella skador och gränssnittet mellan ben och brosk. Protokollet skall kunna tillämpas på alla MRT-apparater.[16] ASAS har även tagit fram rekommendationer för vilka kliniska uppgifter som bör finnas vid remittering för bilddiagnostik och vad radiologen bör rapportera i svaret.[17, 18] Området är under utveckling och uppdatering av definition för positiv MRT och klassifikationskriterier för axSpA har nyligen presenterats men är ännu ej publicerade.
Negativa prognostiska faktorer för progress av AS-relaterade radiografiska förändringar i kotpelaren, mätt med modifierade Stoke Ankylosing Spondylitis Spine Score (mSASSS) [19] är bland annat manligt kön, sedan tidigare förekomst av radiografiska förändringar, rökning, förhöjd sjukdomsaktivitet, laboratoriemässig inflammatorisk aktivitet, inflammatoriska förändringar på MR av kotpelaren och övervikt.[20-23] De strukturella förändringarna i kotpelaren kan påverka ryggrörligheten och den fysiska funktionen, vilket även påverkar livskvaliteten.[24]
Flertalet studier rapporterar att 10-40% av patienter med nr-axSpA progredierar till r-axSpA under en period på 2-10 år.[25] I en nyligen publicerad 10-årsuppföljning av en kohort av patienter med axSpA (< 3 års duration) var progressionstakten låg; <10% progredierade från nr- till r-axSpA (mod NY kriterier). Om hänsyn togs till exponering för TNF-inhibitorer progredierade <5%.[26] Vid förekomst av signifikanta benmärgsödem på MRT,[26-28] HLA-B27 [26-28], förhöjd CRP eller ASDAS [26, 29] ökar risken avsevärt. I en studie visade förekomst av kronisk inflammatorisk ryggsmärta i kombination med kraftig inflammation i sakroiliakalederna med MRT och HLA-B27 ett positivt prediktivt värde på 92% för att utveckla AS vid åtta års uppföljning.[27].
Icke biologiska läkemedel
COX-hämmare
Den basala farmakologiska behandlingen av axSpA är COX-hämmare. Det finns en betydande dokumentation avseende symtomlindrande effekt och säkerhet i korttidsstudier.[30, 31] Det finns ingen tydlig evidens för att rekommendera någon specifik COX-hämmare framför övriga. En RCT av diklofenak jämfört med placebo tydde inte på att kontinuerlig medicinering med diklofenak bromsade syndesmofytutveckling vid AS,[32] medan en RCT av kontinuerlig celecoxib medicinering jämfört med medicinering vid behov talade för en sådan effekt.[33] I en posthoc-analys av celecoxibstudien sågs en mer påtaglig bromsande radiografisk effekt hos AS-patienter med förhöjd SR eller CRP,[34] vilket även en observationsstudie talat för.[35] En annan RCT som jämförde tillägg med kontinuerligt celecoxib till golimumab mot golimumab i monoterapi hos patienter med riskfaktorer för radiografisk progression fann ingen signifikant skillnad i syndesmofytutveckling över 2 år.[36] Sammantaget behövs mer data för att klarlägga om COX-hämmare har bromsande effekt på radiografisk progress eller ej.
Det finns inga placebokontrollerade studier som specifikt utvärderat effekten av COX-hämmare vid nr-axSpA, men i en jämförande studie av naproxen vs. naproxen i kombination med infliximab sågs att 37% uppnådde partiell remission i behandlingsarmen som enbart fick naproxen jämfört med 60% i kombinationsarmen, vilket visar att COX-hämmare kan vara tillräcklig behandling för många patienter.[37, 38]
Få studier belyser säkerhet vid långtidsbehandling med COX-hämmare vid axSpA men det finns en stor klinisk erfarenhet.[30, 31, 39] Samma försiktighet och kontraindikationer ska beaktas som vid behandling med COX-hämmare vid andra sjukdomstillstånd.
Kortison
Det finns god klinisk erfarenhet av behandling med lokala kortisoninjektioner vid engagemang av perifera leder och sakroiliakaleder.[1]
Behandling med peroralt kortison i hög dos eller under lång tid rekommenderas inte p.g.a. biverkningsriskerna, vilket är i överenstämmelse med internationella behandlingsrekommendationer.[1] Detta trots att man i en liten, två veckors, placebokontrollerad RCT av AS-patienter med hög sjukdomsaktivitet såg signifikant minskning av BASDAI vid behandling med prednisolon 50 mg/dag jämfört med placebo. Det primära utfallsmåttet 50% förbättring av BASDAI (BASDAI50) uppnåddes dock inte.[40]. I en annan liten 24-veckors RCT jämfördes peroral prednisolon-behandling i en nedtrappande dos från 60 mg/dag till 5 mg/dag efter 7 veckor med placebo hos patienter med aktiv axSpA. BASDAI50 uppnåddes av signifikant fler patienter i prednisolon-gruppen jämfört med i placebo-gruppen.[41] Det saknas RCTs av peroral behandling med kortison under längre tid.
csDMARDs
Vid axSpA där perifer artrit är den dominerande sjukdomsyttringen kan behandling med sulfasalazin övervägas. Den eventuella effekten av metotrexat eller leflunomid vid perifer ledsjukdom, vid axSpA, är inte adekvat studerad.
Randomiserade kontrollerade studier av AS har visat att sulfasalazin kan ha viss effekt på den perifera ledkomponenten, men ingen eller viss effekt på det axiala engagemanget.[2, 42-44] Tre RCT av metotrexat (7,5-10 mg/v) vid AS, med totalt endast 116 patienter, ger inte tillräckligt stöd för nytta av denna behandling.[43, 45] Två mindre studier på leflunomid vid AS talar för att det saknar effekt på axial sjukdom, men en av dem antyder en effekt på perifer ledsjukdom.[46, 47]
bDMARDs
TNF-hämmare
Det finns fem godkända TNF-hämmare för behandling av axSpA – adalimumab, certolizumab , etanercept, golimumab och infliximab, varav infliximab endast har AS-indikation. Det finns inga RCTs som jämfört TNF-hämmare mot varandra vid axSpA. I en indirekt jämförelse mellan preparaten fann man dock ingen skillnad i effekt.[48] Samtliga preparat har visats ha god effekt vad gäller förbättring av inflammationsgrad, funktion och hälsorelaterad livskvalitet på patienter med hög sjukdomsaktivitet som sviktat på traditionell behandling, vid AS med en ASAS20 respons i nivån 58-61% (median för placebo: 21%) och ASAS40-respons i nivån 39-47% (median för placebo: 12%).[49-54]
Vid nr-axSpA är behandling med TNF-hämmare indicerat vid säker diagnos, hög sjukdomsaktivitet, svikt på behandling med COX-hämmare och objektiva tecken på aktiv inflammation, antingen i form av förhöjt CRP eller signifikant inflammation på MRT.[53, 55-57] Preparaten har visats ha god klinisk effekt på sjukdomsaktivitet vid nr-axSpA. Efter 12-16 veckors behandling erhölls ASAS20 respons i nivån 44-71% jämfört med placebo 31-40%, och ASAS40 respons 32-57% jämfört med placebo 15-23%.[53, 55-59]
Doseringen för infliximab har genomgående varit 5 mg/kg kroppsvikt i RCTs. Beprövad erfarenhet i Sverige talar dock för att många patienter svarar på lägre dos (3 mg/kg kroppsvikt). Vid behandling med infliximab 3 mg/kg kroppsvikt och otillräcklig effekt bör därför dosen ökas till 5 mg/kg kroppsvikt, alternativt doseringsintervallen kortas, innan behandlingsförsöket avslutas. Vid behov av dosökning av infliximab talar observationsdata från IBD för en likvärdig effekt av höjd dos respektive tätat intervall.[60] Infliximab i subkutan form har numera också indikation vid axSpA, men ingen RCT med denna beredningsform har utförts vid axSpA.
Det finns endast enstaka studier av patienter med axSpA som direkt jämfört effekten av TNF-hämmare (etanercept) gentemot csDMARD-preparat (sulfasalazin), vilka visade bättre effekt för etanercept.[61, 62] I RCTs av TNF-hämmare har samtidig behandling med metotrexat eller annat csDMARD varierat mellan 0 och ca. 40 %. Inga RCTs har utvärderat effekten av samtidigt startad behandling med csDMARD i kombination med TNF-hämmare jämfört med endast TNF-hämmare. Kombinationsbehandling med csDMARD har i vissa registerstudier, bl.a. baserat på svenska data, varit associerat med att patienterna i högre grad stått kvar på
TNF-hämmaren [63-67]. Denna association har dock inte påvisats i andra registerstudier, [68, 69] varför säkra slutsatser om huruvida kombinationsbehandling bidrar till att kvarstå längre på behandling med TNF-hämmare inte kan dras.
Placebokontrollerade studier vid axSpA löper vanligtvis över 4-6 månader, och kan därför inte förväntas påvisa en sjukdomsmodifierande effekt mätt med röntgen. Vid jämförelse av radiografisk progress hos AS-patienter, behandlade med någon av TNF-hämmarna adalimumab, etanercept och infliximab, med den hos en historisk AS-kohort fanns ingen signifikant skillnad efter 2 års uppföljning.[70-72] Observationsstudier tyder inte heller på någon tydlig effekt på gruppnivå efter kort tids behandling (<2 år) med TNF-hämmare, men indikerar en viss bromsande effekt efter längre tids behandling, vilken möjligen är kopplad till minskad inflammatorisk aktivitet.[73-80] Numbers needed to treat (NNT) för att undvika en mätbar progress är generellt hög i dessa studier,[81] men kunskapen är i nuläget otillräcklig för specifika patientgrupper, speciellt för individer med snabb progress eller kända riskfaktorer för progress, där effekten av långtidsbehandling skulle kunna vara av betydelse. RCTs som använt MRT-score som utfallsmått visar att TNF-hämmare reducerar benmärgsödem.[55-57, 82-84]
I en RCT bestående av totalt 859 bionaiva patienter med aktiv r-axSpA jämfördes radiografisk progress efter 2 år mellan en adalimumab biosimilar och IL17-hämmaren sekukinumab. Den radiografiska progressen i kotpelaren var låg under uppföljningstiden och skiljde sig inte signifikant mellan grupperna.[85]
Det är för närvarande inte klarlagt om tidig behandling med TNF-hämmare förhindrar utveckling från nr-axSpA till AS, men observationella jämförelser talar för att behandling med TNF-hämmare kan bromsa utveckling av strukturella förändringar i sakroiliakalederna.[26, 86]
IL17-hämmare
Det finns tre godkända IL17-hämmare för behandling av axSpA. Sekukinumab (Cosentyx®) och ixekizumab (Taltz®) vilka hämmar IL17 A, samt bimekizumab (Bimzelx®) som hämmar IL17 A och F). Preparaten har indikation för behandling av AS och nr-axSpA vid svikt på konventionell behandling. Vid nr-axSpA krävs enligt indikationen även objektiva tecken på inflammation i form av förhöjt CRP och/eller ödem vid MRT av sakroiliakaleder. Alla IL17-hämmare har visats ha god effekt vad gäller förbättring av inflammationsgrad, funktion och hälsorelaterad livskvalitet på patienter med hög sjukdomsaktivitet. RCTs som kunnat påvisa en sjukdomsmodifierande effekt av IL17-hämmare mätt med röntgen vid axSpA saknas. Vid jämförelse av radiografisk progress hos AS-patienter behandlade med sekukinumab med en historisk kohort av bio-naiva patienter som behandlats med COX-hämmare fanns ingen signifikant skillnad efter 2 års uppföljning.[87] De tre preparaten har dock visats reducera benmärgsödem vid MRT-undersökning.[88-91]
I en RCT jämfördes behandling med sekukinumab med en adalimumab biosimilar avseende radiografisk progress. Ingen signifikant skillnad sågs, var god se även ovan stycke.[85]
Sekukinumab har vid AS studerats i 2 indikationsgrundande RCTs, I och II, med sammantaget 590 patienter, varav 69% var TNF-hämmar-naiva.[92] I studie I administerades sekukinumab intravenöst initialt (varför resultat från denna ej rapporteras mer här) och i studie II genomgående subkutant. I studie II (n=219) var ASAS20/40 respons i sekukinumab 150 mg-gruppen 61/36% jämfört med i placebogruppen 28/11% efter 16 veckor. Effekten av sekukinumab i studie II studerades också uppdelat på TNF-hämmar-naiva och tidigare TNF-hämmar-behandlade patienter. Efter 16 veckor uppnådde 68/43% ASAS20/40 respons av TNF-hämmar-naiva patienter jämfört med placebo 31/18%, medan 50/25% uppnådde ASAS20/40 respons hos tidigare TNF-hämmar-behandlade patienter jämfört med placebo 24/0%.[93]
Vid nr-axSpA baseras indikationen för sekukinumab på en RCT med 555 patienter.[88] Studien bestod av 3 armar; sekukinumab 150 mg var 4:e vecka med laddningsdos vecka 1, 2, 3 (LD), sekukinumab 150 mg var 4:e vecka utan laddningsdos (NL) och placebo. 90% av patienterna var bio-naiva. Primärt utfallsmått var ASAS40 respons vecka 16 för LD och vecka 52 för NL. Vid 16 veckor var utfallet likartat i båda behandlingsarmarna, ASAS40 uppnåddes av 42% i LD och 42% i NL vs. 29% i placebogruppen. Vid 52 veckor var responsen 35% och 40% vs. 20% för placebo. Trots den höga behandlingseffekten i placebogruppen vecka 16 uppnåddes de primära utfallsmåtten. Studien var inte designad att visa skillnader mellan de båda behandlingsarmarna men mot bakgrund av resultaten kan behandlande reumatolog överväga att avstå laddningsdos (vilket skiljer sig från dosering enligt FASS).
Sekukinumab 150 mg var 4:e vecka är rekommenderad dos vid axSpA, men för AS inbegriper indikationen även doseringen 300 mg var 4:e vecka som alternativ vid otillräckligt behandlingssvar. I en RCT med 322 patienter randomiserades patienter med AS som inte uppnått stabilt inaktiv sjukdom (ASDAS <1.3) efter 16 veckor på 150 mg var 4:e vecka till fortsatt samma dos eller upptrappning till 300 mg var 4:e vecka. Efter 52 veckor sågs ingen skillnad mellan armarna (150 vs. 300 mg) avseende inaktiv sjukdom (7% vs. 9%), ASAS40 (10% vs. 8%) eller ASAS20 (19% vs. 21%).[94]
Ixekizumabs godkännande för behandling av AS, baseras på 2 RCTs med drygt 300 patienter i respektive studie.[95] I den första studien randomiserades 341 bio-naiva patienter till 4 behandlingsarmar (80 mg var 4:e respektive varannan vecka, adalimumab [jämförelsearm] och placebo). Med den godkända doseringen av ixekizumab (80mg var 4:e vecka) uppnådde 64/48% ASAS20/40 vid vecka 16, jmf med 59/36% för adalimumab och 40/18% för placebo. Behandlingseffekten för ixekizumab hos denna patientpopulation var således god och jämförbar med den man sett i tidigare studier med TNF-hämmare. I den andra studien inkluderades uteslutande patienter som inte svarat på eller haft biverkningar av TNF-hämmare, 1/3 hade provat 2 st TNF-hämmare.[89] Med den godkända doseringen av ixekizumab uppnådde 48/25% ASAS20/40 vid vecka 16, jmf med 30/13% för placebo.
Vid nr-axSpA är ixekizumab studerat i en RCT med 303 bio-naiva patienter som randomiserades till 2 behandlingsarmar (80 mg var 4:e resp. varannan vecka) och placebo.[90] Med den godkända doseringen ixekizumab uppnådde 35% ASAS40 vid vecka 16, jmf med 19% för placebo, och vid 52 veckor sågs fortsatt ASAS40 respons hos 30% med ixekizumab jmf med 13% i placebogruppen.
Bimekizumab är godkänt för behandling av AS baserat på en RCT med 332 patienter.[91] Majoriteten (84%) var bio-naiva. Efter 16 veckor uppnåddes det primära utfallsmåttet ASAS20/40 hos 66/45% vs 43/22% i placebogruppen, vilket är i samma nivå som för TNF-hämmare och andra IL17-hämmare. I en separat analys av de bio-erfarna var behandlingseffekten likartad (ASAS40: 40% vs 18% i placebogruppen). Antalet bio-erfarna patienter var dock litet (n=57), varför resultatet bör tolkas med viss försiktighet.
Vid nr-axSpA är bimekizumab studerat i en RCT med 254 patienter, varav hälften fick placebo.[91] 90% var bio-naiva. Det primära utfallsmåttet ASAS20/40 uppnåddes efter 16 veckors behandling hos 69/48% vs 38/21% i placebogruppen. Effekten hos de bio-erfarna i denna studie var god (ASAS40 60% vs 12% i placebogruppen) men antalet patienter ytterst få (n=27). Behandlingseffekten för bimekizumab i denna patientgrupp är likartad den man sett för andra IL17-hämmare, subkutana TNF-hämmare och upadacitinib.
tsDMARDs
JAK-hämmare
Det finns två JAK-hämmare som är godkända för behandling av axSpA, upadacitinib (Rinvoq®) och tofacitinib (Xeljanz®). Båda preparaten har indikation för behandling av patienter med AS som sviktat på konventionell behandling, medan upadacitinib också är godkänt för nr-axSpA. Vid nr-axSpA krävs enligt indikationen även objektiva tecken på inflammation i form av förhöjt CRP och/eller ödem vid MRT av sakroiliakaleder. Preparaten har visat god effekt vad gäller förbättring av inflammationsgrad, funktion och hälsorelaterad livskvalitet på patienter med hög sjukdomsaktivitet. Upadacitinib har vid nr-axSpA visats minska benmärgsödem på MRT i kotpelare och sakroiliakaleder och tofacitinib har vid AS visats minska benmärgsödem på MRT i kotpelare jämfört med placebo.[96-99]
Upadacitinib är en hämmare av JAK1 eller JAK1/3 signalering och har studerats i 3 RCTs. I den första (fas II/III) studerades bio-naiva patienter med AS (n=187). Efter 14 veckors behandling uppnåddes ASAS20/40 av 65/52% i gruppen behandlad med upadacitinib 15 mg/dag, vilket var signifikant fler jämfört med 40/26% i placebogruppen.[96] I den andra AS-studien inkluderades endast patienter som haft otillräcklig effekt eller biverkningar av behandling med ≥1 bDMARD.[100] Majoriteten (74%) hade provat 1 TNF-hämmare. 420 patienter randomiserades 1:1 till aktiv behandling eller placebo. Vid utvärdering efter 14 veckor uppnådde 65/45% i behandlingsgruppen och 38/18% i placebogruppen ASAS20/40. Resultaten i denna studie är således, vid indirekt jämförelse, likartade med vad man tidigare sett i prövningar med bDMARDs och JAK-hämmare bland bio-naiva patienter. Den tredje studien inkluderade 314 patienter med aktiv nr-axSpA.[99] Majoriteten var bio-naiva, ca. 1/3 hade tidigare provat någon bDMARD. ASAS20/40 uppnåddes av 67/45% jämfört med 44/23% i placebogruppen i hela studiepopulationen efter 14 veckor. ASAS40-respons för bio-naiva var 51% jämfört med 33% hos de bio-erfarna. Sammantaget är dessa resultat jämförbara med liknande studier med TNF/IL17A-hämmare på denna patientgrupp.
Tofacitinib är en hämmare av JAK1 och 3 signalering med viss effekt på JAK2. Tofacitinib är godkänt för behandling av patienter med aktiv AS som haft otillräckligt behandlingssvar på konventionell behandling. Preparatet har studerats i en fas III studie med 269 patienter med AS, varav ca 80% var bio-naiva.[101] Efter 16 veckors behandling av bio-naiva patienter (n= 102) uppnådde 62/45% ASAS20/40 respons (jfr placebo 33/14%). Vad gäller bio-erfarna patienter (n=31) uppnådde 39/26% ASAS20/40 (jfr placebo 16/6.5%).
Byte av verkningsmekanism för b/tsDMARDs vid behandlingssvikt
Randomiserade studier som stödjer byte av verkningsmekanism vid behandlingssvikt saknas. Vid en indirekt jämförelse av randomiserade studier på AS-patienter som sviktat på minst en biologisk behandling uppnåddes ASAS40 respons av 26/6,5% med tofacitinib/placebo, 45/18% med upadacitinib/placebo, 25/0% med sekukinumab/placebo, 25/13% med ixekizumab/placebo och 40/18% med bimekizumab/placebo under de placebokontrollerade faserna, medan motsvarande studier på TNF-hämmare saknas. I flera observationsstudier har setts att patienter som har sviktat på en TNF-hämmare har lika god, eller bättre, effekt av att byta till en andra TNF-hämmare, som att byta till sekukinumab.[102-106] Likväl, vid upprepad behandlingssvikt på en preparattyp rekommenderar vi att byta till preparat med annan verkningsmekanism.
bDMARDS och tsDMARDs som har studerats vid AS, utan eller med ringa effekt
Studier som beskriver detta finns i Appendix, Text 1.
Instrument för bedömning och utvärdering av sjukdomsaktivitet och funktion
Nedan angivna instrument utgör stöd för klinikern vid beslut om behandling. En sammanvägning av samtliga faktorer som påverkar sjukdomens svårighetsgrad bör göras och nivån av sjukdomsaktivitet definieras i slutändan av behandlande reumatolog.
Utvärdering av axial sjukdom bör omfatta följande dimensioner:
- Läkarens globala sjukdomsskattning
- Smärta (VAS)
- Patientens globala sjukdomsskattning (VAS)
- Sjukdomsaktivitet (ASDAS och/eller BASDAI*)
- Funktion (BASFI*)
- CRP och/eller SR
- Rörlighet i ryggen (förslagsvis BASMI*) – ej obligatorisk i svensk uppföljning
* De svenska versionerna kan laddas ner från http://srq.nu/for-vardgivare/for-anvandare/
Utvärdering bör göras enligt de första sex punkterna enligt ovan, men det bör läggas störst tyngdpunkt på mått reflekterande inflammatorisk aktivitet (i första hand ASDAS med CRP).
För värdering av patienternas hälsa finns ett validerat instrument, ASAS-hälsoindex (HI), som kan användas vid såväl axial som perifer SpA och är framtaget i samarbete med patienter.[107] ASAS-OMERACT anger ASAS-HI som ett core outcome.[108] Instrumentet är validerat i en svensk kontext och validitet och reliabilitet var god.[109]. Formulär för ASAS-HI finns på https://www.asas-group.org/instruments/asas-health-index/.
Vid samtidigt förekommande perifer ledsjukdom görs uppföljning och utvärdering av detta som vid PsA (se nedan).
Vid nr-axSpA är b/tsDMARDs enbart godkända vid objektiva tecken till inflammation, i form av förhöjt CRP och/eller benmärgsödem på MRT, vilket baseras på resultat från de studier som ligger till grund för indikationen. Utöver detta rekommenderas inte MRT för utvärdering av sjukdomsaktivitet inför beslut om behandlingsstart eller utvärdering av behandling. MRT kan dock vara vägledande i situationer där det är oklart om symptomen beror på inflammation eller andra orsaker.[1]
Responsmått/Remission
ASDAS (Axial Spondyloarthritis Disease Activity Score) med CRP är det bäst validerade indexet för utvärdering av sjukdomsaktivitet och behandlingseffekt vid axSpA och rekommenderas av ASAS (Tabell 4).[110, 111] Inaktiv sjukdom <1.3, låg 1.3-2.0, hög sjukdomsaktivitet 2.1-3.5, mycket hög sjukdomsaktivitet >3.5. Förbättring: Δ ≥1.1. Uttalad förbättring: Δ ≥2.0. Remission definieras lämpligen genom ASDAS-värde <1.3 alternativt ASAS kriterier för partiell remission (definieras genom absoluta värden för samtliga 4 ingående VAS-skalor <2) (Tabell 5).
Ett annat ofta använt mått i kliniska studier för att definiera signifikant klinisk förbättring är en relativ förbättring av BASDAI på >50% eller mer än 2 skalstegs förbättring (skala 0-10) samt effekt enligt värdering av reumatologspecialist.
Treat-to-target
Målstyrd behandling, treat-to-target, vid axSpA har diskuterats och inaktiv sjukdom alternativt låg sjukdomsaktivitet har föreslagits som mål.[112] Det vetenskapliga underlaget för treat-to-target strategi är ännu mycket begränsat. I en 1-årig studie av 160 patienter jämfördes treat-to-target (uppföljning var 4.e vecka) hos patienter med axSpA och ASDAS ≥2.1 med standardbehandling (uppföljning var 12:e vecka). I treat-to-target-gruppen intensifierades behandlingen i syfte att uppnå ASDAS <2.1. Studiens primära utfall var andelen patienter som förbättrades ≥30% i ASAS-HI,[113] vilket uppnåddes av 47% i treat-to-target-gruppen jämfört med 34% i gruppen med standardbehandling, en skillnad som inte var statistiskt signifikant.[114] Vissa sekundära utfall uppnåddes såsom ASDAS låg sjukdomsaktivitet, treat-to-target 52% jmf standardbehandling 35%. Andelen patienter som erhöll bDMARD var signifikant högre vid treat-to-target, 56% jmf med 27% vid standardbehandling. Det primära utfallet uppnåddes således inte i studien och mer underlag avseende treat-to-target-strategi behövs, även beträffande val av mål för behandlingen.
Behandlingslängd/Dosreduktion bDMARDs
Det vetenskapliga underlaget för dosreduktion eller utsättande av TNF-hämmare utgörs av ett antal observationsstudier samt fem randomiserade studier.[115-119]
I en studie randomiserades 313 patienter med tidig axSpA (AS och nr-axSpA) i stabil remission efter 48 veckor med certolizumab i ordinarie dos, till fortsatt normaldosering, halverad dos (200 mg var 4:e vecka) eller placebo. Efter ytterligare 48 veckor bibehöll 84%, 79%, respektive 20% låg sjukdomsaktivitet (ASDAS <2.1).[116]
I en annan RCT randomiserades 305 nr-axSpA patienter som uppnått inaktiv sjukdom efter 28 veckors behandling med adalimumab till fortsatt behandling respektive placebo. En signifikant lägre andel av de som fortsatte med TNF-hämmarbehandlingen utvecklade sjukdomsskov jämfört med de som övergick till placebo (47% vs. 70%).[115].
Ytterligare tre mindre RCTs jämförde fortsatt normaldosering mot en stegvis förlängning av doseringsintervallet för TNF-hämmare bland 58, 55 respektive 40 axSpA-patienter med stabil remission eller låg sjukdomsaktivitet (under minst 6 eller 12 månader).[117-119] Något förenklat kan man säga att dosreduktionsgrupperna halverade TNF-hämmardoserna utan skillnader i sjukdomsaktivitet jämfört med grupperna som fortsatte med normaldosering. Sjukdomsskov var dock något vanligare vid dosreduktion.
I observationsstudier av axSpA är dosreduktion eller ökat intervall av TNF-hämmare mest studerat hos patienter med AS och visar bibehållen remission/låg sjukdomsaktivitet hos 53-100% av patienterna efter en genomsnittlig uppföljningstid på ett år.[120-122]
Utsättning av ixekizumab vid remission av axSpA [123] studerades hos 155 patienter från de indikationsgrundande RCT:erna som uppnått ASDAS-remission. De randomiserades till fortsatt behandling eller placebo. Vid utvärdering efter 60 veckor var 76% i behandlingsgruppen fria från sjukdomsskov vs. 36% i placebogruppen.[124] Man såg ingen skillnad mellan r-axSpA och nr-axSpA i utfallet.[123] Prediktorer för sjukdomsskov var högre ASDAS-värden över tid, högt BMI och högt CRP vid randomiseringen.[123] Bland patienterna i placebogruppen som fick sjukdomsskov, uppnådde 96% åter låg sjukdomsaktivitet eller remission inom 16 veckor efter återstart av ixekizumab.[124]
Hos patienter med axSpA som uppnått varaktig (minst 6 månader) och låg sjukdomsaktivitet föreslås utifrån detta i första hand att dosreducering av bDMARD (snarare än utsättning) görs för att bibehålla behandlingsmålet.
Perifer SpA
Perifer SpA
Perifer SpA (pSpA) används för att beskriva gruppen av patienter med kännetecken för SpA, med symtom och undersökningsfynd övervägande perifert till skillnad från axialt. ASAS publicerade klassifikationskriterier för pSpA 2011, vilka kan tillämpas på patienter med artrit, entesit eller daktylit.[249] Förutom att ha minst ett av dessa manifestationer omfattar kriterierna två olika scenarier med olika SpA-kännetecken, Figur 2.[249, 250]. I en stor studie av 4185 patienter med SpA bedömdes 17 % ha pSpA (som inte var PsA) enligt ASAS klassifikationskriterier. .[251]
Ett par RCTs har utförts för att studera effekten av TNF-hämmare vid pSpA utifrån ovanstående klassifikationskriterier. I en studie undersöktes effekten av adalimumab hos patienter med pSpA (dock ej psoriasis eller PsA). Patienter med aktiv sjukdom och med otillräcklig effekt eller biverkningar av COX-hämmare randomiserades till adalimumab (n=84) eller placebo (n=81).[252] Totalt var 61% av patienterna HLA-B27 positiva, 15 % hade haft irit, 8% hade infektionsrelaterat reaktivt insjuknande, och 5% hade IBD. Primärt utfall var andelen patienter med 40% förbättring av sjukdomsaktivitet enligt Peripheral SpA Response Criteria (PSpARC40 [252]) vid vecka 12. Signifikant fler adalimumab-behandlade uppnådde PSpARC40 respons jämfört med placebo (39 vs. 20%).
Inducering av klinisk remission med golimumab hos patienter med mycket tidig, aktiv pSpA (symptom <12 veckor) utvärderades i en annan studie.[253] Patienterna randomiserades till golimumab (n=40) eller placebo (n=20). Totalt var 55% av patienterna HLA-B27 positiva, 2% hade tidigare irit, 13% hade infektionsrelaterat reaktivt insjuknande, 2% hade IBD och 42% hade psoriasis. Primärt utfall var andelen patienter med klinisk remission vid vecka 24, definierat som frånvaro av artrit, entesit och daktylit. Signifikant högre andel uppnådde klinisk remission med golimumab jämfört med placebo (75 vs. 20%). Andelen patienter som uppnådde PSpARC40% respons var också signifikant högre i golimumab gruppen jämfört med placebo (50 vs. 15%).
Bedömning och utvärdering avseende sjukdomsaktivitet kan göras, för perifer sjukdom och för ev. axiala komponenter av sjukdomen, som vid PsA respektive axSpA (se ovan).
Sammanfattningsvis, i avsaknad av studier finns ingen evidens för att använda csDMARD eller tsDMARD vid pSpA enligt ASAS definition (förutom vid PsA). Det finns å andra sidan visst stöd från ett par RCTs enligt ovan som visar en god effekt av TNF-hämmare. Inget av preparaten har dock godkänd indikation för behandling av pSpA, medan flera har indikation för associerade sjukdomar, såsom psoriasis och IBD, och från studier av axSpA och psoriasisartrit finns stöd för effekt på specifika muskuloskeletala sjukdomsmanifestationer (var god se avsnittet om särskilda manifestationer vid SpA nedan).
Särskilda manifestationer vid SpA
Psoriasis
Vid närvaro av måttlig till svår psoriasis vid PsA (BSA >3% eller psoriasis lokaliserad till ansikte, genitalia, hårbotten, naglar, händer och fötter med en uttalad negativ inverkan på patientens livskvalitet) bör effekten av preparaten på hudkomponenten också vägas in vid val av terapi.
Bland cs/tsDMARDs har metotrexat och ciklosporin A måttlig effekt på psoriasis,[125, 163, 164] dock är ciklosporin behäftat med risk för njurbiverkningar vid längre tids behandling. Leflunomid och apremilast har liten effekt, sulfasalazin har ingen säker effekt på psoriasis.[5, 159, 165] Effekten av tofacitinib och upadacitinib på psoriasis bland bDMARD-naiva patienter är jämförbar med adalimumab, men ingen av JAK-hämmarna är godkända för enbart psoriasis.[214, 215]
Bland bDMARDs har IL17-, IL23- och IL-12/23- hämmare bättre effekt [136, 164, 188-190, 202-205, 254] på psoriasis än TNF-hämmare, som likväl uppvisar god effekt.[5] Etanercept är mindre effektivt jämfört med andra TNF-hämmare.[164] Abatacept har mycket begränsad effekt på psoriasis.[5, 136] Vid behandling med TNF-hämmare finns visst stöd för att tillägg av metotrexat kan ge bättre effekt på psoriasis.[255]
Irit
Vid SpA är främre uveit (irit) den vanligaste formen av uveit. Studier ger stöd för att behandling med TNF-hämmare av monoklonal antikroppstyp har en bättre skyddande effekt mot irit vid AS, jämfört med etanercept och IL17A-hämmare.[256-260] En studie har också visat skyddande effekt av IL17A/F-hämmare jämfört med placebo,[261] men ingen direkt jämförande studie mellan IL17A/F-hämmare och TNF-hämmare eller annan DMARD är publicerad. För övriga DMARDs som rekommenderas vid axSpA/PsA är evidensen för begränsad för att uttala sig om eventuell effekt på SpA-associerad irit. Vid svårbehandlad eller frekvent recidiverande irit rekommenderas därför i första hand behandling med TNF-hämmare av monoklonal antikroppstyp om bDMARD terapi är motiverad.
Inflammatorisk tarmsjukdom
IL17A-hämmare och IL17-receptor hämmare har i fas 2 studier kopplats till ökad inflammatorisk aktivitet vid Crohns sjukdom och IL17-hämning rekommenderas därför inte vid inflammatorisk tarmsjukdom.[262, 263] Infliximab, adalimumab, upadacitinib, guselkumab, risankizumab och ustekinumab har indikationerna ulcerös colit och Crohns sjukdom, medan golimumab och tofacitinib har indikation ulcerös colit. Vid signifikant IBD-problematik bör därför preparat med god effekt på denna sjukdom i första hand ges när bDMARD/tsDMARD terapi är motiverad. Bland csDMARD har sulfasalazin även indikation ulcerös colit och Crohns sjukdom.
Daktyliter
En studie har visat bättre effekt mot daktylit, vid PsA, av kortisoninjektion i flexorsenskidan, jämfört med 4 veckors behandling med ibuprofen.[144] Stöd för effekt av metotrexat mot daktylit kommer en randomiserad studie där likartad effekt sågs för metotrexat som för etanercept.[147, 149] I okontrollerade studier har också förbättring noterats under behandling med metotrexat respektive leflunomid,[161, 264] medan två RCTs inte rapporterat effekt av sulfasalazin mot daktyliter.[146, 265]
En RCT har utvärderat effekten av golimumab i kombination med metotrexat jämfört med metotrexat enbart, med daktyliter som primärt utfallsmått vid PsA.[266] I denna studie sågs både klinisk och objektiv (MRT) förbättring i båda grupperna, men signifikant bättre effekt sågs för flera utfall för kombinationsbehandling. Det finns även stöd från studier, vid PsA, som inte har daktylit som primärt utfall, för andra TNF-hämmare, IL17-hämmare, JAK-hämmare, IL23-hämmare, ustekinumab och apremilast.[188-190, 203-205, 217, 221, 267, 268] I en meta-analys som jämfört effekten mot daktyliter i RCTs av TNF-hämmare (infliximab, adalimumab och golimumab) mot andra bDMARDs (ustekinumab, sekukinumab och ixekizumab tillsammans), fann man ingen skillnad.[269]
Sammantaget finns stöd för att behandling mot daktyliter kan innefatta kortisoninjektion i flexorsenskida, metotrexat, TNF-hämmare och övriga, för PsA godkända, bDMARD och tsDMARD, med undantag för abatacept.
Entesiter
Bland csDMARDs finns starkast stöd för effekt mot entesiter för metotrexat, där man i en randomiserad studie av PsA fann en likvärdig reduktion av entesiter i gruppen som behandlades med metotrexat som hos de som fick etanercept.[149] Behandlingseffekt mot entesiter har även utvärderat med helkropps MRT i en studie vid tidig axSpA, där en tydlig reduktion av entesiter såg bland de som fick etanercept, medan ingen effekt sågs för sulfasalazin.[61] En mindre RCT har inte heller visat effekt av sulfasalazin mot entesiter.[146]
Det finns stöd för behandlingseffekt i form av minskat antal entesiter (enligt klinisk bedömning), vid samtidig perifer artritsjukdom vid PsA, från RCTs för TNF-hämmare, IL17-hämmare, JAK-hämmare, IL23-hämmare, ustekinumab och apremilast.[188-190, 203, 205, 215, 217, 268, 270] Entesit som primärt utfall har endast studerats i en liten RCT där man fann att ustekinumab var något effektivare än TNF-hämmare.[210] I en meta-analys som jämfört effekten mot entesiter i RCTs av TNF-hämmare (infliximab, adalimumab och golimumab) mot andra bDMARDs (ustekinumab, sekukinumab och ixekizumab tillsammans), fann man ingen skillnad.[269] I en head-to-head studie mellan sekukinumab och adalimumab sågs vidare likvärdig förbättring av entesiter, vilket även sågs i efter 1 års behandling i en head-to-head studie mellan ixekizumab och adalimumab (där dock en något bättre effekt av ixekizumab sågs efter 24 veckor.[271]
Förekomst av entesit bör vägas in i den totala bedömningen av sjukdomsaktivitet vid start och utvärdering av DMARD. Kliniskt är det mycket svårt att skilja entesit från den palpationsömhet som föreligger hos individer med kronisk generaliserad smärta. Ultraljud kan vara till nytta för att skilja andra sjukdomsprocesser (artrit, bursit, tenovaginit) från entesit eller helt fria från misstanke om inflammatorisk process i det ömma området. Det finns en överenskommen definition för ultraljudsverifierad entesit.[272, 273] Studier som utvärderar kliniska implikationer av denna definition pågår.
Hos patient med säkerställd SpA är SRFs hållning att otvetydig entesit (diagnosticerad med till exempel bilddiagnostik eller tydlig klinisk svullnad och värmeökning) i sig kan utgöra behandlingsindikation för DMARD. Baserat på ovanstående finns visst stöd för att metotrexat kan provas innan TNF-hämmare eller andra b/tsDMARDs vid entesiter.
Säkerhetsaspekter
För kontraindikationer, varningar och försiktighet, se FASS. Var god se även SRFs riktlinjer och rekommendationer avseende säker läkemedelsbehandling, läkemedelsbehandling och kardiovaskulär risk samt läkemedelsbehandling i samband med graviditet och amning.
RCTs designade för att utvärdera behandlingseffekt vid reumatisk sjukdom, samt meta-analyser av sådana, visar i allmänhet inga större risker för allvarliga biverkningar jmf med placebo. Dock är dessa studier inte i första hand designade för att studera säkerhetsaspekter, speciellt inte över ett längre tidsperspektiv. Nedan följer en genomgång, följt av rekommendationer, för tillstånd av särskilt kliniskt intresse. Det finns en stor mängd studier av dessa aspekter och denna genomgång ger inte en fullständig beskrivning av samtliga.
COX-hämmare
Samma försiktighet och kontraindikationer ska beaktas som vid behandling med COX-hämmare vid andra sjukdomstillstånd.
Då COX-hämmare används skall de ges i lägsta effektiva dos, med individuell riskbedömning, och vid långvarig behandling ska regelbunden kontroll av njurfunktion och blodtryck genomföras. COX-hämmare kan påverka tarmslemhinnans barriärfunktion och bör undvikas hos patienter med bakomliggande inflammatorisk tarmsjukdom. Försiktighet rekommenderas även hos patienter med känd leversjukdom. Profylax med protonpumpshämmare rekommenderas vid ökad gastrointestinal risk och långvarig behandling med COX-hämmare. Cox-2-selektiva hämmare är associerade med lägre gastrointestinal risk men ökad kardiovaskulär risk. För mer information avseende risk-nytta-avvägning vid behandling med COX-hämmare generellt (dvs inte specifikt vid reumatisk sjukdom) se janusinfo.se.
Infektioner
I en stor RCT, CIRT-studien på patienter med kardiovaskulär sjukdom (n=4786), sågs en något ökad risk för mildare infektioner hos de som behandlades med metotrexat jmf med placebo, men ingen skillnad för måttliga och allvarliga infektioner.[274] Större studier specifikt på axSpA och PsA populationer saknas.
Incidensen för allvarliga infektionsepisoder hos patienter med PsA som behandlas med TNF-hämmare har rapporterats kring 2,2 och 2,7 per 100 personår,[275, 276] vilket är något lägre än vad som visats för RA (incidens 4,2 per 100 personår).[275]
I en head-to head studie av adalimumab vs. sekukinumab vid PsA, rapporterades liknande frekvenser av infektioner och allvarliga infektioner, men numeriskt fler fall av candida i sekukinumab gruppen.[192] I motsvarande studie för adalimumab vs. ixekizumab, rapporterades numeriskt något fler allvarliga infektioner för adalimumab än för ixekizumab (8 jmf 4) och fler fall av candida med ixekizumab (7 jmf 2).[195] Det saknas direkta jämförelser mellan IL17-hämmare vid PsA men vid indirekt jämförelse och extrapolerat från direkta jämförelser i studier på psoriasis kan bimekizumab medföra ytterligare högre risk för mukokutana svampinfektioner än andra IL17-hämmare.[277, 278] I studien med direkt jämförelse på psoriasis var dock dosen bimekizumab högre än vad som används vid reumatologiska indikationer.[277]
Tre större observationsstudier har visat att behandling med ustekinumab är kopplat till en lägre risk för allvarliga (sjukhusvårdade) infektioner hos patienter med PsA eller psoriasis, jämfört med behandling med TNF-hämmare.[276, 279, 280] I en av dessa studier jämfördes även TNF-hämmare direkt med IL17A-hämmare och ingen skillnad sågs avseende risk för allvarliga infektioner.[276] I den andra studien sågs även högre risk för allvarliga infektioner av apremilast, sekukinumab och ixekizumab jmf med ustekinumab.[279] I den tredje sågs lägre risk för infektioner för ustekinumab och etanercept jämfört med adalimumab.[280] En nordisk studie har också beskrivit likartad risk för allvarliga infektioner vid behandling med adalimumab och sekukinumab.[281] En metaanalys har inte påvisat någon ökad infektionsrisk med apremilast i relation till placebo.[282]
I randomiserade registreringsstudier har numeriskt liknande antal allvarliga infektioner rapporterats vid behandling med tofacitinib och upadacitinib (i rekommenderad dos) jmf med adalimumab.[214, 215, 283] Vid RA ses en högre risk för herpes zoster vid behandling med JAK-hämmare jmf med andra b/tsDMARDs vid RA,[284] vilket också observerats i en meta-analys på psoriasis och psoriasisartrit.[285]
För salazopyrin, leflunomid, abatacept och IL-23-hämmare, saknas jämförande studier avseende risk för infektioner vid axSpA och PsA.
Metotrexat ökar alltså sannolikt inte påtagligt risken för allvarliga infektioner på gruppnivå. För de patienter med PsA som bedöms ha en ökad risk för infektioner kan ustekinumab vara förknippat med en uppemot halverad risk för allvarliga infektioner jämfört med TNF-hämmare. För TNF-hämmare, IL17-hämmare och JAK-hämmare saknas entydigt stöd för att endera är säkrare med hänsyn till allvarliga infektioner (vid FASS-dos), men IL17-hämmare ger ökad risk för mukokutana candidainfektioner och JAK-hämmare är kopplade till en ökad risk för herpes zoster.
Multipel skleros (MS)
Metotrexat har undersökts som behandling mot MS i flera studier, men i en Cochrane analys identifierades bara en studie med tillräcklig kvalitet för att inkluderas. I denna sågs en icke-signifikant trend till bättre utfall för metotrexat.[286] Sulfasalazin studerades i en fas III studie på MS och påvisade ingen effekt.[287] Leflunomid metaboliseras snabbt till teriflunomid, vilket är godkänt som behandling mot MS.[288]
Behandling med TNF-hämmare vid axSpA och PsA har misstänkts vara kopplat till en ökad risk för MS, baserat på observationsstudier och fallrapporter.[289] Sambandet är dock inte helt klarlagt och kan vara svårt att skilja från ev. översjuklighet i MS hos patienter med autoimmun sjukdom (t.ex. PsA).[290] En tidig fas II studie av TNF-hämmaren lenercept vid MS visade dock en ökad frekvens av skov i den behandlade gruppen jämfört med placebo [291] och negativ effekt sågs även i en tidig fas I studie på infliximab vid MS.[292]
Två fas II studier av IL-12/23 hämmare vid MS (ustekinumab [293] och briakinumab [294]) påvisade inte någon kliniskt relevant gynnsam effekt (för briakinumab sågs något bättre utfall), men inte heller någon negativ effekt. En liten ”proof of concept” studie av sekukinumab vid MS visade en trend till bättre utfall för sekukinumab.[295] En fas II studie på abatacept vid MS påvisade inte någon effekt.[296]
För JAK-hämmare, apremilast och rena IL23-hämmare saknas tillräckligt med data.
Behandling med TNF-hämmare rekommenderas därför inte till patienter med samtidig MS. IL17A-hämmare, IL12/23-hämmare, metotrexat, salazopyrin, leflunomid och abatacept kan övervägas, men ev. interaktioner och potentiellt förstärkt immunsuppression vid kombination med MS-läkemedel måste beaktas.
Malignitet
En större (8703 patienter, median uppföljningstid 5,6 år) observationsstudie baserad på svenska och danska register, har inte påvisat någon ökad risk för malignitet vid SpA behandlad med TNF-hämmare.[297]
JAK-hämmare
Kunskapsläget kring säkerhet vid behandling med JAK-hämmare är snabbt föränderligt och är generellt sett sämre jämfört med flertalet bDMARDs. Därför bör varje förskrivande läkare vara observant på ny information och rekommendationer från myndigheter.
En randomiserad säkerhetsstudie på patienter med RA som behandlats med tofacitinib eller TNF-hämmare har visat att tofacitinib är förknippat med en högre risk för allvarlig kardiovaskulär sjukdom, venös tromboembolism och malignitet.[298] Denna studie inkluderade enbart patienter ≥50 år och med minst en riskfaktor för kardiovaskulär sjukdom (rökning, hypertoni, HDL <1,03, diabetes, tidigare kranskärlssjukdom eller ärftlighet för sådan vid yngre åldrar, extra-artikulär RA), och i en posthoc analys påvisades ingen riskökning bland de studiedeltagare som både var <65 år och aldrig hade rökt.[299] En ökad risk för venös tromboembolism (i synnerhet lungemboli) vid behandling med JAK-hämmare har också rapporterats i observationsstudier.[300]
EMA har gjort bedömningen att dessa fynd har relevans för alla JAK-hämmare godkända för användning vid inflammatorisk sjukdom. Enligt EMA bör JAK-hämmare bara användas om inget lämpligt behandlingsalternativ finns för patienter över 65 år, patienter med ökad risk för allvarlig hjärtkärlsjukdom, rökare (inkl. de som tidigare rökt under lång tid) och patienter med andra riskfaktorer för malignitet. EMA rekommenderar också att använda JAK-hämmare med försiktighet till patienter med andra riskfaktorer för venös tromboembolism, utöver de ovan angivna, och att reducera dosen för patienter med risk för venös tromboembolism, allvarlig hjärtkärlsjukdom och malignitet.[301]
Det är i nuläget inte säkerställt huruvida dessa risker kan extrapoleras till SpA och PsA, och ej heller om det är en effekt kopplat specifikt till tofacitinib eller till hela gruppen av JAK-hämmare. Vid en indirekt jämförelse av data från olika studier föreföll dock risken för allvarlig kardiovaskulär sjukdom, venös tromboembolism respektive malignitet bland tofacitinib behandlade PsA patienter <65 år och som aldrig rökt (n=442) att ligga på samma nivå som för motsvarande grupp med RA,[302] där ingen riskökning setts för tofacitinib vs. TNF-hämmare. I en observationsstudie, som jämförde utveckling av kardiovaskulär sjukdom och solida tumörer, vid behandling med JAK-hämmare, IL17-hämmare och TNF-hämmare, hos personer med axSpA och PsA, sågs ingen skillnad i risk (medianuppföljning ca 400 dagar).[303]
SRF uppmanar till att beakta den ovanstående säkerhetsinformationen, samt EMA:s rekommendationer baserade på denna, vid förskrivning av JAK-hämmare mot SpA och PsA.
Referenser
Hänvisad litteratur
- Ramiro S, Nikiphorou E, Sepriano A, et al. ASAS-EULAR recommendations for the management of axial spondyloarthritis: 2022 update. Ann Rheum Dis 2023;82:19-34.
- Ward MM, Deodhar A, Gensler LS, et al. 2019 Update of the American College of Rheumatology/Spondylitis Association of America/Spondyloarthritis Research and Treatment Network Recommendations for the Treatment of Ankylosing Spondylitis and Nonradiographic Axial Spondyloarthritis. Arthritis Rheumatol 2019;71:1599-613.
- Gossec L, Kerschbaumer A, Ferreira RJO, et al. EULAR recommendations for the management of psoriatic arthritis with pharmacological therapies: 2023 update. Ann Rheum Dis 2024;83:706-19.
- Singh JA, Guyatt G, Ogdie A, et al. Special Article: 2018 American College of Rheumatology/National Psoriasis Foundation Guideline for the Treatment of Psoriatic Arthritis. Arthritis Rheumatol 2019;71:5-32.
- Coates LC, Soriano ER, Corp N, et al. Group for Research and Assessment of Psoriasis and Psoriatic Arthritis (GRAPPA): updated treatment recommendations for psoriatic arthritis 2021. Nat Rev Rheumatol 2022;18:465-79.
- van der Linden S, Valkenburg HA, Cats A. Evaluation of diagnostic criteria for ankylosing spondylitis. A proposal for modification of the New York criteria. Arthritis Rheum 1984;27:361-8.
- Rudwaleit M, van der Heijde D, Landewe R, et al. The development of Assessment of SpondyloArthritis international Society classification criteria for axial spondyloarthritis (part II): validation and final selection. Ann Rheum Dis 2009;68:777-83.
- Boel A, Molto A, van der Heijde D, et al. Do patients with axial spondyloarthritis with radiographic sacroiliitis fulfil both the modified New York criteria and the ASAS axial spondyloarthritis criteria? Results from eight cohorts. Ann Rheum Dis 2019;78:1545-9.
- Bakland G, Alsing R, Singh K, et al. Assessment of SpondyloArthritis International Society criteria for axial spondyloarthritis in chronic back pain patients with a high prevalence of HLA-B27. Arthritis Care Res (Hoboken) 2013;65:448-53.
- Strand V, Rao SA, Shillington AC, et al. Prevalence of axial spondyloarthritis in United States rheumatology practices: Assessment of SpondyloArthritis International Society criteria versus rheumatology expert clinical diagnosis. Arthritis Care Res (Hoboken) 2013;65:1299-306.
- Lindström U, Bremander A, Bergman S, et al. Patients with axial SPA have similar prevalence compared to AS, but worse perceived health. Results from a population based study. Ann Rheum Dis 2013;72:(Suppl3):667.
- Sieper J, Rudwaleit M, Baraliakos X, et al. The Assessment of SpondyloArthritis international Society (ASAS) handbook: a guide to assess spondyloarthritis. Ann Rheum Dis 2009;68 Suppl 2:ii1-44.
- Maksymowych WP, Lambert RG, Baraliakos X, et al. Data-driven definitions for active and structural MRI lesions in the sacroiliac joint in spondyloarthritis and their predictive utility. Rheumatology (Oxford) 2021;60:4778-89.
- Lambert RG, Bakker PA, van der Heijde D, et al. Defining active sacroiliitis on MRI for classification of axial spondyloarthritis: update by the ASAS MRI working group. Ann Rheum Dis 2016;75:1958-63.
- Poddubnyy D, Diekhoff T, Baraliakos X, et al. Diagnostic evaluation of the sacroiliac joints for axial spondyloarthritis: should MRI replace radiography? Ann Rheum Dis 2022;81:1486-90.
- Lambert RGW, Baraliakos X, Bernard SA, et al. Development of international consensus on a standardised image acquisition protocol for diagnostic evaluation of the sacroiliac joints by MRI: an ASAS-SPARTAN collaboration. Ann Rheum Dis 2024;83:1628-35.
- Diekhoff T, Giraudo C, Machado PM, et al. Clinical information on imaging referrals for suspected or known axial spondyloarthritis: recommendations from the Assessment of Spondyloarthritis International Society (ASAS). Ann Rheum Dis 2024;83:1636-43.
- Diekhoff T, Eshed I, Giraudo C, et al. Reporting Sacroiliac Joint Imaging Performed for Known or Suspected Axial Spondyloarthritis: Assessment of SpondyloArthritis International Society Recommendations. Radiology 2024;311:e231786.
- Creemers MC, Franssen MJ, van’t Hof MA, et al. Assessment of outcome in ankylosing spondylitis: an extended radiographic scoring system. Ann Rheum Dis 2005;64:127-9.
- Poddubnyy D, Haibel H, Listing J, et al. Baseline radiographic damage, elevated acute-phase reactant levels, and cigarette smoking status predict spinal radiographic progression in early axial spondylarthritis. Arthritis Rheum 2012;64:1388-98.
- van Tubergen A, Ramiro S, van der Heijde D, et al. Development of new syndesmophytes and bridges in ankylosing spondylitis and their predictors: a longitudinal study. Ann Rheum Dis 2012;71:518-23.
- Deminger A, Klingberg E, Geijer M, et al. A five-year prospective study of spinal radiographic progression and its predictors in men and women with ankylosing spondylitis. Arthritis Res Ther 2018;20:162.
- van der Heijde D, Ostergaard M, Reveille JD, et al. Spinal Radiographic Progression and Predictors of Progression in Patients With Radiographic Axial Spondyloarthritis Receiving Ixekizumab Over 2 Years. J Rheumatol 2022;49:265-73.
- Machado P, Landewe R, Braun J, et al. A stratified model for health outcomes in ankylosing spondylitis. Ann Rheum Dis 2011;70:1758-64.
- Protopopov M, Poddubnyy D. Radiographic progression in non-radiographic axial spondyloarthritis. Expert Rev Clin Immunol 2018;14:525-33.
- Molto A, Lopez-Medina C, Sepriano A, et al. Sacroiliac radiographic progression over 10 years in axSpA: data from the DESIR inception cohort. Ann Rheum Dis 2024;83:858-64.
- Bennett AN, McGonagle D, O’Connor P, et al. Severity of baseline magnetic resonance imaging-evident sacroiliitis and HLA-B27 status in early inflammatory back pain predict radiographically evident ankylosing spondylitis at eight years. Arthritis Rheum 2008;58:3413-8.
- Dougados M, Sepriano A, Molto A, et al. Sacroiliac radiographic progression in recent onset axial spondyloarthritis: the 5-year data of the DESIR cohort. Ann Rheum Dis 2017;76:1823-8.
- Poddubnyy D, Rudwaleit M, Haibel H, et al. Rates and predictors of radiographic sacroiliitis progression over 2 years in patients with axial spondyloarthritis. Ann Rheum Dis 2011;70:1369-74.
- Zochling J, van der Heijde D, Burgos-Vargas R, et al. ASAS/EULAR recommendations for the management of ankylosing spondylitis. Ann Rheum Dis 2006;65:442-52.
- Zochling J, van der Heijde D, Dougados M, et al. Current evidence for the management of ankylosing spondylitis: a systematic literature review for the ASAS/EULAR management recommendations in ankylosing spondylitis. Ann Rheum Dis 2006;65:423-32.
- Sieper J, Listing J, Poddubnyy D, et al. Effect of continuous versus on-demand treatment of ankylosing spondylitis with diclofenac over 2 years on radiographic progression of the spine: results from a randomised multicentre trial (ENRADAS). Ann Rheum Dis 2016;75:1438-43.
- Wanders A, Heijde D, Landewe R, et al. Nonsteroidal antiinflammatory drugs reduce radiographic progression in patients with ankylosing spondylitis: a randomized clinical trial. Arthritis Rheum 2005;52:1756-65.
- Kroon F, Landewe R, Dougados M, et al. Continuous NSAID use reverts the effects of inflammation on radiographic progression in patients with ankylosing spondylitis. Ann Rheum Dis 2012;71:1623-9.
- Poddubnyy D, Rudwaleit M, Haibel H, et al. Effect of non-steroidal anti-inflammatory drugs on radiographic spinal progression in patients with axial spondyloarthritis: results from the German Spondyloarthritis Inception Cohort. Ann Rheum Dis 2012;71:1616-22.
- Proft F, Torgutalp M, Muche B, et al. Comparison of the effect of treatment with NSAIDs added to anti-TNF therapy versus anti-TNF therapy alone on the progression of structural damage in the spine over 2 years in patients with radiographic axial spondyloarthritis from the randomised-controlled CONSUL trial. Ann Rheum Dis 2024;83:599-607.
- Sieper J, Lenaerts J, Wollenhaupt J, et al. Efficacy and safety of infliximab plus naproxen versus naproxen alone in patients with early, active axial spondyloarthritis: results from the double-blind, placebo-controlled INFAST study, Part 1. Ann Rheum Dis 2014;73:101-7.
- Sieper J, Rudwaleit M, Lenaerts J, et al. Partial remission in ankylosing spondylitis and non-radiographic axial spondyloarthritis in treatment with infliximab plus naproxen or naproxen alone: associations between partial remission and baseline disease characteristics. Rheumatology (Oxford) 2016;55:1946-53.
- Kristensen LE, Jakobsen AK, Askling J, et al. Safety of Etoricoxib, Celecoxib, and Nonselective Nonsteroidal Antiinflammatory Drugs in Ankylosing Spondylitis and Other Spondyloarthritis Patients: A Swedish National Population-Based Cohort Study. Arthritis Care Res (Hoboken) 2015;67:1137-49.
- Haibel H, Fendler C, Listing J, et al. Efficacy of oral prednisolone in active ankylosing spondylitis: results of a double-blind, randomised, placebo-controlled short-term trial. Ann Rheum Dis 2014;73:243-6.
- Mishra D, Dhir V, Naidu G, et al. Efficacy of a step-down regimen of oral prednisolone in axial spondyloarthritis: result of a double-blind randomized controlled trial (COBRA-AS Study). Rheumatology (Oxford) 2021;60:1932-41.
- Chen J, Lin S, Liu C. Sulfasalazine for ankylosing spondylitis. The Cochrane database of systematic reviews 2014:CD004800.
- van der Heijde D, Ramiro S, Landewe R, et al. 2016 update of the ASAS-EULAR management recommendations for axial spondyloarthritis. Ann Rheum Dis 2017;76:978-91.
- Khanna Sharma S, Kadiyala V, Naidu G, et al. A randomized controlled trial to study the efficacy of sulfasalazine for axial disease in ankylosing spondylitis. Int J Rheum Dis 2018;21:308-14.
- Chen J, Veras MM, Liu C, et al. Methotrexate for ankylosing spondylitis. The Cochrane database of systematic reviews 2013:CD004524.
- van Denderen JC, van der Paardt M, Nurmohamed MT, et al. Double blind, randomised, placebo controlled study of leflunomide in the treatment of active ankylosing spondylitis. Ann Rheum Dis 2005;64:1761-4.
- Haibel H, Rudwaleit M, Braun J, et al. Six months open label trial of leflunomide in active ankylosing spondylitis. Ann Rheum Dis 2005;64:124-6.
- Maxwell LJ, Zochling J, Boonen A, et al. TNF-alpha inhibitors for ankylosing spondylitis. Cochrane Database Syst Rev 2015:CD005468.
- Davis JC, Jr., Van Der Heijde D, Braun J, et al. Recombinant human tumor necrosis factor receptor (etanercept) for treating ankylosing spondylitis: a randomized, controlled trial. Arthritis Rheum 2003;48:3230-6.
- van der Heijde D, Dijkmans B, Geusens P, et al. Efficacy and safety of infliximab in patients with ankylosing spondylitis: results of a randomized, placebo-controlled trial (ASSERT). Arthritis Rheum 2005;52:582-91.
- van der Heijde D, Kivitz A, Schiff MH, et al. Efficacy and safety of adalimumab in patients with ankylosing spondylitis: results of a multicenter, randomized, double-blind, placebo-controlled trial. Arthritis Rheum 2006;54:2136-46.
- Inman RD, Davis JC, Jr., Heijde D, et al. Efficacy and safety of golimumab in patients with ankylosing spondylitis: results of a randomized, double-blind, placebo-controlled, phase III trial. Arthritis Rheum 2008;58:3402-12.
- Landewe R, Braun J, Deodhar A, et al. Efficacy of certolizumab pegol on signs and symptoms of axial spondyloarthritis including ankylosing spondylitis: 24-week results of a double-blind randomised placebo-controlled Phase 3 study. Ann Rheum Dis 2014;73:39-47.
- McLeod C, Bagust A, Boland A, et al. Adalimumab, etanercept and infliximab for the treatment of ankylosing spondylitis: a systematic review and economic evaluation. Health Technol Assess 2007;11:1-158, iii-iv.
- Sieper J, van der Heijde D, Dougados M, et al. Efficacy and safety of adalimumab in patients with non-radiographic axial spondyloarthritis: results of a randomised placebo-controlled trial (ABILITY-1). Ann Rheum Dis 2013;72:815-22.
- Dougados M, Wood E, Combe B, et al. Evaluation of the nonsteroidal anti-inflammatory drug-sparing effect of etanercept in axial spondyloarthritis: results of the multicenter, randomized, double-blind, placebo-controlled SPARSE study. Arthritis Res Ther 2014;16:481.
- Sieper J, van der Heijde D, Dougados M, et al. A randomized, double-blind, placebo-controlled, sixteen-week study of subcutaneous golimumab in patients with active nonradiographic axial spondyloarthritis. Arthritis Rheumatol 2015;67:2702-12.
- Barkham N, Keen HI, Coates LC, et al. Clinical and imaging efficacy of infliximab in HLA-B27-Positive patients with magnetic resonance imaging-determined early sacroiliitis. Arthritis Rheum 2009;60:946-54.
- Dougados M, van der Heijde D, Sieper J, et al. Symptomatic efficacy of etanercept and its effects on objective signs of inflammation in early nonradiographic axial spondyloarthritis: a multicenter, randomized, double-blind, placebo-controlled trial. Arthritis Rheumatol 2014;66:2091-102.
- Katz L, Gisbert JP, Manoogian B, et al. Doubling the infliximab dose versus halving the infusion intervals in Crohn’s disease patients with loss of response. Inflamm Bowel Dis 2012;18:2026-33.
- Song IH, Hermann K, Haibel H, et al. Effects of etanercept versus sulfasalazine in early axial spondyloarthritis on active inflammatory lesions as detected by whole-body MRI (ESTHER): a 48-week randomised controlled trial. Ann Rheum Dis 2011;70:590-6.
- Braun J, van der Horst-Bruinsma IE, Huang F, et al. Clinical efficacy and safety of etanercept versus sulfasalazine in patients with ankylosing spondylitis: a randomized, double-blind trial. Arthritis Rheum 2011;63:1543-51.
- Lie E, Kristensen LE, Forsblad-d’Elia H, et al. The effect of comedication with conventional synthetic disease modifying antirheumatic drugs on TNF inhibitor drug survival in patients with ankylosing spondylitis and undifferentiated spondyloarthritis: results from a nationwide prospective study. Ann Rheum Dis 2015;74:970-8.
- Nissen MJ, Ciurea A, Bernhard J, et al. The Effect of Comedication With a Conventional Synthetic Disease-Modifying Antirheumatic Drug on Drug Retention and Clinical Effectiveness of Anti-Tumor Necrosis Factor Therapy in Patients With Axial Spondyloarthritis. Arthritis Rheumatol 2016;68:2141-50.
- Heinonen AV, Aaltonen KJ, Joensuu JT, et al. Effectiveness and Drug Survival of TNF Inhibitors in the Treatment of Ankylosing Spondylitis: A Prospective Cohort Study. J Rheumatol 2015;42:2339-46.
- George MD, Baker JF, Ogdie A. Comparative Persistence of Methotrexate and Tumor Necrosis Factor Inhibitors in Rheumatoid Arthritis, Psoriatic Arthritis, and Ankylosing Spondylitis. J Rheumatol 2020;47:826-34.
- Nissen M, Delcoigne B, Di Giuseppe D, et al. The impact of a csDMARD in combination with a TNF inhibitor on drug retention and clinical remission in axial spondyloarthritis. Rheumatology (Oxford) 2022;61:4741-51.
- Glintborg B, Ostergaard M, Krogh NS, et al. Predictors of treatment response and drug continuation in 842 patients with ankylosing spondylitis treated with anti-tumour necrosis factor: results from 8 years’ surveillance in the Danish nationwide DANBIO registry. Ann Rheum Dis 2010;69:2002-8.
- Sepriano A, Ramiro S, van der Heijde D, et al. Effect of Comedication With Conventional Synthetic Disease-Modifying Antirheumatic Drugs on Retention of Tumor Necrosis Factor Inhibitors in Patients With Spondyloarthritis: A Prospective Cohort Study. Arthritis & rheumatology 2016;68:2671-9.
- van der Heijde D, Landewe R, Baraliakos X, et al. Radiographic findings following two years of infliximab therapy in patients with ankylosing spondylitis. Arthritis Rheum 2008;58:3063-70.
- van der Heijde D, Landewe R, Einstein S, et al. Radiographic progression of ankylosing spondylitis after up to two years of treatment with etanercept. Arthritis Rheum 2008;58:1324-31.
- van der Heijde D, Salonen D, Weissman BN, et al. Assessment of radiographic progression in the spines of patients with ankylosing spondylitis treated with adalimumab for up to 2 years. Arthritis Res Ther 2009;11:R127.
- Haroon N, Inman RD, Learch TJ, et al. The impact of tumor necrosis factor alpha inhibitors on radiographic progression in ankylosing spondylitis. Arthritis Rheum 2013;65:2645-54.
- Molnar C, Scherer A, Baraliakos X, et al. TNF blockers inhibit spinal radiographic progression in ankylosing spondylitis by reducing disease activity: results from the Swiss Clinical Quality Management cohort. Ann Rheum Dis 2018;77:63-9.
- Maas F, Arends S, Brouwer E, et al. Reduction in Spinal Radiographic Progression in Ankylosing Spondylitis Patients Receiving Prolonged Treatment With Tumor Necrosis Factor Inhibitors. Arthritis Care Res (Hoboken) 2017;69:1011-9.
- Sari I, Lee S, Tomlinson G, et al. Factors Predictive of Radiographic Progression in Ankylosing Spondylitis. Arthritis Care Res (Hoboken) 2021;73:275-81.
- van der Heijde D, Baraliakos X, Hermann KA, et al. Limited radiographic progression and sustained reductions in MRI inflammation in patients with axial spondyloarthritis: 4-year imaging outcomes from the RAPID-axSpA phase III randomised trial. Ann Rheum Dis 2018;77:699-705.
- Karmacharya P, Duarte-Garcia A, Dubreuil M, et al. Effect of Therapy on Radiographic Progression in Axial Spondyloarthritis: A Systematic Review and Meta-Analysis. Arthritis Rheumatol 2020;72:733-49.
- Park JW, Kim MJ, Lee JS, et al. Impact of Tumor Necrosis Factor Inhibitor Versus Nonsteroidal Antiinflammatory Drug Treatment on Radiographic Progression in Early Ankylosing Spondylitis: Its Relationship to Inflammation Control During Treatment. Arthritis Rheumatol 2019;71:82-90.
- Torgutalp M, Rios Rodriguez V, Dilbaryan A, et al. Treatment with tumour necrosis factor inhibitors is associated with a time-shifted retardation of radiographic spinal progression in patients with axial spondyloarthritis. Ann Rheum Dis 2022;81:1252-9.
- Boers N, Michielsens CAJ, van der Heijde D, et al. The effect of tumour necrosis factor inhibitors on radiographic progression in axial spondyloarthritis: a systematic literature review. Rheumatology (Oxford) 2019;58:1907-22.
- Baraliakos X, Davis J, Tsuji W, et al. Magnetic resonance imaging examinations of the spine in patients with ankylosing spondylitis before and after therapy with the tumor necrosis factor alpha receptor fusion protein etanercept. Arthritis Rheum 2005;52:1216-23.
- Braun J, Landewe R, Hermann KG, et al. Major reduction in spinal inflammation in patients with ankylosing spondylitis after treatment with infliximab: results of a multicenter, randomized, double-blind, placebo-controlled magnetic resonance imaging study. Arthritis Rheum 2006;54:1646-52.
- Lambert RG, Salonen D, Rahman P, et al. Adalimumab significantly reduces both spinal and sacroiliac joint inflammation in patients with ankylosing spondylitis: a multicenter, randomized, double-blind, placebo-controlled study. Arthritis Rheum 2007;56:4005-14.
- Baraliakos X, Ostergaard M, Poddubnyy D, et al. Effect of Secukinumab Versus Adalimumab Biosimilar on Radiographic Progression in Patients With Radiographic Axial Spondyloarthritis: Results From a Head-to-Head Randomized Phase IIIb Study. Arthritis Rheumatol 2024;76:1278-87.
- Dougados M, Maksymowych WP, Landewe RBM, et al. Evaluation of the change in structural radiographic sacroiliac joint damage after 2 years of etanercept therapy (EMBARK trial) in comparison to a contemporary control cohort (DESIR cohort) in recent onset axial spondyloarthritis. Ann Rheum Dis 2018;77:221-7.
- Braun J, Haibel H, de Hooge M, et al. Spinal radiographic progression over 2 years in ankylosing spondylitis patients treated with secukinumab: a historical cohort comparison. Arthritis Res Ther 2019;21:142.
- Deodhar A, Blanco R, Dokoupilova E, et al. Improvement of Signs and Symptoms of Nonradiographic Axial Spondyloarthritis in Patients Treated With Secukinumab: Primary Results of a Randomized, Placebo-Controlled Phase III Study. Arthritis Rheumatol 2021;73:110-20.
- Deodhar A, Poddubnyy D, Pacheco-Tena C, et al. Efficacy and Safety of Ixekizumab in the Treatment of Radiographic Axial Spondyloarthritis: Sixteen-Week Results From a Phase III Randomized, Double-Blind, Placebo-Controlled Trial in Patients With Prior Inadequate Response to or Intolerance of Tumor Necrosis Factor Inhibitors. Arthritis Rheumatol 2019;71:599-611.
- Deodhar A, van der Heijde D, Gensler LS, et al. Ixekizumab for patients with non-radiographic axial spondyloarthritis (COAST-X): a randomised, placebo-controlled trial. Lancet 2020;395:53-64.
- van der Heijde D, Deodhar A, Baraliakos X, et al. Efficacy and safety of bimekizumab in axial spondyloarthritis: results of two parallel phase 3 randomised controlled trials. Ann Rheum Dis 2023;82:515-26.
- Baeten D, Sieper J, Braun J, et al. Secukinumab, an Interleukin-17A Inhibitor, in Ankylosing Spondylitis. N Engl J Med 2015;373:2534-48.
- Sieper J, Deodhar A, Marzo-Ortega H, et al. Secukinumab efficacy in anti-TNF-naive and anti-TNF-experienced subjects with active ankylosing spondylitis: results from the MEASURE 2 Study. Ann Rheum Dis 2017;76:571-92.
- Deodhar A, Kivitz AJ, Magrey M, et al. A secukinumab dose-escalation study in patients with ankylosing spondylitis not achieving inactive disease after 16 weeks of treatment. Rheumatology (Oxford) 2025;64:1864-72.
- Dougados M, Wei JC, Landewe R, et al. Efficacy and safety of ixekizumab through 52 weeks in two phase 3, randomised, controlled clinical trials in patients with active radiographic axial spondyloarthritis (COAST-V and COAST-W). Ann Rheum Dis 2020;79:176-85.
- van der Heijde D, Song IH, Pangan AL, et al. Efficacy and safety of upadacitinib in patients with active ankylosing spondylitis (SELECT-AXIS 1): a multicentre, randomised, double-blind, placebo-controlled, phase 2/3 trial. Lancet 2019;394:2108-17.
- van der Heijde D, Deodhar A, Wei JC, et al. Tofacitinib in patients with ankylosing spondylitis: a phase II, 16-week, randomised, placebo-controlled, dose-ranging study. Ann Rheum Dis 2017;76:1340-7.
- Ostergaard M, Wu J, Fallon L, et al. Tofacitinib Reduces Spinal Inflammation in Vertebral Bodies and Posterolateral Elements in Ankylosing Spondylitis: Results from a Phase 2 Trial. Rheumatol Ther 2023;10:1001-20.
- Deodhar A, Van den Bosch F, Poddubnyy D, et al. Upadacitinib for the treatment of active non-radiographic axial spondyloarthritis (SELECT-AXIS 2): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2022;400:369-79.
- van der Heijde D, Baraliakos X, Sieper J, et al. Efficacy and safety of upadacitinib for active ankylosing spondylitis refractory to biological therapy: a double-blind, randomised, placebo-controlled phase 3 trial. Ann Rheum Dis 2022;81:1515-23.
- Deodhar A, Sliwinska-Stanczyk P, Xu H, et al. Tofacitinib for the treatment of ankylosing spondylitis: a phase III, randomised, double-blind, placebo-controlled study. Ann Rheum Dis 2021.
- Min HK, Kim HR, Lee SH, et al. Retention rate and effectiveness of secukinumab vs TNF inhibitor in ankylosing spondylitis patients with prior TNF inhibitor exposure. Rheumatology (Oxford) 2021;60:5743-52.
- Min HK, Kim HR, Lee SH, et al. Clinical efficacy of alternative TNF inhibitor and secukinumab between primary non-responder and secondary non-responder of prior TNF inhibitor in ankylosing spondylitis. Mod Rheumatol 2023;33:194-201.
- Glintborg B, Lindstrom U, Giuseppe DD, et al. One-Year Treatment Outcomes of Secukinumab Versus Tumor Necrosis Factor Inhibitors in Spondyloarthritis: Results From Five Nordic Biologic Registries Including More Than 10,000 Treatment Courses. Arthritis Care Res (Hoboken) 2022;74:748-58.
- Micheroli R, Tellenbach C, Scherer A, et al. Effectiveness of secukinumab versus an alternative TNF inhibitor in patients with axial spondyloarthritis previously exposed to TNF inhibitors in the Swiss Clinical Quality Management cohort. Ann Rheum Dis 2020;79:1203-9.
- van Es I, Vriezekolk JE, den Broeder N, et al. Cycle versus swap strategy after TNFi discontinuation in psoriatic arthritis and axial spondyloarthritis: a quasi-experimental study. RMD Open 2025;11.
- Kiltz U, van der Heijde D, Boonen A, et al. Measurement properties of the ASAS Health Index: results of a global study in patients with axial and peripheral spondyloarthritis. Ann Rheum Dis 2018;77:1311-7.
- Navarro-Compan V, Boel A, Boonen A, et al. The ASAS-OMERACT core domain set for axial spondyloarthritis. Semin Arthritis Rheum 2021;51:1342-9.
- Feldthusen C, Hallstrom M, d’Elia A, et al. The ASAS Health Index and Environmental Factors Item Set: validity and reliability of the Swedish translations in Swedish patients with ankylosing spondylitis. Scand J Rheumatol 2024;53:104-11.
- Lukas C, Landewe R, Sieper J, et al. Development of an ASAS-endorsed disease activity score (ASDAS) in patients with ankylosing spondylitis. Ann Rheum Dis 2009;68:18-24.
- Machado P, Landewe R, Lie E, et al. Ankylosing Spondylitis Disease Activity Score (ASDAS): defining cut-off values for disease activity states and improvement scores. Ann Rheum Dis 2011;70:47-53.
- Smolen JS, Braun J, Dougados M, et al. Treating spondyloarthritis, including ankylosing spondylitis and psoriatic arthritis, to target: recommendations of an international task force. Ann Rheum Dis 2014;73:6-16.
- Kiltz U, van der Heijde D, Boonen A, et al. Development of a health index in patients with ankylosing spondylitis (ASAS HI): final result of a global initiative based on the ICF guided by ASAS. Ann Rheum Dis 2015;74:830-5.
- Molto A, Lopez-Medina C, Van den Bosch FE, et al. Efficacy of a tight-control and treat-to-target strategy in axial spondyloarthritis: results of the open-label, pragmatic, cluster-randomised TICOSPA trial. Ann Rheum Dis 2021;80:1436-44.
- Landewe R, Sieper J, Mease P, et al. Efficacy and safety of continuing versus withdrawing adalimumab therapy in maintaining remission in patients with non-radiographic axial spondyloarthritis (ABILITY-3): a multicentre, randomised, double-blind study. Lancet 2018;392:134-44.
- Landewe RB, van der Heijde D, Dougados M, et al. Maintenance of clinical remission in early axial spondyloarthritis following certolizumab pegol dose reduction. Ann Rheum Dis 2020;79:920-8.
- Michielsens CA, den Broeder N, van den Hoogen FH, et al. Treat-to-target dose reduction and withdrawal strategy of TNF inhibitors in psoriatic arthritis and axial spondyloarthritis: a randomised controlled non-inferiority trial. Ann Rheum Dis 2022;81:1392-9.
- Uhrenholt L, Christensen R, Dreyer L, et al. Disease activity-guided tapering of biologics in patients with inflammatory arthritis: a pragmatic, randomized, open-label, equivalence trial. Scand J Rheumatol 2023;52:481-92.
- Ruwaard J, MJ LA, Kneepkens EL, et al. Interval prolongation of etanercept in rheumatoid arthritis, ankylosing spondylitis, and psoriatic arthritis: a randomized controlled trial. Scand J Rheumatol 2023;52:129-36.
- 1Navarro-Compan V, Plasencia-Rodriguez C, de Miguel E, et al. Anti-TNF discontinuation and tapering strategies in patients with axial spondyloarthritis: a systematic literature review. Rheumatology (Oxford) 2016;55:1188-94.
- Cantini F, Niccoli L, Cassara E, et al. Duration of remission after halving of the etanercept dose in patients with ankylosing spondylitis: a randomized, prospective, long-term, follow-up study. Biologics : targets & therapy 2013;7:1-6.
- 122 Damiani A, Bartoli F, Pacini G, et al. Persistence of remission after lengthening of golimumab in inflammatory joint diseases. Clin Exp Rheumatol 2023;41:1088-95.
- 123 Landewe RB, Gensler LS, Poddubnyy D, et al. Continuing versus withdrawing ixekizumab treatment in patients with axial spondyloarthritis who achieved remission: efficacy and safety results from a placebo-controlled, randomised withdrawal study (COAST-Y). Ann Rheum Dis 2021;80:1022-30.
- 124 Landewe RBM, Poddubnyy D, Rahman P, et al. Recapture and retreatment rates with ixekizumab after withdrawal of therapy in patients with axial spondyloarthritis: results at week 104 from a randomised placebo-controlled withdrawal study. Ann Rheum Dis 2023;82:212-6.
- 125 Ritchlin CT, Colbert RA, Gladman DD. Psoriatic Arthritis. N Engl J Med 2017;376:2095-6.
- 126 Alinaghi F, Calov M, Kristensen LE, et al. Prevalence of psoriatic arthritis in patients with psoriasis: A systematic review and meta-analysis of observational and clinical studies. J Am Acad Dermatol 2019;80:251-65 e19.
- 127 Exarchou S, Wallman JK, Di Giuseppe D, et al. The National Prevalence of Clinically Diagnosed Psoriatic Arthritis in Sweden in 2017. J Rheumatol 2023;50:781-8.
- 128 Taylor W, Gladman D, Helliwell P, et al. Classification criteria for psoriatic arthritis: development of new criteria from a large international study. Arthritis Rheum 2006;54:2665-73.
- 129 Lindqvist UR, Alenius GM, Husmark T, et al. The Swedish early psoriatic arthritis register– 2-year followup: a comparison with early rheumatoid arthritis. J Rheumatol 2008;35:668-73.
- 130 Theander E, Husmark T, Alenius GM, et al. Early psoriatic arthritis: short symptom duration, male gender and preserved physical functioning at presentation predict favourable outcome at 5-year follow-up. Results from the Swedish Early Psoriatic Arthritis Register (SwePsA). Ann Rheum Dis 2014;73:407-13.
- 131 Helliwell PS, Ruderman EM. Natural History, Prognosis, and Socioeconomic Aspects of Psoriatic Arthritis. Rheum Dis Clin North Am 2015;41:581-91.
- 132 Bond SJ, Farewell VT, Schentag CT, et al. Predictors for radiological damage in psoriatic arthritis: results from a single centre. Ann Rheum Dis 2007;66:370-6.
- 133 Ritchlin CT, Kavanaugh A, Gladman DD, et al. Treatment recommendations for psoriatic arthritis. Ann Rheum Dis 2009;68:1387-94.
- 134 Gladman DD, Mease PJ, Choy EH, et al. Risk factors for radiographic progression in psoriatic arthritis: subanalysis of the randomized controlled trial ADEPT. Arthritis Res Ther 2010;12:R113.
- 135 Cresswell L, Chandran V, Farewell VT, et al. Inflammation in an individual joint predicts damage to that joint in psoriatic arthritis. Ann Rheum Dis 2011;70:305-8.
- 136 Gossec L, Baraliakos X, Kerschbaumer A, et al. EULAR recommendations for the management of psoriatic arthritis with pharmacological therapies: 2019 update. Ann Rheum Dis 2020;79:700-12.
- 137 Brockbank JE, Stein M, Schentag CT, et al. Dactylitis in psoriatic arthritis: a marker for disease severity? Ann Rheum Dis 2005;64:188-90.
- 138 Geijer M, Lindqvist U, Husmark T, et al. The Swedish Early Psoriatic Arthritis Registry 5-year Followup: Substantial Radiographic Progression Mainly in Men with High Disease Activity and Development of Dactylitis. J Rheumatol 2015;42:2110-7.
- 139 El Miedany Y, El Gaafary M, Youssef S, et al. Tailored approach to early psoriatic arthritis patients: clinical and ultrasonographic predictors for structural joint damage. Clin Rheumatol 2015;34:307-13.
- 140 Haroon M, Gallagher P, FitzGerald O. Diagnostic delay of more than 6 months contributes to poor radiographic and functional outcome in psoriatic arthritis. Ann Rheum Dis 2015;74:1045-50.
- 141 Snoeck Henkemans SVJ, de Jong PHP, Luime JJ, et al. Window of opportunity in psoriatic arthritis: the earlier the better? RMD Open 2024;10.
- 142 Kavanaugh A, Coates LC, van der Windt DA, et al. GRAPPA Treatment Recommendations: Updates and Methods. J Rheumatol Suppl 2020;96:41-5.
- 143 Gossec L, Smolen JS, Ramiro S, et al. European League Against Rheumatism (EULAR) recommendations for the management of psoriatic arthritis with pharmacological therapies: 2015 update. Ann Rheum Dis 2016;75:499-510.
- 144 Girolimetto N, Macchioni P, Citriniti G, et al. Effectiveness of steroid injection for hand psoriatic dactylitis: results from a multicentre prospective observational study. Clin Rheumatol 2020;39:3383-92.
- 145 Kingsley GH, Kowalczyk A, Taylor H, et al. A randomized placebo-controlled trial of methotrexate in psoriatic arthritis. Rheumatology (Oxford) 2012;51:1368-77.
- 146 Clegg DO, Reda DJ, Mejias E, et al. Comparison of sulfasalazine and placebo in the treatment of psoriatic arthritis. A Department of Veterans Affairs Cooperative Study. Arthritis Rheum 1996;39:2013-20.
- 147 Ye W, Coates LC. Should Methotrexate Have Any Place in the Treatment of Psoriatic Arthritis? Rheum Dis Clin North Am 2019;45:325-39.
- 148 Baranauskaite A, Raffayova H, Kungurov NV, et al. Infliximab plus methotrexate is superior to methotrexate alone in the treatment of psoriatic arthritis in methotrexate-naive patients: the RESPOND study. Ann Rheum Dis 2012;71:541-8.
- 149 Mease PJ, Gladman DD, Collier DH, et al. Etanercept and Methotrexate as Monotherapy or in Combination for Psoriatic Arthritis: Primary Results From a Randomized, Controlled Phase III Trial. Arthritis Rheumatol 2019;71:1112-24.
- 150 van Mens LJJ, de Jong HM, Fluri I, et al. Achieving remission in psoriatic arthritis by early initiation of TNF inhibition: a double-blind, randomised, placebo-controlled trial of golimumab plus methotrexate versus placebo plus methotrexate. Ann Rheum Dis 2019;78:610-6.
- 151 Willkens RF, Williams HJ, Ward JR, et al. Randomized, double-blind, placebo controlled trial of low-dose pulse methotrexate in psoriatic arthritis. Arthritis Rheum 1984;27:376-81.
- 152 Lacaille D, Stein HB, Raboud J, et al. Longterm therapy of psoriatic arthritis: intramuscular gold or methotrexate? J Rheumatol 2000;27:1922-7.
- 153 Scarpa R, Peluso R, Atteno M, et al. The effectiveness of a traditional therapeutical approach in early psoriatic arthritis: results of a pilot randomised 6-month trial with methotrexate. Clin Rheumatol 2008;27:823-6.
- 154 Appani SK, Devarasetti PK, Irlapati RVP, et al. Methotrexate achieves major cDAPSA response, and improvement in dactylitis and functional status in psoriatic arthritis. Rheumatology (Oxford) 2019;58:869-73.
- 155 Grubisic F. Is methotrexate effective and safe in patients with psoriatic arthritis? A Cochrane Review summary with commentary. Int J Rheum Dis 2021;24:132-4.
- 156 Lie E, van der Heijde D, Uhlig T, et al. Effectiveness and retention rates of methotrexate in psoriatic arthritis in comparison with methotrexate-treated patients with rheumatoid arthritis. Ann Rheum Dis 2010;69:671-6.
- 157 Lindstrom U, di Giuseppe D, Exarchou S, et al. Methotrexate treatment in early psoriatic arthritis in comparison to rheumatoid arthritis: an observational nationwide study. RMD Open 2023;9.
- 158 Coates LC, Moverley AR, McParland L, et al. Effect of tight control of inflammation in early psoriatic arthritis (TICOPA): a UK multicentre, open-label, randomised controlled trial. Lancet 2015;386:2489-98.
- 159 Kaltwasser JP, Nash P, Gladman D, et al. Efficacy and safety of leflunomide in the treatment of psoriatic arthritis and psoriasis: a multinational, double-blind, randomized, placebo-controlled clinical trial. Arthritis Rheum 2004;50:1939-50.
- 160 Ravindran V, Scott DL, Choy EH. A systematic review and meta-analysis of efficacy and toxicity of disease modifying anti-rheumatic drugs and biological agents for psoriatic arthritis. Ann Rheum Dis 2008;67:855-9.
- 161 Behrens F, Finkenwirth C, Pavelka K, et al. Leflunomide in psoriatic arthritis: results from a large European prospective observational study. Arthritis Care Res (Hoboken) 2013;65:464-70.
- 162 Spadaro A, Riccieri V, Sili-Scavalli A, et al. Comparison of cyclosporin A and methotrexate in the treatment of psoriatic arthritis: a one-year prospective study. Clin Exp Rheumatol 1995;13:589-93.
- 163 Soriano A, Pipitone N, Salvarani C. Cyclosporine in psoriatic arthropathy. Clin Exp Rheumatol 2015;33:S101-3.
- 164 Svenska_Sällskapet_för_Dermatologi_och_Venerologi. SSDV:s behandlingsrekommendationer för systemisk behandling av psoriasis (2024-04-15). 2024.
- 165 Mushtaq S, Sarkar R. Sulfasalazine in dermatology: A lesser explored drug with broad therapeutic potential. Int J Womens Dermatol 2020;6:191-8.
- 166 Mulder MLM, Vriezekolk JE, van Hal TW, et al. Comparing methotrexate monotherapy with methotrexate plus leflunomide combination therapy in psoriatic arthritis (COMPLETE-PsA): a double-blind, placebo-controlled, randomised, trial. Lancet Rheumatol 2022;4:e252-61.
- 167 Fraser AD, van Kuijk AW, Westhovens R, et al. A randomised, double blind, placebo controlled, multicentre trial of combination therapy with methotrexate plus ciclosporin in patients with active psoriatic arthritis. Ann Rheum Dis 2005;64:859-64.
- 168 Mease PJ, Kivitz AJ, Burch FX, et al. Etanercept treatment of psoriatic arthritis: safety, efficacy, and effect on disease progression. Arthritis Rheum 2004;50:2264-72.
- 169 Antoni C, Krueger GG, de Vlam K, et al. Infliximab improves signs and symptoms of psoriatic arthritis: results of the IMPACT 2 trial. Ann Rheum Dis 2005;64:1150-7.
- 170 Mease PJ, Gladman DD, Ritchlin CT, et al. Adalimumab for the treatment of patients with moderately to severely active psoriatic arthritis: results of a double-blind, randomized, placebo-controlled trial. Arthritis Rheum 2005;52:3279-89.
- 171 Kavanaugh A, McInnes I, Mease P, et al. Golimumab, a new human tumor necrosis factor alpha antibody, administered every four weeks as a subcutaneous injection in psoriatic arthritis: Twenty-four-week efficacy and safety results of a randomized, placebo-controlled study. Arthritis Rheum 2009;60:976-86.
- 172 Mease PJ, Fleischmann R, Deodhar AA, et al. Effect of certolizumab pegol on signs and symptoms in patients with psoriatic arthritis: 24-week results of a Phase 3 double-blind randomised placebo-controlled study (RAPID-PsA). Ann Rheum Dis 2014;73:48-55.
- 173 Saad AA, Symmons DP, Noyce PR, et al. Risks and benefits of tumor necrosis factor-alpha inhibitors in the management of psoriatic arthritis: systematic review and metaanalysis of randomized controlled trials. J Rheumatol 2008;35:883-90.
- 174 Lemos LL, de Oliveira Costa J, Almeida AM, et al. Treatment of psoriatic arthritis with anti-TNF agents: a systematic review and meta-analysis of efficacy, effectiveness and safety. Rheumatol Int 2014;34:1345-60.
- 175 van der Heijde D, Kavanaugh A, Gladman DD, et al. Infliximab inhibits progression of radiographic damage in patients with active psoriatic arthritis through one year of treatment: Results from the induction and maintenance psoriatic arthritis clinical trial 2. Arthritis Rheum 2007;56:2698-707.
- 176 Kavanaugh A, van der Heijde D, McInnes IB, et al. Golimumab in psoriatic arthritis: one-year clinical efficacy, radiographic, and safety results from a phase III, randomized, placebo-controlled trial. Arthritis Rheum 2012;64:2504-17.
- 177 van der Heijde D, Fleischmann R, Wollenhaupt J, et al. Effect of different imputation approaches on the evaluation of radiographic progression in patients with psoriatic arthritis: results of the RAPID-PsA 24-week phase III double-blind randomised placebo-controlled study of certolizumab pegol. Ann Rheum Dis 2014;73:233-7.
- 178 Svenska_Sällskapet_för_Dermatologi_och_Venerologi. SSDV:s behandlingsrekommendationer för systemisk behandling av psoriasis (2022-05-25). 2022.
- 179 Glintborg B, Gudbjornsson B, Krogh NS, et al. Impact of different infliximab dose regimens on treatment response and drug survival in 462 patients with psoriatic arthritis: results from the nationwide registries DANBIO and ICEBIO. Rheumatology (Oxford) 2014;53:2100-9.
- 180 Behrens F, Canete JD, Olivieri I, et al. Tumour necrosis factor inhibitor monotherapy vs combination with MTX in the treatment of PsA: a systematic review of the literature. Rheumatology (Oxford) 2015;54:915-26.
- 181 Lindstrom U, Di Giuseppe D, Delcoigne B, et al. Effectiveness and treatment retention of TNF inhibitors when used as monotherapy versus comedication with csDMARDs in 15 332 patients with psoriatic arthritis. Data from the EuroSpA collaboration. Ann Rheum Dis 2021;80:1410-8.
- 182 Kristensen LE, Gulfe A, Saxne T, et al. Efficacy and tolerability of anti-tumour necrosis factor therapy in psoriatic arthritis patients: results from the South Swedish Arthritis Treatment Group register. Ann Rheum Dis 2008;67:364-9.
- 183 Fagerli KM, Lie E, van der Heijde D, et al. The role of methotrexate co-medication in TNF-inhibitor treatment in patients with psoriatic arthritis: results from 440 patients included in the NOR-DMARD study. Ann Rheum Dis 2014;73:132-7.
- 184 Thomas ML, Shaddick G, Charlton R, et al. Tumor Necrosis Factor Inhibitor Monotherapy Versus Combination Therapy for the Treatment of Psoriatic Arthritis: Combined Analysis of European Biologics Databases. J Rheumatol 2021;48:48-57.
- 185 Hanna S, Dujardin T, Gaudin P, et al. bDMARD drug survival in combination therapy with methotrexate in psoriatic arthritis: A systematic literature review and meta-analysis. Joint Bone Spine 2025;92:105854.
- 186 Regierer AC, Kiefer D, Schett G, et al. No difference in clinical parameters and drug retention in PsA patients receiving b/tsDMARD monotherapy versus combination with methotrexate: data from the RABBIT-SpA registry. RMD Open 2024;10.
- 187 Eder L, Thavaneswaran A, Chandran V, et al. Tumour necrosis factor alpha blockers are more effective than methotrexate in the inhibition of radiographic joint damage progression among patients with psoriatic arthritis. Ann Rheum Dis 2014;73:1007-11.
- 188 Mease PJ, McInnes IB, Kirkham B, et al. Secukinumab Inhibition of Interleukin-17A in Patients with Psoriatic Arthritis. N Engl J Med 2015;373:1329-39.
- 189 Mease PJ, van der Heijde D, Ritchlin CT, et al. Ixekizumab, an interleukin-17A specific monoclonal antibody, for the treatment of biologic-naive patients with active psoriatic arthritis: results from the 24-week randomised, double-blind, placebo-controlled and active (adalimumab)-controlled period of the phase III trial SPIRIT-P1. Ann Rheum Dis 2017;76:79-87.
- 190 McInnes IB, Asahina A, Coates LC, et al. Bimekizumab in patients with psoriatic arthritis, naive to biologic treatment: a randomised, double-blind, placebo-controlled, phase 3 trial (BE OPTIMAL). Lancet 2023;401:25-37.
- 191 McInnes IB, Mease PJ, Kirkham B, et al. Secukinumab, a human anti-interleukin-17A monoclonal antibody, in patients with psoriatic arthritis (FUTURE 2): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2015;386:1137-46.
- 192 McInnes IB, Behrens F, Mease PJ, et al. Secukinumab versus adalimumab for treatment of active psoriatic arthritis (EXCEED): a double-blind, parallel-group, randomised, active-controlled, phase 3b trial. Lancet 2020;395:1496-505.
- 193 Baraliakos X, Gossec L, Pournara E, et al. Secukinumab in patients with psoriatic arthritis and axial manifestations: results from the double-blind, randomised, phase 3 MAXIMISE trial. Ann Rheum Dis 2021;80:582-90.
- 194 Nash P, Kirkham B, Okada M, et al. Ixekizumab for the treatment of patients with active psoriatic arthritis and an inadequate response to tumour necrosis factor inhibitors: results from the 24-week randomised, double-blind, placebo-controlled period of the SPIRIT-P2 phase 3 trial. Lancet 2017;389:2317-27.
- 195 Mease PJ, Smolen JS, Behrens F, et al. A head-to-head comparison of the efficacy and safety of ixekizumab and adalimumab in biological-naive patients with active psoriatic arthritis: 24-week results of a randomised, open-label, blinded-assessor trial. Ann Rheum Dis 2020;79:123-31.
- 196 McGonagle D, Kavanaugh A, McInnes IB, et al. Association of the clinical components in the distal interphalangeal joint synovio-entheseal complex and subsequent response to ixekizumab or adalimumab in psoriatic arthritis. Rheumatology (Oxford) 2024;63:3115-23.
- 197 Coates LC, Kishimoto M, Gottlieb A, et al. Ixekizumab efficacy and safety with and without concomitant conventional disease-modifying antirheumatic drugs (cDMARDs) in biologic DMARD (bDMARD)-naive patients with active psoriatic arthritis (PsA): results from SPIRIT-P1. RMD open 2017;3:e000567.
- 198 Nash P, Behrens F, Orbai AM, et al. Ixekizumab is efficacious when used alone or when added to conventional synthetic disease-modifying antirheumatic drugs (cDMARDs) in patients with active psoriatic arthritis and previous inadequate response or intolerance to tumour necrosis factor inhibitors. RMD open 2018;4:e000692.
- 199 Merola JF, Landewe R, McInnes IB, et al. Bimekizumab in patients with active psoriatic arthritis and previous inadequate response or intolerance to tumour necrosis factor-alpha inhibitors: a randomised, double-blind, placebo-controlled, phase 3 trial (BE COMPLETE). Lancet 2023;401:38-48.
- 200 McInnes IB, Mease PJ, Tanaka Y, et al. Efficacy and Safety of Bimekizumab in Patients With Psoriatic Arthritis With or Without Methotrexate: 52-Week Results From Two Phase 3 Studies. ACR Open Rheumatol 2024;6:720-31.
- 201 Mease PJ, Ritchlin CT, Coates LC, et al. Inhibition of structural damage progression with the selective interleukin-23 inhibitor guselkumab in participants with active PsA: results through week 24 of the phase 3b, randomised, double-blind, placebo-controlled APEX study. Ann Rheum Dis 2025.
- 202 Deodhar A, Helliwell PS, Boehncke WH, et al. Guselkumab in patients with active psoriatic arthritis who were biologic-naive or had previously received TNFalpha inhibitor treatment (DISCOVER-1): a double-blind, randomised, placebo-controlled phase 3 trial. Lancet 2020;395:1115-25.
- 203 Mease PJ, Rahman P, Gottlieb AB, et al. Guselkumab in biologic-naive patients with active psoriatic arthritis (DISCOVER-2): a double-blind, randomised, placebo-controlled phase 3 trial. Lancet 2020;395:1126-36.
- 204 Kristensen LE, Keiserman M, Papp K, et al. Efficacy and safety of risankizumab for active psoriatic arthritis: 24-week results from the randomised, double-blind, phase 3 KEEPsAKE 1 trial. Ann Rheum Dis 2022;81:225-31.
- 205 Ostor A, Van den Bosch F, Papp K, et al. Efficacy and safety of risankizumab for active psoriatic arthritis: 24-week results from the randomised, double-blind, phase 3 KEEPsAKE 2 trial. Ann Rheum Dis 2022;81:351-8.
- 206 Coates LC, Gossec L, Theander E, et al. Efficacy and safety of guselkumab in patients with active psoriatic arthritis who are inadequate responders to tumour necrosis factor inhibitors: results through one year of a phase IIIb, randomised, controlled study (COSMOS). Ann Rheum Dis 2022;81:359-69.
- 207 McInnes IB, Kavanaugh A, Gottlieb AB, et al. Efficacy and safety of ustekinumab in patients with active psoriatic arthritis: 1 year results of the phase 3, multicentre, double-blind, placebo-controlled PSUMMIT 1 trial. Lancet 2013;382:780-9.
- 208 Ritchlin C, Rahman P, Kavanaugh A, et al. Efficacy and safety of the anti-IL-12/23 p40 monoclonal antibody, ustekinumab, in patients with active psoriatic arthritis despite conventional non-biological and biological anti-tumour necrosis factor therapy: 6-month and 1-year results of the phase 3, multicentre, double-blind, placebo-controlled, randomised PSUMMIT 2 trial. Ann Rheum Dis 2014;73:990-9.
- 209 Kavanaugh A, Ritchlin C, Rahman P, et al. Ustekinumab, an anti-IL-12/23 p40 monoclonal antibody, inhibits radiographic progression in patients with active psoriatic arthritis: results of an integrated analysis of radiographic data from the phase 3, multicentre, randomised, double-blind, placebo-controlled PSUMMIT-1 and PSUMMIT-2 trials. Ann Rheum Dis 2014;73:1000-6.
- 210 Araujo EG, Englbrecht M, Hoepken S, et al. Effects of ustekinumab versus tumor necrosis factor inhibition on enthesitis: Results from the enthesial clearance in psoriatic arthritis (ECLIPSA) study. Semin Arthritis Rheum 2019;48:632-7.
- 211 Mease P, Genovese MC, Gladstein G, et al. Abatacept in the treatment of patients with psoriatic arthritis: results of a six-month, multicenter, randomized, double-blind, placebo-controlled, phase II trial. Arthritis Rheum 2011;63:939-48.
- 212 Mease PJ, Gottlieb AB, van der Heijde D, et al. Efficacy and safety of abatacept, a T-cell modulator, in a randomised, double-blind, placebo-controlled, phase III study in psoriatic arthritis. Ann Rheum Dis 2017;76:1550-8.
- 213 Strand V, Alemao E, Lehman T, et al. Improved patient-reported outcomes in patients with psoriatic arthritis treated with abatacept: results from a phase 3 trial. Arthritis Res Ther 2018;20:269.
- 214 McInnes IB, Anderson JK, Magrey M, et al. Trial of Upadacitinib and Adalimumab for Psoriatic Arthritis. N Engl J Med 2021;384:1227-39.
- 215 Mease P, Hall S, FitzGerald O, et al. Tofacitinib or Adalimumab versus Placebo for Psoriatic Arthritis. N Engl J Med 2017;377:1537-50.
- 216 Gladman D, Rigby W, Azevedo VF, et al. Tofacitinib for Psoriatic Arthritis in Patients with an Inadequate Response to TNF Inhibitors. N Engl J Med 2017;377:1525-36.
- 217 Mease PJ, Lertratanakul A, Anderson JK, et al. Upadacitinib for psoriatic arthritis refractory to biologics: SELECT-PsA 2. Ann Rheum Dis 2021;80:312-20.
- 218 Nash P, Richette P, Gossec L, et al. Upadacitinib as monotherapy and in combination with non-biologic disease-modifying antirheumatic drugs for psoriatic arthritis. Rheumatology (Oxford) 2022;61:3257-68.
- 219 Kavanaugh A, Mease PJ, Gomez-Reino JJ, et al. Treatment of psoriatic arthritis in a phase 3 randomised, placebo-controlled trial with apremilast, an oral phosphodiesterase 4 inhibitor. Ann Rheum Dis 2014;73:1020-6.
- 220 Cutolo M, Myerson GE, Fleischmann RM, et al. A Phase III, Randomized, Controlled Trial of Apremilast in Patients with Psoriatic Arthritis: Results of the PALACE 2 Trial. J Rheumatol 2016;43:1724-34.
- 221 Edwards CJ, Blanco FJ, Crowley J, et al. Apremilast, an oral phosphodiesterase 4 inhibitor, in patients with psoriatic arthritis and current skin involvement: a phase III, randomised, controlled trial (PALACE 3). Ann Rheum Dis 2016;75:1065-73.
- 222 Wells AF, Edwards CJ, Kivitz AJ, et al. Apremilast monotherapy in DMARD-naive psoriatic arthritis patients: results of the randomized, placebo-controlled PALACE 4 trial. Rheumatology (Oxford) 2018;57:1253-63.
- 223 Nash P, Ohson K, Walsh J, et al. Early and sustained efficacy with apremilast monotherapy in biological-naive patients with psoriatic arthritis: a phase IIIB, randomised controlled trial (ACTIVE). Ann Rheum Dis 2018;77:690-8.
- 224 Gossec L, Coates LC, Gladman DD, et al. Treatment of early oligoarticular psoriatic arthritis with apremilast: primary outcomes at week 16 from the FOREMOST randomised controlled trial. Ann Rheum Dis 2024;83:1480-8.
- 225 Gyldenlove M, Alinaghi F, Zachariae C, et al. Combination Therapy with Apremilast and Biologics for Psoriasis: A Systematic Review. Am J Clin Dermatol 2022;23:605-13.
- 226 Smolen JS, Siebert S, Korotaeva TV, et al. Effectiveness of IL-12/23 inhibition (ustekinumab) versus tumour necrosis factor inhibition in psoriatic arthritis: observational PsABio study results. Ann Rheum Dis 2021;80:1419-28.
- 227 Zhang H, Wen J, Alexander GC, et al. Comparative effectiveness of biologics and targeted therapies for psoriatic arthritis. RMD Open 2021;7.
- 228 Lindstrom U, Glintborg B, Di Giuseppe D, et al. Comparison of treatment retention and response to secukinumab versus tumour necrosis factor inhibitors in psoriatic arthritis. Rheumatology (Oxford) 2021;60:3635-45.
- 229 Glintborg B, Di Giuseppe D, Wallman JK, et al. Uptake and effectiveness of newer biologic and targeted synthetic disease-modifying antirheumatic drugs in psoriatic arthritis: results from five Nordic biologics registries. Ann Rheum Dis 2023;82:820-8.
- 230 Guimaraes F, Ferreira M, Soares C, et al. Cycling versus swapping strategies in psoriatic arthritis: results from the rheumatic diseases Portuguese register. ARP Rheumatol 2023.
- 231 Pina Vegas L, Hoisnard L, Bastard L, et al. Long-term persistence of second-line biologics in psoriatic arthritis patients with prior TNF inhibitor exposure: a nationwide cohort study from the French health insurance database (SNDS). RMD Open 2022;8.
- 232 Hansen RL, Jorgensen TS, Egeberg A, et al. Adherence to therapy of ixekizumab and secukinumab in psoriatic arthritis patients using first- or second-line IL-17A inhibitor treatment: a Danish population-based cohort study. Rheumatology (Oxford) 2024;63:1593-8.
- 233 Schoels MM, Aletaha D, Alasti F, et al. Disease activity in psoriatic arthritis (PsA): defining remission and treatment success using the DAPSA score. Ann Rheum Dis 2016;75:811-8.
- 234 Aletaha D, Alasti F, Smolen JS. Disease activity states of the DAPSA, a psoriatic arthritis specific instrument, are valid against functional status and structural progression. Ann Rheum Dis 2017;76:418-21.
- 235 Healy PJ, Helliwell PS. Measuring clinical enthesitis in psoriatic arthritis: assessment of existing measures and development of an instrument specific to psoriatic arthritis. Arthritis Rheum 2008;59:686-91.
- 236 Coates LC, Fransen J, Helliwell PS. Defining minimal disease activity in psoriatic arthritis: a proposed objective target for treatment. Ann Rheum Dis 2010;69:48-53.
- 237 Coates LC, Helliwell PS. Validation of minimal disease activity criteria for psoriatic arthritis using interventional trial data. Arthritis Care Res (Hoboken) 2010;62:965-9.
- 238 Coates LC, Helliwell PS. Defining Low Disease Activity States in Psoriatic Arthritis using Novel Composite Disease Instruments. J Rheumatol 2016;43:371-5.
- 239 Finlay AY. Current severe psoriasis and the rule of tens. Br J Dermatol 2005;152:861-7.
- 240 Fredriksson T, Pettersson U. Severe psoriasis–oral therapy with a new retinoid. Dermatologica 1978;157:238-44.
- 241 Coates LC, Mahmood F, Freeston J, et al. Long-term follow-up of patients in the TIght COntrol of inflammation in early Psoriatic Arthritis (TICOPA) trial. Rheumatology (Oxford) 2020;59:807-10.
- 242 Fong W, Holroyd C, Davidson B, et al. The effectiveness of a real life dose reduction strategy for tumour necrosis factor inhibitors in ankylosing spondylitis and psoriatic arthritis. Rheumatology (Oxford) 2016;55:1837-42.
- 243 Cantini F, Niccoli L, Cassara E, et al. Sustained maintenance of clinical remission after adalimumab dose reduction in patients with early psoriatic arthritis: a long-term follow-up study. Biologics : targets & therapy 2012;6:201-6.
- 244 Huynh DH, Boyd TA, Etzel CJ, et al. Persistence of low disease activity after tumour necrosis factor inhibitor (TNFi) discontinuation in patients with psoriatic arthritis. RMD open 2017;3:e000395.
- 245 Harrold LR, Stolshek BS, Rebello S, et al. Rebound in Measures of Disease Activity and Symptoms in Corrona Registry Patients with Psoriatic Arthritis Who Discontinue Tumor Necrosis Factor Inhibitor Therapy after Achieving Low Disease Activity. J Rheumatol 2018;45:78-82.
- 246 Snoeck Henkemans SVJ, Vis M, Koc GH, et al. Disease-modifying antirheumatic drug-free remission in psoriatic arthritis: is it attainable and sustainable? A large longitudinal study. Ann Rheum Dis 2025;84:1130-9.
- 247 Araujo EG, Finzel S, Englbrecht M, et al. High incidence of disease recurrence after discontinuation of disease-modifying antirheumatic drug treatment in patients with psoriatic arthritis in remission. Ann Rheum Dis 2015;74:655-60.
- 248 Coates LC, Pillai SG, Tahir H, et al. Withdrawing Ixekizumab in Patients With Psoriatic Arthritis Who Achieved Minimal Disease Activity: Results From a Randomized, Double-Blind Withdrawal Study. Arthritis Rheumatol 2021;73:1663-72.
- 249 Rudwaleit M, van der Heijde D, Landewe R, et al. The Assessment of SpondyloArthritis International Society classification criteria for peripheral spondyloarthritis and for spondyloarthritis in general. Ann Rheum Dis 2011;70:25-31.
- 250 Gladman DD. Editorial: What is peripheral spondyloarthritis? Arthritis & rheumatology 2015;67:865-8.
- 251 Ziade N, Rassi J, Elzorkany B, et al. What is peripheral spondyloarthritis? Identifying proportion, phenotype and burden in post hoc analysis of the ASAS-PerSpA study. Semin Arthritis Rheum 2022;55:152012.
- 252 Mease P, Sieper J, Van den Bosch F, et al. Randomized controlled trial of adalimumab in patients with nonpsoriatic peripheral spondyloarthritis. Arthritis Rheumatol 2015;67:914-23.
- 253 Carron P, Varkas G, Cypers H, et al. Anti-TNF-induced remission in very early peripheral spondyloarthritis: the CRESPA study. Ann Rheum Dis 2017;76:1389-95.
- 254 Mease PJ, McInnes IB, Tam LS, et al. Comparative effectiveness of guselkumab in psoriatic arthritis: updates to a systematic literature review and network meta-analysis. Rheumatology (Oxford) 2023;62:1417-25.
- 255 Xie Y, Liu Y, Liu Y. Are biologics combined with methotrexate better than biologics monotherapy in psoriasis and psoriatic arthritis: A meta-analysis of randomized controlled trials. Dermatol Ther 2021;34:e14926.
- 256 Lie E, Lindstrom U, Zverkova-Sandstrom T, et al. Tumour necrosis factor inhibitor treatment and occurrence of anterior uveitis in ankylosing spondylitis: results from the Swedish biologics register. Ann Rheum Dis 2017;76:1515-21.
- 257 van Bentum RE, Heslinga SC, Nurmohamed MT, et al. Reduced Occurrence Rate of Acute Anterior Uveitis in Ankylosing Spondylitis Treated with Golimumab – The GO-EASY Study. J Rheumatol 2019;46:153-9.
- 258 Kim MJ, Lee EE, Lee EY, et al. Preventive effect of tumor necrosis factor inhibitors versus nonsteroidal anti-inflammatory drugs on uveitis in patients with ankylosing spondylitis. Clin Rheumatol 2018;37:2763-70.
- 259 van der Horst-Bruinsma I, van Bentum R, Verbraak FD, et al. The impact of certolizumab pegol treatment on the incidence of anterior uveitis flares in patients with axial spondyloarthritis: 48-week interim results from C-VIEW. RMD Open 2020;6.
- 260 Lindstrom U, Bengtsson K, Olofsson T, et al. Anterior uveitis in patients with spondyloarthritis treated with secukinumab or tumour necrosis factor inhibitors in routine care: does the choice of biological therapy matter? Ann Rheum Dis 2021;80:1445-52.
- 261 Brown MA, Rudwaleit M, van Gaalen FA, et al. Low uveitis rates in patients with axial spondyloarthritis treated with bimekizumab: pooled results from phase 2b/3 trials. Ann Rheum Dis 2024;83:1722-30.
- 262 Hueber W, Sands BE, Lewitzky S, et al. Secukinumab, a human anti-IL-17A monoclonal antibody, for moderate to severe Crohn’s disease: unexpected results of a randomised, double-blind placebo-controlled trial. Gut 2012;61:1693-700.
- 263 Targan SR, Feagan B, Vermeire S, et al. A Randomized, Double-Blind, Placebo-Controlled Phase 2 Study of Brodalumab in Patients With Moderate-to-Severe Crohn’s Disease. Am J Gastroenterol 2016;111:1599-607.
- 264 Coates LC, Helliwell PS. Methotrexate Efficacy in the Tight Control in Psoriatic Arthritis Study. J Rheumatol 2016;43:356-61.
- 265 Dougados M, vam der Linden S, Leirisalo-Repo M, et al. Sulfasalazine in the treatment of spondylarthropathy. A randomized, multicenter, double-blind, placebo-controlled study. Arthritis Rheum 1995;38:618-27.
- 266 Vieira-Sousa E, Alves P, Rodrigues AM, et al. GO-DACT: a phase 3b randomised, double-blind, placebo-controlled trial of GOlimumab plus methotrexate (MTX) versus placebo plus MTX in improving DACTylitis in MTX-naive patients with psoriatic arthritis. Ann Rheum Dis 2020;79:490-8.
- 267 Rose S, Toloza S, Bautista-Molano W, et al. Comprehensive treatment of dactylitis in psoriatic arthritis. J Rheumatol 2014;41:2295-300.
- 268 Nash P, Coates LC, Fleischmann R, et al. Efficacy of Tofacitinib for the Treatment of Psoriatic Arthritis: Pooled Analysis of Two Phase 3 Studies. Rheumatology and therapy 2018;5:567-82.
- 269 Mourad A, Gniadecki R. Treatment of Dactylitis and Enthesitis in Psoriatic Arthritis with Biologic Agents: A Systematic Review and Metaanalysis. J Rheumatol 2020;47:59-65.
- 270 Orbai AM, Weitz J, Siegel EL, et al. Systematic review of treatment effectiveness and outcome measures for enthesitis in psoriatic arthritis. J Rheumatol 2014;41:2290-4.
- 271 Kaeley GS, Schett G, Conaghan PG, et al. Enthesitis in patients with psoriatic arthritis treated with secukinumab or adalimumab: a post hoc analysis of the EXCEED study. Rheumatology (Oxford) 2024;63:41-9.
- 272 Terslev L, Naredo E, Iagnocco A, et al. Defining enthesitis in spondyloarthritis by ultrasound: results of a Delphi process and of a reliability reading exercise. Arthritis Care Res (Hoboken) 2014;66:741-8.
- 273 Balint PV, Terslev L, Aegerter P, et al. Reliability of a consensus-based ultrasound definition and scoring for enthesitis in spondyloarthritis and psoriatic arthritis: an OMERACT US initiative. Ann Rheum Dis 2018;77:1730-5.
- 274 Solomon DH, Glynn RJ, Karlson EW, et al. Adverse Effects of Low-Dose Methotrexate: A Randomized Trial. Ann Intern Med 2020;172:369-80.
- 275 Christensen IE, Lillegraven S, Mielnik P, et al. Serious infections in patients with rheumatoid arthritis and psoriatic arthritis treated with tumour necrosis factor inhibitors: data from register linkage of the NOR-DMARD study. Ann Rheum Dis 2022;81:398-401.
- 276 Li X, Andersen KM, Chang HY, et al. Comparative risk of serious infections among real-world users of biologics for psoriasis or psoriatic arthritis. Ann Rheum Dis 2020;79:285-91.
- 277 Reich K, Warren RB, Lebwohl M, et al. Bimekizumab versus Secukinumab in Plaque Psoriasis. N Engl J Med 2021;385:142-52.
- 278 Blauvelt A, Gooderham M, Iversen L, et al. Efficacy and safety of ixekizumab for the treatment of moderate-to-severe plaque psoriasis: Results through 108 weeks of a randomized, controlled phase 3 clinical trial (UNCOVER-3). J Am Acad Dermatol 2017;77:855-62.
- 279 Jin Y, Lee H, Lee MP, et al. Risk of Hospitalization for Serious Infection After Initiation of Ustekinumab or Other Biologics in Patients With Psoriasis or Psoriatic Arthritis. Arthritis Care Res (Hoboken) 2022;74:1792-805.
- 280 Bastard L, Claudepierre P, Penso L, et al. Risk of serious infection associated with different classes of targeted therapies used in psoriatic arthritis: a nationwide cohort study from the French Health Insurance Database (SNDS). RMD Open 2024;10.
- 281 Glintborg B, Di Giuseppe D, Wallman JK, et al. Is the risk of infection higher during treatment with secukinumab than with TNF inhibitors? An observational study from the Nordic countries. Rheumatology (Oxford) 2023;62:647-58.
- 282 Alharthy RF, Alharthy JM, Bawazir RO, et al. The Efficacy and Safety of Apremilast in the Management of Psoriatic Arthritis: A Systematic Review and Meta-Analysis. Cureus 2024;16:e55773.
- 283 Fleischmann R, Mysler E, Hall S, et al. Efficacy and safety of tofacitinib monotherapy, tofacitinib with methotrexate, and adalimumab with methotrexate in patients with rheumatoid arthritis (ORAL Strategy): a phase 3b/4, double-blind, head-to-head, randomised controlled trial. Lancet 2017;390:457-68.
- 284 Curtis JR, Xie F, Yun H, et al. Real-world comparative risks of herpes virus infections in tofacitinib and biologic-treated patients with rheumatoid arthritis. Ann Rheum Dis 2016;75:1843-7.
- 285 Chiu HY, Hung YT, Huang SW, et al. Comparative risk of herpes zoster in patients with psoriatic disease on systemic treatments: a systematic review and network meta-analysis. Ther Adv Chronic Dis 2022;13:20406223221091188.
- 286 Gray O, McDonnell GV, Forbes RB. Methotrexate for multiple sclerosis. Cochrane Database Syst Rev 2004:CD003208.
- 287 Noseworthy JH, O’Brien P, Erickson BJ, et al. The Mayo Clinic-Canadian Cooperative trial of sulfasalazine in active multiple sclerosis. Neurology 1998;51:1342-52.
- 288 O’Connor P, Wolinsky JS, Confavreux C, et al. Randomized trial of oral teriflunomide for relapsing multiple sclerosis. N Engl J Med 2011;365:1293-303.
- 289 Kopp TI, Delcoigne B, Arkema EV, et al. Risk of neuroinflammatory events in arthritis patients treated with tumour necrosis factor alpha inhibitors: a collaborative population-based cohort study from Denmark and Sweden. Ann Rheum Dis 2020;79:566-72.
- 290 Kunchok A, Aksamit AJ, Jr., Davis JM, 3rd, et al. Association Between Tumor Necrosis Factor Inhibitor Exposure and Inflammatory Central Nervous System Events. JAMA Neurol 2020;77:937-46.
- 291 TNF neutralization in MS: results of a randomized, placebo-controlled multicenter study. The Lenercept Multiple Sclerosis Study Group and The University of British Columbia MS/MRI Analysis Group. Neurology 1999;53:457-65.
- 292 van Oosten BW, Barkhof F, Truyen L, et al. Increased MRI activity and immune activation in two multiple sclerosis patients treated with the monoclonal anti-tumor necrosis factor antibody cA2. Neurology 1996;47:1531-4.
- 293 Segal BM, Constantinescu CS, Raychaudhuri A, et al. Repeated subcutaneous injections of IL12/23 p40 neutralising antibody, ustekinumab, in patients with relapsing-remitting multiple sclerosis: a phase II, double-blind, placebo-controlled, randomised, dose-ranging study. Lancet Neurol 2008;7:796-804.
- 294 Vollmer TL, Wynn DR, Alam MS, et al. A phase 2, 24-week, randomized, placebo-controlled, double-blind study examining the efficacy and safety of an anti-interleukin-12 and -23 monoclonal antibody in patients with relapsing-remitting or secondary progressive multiple sclerosis. Mult Scler 2011;17:181-91.
- 295 Havrdova E, Belova A, Goloborodko A, et al. Activity of secukinumab, an anti-IL-17A antibody, on brain lesions in RRMS: results from a randomized, proof-of-concept study. J Neurol 2016;263:1287-95.
- 296 Khoury SJ, Rochon J, Ding L, et al. ACCLAIM: A randomized trial of abatacept (CTLA4-Ig) for relapsing-remitting multiple sclerosis. Mult Scler 2017;23:686-95.
- 297 Hellgren K, Dreyer L, Arkema EV, et al. Cancer risk in patients with spondyloarthritis treated with TNF inhibitors: a collaborative study from the ARTIS and DANBIO registers. Ann Rheum Dis 2017;76:105-11.
- 298 Ytterberg SR, Bhatt DL, Mikuls TR, et al. Cardiovascular and Cancer Risk with Tofacitinib in Rheumatoid Arthritis. N Engl J Med 2022;386:316-26.
- 299 Kristensen LE, Danese S, Yndestad A, et al. Identification of two tofacitinib subpopulations with different relative risk versus TNF inhibitors: an analysis of the open label, randomised controlled study ORAL Surveillance. Ann Rheum Dis 2023;82:901-10.
- 300 Molander V, Bower H, Frisell T, et al. Venous thromboembolism with JAK inhibitors and other immune-modulatory drugs: a Swedish comparative safety study among patients with rheumatoid arthritis. Ann Rheum Dis 2023;82:189-97.
- 301 Läkemedelsverket. Riskminskningsåtgärder för användning av JAK-hämmare för kroniska inflammatoriska sjukdomar. https://www.lakemedelsverket.se/sv/nyheter/ema-rekommenderar-riskminskningsatgarder-for-anvandning-av-jak-hammare-for-kroniska-inflammatoriska-sjukdomar?tm_campaign=lv_nyhetsbrev&utm_medium=email&utm_source=newsletter. 2022.
- 302 Kristensen LE, Deodhar A, Leung YY, et al. Risk Stratification of Patients with Psoriatic Arthritis and Ankylosing Spondylitis for Treatment with Tofacitinib: A Review of Current Clinical Data. Rheumatol Ther 2024;11:487-99.
- 303 Zhao SS, Riley D, Hernandez G, et al. Comparative safety of JAK inhibitors versus TNF or IL-17 inhibitors for cardiovascular disease and cancer in psoriatic arthritis and axial spondyloarthritis. Clin Ther 2025;47:293-7.
- 304 Smolen JS, van der Heijde D, Machold KP, et al. Proposal for a new nomenclature of disease-modifying antirheumatic drugs. Ann Rheum Dis 2014;73:3-5.
- 305 Anderson JJ, Baron G, van der Heijde D, et al. Ankylosing spondylitis assessment group preliminary definition of short-term improvement in ankylosing spondylitis. Arthritis Rheum 2001;44:1876-86.
- 306 Brandt J, Listing J, Sieper J, et al. Development and preselection of criteria for short term improvement after anti-TNF alpha treatment in ankylosing spondylitis. Ann Rheum Dis 2004;63:1438-44.
- 307 American College of Rheumatology Committee to Reevaluate Improvement C. A proposed revision to the ACR20: the hybrid measure of American College of Rheumatology response. Arthritis Rheum 2007;57:193-202.
- 308 Schoels M, Aletaha D, Funovits J, et al. Application of the DAREA/DAPSA score for assessment of disease activity in psoriatic arthritis. Ann Rheum Dis 2010;69:1441-7.
- 309 Tan AL, Marzo-Ortega H, O’Connor P, et al. Efficacy of anakinra in active ankylosing spondylitis: a clinical and magnetic resonance imaging study. Ann Rheum Dis 2004;63:1041-5.
- 310 Haibel H, Rudwaleit M, Listing J, et al. Open label trial of anakinra in active ankylosing spondylitis over 24 weeks. Ann Rheum Dis 2005;64:296-8.
- 311 Song IH, Heldmann F, Rudwaleit M, et al. Different response to rituximab in tumor necrosis factor blocker-naive patients with active ankylosing spondylitis and in patients in whom tumor necrosis factor blockers have failed: a twenty-four-week clinical trial. Arthritis Rheum 2010;62:1290-7.
- 312 Song IH, Heldmann F, Rudwaleit M, et al. Treatment of active ankylosing spondylitis with abatacept: an open-label, 24-week pilot study. Ann Rheum Dis 2011;70:1108-10.
- 313 Pathan E, Abraham S, Van Rossen E, et al. Efficacy and safety of apremilast, an oral phosphodiesterase 4 inhibitor, in ankylosing spondylitis. Ann Rheum Dis 2013;72:1475-80.
- 314 Taylor PC, van der Heijde D, Landewe R, et al. A Phase III Randomized Study of Apremilast, an Oral Phosphodiesterase 4 Inhibitor, for Active Ankylosing Spondylitis. J Rheumatol 2021;48:1259-67.
- 315 Sieper J, Porter-Brown B, Thompson L, et al. Assessment of short-term symptomatic efficacy of tocilizumab in ankylosing spondylitis: results of randomised, placebo-controlled trials. Ann Rheum Dis 2014;73:95-100.
- 316 Sieper J, Braun J, Kay J, et al. Sarilumab for the treatment of ankylosing spondylitis: results of a Phase II, randomised, double-blind, placebo-controlled study (ALIGN). Ann Rheum Dis 2015;74:1051-7.
- 317 Poddubnyy D, Hermann KG, Callhoff J, et al. Ustekinumab for the treatment of patients with active ankylosing spondylitis: results of a 28-week, prospective, open-label, proof-of-concept study (TOPAS). Ann Rheum Dis 2014;73:817-23.
- 318 Deodhar A, Gensler LS, Sieper J, et al. Three Multicenter, Randomized, Double-Blind, Placebo-Controlled Studies Evaluating the Efficacy and Safety of Ustekinumab in Axial Spondyloarthritis. Arthritis Rheumatol 2019;71:258-70.
- 319 Baeten D, Ostergaard M, Wei JC, et al. Risankizumab, an IL-23 inhibitor, for ankylosing spondylitis: results of a randomised, double-blind, placebo-controlled, proof-of-concept, dose-finding phase 2 study. Ann Rheum Dis 2018;77:1295-302.
- 320 Jung N, Hellmann M, Hoheisel R, et al. An open-label pilot study of the efficacy and safety of anakinra in patients with psoriatic arthritis refractory to or intolerant of methotrexate (MTX). Clin Rheumatol 2010;29:1169-73.
- 321 Jimenez-Boj E, Stamm TA, Sadlonova M, et al. Rituximab in psoriatic arthritis: an exploratory evaluation. Ann Rheum Dis 2012;71:1868-71.
- 322 Wendling D, Dougados M, Berenbaum F, et al. Rituximab treatment for spondyloarthritis. A nationwide series: data from the AIR registry of the French Society of Rheumatology. J Rheumatol 2012;39:2327-31.
- 323 Mease PJ. Is there a role for rituximab in the treatment of spondyloarthritis and psoriatic arthritis? J Rheumatol 2012;39:2235-7.
- 324 Hughes M, Chinoy H. Successful use of tocilizumab in a patient with psoriatic arthritis. Rheumatology (Oxford) 2013;52:1728-9.
- 325 Ogata A, Umegaki N, Katayama I, et al. Psoriatic arthritis in two patients with an inadequate response to treatment with tocilizumab. Joint Bone Spine 2012;79:85-7.
Flödesschema
Flödesschema axial spondylartrit