Vaccination av patienter med inflammatoriska reumatiska sjukdomar
Introduktion
Rekommendation från Svensk Reumatologisk Förening inför 2026.
Arbetsgrupp: Karin Bengtsson, Francesca Faustini, Johanna Sundbaum, Linda Mark, Theodoros Lappas*, Meliha C. Kapetanovic*, *huvudansvarig för denna rekommendation, medlem i EULAR task force grupp för vaccination
Detta är ett dokument som tagits fram av arbetsgruppen för läkemedelssäkerhet på uppdrag av Svensk Reumatologisk Förening (SRF). Nedanstående rekommendationer skall ses som ett underlag i det kliniska beslutsfattandet och baseras på aktuellt kunskapsläge inom området. Behandlande läkare bör dock noggrant väga för- och nackdelar med vaccination i varje enskilt patientfall med inflammatorisk reumatisk sjukdom (IRS). Referenslista innehåller endast ett urval av publikationer (framför allt reviews) och hänvisning till myndigheternas hemsidor med mer information och originalpublikationer.
Reviderade vaccinationsrekommendationer från EULAR publicerades sommaren 2019 (1). För närvarande pågår arbete med uppdatering av dessa rekommendationer. I vissa fall avviker rekommendationen från SRF något från EULAR:s vilket framgår under respektive punkt. Nytt i årets dokument är: uppdaterad information om vaccination mot COVID-19 (sida 12-14). Rekommendationer om vaccination mot COVID-19, RS virus, TBE, mpox och kikhosta finns inte i EULAR dokumentet.
Efter gruppens senaste uppdatering av dokumentet i november 2025 publicerade Folkhälsomyndigheten 2026-01-09 en ny utgåva av rekommendationer om vaccination mot pneumokocker till riskgrupper. Nytt i denna uppdatering är att alla riskgrupper rekommenderas vaccination med konjugerat pneumokockvaccin som innehåller minst 20 serotyper. Rekommendationer om val av vaccin är bland annat grundade på en hälsoekonomisk analys genomförd av Folkhälsomyndigheten. Eftersom samma rekommendation accepteras i EULAR arbetsgruppen väljer vi att lägga till detta i årets dokument.
Sammanfattning
Övergripande principer
(för detaljer se respektive punkt längre ner på sidan)
- Relevant anamnestisk vaccinationsstatus och indikation för nya vaccinationer bör uppdateras av behandlande läkare.
- Varje patient bör ha ett individuellt vaccinationsprogram utformat i samråd mellan patient och behandlande läkare. Implementering bör ske i samarbete mellan patient, behandlande läkare och eventuell annan relevant vårdgivare.
- Patienter med IRS bör i idealfallet vaccineras när sjukdomen är stabil.
- Vaccination bör i idealfallet genomföras före start av immunmodulerande behandling och i synnerhet före planerad behandling med rituximab. Vaccination rekommenderas därför om möjligt cirka fyra veckor före start av rituximab eller ny behandlingsomgång och sex månader efter senaste infusion. Tidpunkt för säsongsinfluensavaccination är av naturliga skäl svårare att anpassa. Generellt rekommenderas inte utsättning av redan pågående immunmodulerande terapi inför vaccination.
- Levande försvagade vaccin skall undvikas när så är möjligt till immunsupprimerade IRS-patienter (lista över vissa aktuella levande vacciner tillgängliga i Sverige sid 20).
Rekommendationer
- Årlig vaccination mot säsongsinfluensa bör starkt övervägas till patienter med IRS.
- Pneumokockvaccination bör starkt övervägas till patienter med IRS. Alla patienter som tillhör riskgrupp rekommenderas vaccination med konjugerat pneumokockvaccin.
- Årlig vaccination mot COVID-19 rekommenderas starkt till patienter med reumatiska sjukdomar. Rekommendationen gäller oavsett tidigare antal doser. Vaccinet uppdateras beroende på vilka virusvarianter cirkulerar.
- Patienter med IRS skall vaccineras mot stelkramp enligt samma regler som befolkningen i övrigt. Under pågående behandling med B-cellsdepleterande behandling bör dessutom passiv immunisering med tetanusimmunoglobulin övervägas i samband med skada där risk för stelkramp finns.
- Vaccination mot bältros rekommenderas till vuxna patienter med IRS som har en ökad risk för sjukdomen på grund av ålder, sjukdom eller läkemedelsbehandling. Icke-levande vaccin mot herpes zosterinfektion finns tillgängligt i Sverige och rekommenderas till patienter med IRS.
- Human papillomavirusvaccination bör övervägas till ovaccinerade IRS-patienter upp till 26 års ålder och kan även övervägas till vissa högriskgrupper till och med 45 års ålder.
- Hepatit A och/eller B-vaccination bör ges till IRS-patienter med ökad risk för sådan smitta.
- Patienter med IRS som planerar resor bör vaccineras enligt allmänna rekommendationer med undantag för levande försvagade vaccin.
- Immunokompetenta familjemedlemmar till patienter med IRS bör uppmuntras att vaccineras enligt nationella riktlinjer.
- Vaccination med levande vaccin till barn som exponerats för immunmodulerande läkemedel under andra delen av graviditeten eller under amning sker enligt rekommendationer beskrivna i dokumentet: ”Nationell vägledning för vaccination med levande försvagade vaccin”, https://www.rikshandboken-bhv.se
- Vaccination mot RS virus kan ges till patienter från 60 år med IRS och nedsatt immunförsvar pga sjukdom eller immunsupprimerande behandling.
- Hypospleniska/aspleniska patienter med IRS rekommenderas vaccination i samråd med infektionsläkare.
- Vaccination mot TBE bör (i överensstämmelse med allmänna rekommendationer) övervägas till IRS-patienter som vistas i endemiska områden för TBE
Innehåll
Övergripande principer
1. Relevant anamnestisk vaccinationsstatus och indikation för nya vaccinationer bör uppdateras av behandlande läkare.
Vaccinationsstatus framför allt avseende influensa, pneumokocker, humant papillomavirus (HPV), COVID-19, hepatit A och B och tick-borne encephalitis (TBE) behövs för att kunna ge rekommendationer om vaccinationer för den individuella patienten med IRS. På sidan 22-23 finns en tabell över de vanligaste smittämnena och motsvarande tillgängliga vacciner. Komplettering med vaccinationer som saknas jämfört med det nationella vaccinationsprogrammet bör övervägas. Problem, sjukdomsskov och biverkningar vid tidigare vaccinationer bör efterfrågas, eftersom dessa kan utgöra (relativ) kontraindikation för framtida vaccinationer.
2. Varje patient bör ha ett individuellt vaccinationsprogram utformat i samråd mellan patient och behandlande läkare. Implementering bör ske i samarbete mellan patient, behandlande läkare och eventuell annan relevant vårdgivare.
Detta är en rekommendation från EULAR som införts med starkt stöd av gruppens patientrepresentanter. Rent generellt har betydelsen av patientens behov och preferenser uppmärksammats även i nya EULAR rekommendationer för behandling av RA, psoriasisartrit och spondylartrit. Personcentrerad vård har visats sig vara betydelsefull för olika aspekter av behandling av kronisk sjukdom inkluderande säkerhet, effektivitet och kostnader. En stor undersökning bland RA patienter i Storbritannien påvisade en god vaccinationstäckning kopplat till ett nära samarbete med primärvården för implementering av vaccinationsprogram. I en studie från Danmark gav information och rekommendation om vaccination från sjukvårdspersonalen bland patienter med RA bättre vaccinationstäckning för influensa (2). En vanlig orsak till att patienter inte vaccinerats var att man inte fått relevant information (2).
3. Patienter med IRS bör i idealfallet vaccineras när sjukdomen är stabil.
Det finns inga studier som jämför effekt och problem vid vaccination av IRS-patienter med stabil och instabil sjukdom. Flertalet vaccinationsstudier är gjorda på patienter i lugn sjukdomsfas. I en studie från Brasilien påvisades ett minskat antikroppssvar efter influensa A H1N1/2009 vaccin hos patienter med juvenil SLE och hög sjukdomsaktivitet (3). Andra studier som inkluderat IRS-patienter med moderat och hög sjukdomsaktivitet visade ingen ökad frekvens av biverkningar eller skov, och inte heller sämre effekt jämfört med friska kontroller (1). Rekommendationen att helst vaccinera IRS-patienter i stabil fas grundar sig därför på expertåsikt, eftersom det finns teoretiska möjligheter att vaccination kan utlösa skov (1).
4. Vaccination bör i idealfallet genomföras före start av immunmodulerande behandling och i synnerhet före planerad behandling med rituximab. Vaccination rekommenderas därför om möjligt cirka fyra veckor före start av rituximab eller ny behandlingsomgång och sex månader efter senaste infusion. Tidpunkt för säsongsinfluensavaccination är av naturliga skäl svårare att anpassa. Generellt rekommenderas inte utsättning av redan pågående immunmodulerande terapi inför vaccination inför vaccination med icke-levande vaccin.
Ett flertal studier har rapporterat att rituximab minskar antikroppssvaret efter vaccination mot influensa och pneumokocker (1). Vaccination rekommenderas därför om möjligt ca fyra veckor före start av behandlingen eller ny behandlingsomgång och sex månader efter senaste infusion. Tidpunkt för säsongsinfluensavaccination är av naturliga skäl svårare att anpassa.
I ett antal studier (ofta med motsägelsefulla resultat) har man undersökt om utsättning av immunmodulerande behandlingar påverkar vaccinsvar i samband med vaccination med icke-levande vaccin. Sammanfattningsvis i nuläget finns inte stöd för anpassning eller utsättning av immunmodulerande terapi före dessa vaccinationer. Detta är också EULAR-gruppens bedömning (1). Däremot rekommenderas utsättning av immunmodulerande läkemedel under en viss tid inför planerad vaccination med levande vaccin.
Abatacept har visats minska antikroppssvaret efter H1N1 influensavaccination och vaccination mot pneumokocker. I en annan studie fann man protektiva antikroppsnivåer efter influensa och pneumokockvaccination (med polysackaridvaccinet PPV) hos RA patienter behandlade med abatacept och traditionella DMARDs.
Andra biologiska läkemedel har visat sig ha varierande effekt på vaccinationssvar men de flesta av patienterna uppnådde tillräckligt bra svar. Patienter med RA eller spondartrit behandlade med TNF-hämmare hade nedsatt antikroppssvar efter influensa- och pneumokockvaccination i ett antal studier (1). I en meta-analys var behandling med TNF-hämmare hos patienter med RA dock inte associerat med nedsatt svar efter influensa- och pneumokockvaccination (4).
Tocilizumab verkar inte påverka svar efter influensa-, pneumokock- och tetanusvaccination hos patienter med RA eller juvenil idiopatisk artrit (JIA) (1).
Tofacitinib, speciellt i kombination med metotrexat minskade antikroppssvaret efter vaccination med pneumokock- (PPV), men inte influensavaccin (1). Tillfälligt uppehåll med tofacitinib i samband med vaccination har inte haft någon större effekt på svar på PPV. Ungefär 2/3 av patienter med RA vaccinerade med konjugatvaccinet mot pneumokocker (PCV13) under pågående, långvarig behandling med baricitinib uppnådde tillräckligt bra antikroppssvar, men svaret på vaccination mot tetanus var sämre. Samtidig kortisonbehandling påverkade inte vaccinationssvaren (1).
Systemiska steroider, speciellt i hög dos, kan vara en bidragande orsak till nedsatt vaccinationssvar. Kontinuerlig hög steroiddos var associerad med sämre antikroppssvar efter vaccination mot pneumokocker (PPV) i en kohort av patienter med olika IRS som fick ≥ 20 mg/dygn prednisolon eller annan immunsuppressiv terapi och bland patienter med juvenil dermatomyosit med prednisolon ≥20 mg/dygn (1). I en stor kohort av patienter med juvenila autoimmuna reumatiska sjukdomar rapporterades minskat men ändå tillräckligt immunsvar efter influensa A 2009 H1N1-vaccin. Behandling med steroider var starkast kopplad till nedsatt svar. Minskat svar på influensa A 2009 H1N1-vaccin är rapporterat hos SLE patienter under behandling med steroider, azatioprin, mycofenolatmofetil och cyklofosfamid. Antimalariabehandling verkade förbättra antikroppssvaret i den studien. Inadekvat immunogenicitet (dvs. förmåga att indicera ett antikroppssvar) av pneumokockvaccin (PPV) har rapporterats hos SLE-patienter under immunosuppressiv behandling, men antalet patienter var litet i denna studie. Hos patienter med systemisk vaskulit resulterade pneumokockvaccination (med konjugatvaccin PCV7) i lägre men ändå protektiva antikroppsnivåer under behandling med azatioprin, cyklofosfamid och metotrexat jämfört med kontroller (1).
Inverkan av metotrexat på vaccinationssvar har studerats i ett flertal studier. Två studier har demonstrerat minskad effekt av metotrexat på vaccinationssvar efter influensa A 2009 H1N1-vaccination hos patienter med RA och i en grupp patienter med blandade IRS (1). Tillfällig utsättning av metotrexat har visat viss förbättring av svaret efter säsongsinfluensavaccination hos patienter med RA, speciellt om metotrexat varit utsatt två veckor före och två veckor efter vaccination. Vidare har man rapporterat att även utsättning av metotrexat endast två veckor efter influensavaccination kan förbättra vaccinsvaret. Det förbättrade antikroppssvaret vid metotrexatutsättning är dock marginellt och utsättning av metotrexat i samband med säsongsinfluensavaccination rekommenderas inte av EULAR (1,11,12). Sammanfattningsvis bedöms att evidensen för utsättning är svag och att tillräckligt god immunoprotektion uppnås under pågående metotrexatbehandling. Behandling med metotrexat predikterade sämre svar till 7-valent konjugerat vaccin mot pneumokocker (PCV7) och polysackaridvaccinet (PPV) hos RA patienter. Metotrexat var också associerat med lägre nivåer av vaccinspecifika IgG-antikroppar och deras funktionalitet men inte antal vaccinspecifika antikroppsproducerande B-celler hos RA patienter efter vaccination med det 13-valenta konjugatvaccinet mot pneumokocker (PCV13). Takrolimus i kombination med metotrexat minskade antikroppssvaret efter vaccination med PPV23 vid RA, men inte takrolimusmonoterapi.
Sammanfattningsvis har samlade data från flera studier under de senaste åren gett stöd för vaccination mot influensa, pneumokocker, hepatit A och B, tetanus toxoid och Haemophilus influenze B bland patienter med IRS under pågående immunmodulerande behandling med systemiska steroider och DMARDs. I de flesta studier uppnår patienter med IRS tillräckligt bra immunoprotektion och inga allvarliga säkerhetssignaler har rapporterats under en relativt begränsad uppföljningstid.
5. Levande försvagade vaccin skall undvikas när så är möjligt till immunsupprimerade IRS patienter.
Eftersom levande försvagade vaccin innehåller levande virus/bakterier kan dessa potentiellt ge upphov till (allvarliga) infektioner hos immunsupprimerade patienter. Det är emellertid oklart vilken nivå av immunsuppression (av sjukdomen eller dess terapi) som ökar risken för sådan vaccininfektion. Till dess vidare och i väntan på ytterligare studier avråder man i Sverige patienter som behandlas med immunsupprimerande läkemedel från att vaccinera sig med levande försvagade vaccin.
Ett undantag från att undvika levande försvagade vaccin till IRS-patienter finns. Det gäller situationen med revaccination/boosterdos (oftast aktuellt till barn) med det levande försvagade vaccinet mot mässling-påssjuka-röda hund (MPR booster).
Ett levande försvagat vaccin kan däremot ges en månad före start av planerad immunsuppressiv behandling. Om vaccination med ett levande vaccin under pågående immunsupprimerande behandling är nödvändig rekommenderas behandlingsuppehåll. Det saknas vetenskapliga studier om hur långt behandlingsuppehåll som behövs och beror troligen på både läkemedlets halveringstid och dess farmakologiska effekt. För läkemedel med kort halveringstid behövs rimligen kortare uppehåll. Generellt borde behandling med DMARDs kunna återinsättas en månad efter vaccination med det levande försvagade vaccinet.
Lista över de flesta av levande försvagade vaccin som finns registrerade för användning i Sverige (även i tabell på sida 20): vaccin mot mässling-påssjuka-röda hund (MPR) (M-M-RVAXPRO®, Priorix®), oralt vaccin mot rotavirus (Rotarix®, RotaTeq®), vaccin mot gula febern (Stamaril®), vaccin mot tuberkulos (BCG-vaccin®), oralt tyfoidvaccin (Vivotif®) vaccin mot vattkoppor (Varilrix®,Varivax®) och herpes zoster (Zostavax®).
Sammanfattningsvis, som framgår nedan, finns studier där levande vaccin getts till patienter med IRS utan större rapporterade säkerhetsproblem. Studierna har dock begränsningar av olika slag och är oftast små. Den sammanvägda bedömningen är därför att det inte finns tillräckligt stöd för annan rekommendation än att där så är möjligt undvika levande försvagade vaccin till patienter med IRS.
Här följer detaljer om gjorda studier. En restrospektiv studie från Nederländerna rapporterade långvarig persistens av seroprotektiva antikroppsnivåer efter vaccination mot mässling i en stor grupp av barn med juvenil idiopatisk artrit (JIA) (5). Liknande resultat rapporterades i en mindre studie bland barn med SLE från Brasilien (6). En prospektiv fall-kontrollstudie från Tyskland fann protektiva antikroppsnivåer sex månader efter revaccination mot mässling bland 15 patienter med JIA behandlade med lågdos metotrexat som monoterapi eller i kombination med etanercept (7). En randomiserad, multicenter, open-labelstudie från Nederländerna påvisade bra immunogenicitet och säkerhet av MPR-boostervaccin hos patienter med JIA(8). Metotrexat och biologiska läkemedel påverkade inte antikroppssvaret i denna studie men begränsat antal patienter gjorde att man inte kunde dra säkra slutsatser (8).
En amerikansk retrospektiv studie bland 46 3541 Medicarepatienter äldre än 60 år med känd IRS (RA, PsA, AS, IBD, psoriasis), behandlade med olika immunosuppressiva läkemedel varav 633 patients med biologiska läkemedel (551 TNF-hämmare), kunde inte påvisa någon ökad incidens av herpes zoster (HZ) inom 42 dagar efter vaccination med Zostavax (den förmodade vulnerabla perioden för utveckling av HZ) (9). Zostavax®-vaccination minskade incidensen av HZ med ungefär 40% men lägre jämfört den 50% vilket var nivå man såg i Shingles Prevention Study. Patienter med olika sjukdomar och aktuell eller tidigare användning av immunosuppressiva läkemedel vid Zostavax®-vaccination hade en måttligt ökad risk av HZ inom 42 dagar efter vaccination (9).
God säkerhet av levande vaccin mot varicella zoster (vattkoppor) sågs i en mindre studie av JIA patienter behandlade med metotrexat, JIA patienter behandlade med biologiska läkemedel, barn med SLE med känd immunitet mot varicella, och barn med olika reumatiska sjukdomar (JIA, juvenil dermatomyosit, juvenile scleroderma) behandlade med metotrexat. I den senare studien var antikroppssvaret lika bra bland patienter och kontroller och immunosuppressiva läkemedel påverkade inte vaccinationssvaret (1). I en blindad, randomiserad och placebokontrollerad studie bland patienter behandlade med TNF-hämmare (mest för RA och psoriasisartrit i åldrar ≥50 år) vaccinerades patienter med levande vaccin mot varicella zoster eller placebo. Levande vaccinet var immunogent och inga fall av vattkoppoer eller bältros rapporterades fram till 6 veckor efter vaccinationen (10).
Vaccin mot gula febern vaccin gavs till 17 brasilianska RA-patienter behandlade med infliximab utan några sequele and till 31 brasilianska patienter med andra IRS (RA, SLE, SSC, AS), vissa av dessa behandlade med biologiska läkemedel, men detta var en del av re-immunisering och inte primärt svar på virusantigen. Därför kan inte dessa resultat extrapoleras till immunsupprimerade patienter som behöver vaccineras mot gula febern för första gången (1). Nyligen rapporterades tillräckligt bra immunogenicitet mätt sex månader efter vaccination mot gula febern bland 34 franska resenärer med autoimmuna sjukdomar vilka var behandlade med kortison (prednisolon eller motsvarande dos 7 mg/dygn). Patienter behandlade med steroider rapporterade oftare måttliga/svåra lokala biverkningar. Inga allvarliga biverkningar rapporterades på kort sikt (1,11,12).
EULAR-arbetsgruppen anger att levande vaccin kan övervägas med försiktighet till patienter med IRS. Levande vaccin mot herpes zoster (Zostavax®) kan eventuellt ges till patienter med IRS 4 veckor före start och inte under behandling med immunosuppressiva läkemedel (1). I Sverige anser Socialstyrelsen att vaccinet är kontraindicerat till alla immunsupprimerade patienter inkluderande patienter som behandlas med Prednisolon > 20 mg/d eller motsvarande (i enlighet med produktresumén för vaccinet).
I de senaste ACR rekommendationerna publicerades ett förslag om tidsintervall mellan uppehåll av anti-reumatiska behandlingen och vaccination med levande vaccin samt tidsintervall mellan vaccination och återinsättning av behandlingen (13). Det vetenskapliga stödet för dessa rekommendationer grundas framför allt på expertgruppens bedömning då vetenskapligt stöd saknas. I tabell 3 återges en svensk översättning av föreslagna tidsintervaller.
Rekommendationer
1. Årlig vaccination mot säsongsinfluensa bör starkt övervägas till patienter med IRS.
Vaccination mot säsongsinfluensa bör göras i samband med sedvanlig vaccination till befolkning/riskgrupper oavsett pågående anti-reumatisk terapi. Normalt tar det cirka två veckor innan man får ett bra skydd av vaccinet, och effekten varar ungefär sex-nio månader. Det finns visst stöd att en boosterdos av influensavaccin till patienter med IRS kan ge ett bättre antikroppssvar. WHO och Folkhälsomyndigheten förtydligar inför varje influensasäsong om två doser ska rekommenderas till riskpatienter den aktuella säsongen.
I en registerstudie från UK rapporterades minskad risk för influensa relaterad sjuklighet samt sjukhusvård och död i pneumoni bland patienter med autoimmuna reumatiska sjukdomar vaccinerade mot influensa (14).
Det finns tre olika typer av influensavaccin i Sverige: standarddosvacciner, ett inaktiverat förstärkt vaccin och ett levande försvagat vaccin (LAIV)(15). Folkhälsomyndigheten rekommenderar att förstärkta influensavacciner erbjuds till personer som bor på särskilda boenden för äldre. Vaccinationen mot säsongsinfluensa går i de flesta fall att kombinera med ett eller flera andra vaccinationer, till exempel mot COVID-19, bältros eller pneumokocker (15).
Bakgrundsinformation
Data om incidensen av influensa bland patienter med IRS är begränsad. I en nederländsk enkätstudie utförd 2009-2010 var prevalensen av influensa hos patienter med RA 5.9%. Patienter med högre BMI behandlade med anti-TNF hade störst risk. I en stor retrospektiv kohortstudie från USA (2000-2007) hade RA-patienter högre incidens av influensa än kontroller (409 vs 306 fall/100,000 patientår) (1). Bland brasilianska JIA patienter var den observerade frekvensen av akuta luftvägsinfektionen 7.6 och 3.9 per 1000 barn-dagar under 2007 och 2008, och influensavirus var det vanligaste detekterade viruset.
Vaccination med trivalent säsongsinfluensavaccin har rapporterats kunna minska incidensen och bakteriella komplikationer av influensa samt sjukhusvård och mortalitet associerad med influensa/pneumoni hos patienter med IRS. Vaccination mot influensa har visat sig leda till tillräckligt vaccinsvar hos patienter med RA, SLE, AAV, SSc, fibromyalgi och PsA, hos patienter behandlade med cDMARDs, anti-TNF, tocilizumab eller tofacitinib, men vissa studier (inklusive en meta-analys) har visat måttligt nedsatt svar hos patienter med SLE eller RA patienter behandlade med anti-TNF eller metotrexat (1,11-13). Behandling med rituximab var associerad med nedsatt antikroppssvar, men cellmedierat immunsvar var inte påverkat. Biverkningar av influensavaccin bland patienter med IRS verkar vara jämförbara med kontroller, men det finns ingen studie med tillräckligt bra power för att säkert besvara detta.
De studier som har undersökt effektivitet och tolerabilitet av massvaccinationen mot H1N1 influensan år 2009 rapporterade minskat vaccinsvar vid IRS (de flesta RA och SLE). Immunsupprimerade behandlingar minskade vaccinsvaret men de flesta patienter uppnådde protektiva antikroppsnivåer. Metotrexat och abatacept var undantag och dessa behandlingar var associerade med nedsatt vaccinsvar (11-13). Den andra boostervaccindosen uppvisade bättre svar, med seroprotektion i nivå med friska kontroller. Liknande resultat har rapporterats för SLE patienter som vaccinerades mot säsonginfluensa första gången. I de flesta studier påverkade inte vaccination sjukdomsaktiviteten och endast milda biverkningar rapporterades. Aktuell rekommendation angående eventuell extra boosterdos utfärdas inför varje influensasäsong av WHO och Folkhälsomyndigheten.
Årlig influensavaccination är gratis för gravida, äldre än 65 år och personer som tillhör riskgrupper i alla regioner i Sverige.
2. Pneumokockvaccination bör starkt övervägas till patienter med IRS. Enligt Folkhälsomyndighetens senaste uppdatering från januari 2026 rekommenderas vaccination med konjugatvaccin med minst 20 serotyper till alla riskgrupper. Behovet av revaccination är inte säkerställt för konjugatvacciner och är därför inget som hittills rekommenderas.
I Sverige finns för närvarande två typer av pneumokockvaccin, det ”gamla” polysackaridvaccinet Pneumovax® (PPV med skydd mot 23 pneumokockserotyper) samt konjugatvacciner (PCV) som innehåller 13, 15, 20 eller 21 antigen pneumokockserotyper, det senaste ingår i Capvaxive vaccin.
De senaste konjugatvaccinerna (Vaxneuvance, PCV15 och Prevenar20, PCV20 och Capvaxive, PCV21) innehåller antigen mot 15 respektive 20 och 21 pneumokockserotyper och har godkänts för personer 18 år och äldre. Vaccinernas godkännande grundas på randomiserade studier som visade att PCV20 och PCV15 inducerade antikroppssvar som var jämförbara med de inducerade av PCV13 och som i tidigare studier visats ge skydd mot invasiv pneumokocksjukdom
Från och med 1 december 2022 gäller det ett nytt nationellt vaccinationsprogram mot pneumokockinfektion för personer i riskgrupper. Alla personer med nedsatt immunförsvar pga. sjukdom eller behandling omfattas av detta program (16). Detta program har uppdaterats på nytt och 2026-01-09 publicerades nya rekommendationer på Folkhälsomyndighetens hemsida (16). Riskgrupper delas som tidigare in i de med mycket hög risk för allvarlig pneumokocksjukdom och de med ökad risk för sådan sjukdom. En mycket hög risk för allvarlig pneumokocksjukdom har exempelvis patienter med IRS som förutom sin sjukdom eller behandling har flera andra riskfaktorer (lungengagemang eller tidigare haft invasiv pneumokock sjukdom). Alla andra patienter med IRS tillhör gruppen med ökad risk. Nytt i denna utgåva från januari 2026 är att alla riskgrupper rekommenderas vaccination med konjugerat pneumokockvaccin. Rekommendationer om val av vaccin är bland annat grundade på en hälsoekonomisk analys genomförd av Folkhälsomyndigheten (16).
Bakgrundsinformation
Det finns sparsamt med data om prevalensen av pneumokockpneumoni vid IRS. I en retrospektiv kohortstudie (2006–2010) identifierades RA och SLE som tillstånd med ökad risk för pneumokockorsakad sjukdom. Incidensen av invasiv pneumokocksjukdom bland SLE-patienter var 13 gånger högre än hos en allmän population i Nederländerna. Kombination av vaccination med PCV13 and PPV23 var en viktig ändring i EULAR-rekommendationerna, i huvudsak grundad på expertåsikt. Hittills har nästan 100 olika pneumokockserotyper identifierats och 30 av dessa står för 90 % av infektionerna. Trots att polysackaridvaccinet (PPV) med 23 serotyper skyddar mot invasiv pneumokocksjukdom, leder vaccinet inte till immunitet bland barn yngre än 2 år och även i den övriga populationen har skyddet mot pneumoni varit begränsat.
Effektivitet av PPV-vaccinet, baserat på antikroppssvar som surrogatmarkör, och tolerabilitet har framförallt demonstrerats hos patienter med RA, SLE, JIA, PsA och andra inflammatoriska tillstånd. Antikroppssvar efter pneumokockvaccination har visat sig vara nedsatt vid behandling med metotrexat, abatacept, golimumab, tofacitinib and rituximab men verkar inte vara påverkat av certolizumab och belimumab (1,11-13). Inga allvarliga säkerhetssignaler har registrerats i någon av dessa studier. Hos patienter med kryopyrinassocierat periodiskt syndrom, har PPV-vaccinet rapporterats orsaka svår lokal reaktion krävande sjukhusvård. I en randomiserad dubbelblindstudie var skyddseffekten av PPV mot pneumoni bland RA patienter inte bättre än för placebo, vilket betonar att det finns behov av ett mer effektivt vaccin. Flera studier har visat immunogenicitet av PCV7-vaccinet motsvarande det för PPV-vaccinet, vilket innebär nedsatt immunogenicitet vid behandling med metotrexat, abatacept och rituximab och anti-TNF behandling. I en annan studie var en dos PCV-vaccin immunogent hos RA patienter behandlade med etanercept. Immunogeniciteten sjunker efter 1.5 år men medför ändå ett visst fortsatt skydd mot pneumoni.
Det finns en studie av effekt av PCV-vaccination hos belimumab-behandlade SLE patienter. I denna påverkades inte antikroppssvaret av tillägg av belimumab till csDMARD och prednisolon. Bland barn med inflammatoriska tarmsjukdomar, ledde vaccination med PCV-vaccin till adekvat antikroppssvar trots behandling med immunosuppressiva läkemedel inklusive biologiska läkemedel (1,11-13). En randomiserad kontrollstudie som undersökte antikroppssvar efter vaccination med PCV och PPV efter 16-24 veckor demonstrerade adekvat antikroppsvar hos 87% and 94% av RA patienter behandlade med respektive biologiska läkemedel och csDMARDS och signifikant nedsatt svar bland patienter behandlade med rituximab. Prime-boosting med PCV-vaccin förbättrade inte antikroppssvaret. Långvarigt skydd efter vaccination med PPV har evaluerats i 2 studier av RA patienter behandlade med metotrexat och biologiska läkemedel (1).
Vaccination mot pneumokocker (23-valenta polysackaridvaccinet Pneumovax® och i vissa regioner också konjugatvaccinet Prevenar20 och Capvaxive (PCV21) är kostnadsfri för riskgrupper. För personer yngre än 65 år som tillhör riskgrupperna är dessa vaccinationer antingen kostnadsfria eller man betalar ofta en lägre avgift. Observera att många regioner inte har hunnit uppdatera sina rekommendationer enligt Folkhälsomyndigheternas rekommendationer från januari 2026.
3. Vaccination mot COVID-19 rekommenderas starkt till patienter med reumatiska sjukdomar.
Svensk Reumatologisk Förenings rekommendationer avseende covid-19-vaccination utgår från Folkhälsomyndighetens årligen publicerade riktlinjer inför höstsäsongen. Dessa bygger på en samlad bedömning av vetenskaplig evidens, aktuell sjukdomsbörda och mortalitet i covid-19, epidemiologiska trender samt hälsoekonomiska analyser från föregående säsong.
Personer med nedsatt immunförsvar som är 18 år och alla personer 75 år och äldre rekommenderas en vaccindos per år. Personer som rekommenderas en dos vaccin under hösten 2025 kan avstå vaccination om de redan haft bekräftad COVID-19 efter 1 september 2025. Personer med immunhämmande behandlingar kan av läkare individuellt ordineras flera doser samma år, som komplement till Folkhälsomyndighetens generella rekommendation om en dos per år Vaccination mot covid-19 kommer under säsongen 2025/2026 huvudsakligen att ske med mRNA-vaccinet Comirnaty (Pfizer-BioNTech) (18).
Patienter med inflammatorisk reumatisk sjukdom där 2 doser av vaccin mot COVID-19 kan övervägas:
- Patienter som behandlas med rituximab eller annan B-cellsdepletionsterapi
- Patienter på högdos systemiska kortikosteroider (t.ex. prednisolon ≳20 mg/dag under ≥2 veckor).
- Personer med annan allvarlig sjukdom som nedsätter immunförsvaret (t.ex. hematologiska maligniteter, organtransplantation).
- Patienter med interstitiell lungsjukdom eller annan lungsjukdom där risk för allvarlig COVID-19 bedöms vara ökad.
Bakgrundsinformation
Folkhälsomyndigheten publicerade på sin hemsida resultat av en svensk studie om relativ skyddseffekt efter påfyllnadsdos mot COVID-19 till personer 65 år och äldre (17). Resultaten visar att personer i gruppen 65 år och äldre som vaccinerade sig med en påfyllnadsdos under hösten 2022, hade ett förstärkt skydd mot allvarliga konsekvenser av COVID-19 under senaste smittspridningsvågen. Skyddet avtog något, men kvarstod på en hög nivå även 90 dagar eller mer efter den senaste påfyllnadsdosen. Detta jämfört med personer i samma grupp som inte tog någon påfyllnadsdos.
Risken för allvarlig sjukdom vid COVID-19 har gradvis minskat de senaste åren. Det beror bland annat på en allt mer utbredd immunitet efter sjukdom i befolkningen, och på att den virusvariant som cirkulerat de senaste åren är mindre benägen att orsaka allvarlig sjukdom än den ursprungliga (18). En systematisk genomgång av prognos och risk för COVID-19 infektion bland patienter med IRS fanns ingen generell ökad risk för att drabbas av infektion bland patienter jämfört med personer utan någon IRS, ingen övertygande skillnad i risken för en svår infektion mellan olika reumatiska sjukdomar men att ökad sjukdomsaktivitet var associerad med sämre prognos vid COVID-19 infektion, möjligen pga ökad användning av steroider (19). Behandling med rituximab och möjligen JAK-hämmare var associerade med en svårare COVID-19 prognos. Vaccinsvar var sämre än bland personer utan IRS och behandling med rituximab, mycofenolat mofetil och högre ålder predikterade sämre vaccinsvar (19,20). Resultat från EULAR Coronavirus Vaccine (COVAX) register visar att på marknaden tillgängliga vacciner mot COVID-19 tolererades väl av patienter med IRS, allvarliga biverkningar var sällsynta och förekom inte oftare än bland personer utan någon reumatisk sjukdom, skov i grundsjukdomen förekom i 4,4% av patienter (0,6% svårt skov) i samband med vaccination och att genombrottsinfektioner var sällsynta (0,7%) (20). EULAR arbetsgrupp for vaccination mot COVID-19 rekommenderar starkt att patienter med IRS följer nationella rekommendationer om vaccination (21). Både internationella och svenska rekommendationer påtalade behov av påfyllnadsdoser som är uppdaterade för att ge skydd mot aktuella virusvarianter (18, 21). Flera studier inklusive vår nationella studie har visat att patienter som behandlas med rituximab får bättre antikroppssvar om vaccination genomförs minst 6 månader efter senaste rituximab behandling och 2-4 veckor före nästa behandlingsomgång (22,23). Vaccination mot COVID-19 är gratis.
4.Patienter med IRS skall vaccineras med vaccin mot stelkramp enligt samma regler som för befolkningen i övrigt. Under pågående behandling med B-cells depleterande behandling bör dessutom passiv immunisering med tetanusimmunoglobulin övervägas i samband med skada där risk för stelkramp finns.
Hos RA- och SLE-patienter har vaccin mot stelkramp samma effekt som hos friska kontroller. Detta gäller även immunsupprimerade RA-patienter, inklusive de som behandlats med rituximab för (minst) 24 veckor sedan (1). Patienter med IRS rekommenderas tetanus toxoidvaccin enligt rekommendationer för befolkning i övrigt. En prospektiv, multicenterstudie visade att boosterdosen av difteri+tetanus vaccinet (diTe booster) till patienter med RA, SpA och vaskulit ledde till adekvat antikroppssvar mot tetanus, men nedsatt mot difteri jämfört med friska kontroller. Sämre antikroppsvar var associerat till behandling med rituximab och metotrexat (1). Eftersom effektdata saknas för patienter som fått rituximab inom 24 veckor rekommenderas att dessa även får passiv immunisering i de fall de utsätts för allvarlig risk att drabbas av stelkramp. Samråd med infektionsläkare rekommenderas i dessa fall.
Svenska rekommendationer för befolkningen då risk för stelkramp anses föreligga:
- En tidigare injektion stelkrampsvaccin: Vid skadetillfället ges full dos vaccin mot stelkramp och difteri, och patienten uppmanas att själv beställa tid för en tredje injektion efter ca ett år (minst 6 månader).
- Två tidigare injektioner stelkrampsvaccin: Om mer än 6 månader har förflutit efter senaste injektionen ges en tredje injektion (motsvarande den tredje injektionen i grundvaccinationsschemat för vuxna).
- Tre tidigare injektioner stelkrampsvaccin: Om 10 år eller mer har förflutit från tredje injektionen ges en påfyllnadsdos av difteri och stelkrampsvaccin med reducerad antigenhalt. Om däremot kortare tid har förflutit ges normalt inget vaccin.
- Fyra eller fler tidigare injektioner stelkrampsvaccin: En påfyllnadsdos med reducerad antigenhalt ges om 20 år eller mer har förflutit sedan den senaste injektionen.
- Den skadades vaccinationsstatus är okänt: Vid misstanke om att den skadade kan vara ovaccinerad, och där läkare bedömer att det finns risk för stelkramp, ges immunglobulin samt full dos vaccin efter provtagning för bestämning av antikroppsnivå mot stelkramp. Vidare handläggning bestäms utifrån detta svar.
Pris för en påfyllnadsdos på vårdcentralen är ca 500 kr. Priset hos privata vårdgivare varierar.
5. Vaccination mot bältros rekommenderas till vuxna patienter med IRS som har en ökad risk för sjukdomen på grund av ålder, sjukdom eller läkemedelsbehandling. Icke-levande vaccin mot herpes zosterinfektion finns tillgängligt i Sverige och rekommenderas till patienter med IRS
Bakgrundsinformation
Patienter med IRS har en ökad risk att utveckla herpes zoster (HZ); i genomsnitt är risken 1.5–2 gånger ökad jämfört med motsvarande normalbefolkning. En retrospektiv analys av data från en stor nationell databas i USA konfirmerade ett samband mellan SLE, RA samt andra autoimmuna sjukdomar och en ökad risk för HZ (1). Anmärkningsvärt var att yngre personer (<50 år) med SLE, IBD och RA hade en högre förekomst av HZ än äldre friska personer i åldrarna 61–70 år utan känd autoimmun sjukdom eller diabetes. Den ålderspecifika incidensration (IR) av HZ hos RA eller SLE patienter ≥40 år var 1.5-2 gånger högre än risken bland friska äldre individer (IR 8.5 per 1000 personår).
Studier fokuserade på RA rapporterar kontinuerligt en 1.5–2 gånger ökad risk att drabbas av HZ, där högre ålder, hög sjukdomsaktivitet och högre kortisondoser har varit de viktigaste riskfaktorerna. Om behandling med anti-TNF och andra biologiska läkemedel ökar risken för HZ är fortfarande kontroversiellt. Vissa studier rapporterade att anti-TNF behandling var associerad med signifikant större risk för HZ jämfört med csDMARD och dessutom med mer allvarlig HZ-sjukdom, medan andra rapporterade ungefär samma risk för HZ för biologiska läkemedel med olika verkningsmekanismer och csDMARDs. Slutligen har en meta-analys av 26 observationella studier inte funnit någon ökad risk för HZ bland patienter behandlade med olika biologiska läkemedel och csDMARDs. Däremot har man visat att behandling med JAK–hämmare (tofacitinib) fördubblade risken för HZ hos RA patienter jämfört med behandling med biologiska läkemedel. Integrerad analys av data från globala studier av tofacitinib hos patienter med RA rapporterade en IR på 3.9 (3.6 to 4.2) för (alla typer av) HZ och IR för disseminerad eller multidermatomal HZ på 0.3 (0.2 to 0.4). I likhet med tofacitinib är baricitinib också associerad med ökad HZ risk, vilket var huvudanledningen för avbruten behandling i kliniska baracitinibstudier.
Bland patienter med IRS har SLE-patienter i alla åldrar en ökad benägenhet att drabbas av HZ, med en uppskattad årsincidens på 6.4–37.7/1000 patient år, motsvarande 2–10 gånger ökad risk jämfört med befolkningen i övrigt. Risken att utveckla HZ är speciellt ökad hos barn med SLE. Vidare har man rapporterat en ökad trend för inläggning på sjukhus på grund av HZ hos SLE-patienter jämfört med icke-SLE patienter under de senaste 10 åren. Bland de viktigaste riskfaktorerna för HZ hos SLE patienter är användning av steroider och immunsuppressiv behandling med koppling till ökande dos. Nya läkemedel för SLE, anifrolumab och sifalimumab (typ 1-interferon antagonister), verkar också öka risken för HZ.
En ökad risk för HZ har rapporterats också bland patienter med dermatomyosit, polymyosit samt kutan LE.
I en retrospektiv databasstudie som inkluderade patienter med olika immunmedierade sjukdomar (RA, PsA, AS, psoriasis, IBD) var vaccination med levande försvagat herpes zostervaccin (Zostavax®) associerat med minskad incidens av HZ bland patienter äldre än 60 år; detta oavsett medicinering inklusive biologiska läkemedel. Vaccinerade patienter hade minskad incidens av HZ de första 42 dagarna efter vaccination. Inga fall av meningit eller encefalit registrerades under den perioden. Vidare visade sig vaccinet vara immunogent och säkert i en mindre grupp av patienter med SLE och bland steroid-behandlade patienter med olika reumatiska sjukdomar (i dosen 5–20 mg/dygn). Administration av Zostavax® till RA patienter behandlade med metotrexat två veckor före start av tofacitinib visade sig vara säkert och immunogent. Större prospektiva studier med tillräcklig statistisk styrka för bedömning av säkerhet av detta försvagade levande vaccin saknas.
Det nya, adjuvanterat, subenhet, icke-levande vaccinet (Shingrix®) mot herpes zoster har visat sig vara säkrare och mer effektivt än det levande försvagade vaccinet bland personer >50 och >70 år. Effektivitet av detta zostervaccin har inte undersökts bland patienter med IRS men vaccinet har visat sig vara immunogent i mindre studier genomförda bland patienter med reumatiska sjukdomar. Vaccinet har blivit tillgängligt i Sverige på vaccinationscentra under år 2020. Shingrix® kan ges till patienter som tidigare haft bältros. En svensk vaccinationsstudie visade att ca 80% patienter med RA behandlade med JAK-hämmare utvecklade tillräckligt bra antikroppssvar efter vaccination med två doser av subenhetsvaccinet (24). Folkhälsomyndigheten rekommenderar vaccination mot bältros till vuxna personer med immunbrist orsakat av sjukdom eller av läkemedelsbehandling, och de äldre åldersgrupperna med en stegvis introduktion från de äldsta (med start till gruppen 82 år och äldre) ned till 65 års ålder (25).
Shingrix vaccinet fanns inte på marknaden när senaste EULAR rekommendationer publicerades och nämns därför inte i dessa. I de senaste ACR guidelines är vaccination med detta adjuvanterat vaccin mot HZ starkt rekommenderat till alla patienter över 18 år med IRS som behandlas med immunsupprimerande läkemedel (13). För närvarande kostar 2 vaccindoser ca 5000 kronor
6.Human papillomavirusvaccination bör övervägas till yngre IRS-patienter som inte tidigare vaccinerats.
Human papillomavirus (HPV)-infektion inklusive de virussubtyper som medför ökad risk för senare malignitetsutveckling är vanligare hos SLE-patienter än i normalbefolkningen. HPV-vaccination bör övervägas till unga patienter med IRS, särskilt vid SLE-diagnos.
HPV vaccination har ingått i det allmänna vaccinationsprogrammet för flickor sedan 2010. Från och med höstterminen 2020 erbjuds inom allmänna vaccinationsprogrammet ett niovalent vaccin mot HPV (Gardasil 9) även till pojkar och omfattar pojkar födda 2009 och senare (www.folkhalsomyndigheten.se). För att få bäst effekt bör vaccinet ges innan man blivit infekterad med HPV och en exakt övre åldersgräns för vaccination av IRS-patienter är svår att fastslå. Alla vacciner skyddar mot HPV typ 16 och 18. Det är de HPV-typer som oftast orsakar livmoderhalscancer (omkring 70 procent av fallen) och analcancer (76 procent av fallen). Studier av HPV-infektion och konsekvenser av denna hos män med IRS saknas.
Bakgrundsinformation
Bland patienter med IRS har prevalensen av human papillomavirus (HPV)-infektion studerats mest hos patienter med SLE. Ökad risk för HPV-infektion (upp till 3 gånger) har rapporterats bland SLE jämfört med icke-SLE patienter i hela världen (1). I en koreansk SLE- kohort, var prevalensen av högrisk HPV-infektion 24.6% jämfört med 7.9% hos kontroller (p<0.001, odds ratio 3.8, 95%, CI 2.5-5.7) och liknande prevalens rapporterades från en brasiliansk SLE-kohort. Speciellt hög prevalens av HPV rapporterades från en annan brasiliansk SLE-kohort (80,7%) jämfört med 35,7% hos friska kvinnor. I en mexikansk SLE- kohort ökade den kumulativa prevalensen av HPV-infektion från 22,8% från start till 33,8% efter 3 år (p = <0,001). I denna studie var risk för någon typ av HPV-infektion 10.1 per 1000 patientmånader. En systematisk litteraturgenomgång drar slutsatsen att SLE är associerad med en ökad prevalens av cervikal dysplasi men inte cervikal cancer. HPV-infektion, multipla infektioner, hög-risk HPV-typer och persistent infektion var associerad med utveckling av squamous intraepithelial lesions (SIL) under 3 år i en prospektiv studie från Kina (1). Andra variabler associerade med HPV-infektion bland SLE patienter var flera sexuella partners, tidigare HPV infektion, tidigare könssjukdom, och yngre ålder. SLE-sjukdom var en oberoende riskfaktor för HPV-infektion, oavsett de traditionella riskfaktorerna för HPV-infektion och en riskfaktor för hög-risk HPV-subtyper. Effekten av immunsuppressiv terapi för risken att utveckla HPV-infektion är fortfarande kontroversiell, med det finns vissa data som stödjer ett kausalt samband, speciellt relaterat till hög kumulativ dos av systemiska steroider, azatioprin och cyklofosfamid behandling.
Hos patienter med RA observerades en trend till lägre prevalens av HPV-infektion hos patienter före anti-TNF behandling jämfört med kontroller (14 vs. 30 %, p= 0,054). Behandling med anti-TNF (under 6 månader) ökade inte risken för exacerbation och/eller progress av HPV-infektion i en liten kohort av RA-patienter. I en liten kohort med SSc-patienter (begränsad och diffus sjukdom), skilde sig inte prevalensen av HPV-infektion mellan patienter och kontroller (32% vs 38%).
HPV-vaccination med bivalent eller quadrivalent vaccin är effektivt hos majoriteten av unga kvinnliga patienter med IRS. Tre studier genomfördes av vuxna patienter med SLE, och alla visade adekvat svar. Två av tre studier rapporterade SLE-skov i upp till en tredjedel av patienterna efter vaccination. Det finns inga andra studier som undersökt förekomst av skov i reumatiska sjukdomen vid HPV-vaccination bland patienter med IRS. Även om det finns fallrapporter och fallserier om debut av autoimmunsjukdom efter HPV-vaccination, har inte populationsbaserade studier påvisat att quadrivalent HPV-vaccin var associerat med ökad incidens av nydebuterade autoimmuna sjukdomar hos flickor eller kvinnor med existerande autoimmun sjukdom. Quadrivalent HPV-vaccin har associerats med tromboemboliska händelser. Emellertid hade 90% av patienterna med 31 säkerställda tromboemboliska händelser en känd riskfaktor för tromboembolisk sjukdom, därav två med känt antifosfolipidsyndrom.
HPV vaccination för barn är kostnadsfri och pris för vaccination av vuxna på vårdcentral är ca 600 kr/dos. Priser hos privata vårdgivare varierar.
7. Hepatit A och/eller B-vaccination bör ges till IRS-patienter med ökad risk för sådan smitta.
Vaccination rekommenderas endast till riskgrupper för hepatit vilket inkluderar resa till land med endemisk hepatit A och/eller B, ökad expositionsrisk (till exempel medicinsk profession) eller känd exposition för hepatit A och/eller B (infekterad familjemedlem/annan kontakt) (1). Före vaccinationen skall man säkerställa att skyddande nivåer av antikroppar mot hepatit A och/eller B saknas. I en svensk studie rapporterades att 99% av RA-patienter behandlade med TNF-hämmare och/eller metotrexat som fick en extra hepatit A vaccindos före resan utvecklade protektiva antikroppsnivåer.
Bakgrundsinformation
Det finns endast ett fåtal studier av hepatit B-virus (HBV)- infektion hos IRS-patienter, och det saknas säkra uppgifter om incidens och prevalens. Varierande prevalens av hepatit B-bärarskap och ockult HBV- infektion bland patienter med IRS har rapporterats från olika geografiska områden i världen. I Tyskland fann man en låg förekomst av HbsAg-bärarskap (0.2%) och HBV-exponering (anti-HBc Ab positivitet) (5.9%) vid första presentation av reumatisk sjukdom. Prevalensen av HBsAg-positivitet bland patienter med IRS (RA, SLE, SpA) behandlade med metotrexat i Thailand var också låg (0.58%), men en tredjedel av patienter hade varit exponerade för HBV (anti-HBc IgG positivitet) (37,6%). Ingen av dessa patienter fick hepatit B-reaktivering under i medeltal 9,9 år av metotrexatbehandling. I Japan detekterades positiv HBsAg hos 0.8% av RA-patienter vid start av anti-reumatisk behandling, medan 25.1% patienter hade varit exponerade för hepatit B (negativ HbsAg/positiv anti-HBc Ab). En taiwanesisk fall-kontrollstudie av RA-patienter genomförd under en tioårsperiod (1999–2009), visade högre förekomst av HBV hos RA patienter jämfört med icke-RA patienter (RA vs icke-RA = 69.9 vs 60.1 fall per 1000 individer). Hos patienter med SLE var prevalensen av HBV- bärarskap 0,9% i en israelisk studie, medan i Kina var HBV-prevalensen bland pediatriska och vuxna SLE patienter 2–4%. En internationell studie av komorbiditeter vid spondartrit rapporterade en prevalens av HBV-infektion på 3,3%.
Till skillnad från friska individer där vaccin mot hepatit A är starkt immunogent, verkar en dos av vaccin mot hepatit A inte vara tillräcklig för adekvat skydd hos patienter med RA, JIA, juvenil SLE och patienter behandlade med immunsuppressiva läkemedel. Den andra vaccindosen ges efter 6 månader. Om detta inte är möjligt vid exempelvis sista-minuten resor bör man vara medveten om att patienten kanske inte blir skyddad efter första dosen och överväga passiv immunisering till patienter som reser till vissa områden. Hepatit B-vaccin är effektivt för de flesta patienter med IRS.
Kostnaden för vaccination mot hepatit A eller hepatit B på vårdcentral är ca 450-500 kr/dos. Priset hos privata vårdgivare varierar.
8. IRS-patienter som planerar resor bör vaccineras enligt allmänna rekommendationer med undantag för levande försvagade vaccin.
Det är inte känt om patienter med IRS löper ökad risk att drabbas av infektioner som kan förebyggas med vaccination i samband med resor (1). Influensa är endemisk i subtropiskt och tropiskt klimat året runt och är den vanligaste infektionen som kan förebyggas genom vaccinering. Incidensen av influensa hos IRS-patienter är inte känd. Detsamma gäller incidensen av kolera, difteri, hepatit A, meningokockinfektion, polio, rabies, tetanus, fästingburen encefalit, tyfoidfeber och gula febern. Det är visat att patienter med RA och SLE allmänt har en ökad risk för insjuknande i tuberkulos (TBC), men majoriteten av dessa fall beror på reaktivering av latent TBC. BCG-vaccination har inte klart visats kunna förebygga TBC hos vuxna. Två år efter en oavsiktlig revaccination mot gula febern bland 31 kvinnor med olika IRS (RA, SLE, SSc, AS) fanns protektiva nivåer av neutraliserande antikroppar. Patienter behandlade med låg prednisolondos visade adekvat antikroppssvar efter vaccination mot gula febern och inga allvarliga biverkningar rapporterades. Även om inga allvarliga biverkningar rapporterades kan vaccin mot gula febern, BCG, oralt poliovaccin och oralt tyfoidvaccin leda till livshotande infektioner hos immunsupprimerade patienter. Patienter med IRS som planerar resor bör få de vaccinationer som ges enligt allmänna rekommendationer med undantag för BCG-vaccin, oralt poliovaccin, oralt tyfoidvaccin och gula febervaccin, vilka innehåller levande försvagade mikroorganismer.
9. Immunokompetenta familjemedlemmar till patienter med IRS bör uppmuntras att vaccineras enligt nationella riktlinjer.
Denna nya rekommendation från EULAR baseras i huvudsak på expertåsikt och följer riktlinjer från internationella organisationer som Infectious Diseases Society of America (IDSA). Immunokompetenta familjemedlemmar bör vaccineras både med icke-levande och levande försvagade vaccin enligt de nationella riktlinjerna. EULAR-gruppen rekommenderar undantag för oralt poliovaccin. Oralt poliovaccin finns inte registrerat i Sverige. Det inaktiverade poliovaccin som används här kan ges till IRS-patienter och deras familjemedlemmar. Starkt immunsupprimerade patienter bör undvika att hantera blöjor från barn som vaccinerats mot rotavirus under 4 veckor efter vaccinationen. Kontakt med personer med hudlesioner från varicella eller herpes zosterinfektion bör undvikas.
10. Vaccination med levande vaccin till barn som exponerats för immunmodulerande läkemedel under andra delen av graviditeten eller under amning sker enligt rekommendationer beskrivna i dokumentet: ”Nationell vägledning för vaccination med levande försvagade vaccin”, https://www.rikshandboken-bhv.se
Eftersom IgG passerar placentan under andra och framför allt under den tredje trimestern bör levande försvagade vaccin undvikas hos nyfödda barn till mödrar som har fått biologiskt läkemedel under andra graviditetshalvan (efter graviditetsvecka 21). Sex månader efter födelsen beräknar man att barn med prenatal exponering för biologiskt läkemedel har låga eller inte längre detekterbara nivåer av läkemedlet. Ökad risk för infektioner under första levnadsåret har rapporterats bland spädbarn till kvinnor med inflammatorisk tarmsjukdom som behandlats med infliximab i dosen 5 mg/kg i kombination med tiopuriner under hela graviditeten och risken var betydligt större än vid anti-TNF behandling given som monoterapi (26,27). Få infektioner diagnosticerades, alla var vanliga för åldern och svarade bra på behandling Det finns i litteraturen också ett diagnostiserat fall av fatal disseminerad tuberkulos (TBC) hos ett spädbarn som exponerats för infliximab in utero och sedan vaccinerats mot TBC (1).
September 2022 publicerades en vägledning för vaccination med levande försvagade vaccin, av barn som under graviditeten eller vid amning exponerats för immunmodulerande läkemedel (länk till nationell vägledning) (28). Vägledningen är framtagen genom systematisk insamlad evidens samt konsensusdiskussioner av en arbetsgrupp bestående av barnläkare, kliniska farmakologer, en reumatolog och en neurolog. Dokumentet ligger under ”rikshandboken barnhälsovård för professionen” och har en nationell förankring. Vaccination med levande vaccin till barn som exponerats för immunmodulerande läkemedel under andra delen av graviditeten eller under amning sker först efter en dokumenterad individuell läkarbedömning enligt denna vägledning.
Behandling med hydroxyklorokin under graviditet bedöms inte innebära risk vid vaccination av barn med levande försvagat vaccin på grund av dessa läkemedels relativt låga immundämpande effekt, även om formella studier saknas. Sulfasalazin bedöms ha en relativt låg immundämpande effekt men leukopenier är en vanlig biverkan. Det finns ingen kunskap om huruvida barn som exponerats under graviditet drabbas av leukopenier och fetal anemi är beskrivet i en fallstudie. Provtagning enbart för ställningstagande till vaccination är inte motiverat och i så fall borde man avstå från vaccination mot rotavirus. Mer detaljerad information on hur lång tid man borde avstå från levande vaccin för olika DMARDs, biologiska läkemedel eller kortison i motsvarande prednisolon i dosen ≥ 20 mg/dygn framgår från dokumentet.
Viktigt att påtala att dessa rekommendationer skiljer sig från senaste uppdaterade ACR rekommendationer från 2022 kan vaccination mot rotavirus ges till barn före 6 månaders ålder om modern behandlats med TNF- hämmare under graviditeten men inte om modern fått rituximab (11).
Följande levande försvagade vaccin finns registrerade för användning i Sverige (även i tabell sid 20/21): vaccin mot mässling-påssjuka-röda hund (MPR) (M-M-RVAXPRO®, Priorix®), oralt vaccin mot rotavirus (Rotarix®, RotaTeq®), vaccin mot gula febern (Stamaril®), vaccin mot tuberkulos (BCG-vaccin®), oralt tyfoidvaccin (Vivotif®) vaccin mot vattkoppor (Varilrix®, Varivax®) och herpes zoster (Zostavax®).
11. Vaccination mot RS virus kan ges till patienter från 60 år med IRS och nedsatt immunförsvar pg a sjukdom eller immunsupprimerande behandling.
RS virus (respiratory syncytialvirus) är en vanlig orsak till övre luftvägsinfektion och den vanligaste orsaken till nedre luftvägsinfektion hos barn yngre än ett år. RS- virus är en av huvudorsakerna till att spädbarn läggs in på sjukhus i Europa. Viruset kan orsaka akut infektion i nedre luftvägarna och lunginflammation, och kan leda till allvarliga andningsbesvär. En sådan infektion kan också vara allvarlig för vuxna och äldre eftersom den kan orsaka akut luftvägsinfektion, influensaliknande sjukdom eller lunginflammation. Två vaccin mot RS virus är godkända sedan sommaren 2023 inom EU. Vaccinet kan ges till kvinnor under graviditeten för att skydda barnet de första sex månaderna från att insjukna i allvarlig RS-virusorsakad luftvägsinfektion. Vaccinet kan även ge skydd till personer som är 60 år och äldre (29,30). Vaccinet innehåller två rekombinanta stabiliserade RSV prefusion F-antigener som representerar subgrupperna RSV-A och RSV-B och är således icke-levande och kan ges till immunsupprimerade individer. RS-virusvaccin rekommenderas säsongen 2023/2024 till personer som är 75 år och äldre (som fyller år innevarande år). Detta baseras på en högre risk för allvarlig nedre luftvägsinfektion orsakad av RS-virus i åldersgruppen. Vaccin rekommenderas även till personer från 60 år med tillstånd som innebär kraftigt nedsatt immunförsvar på grund av sjukdom eller behandling (30). Några specifika rekommendationer om vaccination mot RS-virus bland patienter med IRS finns inte.
Kostnaden för vaccination mot RS-virus är 2000 kr eller strax däröver och betalas av patienten själv.
12.Vaccination mot TBE
I områden där fästingburen tick-borne encephalitis (TBE) förekommer bör även patienter med IRS vaccineras. Begränsad kunskap finns om TBE-vaccination i denna patientgrupp. En svensk studie visar preliminärt kraftigt nedsatt antikroppssvar hos patienter behandlade med metotrexat och TNF-hämmare, och i den mån det är möjligt är vaccination före behandling att föredra. Extra boosterdos kan också övervägas. Ingen särskild säkerhetsproblematik noterades (31). Kostnaden för vaccination är ca 450 kronor/dos och betalas av patienten själv.
13. Vaccination mot Mpox (tidigare kallad apkoppor)
Mpox orsakas av apkoppsvirus (art av ortopoxvirus) och delas upp i två typer: klad 1 och klad 2, som i sin tur delas upp i klad 1a och klad 1b respektive klad 2a och klad 2b. Klad 1 har rapporterats som allvarligare med väsentligt högre dödlighet än klad 2. Klad 1 är dessutom mer smittsamt. Vaccinet rekommenderas till personer som har en ökad risk för att smittas med mpox och kan ges i förebyggande syfte som preexpositionsprofylax eller efter exponering som postexpositionsprofylax. Vaccinet innehåller ett levande, försvagat vacciniavirus som inte förökar sig hos människor. Vaccinet kan därför ges till personer med immunbrist (32).
14. Vaccination mot kikhosta (pertussis)
Kikhosta orsakas av bakterien Bordetella pertussis. Vaccinet är ett kombinationsvaccin innehållande difteritoxoid, tetanus och acellulär pertussis. Sedan 2022 rekommenderas vaccination mot kikhosta för gravida från gravidvecka 16. Syftet med vaccinationen är att skydda de allra yngsta spädbarnen mot svår sjukdom vid kikhosta. Vaccination ingår i svenska barnvaccinationsprogrammet (första dos ges vid 3 månaders åldern) (33).
15. Splenektomerade eller patienter med IRS med nedsatt mjältfunktion rekommenderas vaccination i samråd med infektionsläkare.
Patienter som är splenektomerade eller har funktionell hyposplenism löper risk att drabbas av s.k. “overwhelming post-splenectomy infection (OPSI)”. OPSI orsakas av inkapslade bakterier (exempelvis S. pneumoniae, H. influenzae B, N. meningitidis) och mortaliteten i OPSI är upp till 70%. OPSI kan komma som sekundärinfektion efter influensa. Det saknas effektivitetsstudier av vaccination till hypospleniska/aspleniska patienter med IRS för att förebygga OPSI. Den generella konsensusrekommendationen är att dessa patienter ska vaccineras mot influensa, pneumokocker, H. influenzae B och N. meningokocker C. När dessa patienter skall resa till områden där andra meningokockstammar är endemiska (A, Y, W135), är vaccination även mot dessa stammar indicerad (34). Vår bedömning är att vaccinering av denna patientgrupp ska värderas och planeras i samråd med infektionskollegor.
Allmänna kommentarer
I många regioner i Sverige är vaccination mot influensa och pneumokocker kostnadsfri för alla personer ≥ 65 år. För personer yngre än 65 år som tillhör riskgrupperna är dessa vaccinationer antingen kostnadsfria eller man betalar ofta en lägre avgift.
Rekommendationer för vaccination för barn med juvenil idiopatisk artrit (JIA) återfinns på barnläkarföreningens hemsida (http://www.blf.net/reumatologi/index.html).
Tabeller och flödesscheman
Tabell 1. Vanliga smittämnen och motsvarande vaccin.
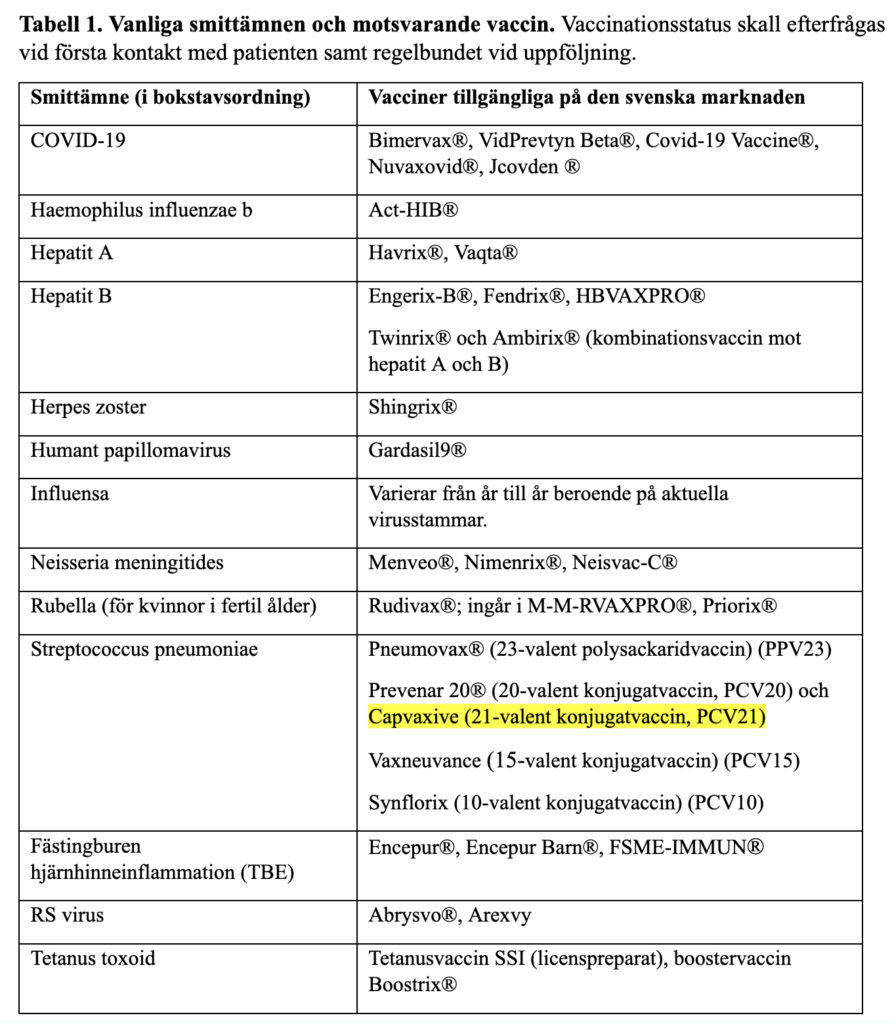
Tabell 2. Exempel på levande försvagade vaccin tillgängliga i Sverige
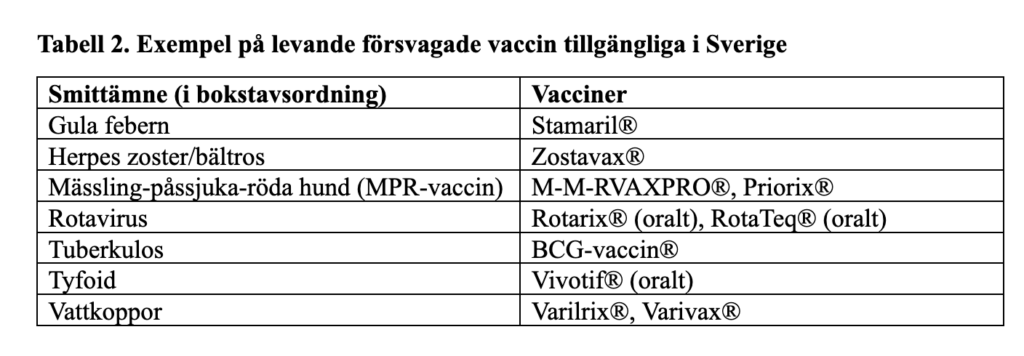
Tabell 3. ACR rekommendationer om uppehåll med aktiv anti-reumatisk behandling vid planerad vaccination med levande vaccin
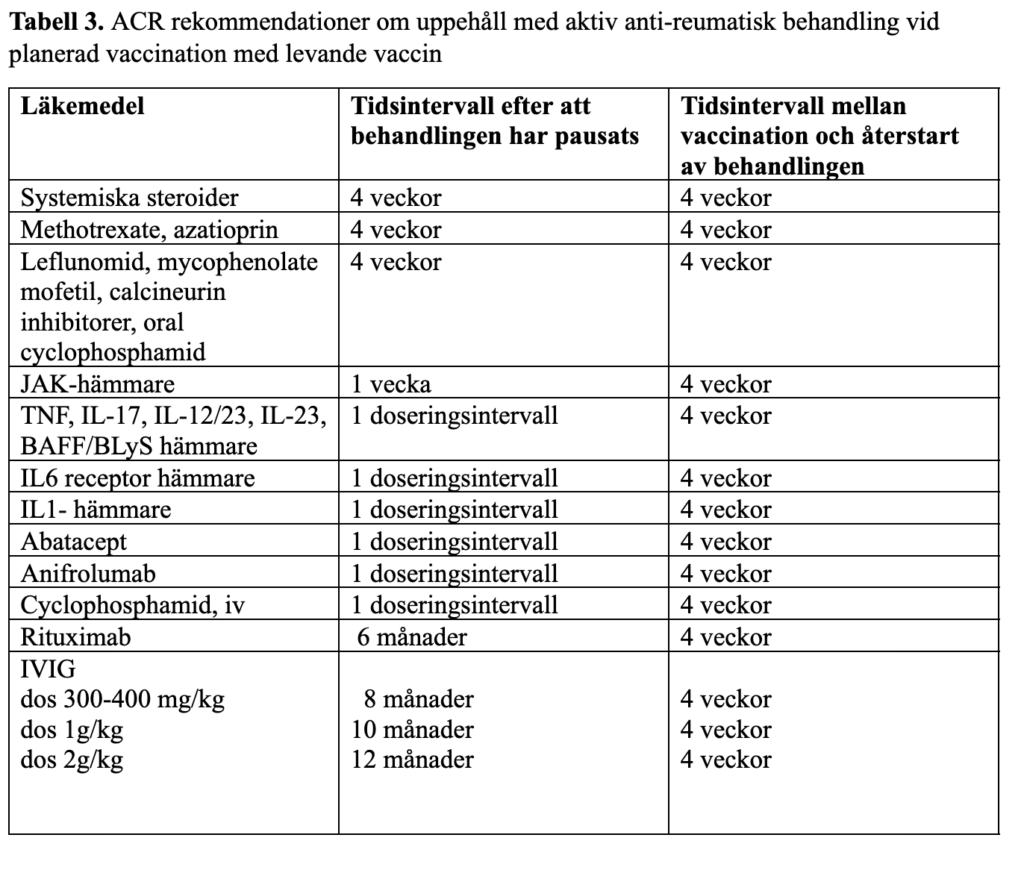
Tabell 4. Riskgrupper som omfattas av det nationella särskilda vaccinationsprogrammet mot pneumokocker.
Tabell 5. Ytterligare grupper med ökad risk för allvarlig pneumokocksjukdom som rekommenderas vaccination.
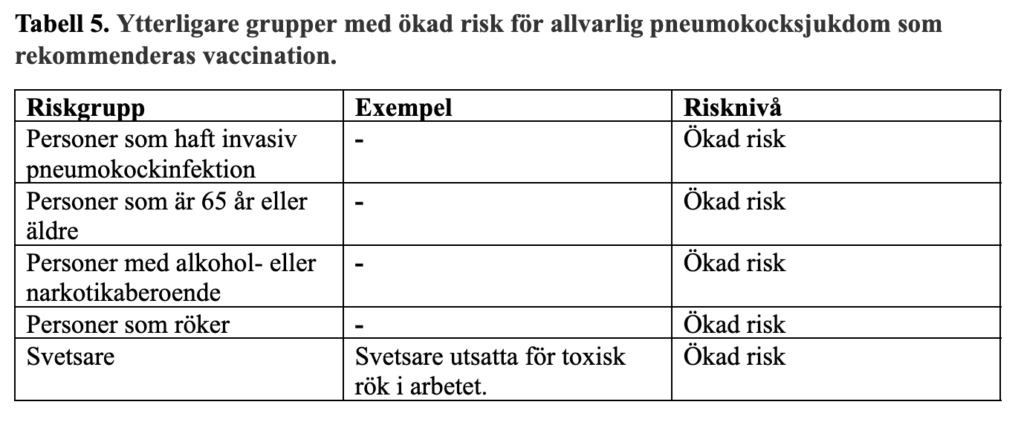
Tabell 6. Vaccinationsrekommendationer för personer 18 år och äldre, utifrån tidigare vaccinationsstatus.
Tabell 7. Förslag på patientgrupper med inflammatorisk reumatisk sjukdom med mycket hög risk för allvarlig pneumokocksjukdom som rekommenderas en dos konjugatvaccin med minst 20 serotyper minst 1 år efter senaste dosen av PCV13/PCV15/PPV23.

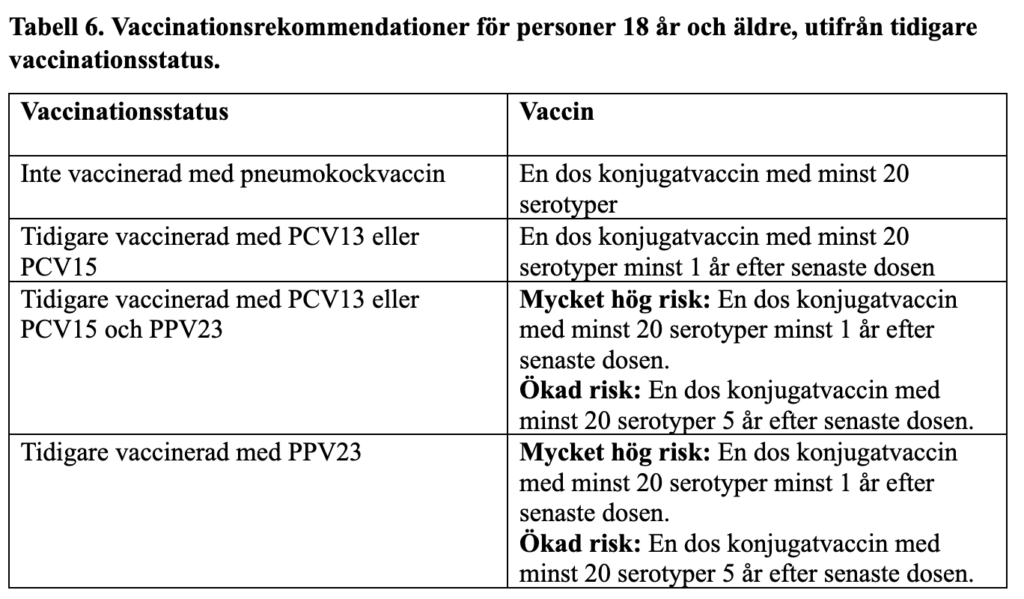
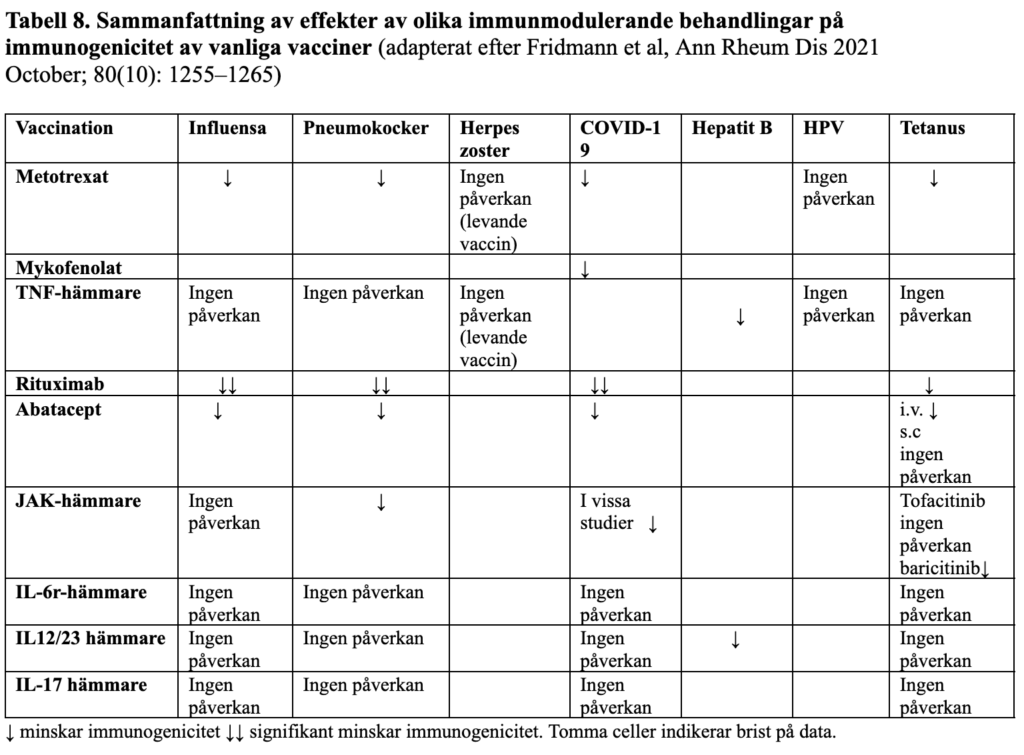
Tabell 8. Sammanfattning av effekter av olika immunmodulerande behandlingar på immunogenicitet av vanliga vacciner.
Referenser
Referenser
- Furer V, Rondaan C, Heijstek MW, Agmon-Levin N, van Assen S, Bijl M, Breedveld FC, D’Amelio R, Dougados M, Kapetanovic MC, van Laar JM, de Thurah A, Landewé RB, Molto A, Müller-Ladner U, Schreiber K, Smolar L, Walker J, Warnatz K, Wulffraat NM, Elkayam O. 2019 update of EULAR recommendations for vaccination in adult patients with autoimmune inflammatory rheumatic diseases. Annals of the rheumatic diseases. 2019 Aug 14.
- Nguyen M, Lindegaard H, Hendricks O, Friis-Moller N. Factors associated with influenza and pneumococcal vaccine uptake among rheumatoid arthritis patients in Denmark invited to participate in a pneumococcal vaccine trial (Immunovax_RA). Scand J Rheumatol. 2017:1-8.
- Campos LM, Silva CA, Aikawa NE, Jesus AA, Moraes JC, Miraglia J, et al. High disease activity: an independent factor for reduced immunogenicity of the pandemic influenza a vaccine in patients with juvenile systemic lupus erythematosus. Arthritis care & research. 2013;65(7):1121-7.
- Hua C, Barnetche T, Combe B, Morel J. Effect of methotrexate, anti-tumor necrosis factor alpha, and rituximab on the immune response to influenza and pneumococcal vaccines in patients with rheumatoid arthritis: a systematic review and meta-analysis. Arthritis care & research. 2014;66(7):1016-26.
- Heijstek MW, van Gageldonk PG, Berbers GA, Wulffraat NM. Differences in persistence of measles, mumps, rubella, diphtheria and tetanus antibodies between children with rheumatic disease and healthy controls: a retrospective cross-sectional study. Annals of the rheumatic diseases. 2012;71(6):948-54.
- Miyamoto M, Ono E, Barbosa C, Terreri M, Hilario M, Salomao R, et al. Vaccine antibodies and T- and B-cell interaction in juvenile systemic lupus erythematosus. Lupus. 2011;20(7):736-44.
- Borte S, Liebert UG, Borte M, Sack U. Efficacy of measles, mumps and rubella revaccination in children with juvenile idiopathic arthritis treated with methotrexate and etanercept. Rheumatology (Oxford, England). 2009;48(2):144-8.
- Heijstek MW, Kamphuis S, Armbrust W, Swart J, Gorter S, de Vries LD, et al. Effects of the live attenuated measles-mumps-rubella booster vaccination on disease activity in patients with juvenile idiopathic arthritis: a randomized trial. JAMA. 2013;309(23):2449-56.
- Zhang J, Xie F, Delzell E, Chen L, Winthrop KL, Lewis JD, et al. Association between vaccination for herpes zoster and risk of herpes zoster infection among older patients with selected immune-mediated diseases. JAMA. 2012;308(1):43-9.
- Curtis JR, Cofield SS, Bridges SL Jr, Bassler J, Deodhar A, Ford TL, Huffstutter J, Jankeel A, Kivitz A, Kamal S, Lindsey S, Messaoudi I, Mendoza N, Michaud K, Mikuls TR, Ridley D, Shergy W, Siegel SAR, Winthrop KL. The Safety and Immunologic Effectiveness of the Live Varicella-Zoster Vaccine in Patients Receiving Tumor Necrosis Factor Inhibitor Therapy: A Randomized Controlled Trial. Ann Intern Med. 2021 Nov;174(11):1510-1518.
- Friedman MA, Curtis JR, Winthrop KL. Impact of disease-modifying antirheumatic drugs on vaccine immunogenicity in patients with inflammatory rheumatic and musculoskeletal diseases. Ann Rheum Dis. 2021 Oct;80(10):1255-1265.
- van Sleen Y, van der Geest KSM, Huckriede ALW, van Baarle D, Brouwer E. Effect of DMARDs on the immunogenicity of vaccines. Nat Rev Rheumatol. 2023 Sep;19(9):560-575.
- Bass AR, Chakravarty E, Akl EA, et al. 2022 American College of Rheumatology Guideline for Vaccinations in Patients With Rheumatic and Musculoskeletal Diseases. Arthritis Care Res (Hoboken). 2023 Mar;75(3):449-464.
- Nakafero G, Grainge MJ, Myles PR, Mallen CD, Zhang W, Doherty M, Nguyen-Van-Tam JS, Abhishek A. Effectiveness of inactivated influenza vaccine in autoimmune rheumatic diseases treated with disease-modifying anti-rheumatic drugs. Rheumatology (Oxford). 2020 Dec 1;59(12):3666-3675.
- Folkhälsomybdigheten. Rekommendationer om influensavaccination till riskgrupper — Folkhälsomyndigheten. https://www.folkhalsomyndigheten.se
- Folkhalsomyndigheten. Vaccinationsprogrammet mot pneumokocker för riskgrupper. https://www.folkhalsomyndigheten.se
- Vårdgivare Skåne. Pneumokockvaccination av riskgrupper https://vardgivare.skane.se/kompetens-utveckling/nyheter/nyheter/2023/pneumokockvaccination-av-riskgrupper
- Folkhalsomyndigheten. Rekommendationer för vaccination mot covid-19. (https://www.folkhalsomyndigheten.se)
- Kroon FPB, Najm A, Alunno A, Schoones JW, Landewé RBM, Machado PM, Navarro-Compán V. Risk and prognosis of SARS-CoV-2 infection and vaccination against SARS-CoV-2 in rheumatic and musculoskeletal diseases: a systematic literature review to inform EULAR recommendations. Ann Rheum Dis. 2022 Mar;81(3):422-432
- Machado PM, Lawson-Tovey S, Strangfeld A, Mateus EF, Hyrich KL, Gossec L, Carmona L, Rodrigues A, Raffeiner B, Duarte C, Hachulla E, Veillard E, Strakova E, Burmester GR, Yardımcı GK, Gomez-Puerta JA, Zepa J, Kearsley-Fleet L, Trefond L, Cunha M, Mosca M, Cornalba M, Soubrier M, Roux N, Brocq O, Durez P, Conway R, Goulenok T, Bijlsma JW, McInnes IB, Mariette X. Safety of vaccination against SARS-CoV-2 in people with rheumatic and musculoskeletal diseases: results from the EULAR Coronavirus Vaccine (COVAX) physician-reported registry. Ann Rheum Dis. 2022 May;81(5):695-709.
- Landewé RBM, Kroon FPB, Alunno A, Najm A, Bijlsma JW, Burmester GR, Caporali R, Combe B, Conway R, Curtis JR, Elkayam O, Gossec L, Heijstek MW, Haupt L, Iagnocco A, Isaacs JD, Juhász IÁ, Makri S, Mariette X, McInnes IB, Mehta P, Mueller-Ladner U, Schulze-Koops H, Smolen JS, Wiek D, Winthrop KL, Navarro-Compán V, Machado PM. EULAR recommendations for the management and vaccination of people with rheumatic and musculoskeletal diseases in the context of SARS-CoV-2: the November 2021 update. Ann Rheum Dis. 2022 Dec;81(12):1628-1639
- Smith JB, Gonzales EG, Li BH, Langer-Gould A. Analysis of Rituximab Use, Time Between Rituximab and SARS-CoV-2 Vaccination, and COVID-19 Hospitalization or Death in Patients With Multiple Sclerosis. JAMA Netw Open. 2022 Dec 1;5(12):e2248664.
- Frodlund M, Nived P, Chatzidionysiou A, Södergren A, Klingberg E, Bengtsson A, Hansson M, Olsson S, Pin E, Klareskog L, Kapetanovic MC. The impact of immunomodulating treatment on the immunogenicity of COVID-19 vaccines in patients with immune-mediated inflammatory rheumatic diseases compared to healthy controls. A Swedish nationwide study (COVID19-REUMA). Vaccine. 2023 May 11;41(20):3247-3257.
- Källmark H, Bergström T, Nagel J, Gullstrand B, Einarsson JT, Bengtsson AA, Kapetanovic MC. Serologic immunogenicity and safety of herpes zoster subunit vaccine in patients with rheumatoid arthritis receiving Janus kinase inhibitors. Rheumatology (Oxford). 2024 Jul 1;63(7):2024-2033.
- Folkhälsomyndighet. Vaccination mot bältros — Folkhälsomyndigheten. https://www.folkhalsomyndigheten.se
- Gisbert JP, Chaparro M. Safety of anti-TNF agents during pregnancy and breastfeeding in women with inflammatory bowel disease. The American journal of gastroenterology. 2013;108(9):1426-38
- Fritzsche J, Pilch A, Mury D, Schaefer C, Weber-Schoendorfer C. Infliximab and adalimumab use during breastfeeding. J Clin Gastroenterol. 2012 Sep;46(8):718-9.
- Vägledning för vaccination med levande försvagade vaccin, av barn som under graviditeten eller vid amning exponerats för immunmodulerande läkemedel. nationell-vagledning-levande-vaccin-immunhammande.pdf (rikshandboken-bhv.se). https://www.rikshandboken-bhv.se/for-bhv/aktuellt-i-barnhalsovarden/vagledning-for-vaccination-med-levande-vaccin-till-barn-som-exponerats-for-immunhammande-lakemedel/ och startsidan https://www.rikshandboken-bhv.se/”
- Vaccin mot RS-virus godkänt. Läkemedelsverket (lakemedelsverket.se)
- Folkhälsomyndigheten. Vaccination mot RS-virus — Folkhälsomyndigheten (https://www.folkhalsomyndigheten.se)
- Hertzell KB, Pauksens K, Rombo L, Knight A, Vene S, Askling HH. Tick-borne encephalitis (TBE) vaccine to medically immunosuppressed patients with rheumatoid arthritis: A prospective, open-label, multi-centre study. Vaccine. 2016 Jan 27;34(5):650-655.
- Folkhälsomyndigheten. Sjukdomsinformation om mpox- Folkhälsomyndigheten (https://wwwfolkhalsomyndigheten.se)
- Folkhälsomyndigheten. Vaccination mot kikhosta. (https://www.folkhalsomyndigheten.se)
- Bianchi FP, Stefanizzi P, Spinelli G, Mascipinto S, Tafuri S. Immunization coverage among asplenic patients and strategies to increase vaccination compliance: a systematic review and meta-analysis. Expert Rev Vaccines. 2021 Mar;20(3):297-308.

