Rekommendationer avseende anti-inflammatorisk och immun-modulerande behandling i samband med graviditet och amning
Introduktion
På uppdrag av Svensk Reumatologisk Förening 2026
Evy Björnehall (ordförande), Aleksandra Antovic, Marie Fischer, Daniel Glinatsi, Karin Hellgren, Carmen Roseman och Muna Saleh.
Syftet med dessa rekommendationer är att sammanfatta aktuella principer för en säker läkemedelshantering inför och under graviditet och amning hos patienter med reumatisk sjukdom.
Riktlinjerna är utformade för att utgöra ett stöd i den kliniska handläggningen. Den kliniska rekommendationen baseras på tillgänglig evidens i litteraturen och, i frånvaro av sådan, på internationell konsensus och beprövad erfarenhet. För nyare preparat där klinisk erfarenhet saknas, eller är begränsad, baseras rekommendationen på respektive preparats produktresumé/FASS-text. Detaljerad sammanfattning med bakgrundsdata och referenser för vart och ett av preparaten återfinns i tabellform.
Det bör också påpekas att det alltid är behandlande reumatolog som ansvarar för handläggning av sina patienter. Referenslistan innefattar nyckelreferenser, men gör inte anspråk på att vara någon fullständig sammanställning av all relevant litteratur på området.
Innehåll
Generella rekommendationer
Data talar för att hög sjukdomsaktivitet i en reumatisk sjukdom under graviditeten innebär ökad risk för negativa graviditets- och förlossningsutfall såsom för tidig födsel och tillväxthämning hos fostret. Uppmuntra därför patienten att planera graviditeten till en period då sjukdomen är lågaktiv, helst sedan minst 6 månader tillbaka (1). Då detta inte alltid är möjligt, och då graviditet i sig kan ge upphov till ökad sjukdomsaktivitet, kommer många patienter att vara i behov av behandling med läkemedel under graviditeten.
En viktig läkemedelsaspekt är risk för teratogena effekter. Den mest vulnerabla perioden för detta är från 4 fullgångna graviditetsveckor fram till vecka 10 med en glidande övergång till vecka 12, det vill säga ofta före tidpunkten för inskrivning på Mödravårdscentralen. Det är därför av stor vikt att patienter (män och kvinnor) med aktuell eller framtida barnönskan noggrant informeras om att graviditet bör planeras så att den medicinska behandlingen i god tid kan justeras. Det är också viktigt att behandlade läkare efterhör att patienten använder sig av en effektiv preventivmetod inför start, och under behandling, med teratogena läkemedel. Om graviditet uppstår hos en kvinna som är exponerad för teratogena läkemedel tiden runt konception och/eller i tidig graviditet är det viktigt med snabbt samråd mellan kvinnan, hennes partner, specialistmödravården samt behandlade reumatolog för att ge kvinnan så bra information som möjligt för att kunna fatta beslut om att fortsätta eller avbryta graviditeten.
Risken att framkalla fosterpåverkan med läkemedel måste alltid vägas mot risken av att inte förebygga eller behandla en kronisk sjukdom. I varje enskilt patientfall bör därför behandlande läkare överväga om indikation föreligger för fortsatt behandling. Lägsta möjliga dos av samtliga preparat skall alltid eftersträvas.
Vaccination av barn
Beträffande rekommendation kring vaccination av barn, som har exponerats för immunmodulerande läkemedel under graviditet eller amning, se rekommendationer avseende levande vaccin till barn vilka har exponerats in utero för biologisk behandling sidorna 14-15.
Nyheter 2026
Texten om flertalet läkemedel har uppdaterats och omformulerats.
De nya EULAR-rekommendationerna har publicerats under året. Hänsyn till dessa har naturligtvis tagits, och i de fall där EULAR-rekommendationerna har avvikit mycket från SRFs rekommendationer har vi granskat underlaget extra noggrant. Grad av evidens, mängd exponerade patienter och farmakokinetik hos läkemedlet i fråga i studierna har vägt tyngst när vi har gjort årets uppdatering.
Tabellen med översikt över läkemedlen i dokumentets början är borttagen inför årets uppdatering, av flera anledningar. Läkemedlen har ökat stort i antal. Betydligt fler kan tas under graviditet eller fram till konstaterad graviditet och möjligheterna att nyansera rekommendationerna saknades i den översiktliga tabellen.
Tabellen med klinisk rekommendation avseende levande vaccin till barn som har exponerats in utero för biologisk behandling har omarbetats för att bli tydligare.
Tillägg av nya läkemedel: avakopan, benralizumab, bimekizumab, bosentan, mepolizumab, obinutuzumab och sildenafil.
Kvinnor
NSAID och glukokortikoider
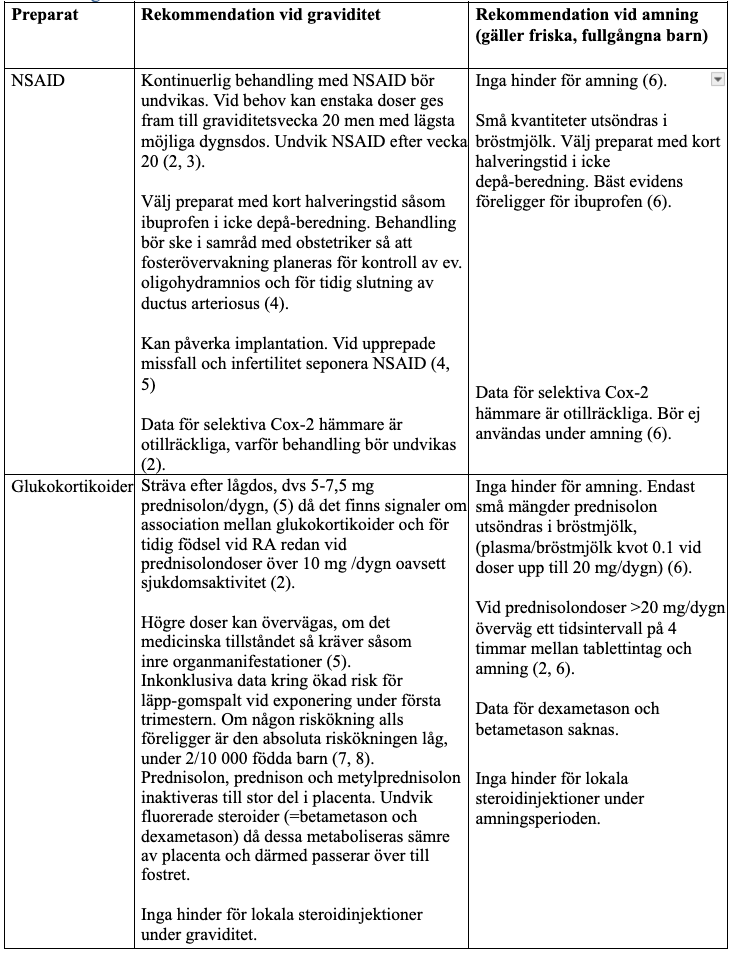
Konventionella syntetiska DMARD
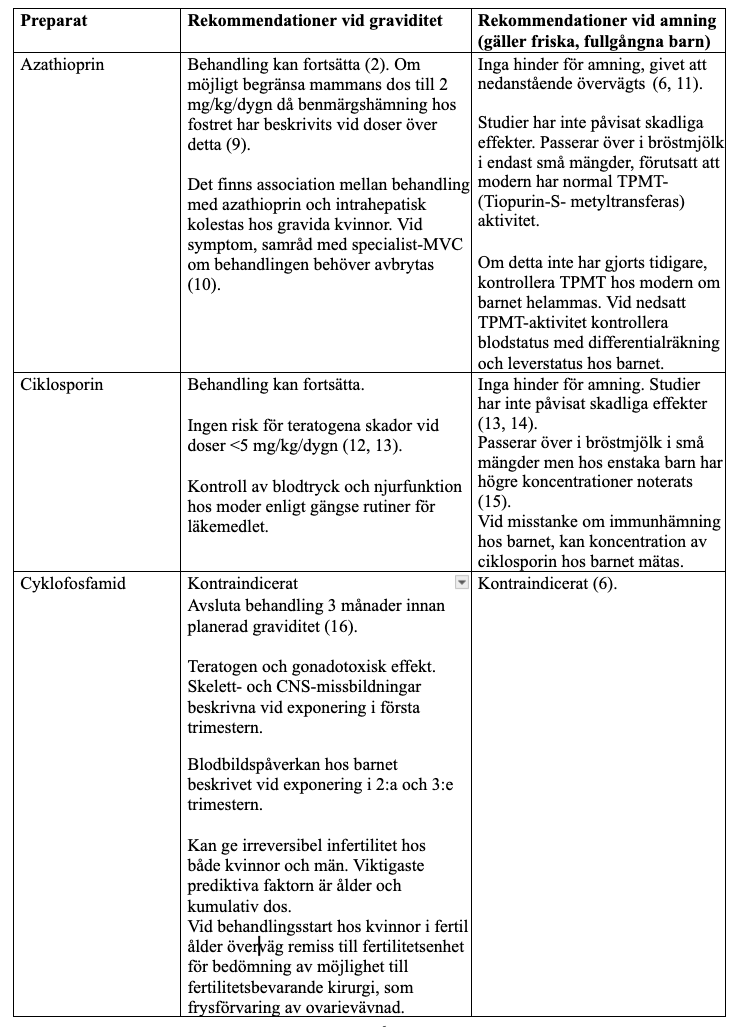
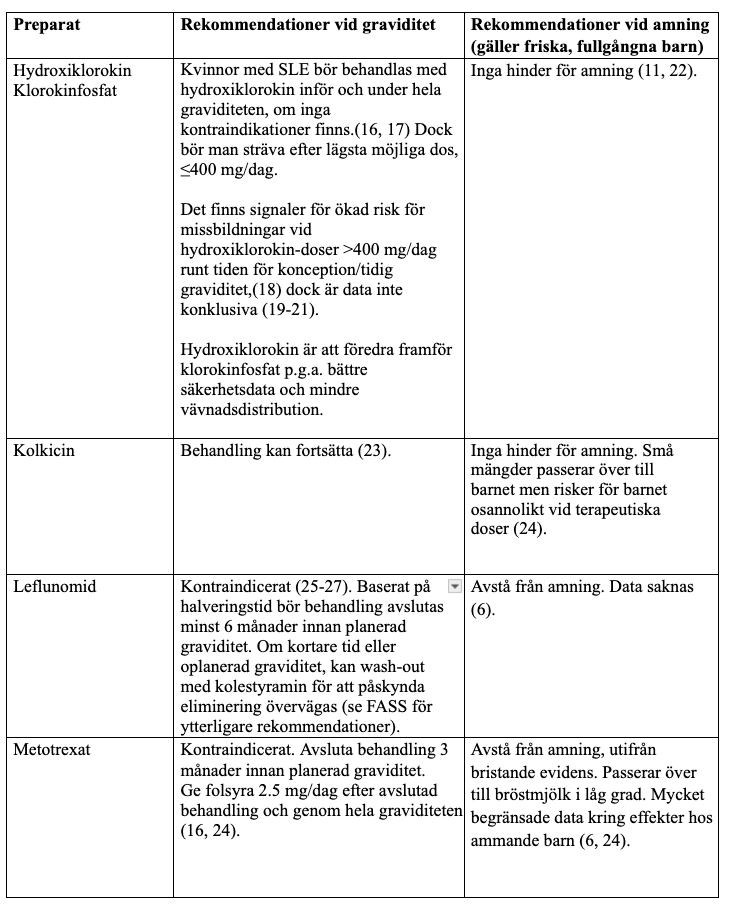
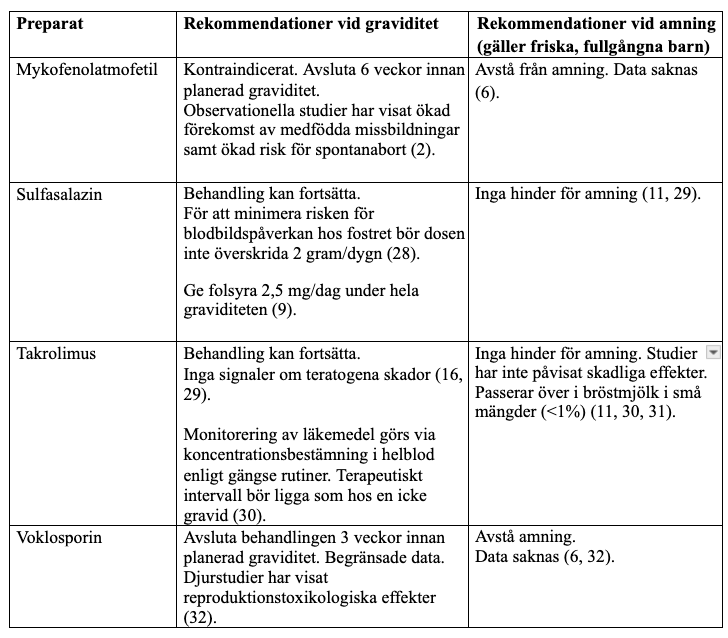
Övriga läkemedel
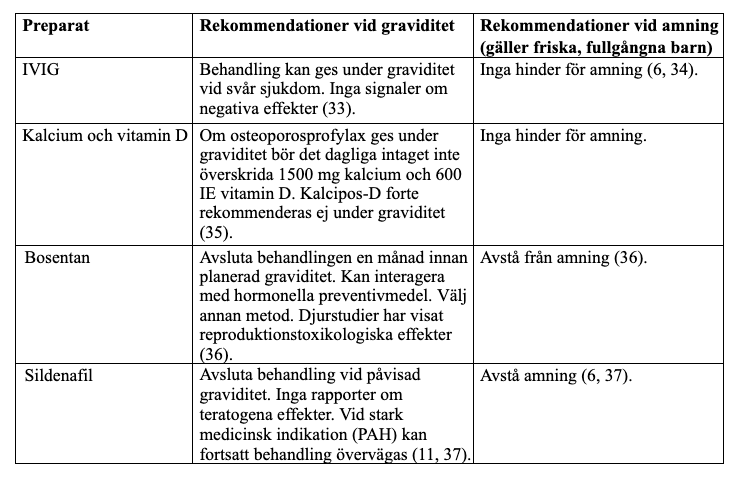
TNF-hämmare
Baserat på ackumulerad evidens och internationell koncensus bedöms det idag generellt som säkert att fortsätta med TNF-hämmare under hela graviditet och under amningsperioden.(1, 37) Data avseende biosimilarer under graviditet och amning är begränsade, men det finns inga signaler om att biosimilarerna har en annan riskprofil än motsvarande originalpreparat. Vår rekommendation är därför att biosimilarerna betraktas på samma sätt som originalpreparaten. För rekommendationer avseende levande vaccin till barn vars mödrar behandlats med TNF hämmare in utero, se sidorna 14-15.
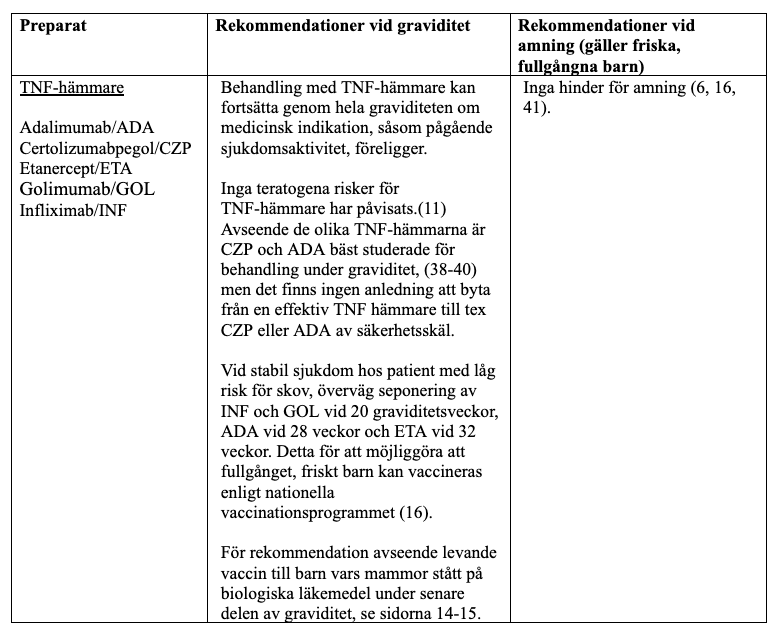
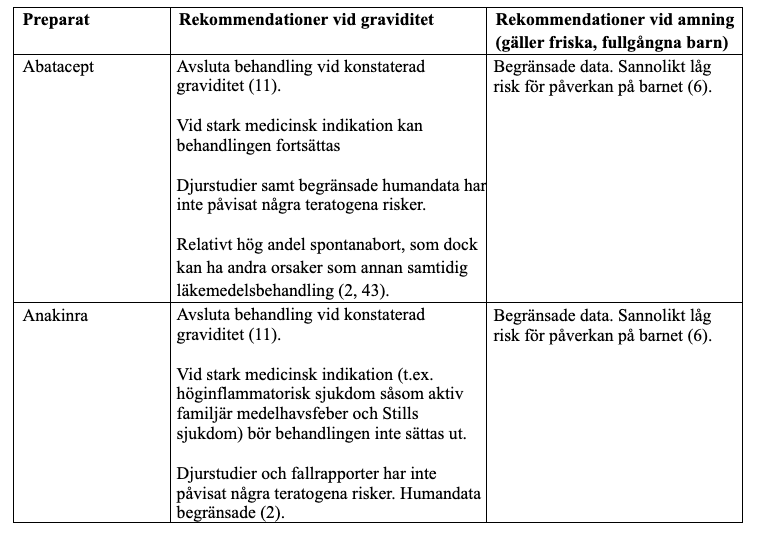
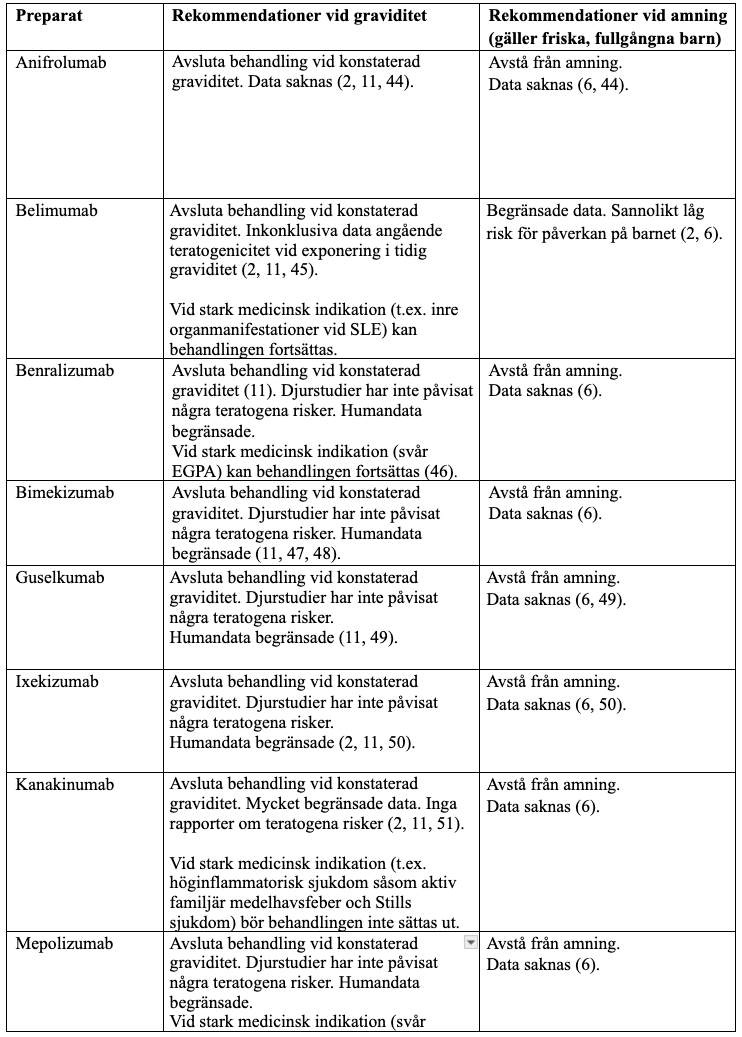
Biologiska läkemedel, icke TNF-hämmare
För antikropps-baserade läkemedel, andra än TNF-hämmare, finns det begränsad evidens avseende behandling under graviditet och amning. Den data som finns inger dock ingen misstanke om teratogenicitet. Transporten av immunglobuliner över placenta, där transporten av IgG1 är effektivast, sker framför allt i senare delen av graviditeten, vilket medför att risken för påverkan av fostret avser vara försumbar tiden innan och fram till konception (42) (OBS avvikande rekommendationer från FASS.) Behandling med monoklonala antikroppar torde därför kunna fortsätta åtminstone fram till konstaterad graviditet utan några risker för fostret, men bör då om möjligt seponeras eftersom så lite evidens för behandling under graviditet finns tillgänglig. För vissa av de biologiska icke TNF-hämmarna gäller dock andra rekommendationer, se tabell för respektive preparat.
Om behandlingen fortsättes av given anledning, ska vaccinationsrekommendationer beaktas (se sidorna 14-15).
Samtliga rekommendationer avseende amning grundas på begränsade till mycket begränsade data, i första hand fallrapporter. Generellt gäller för nedanstående läkemedelsgrupp att substanserna utgörs av stora molekyler, vilka bör brytas ned partiellt eller helt i barnets magtarmkanal vid oralt intag via bröstmjölk. Förekomst av respektive läkemedel i bröstmjölken torde därför vara låg till försumbar.
På samma sätt som för TNF-hämmarna är vår rekommendation att biosimilarerna betraktas på samma sätt som originalpreparaten.
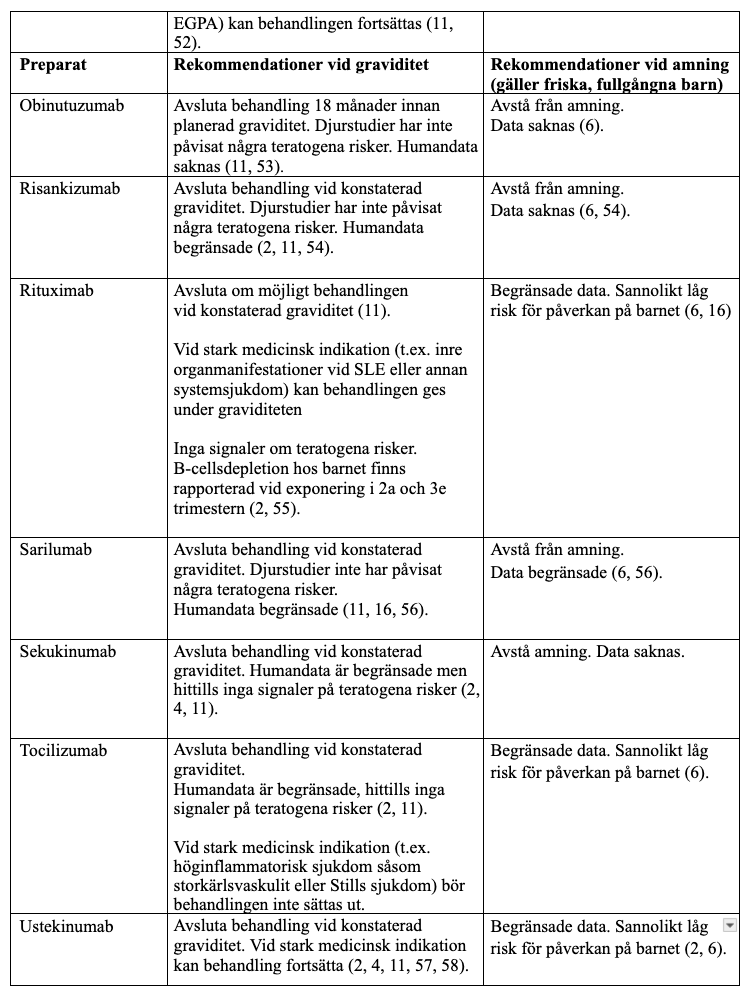
”Targeted” syntetiska läkemedel
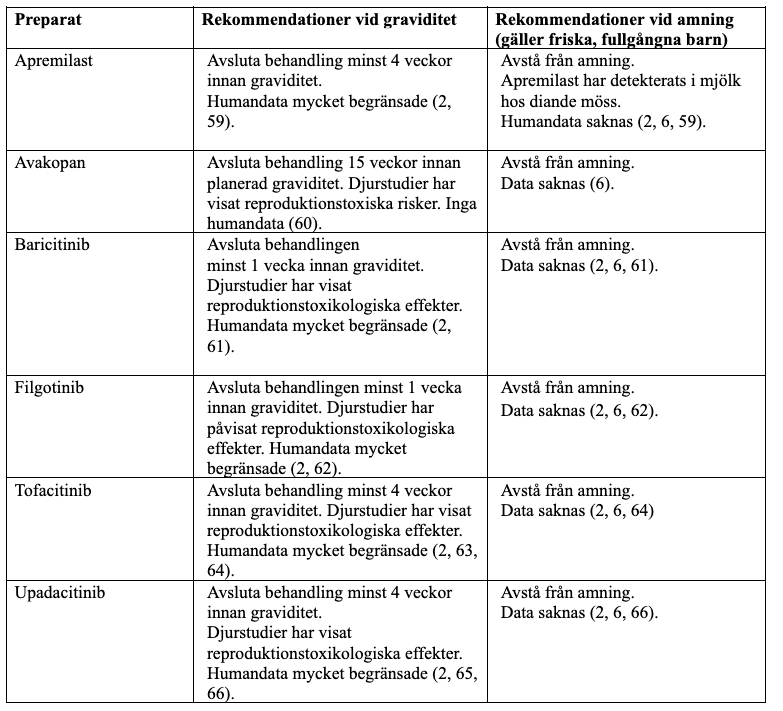
Rekommendationer avseende levande vaccin till barn vid in utero exponering för biologiska läkemedel
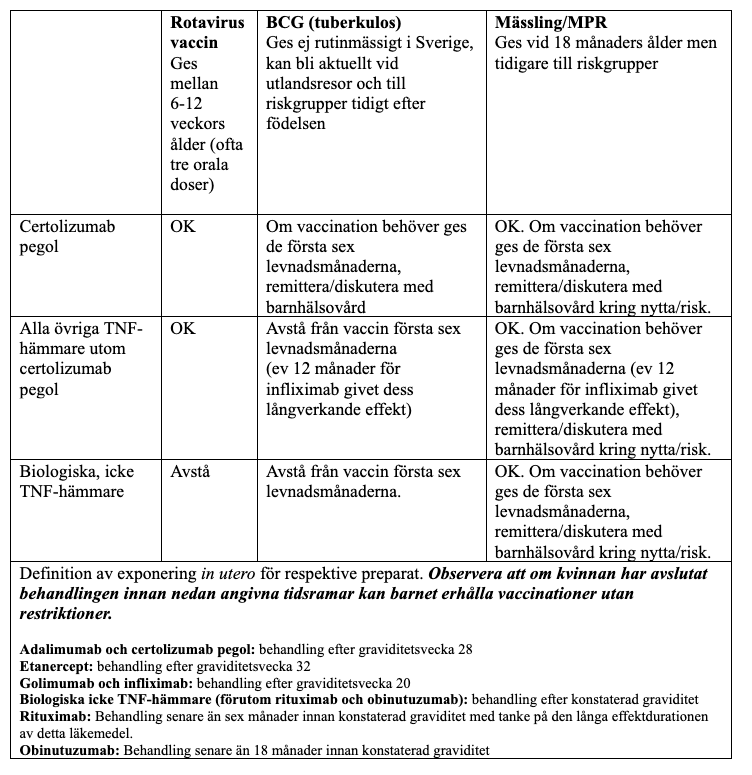
Den transplacentära transporten av monoklonala antikroppar i andra och tredje trimestern får följder när man vill ge levande vaccin till barn vars mödrar behandlats med biologiska läkemedel, framför allt i senare delen av graviditeten. Hittills har en generell tumregel varit att då avstå från levande vaccin till barnen åtminstone de första sex levnadsmånaderna. Nya data talar dock för att levande försvagande vaccin, såsom rotavirus-vaccination, kan ges tidigare än så vid exponering för TNF-hämmare utan några negativa effekter (67-69). Motsvarande data för andra, mer potenta, levande vaccin såsom BCG (tuberkulos), mässling/MPR eller gula febern är mer begränsade.
Frånsett timing är läkemedlets halveringstid och molekylära struktur av betydelse. Fullständiga monoklonala (IgG1) antikroppar (tex adalimumab, golimumab, infliximab,) passerar över placenta i större utsträckning än icke kompletta antikroppar (tex certolizumab pegol och etanercept). Etanercept, som består av dels en TNF-receptordel, dels en Fc-del från IgG1, torde vidare passera placenta i mindre utsträckning än en fullständig antikropp, men i högre grad än certolizumab pegol, vilken saknar Fc-del. Dessutom måste barnets hälsotillstånd samt nytta/risk-balans med att vaccinera för det individuella barnet/familjen noggrant beaktas.
Således måste flera aspekter vägas in när man skall ta ställning till när, och om, man kan ge levande vaccin till dessa barn under deras första levnadsmånader. Viktigt att påpeka är därför att det slutliga beslutet huruvida ett barn skall vaccineras ligger hos barnhälsovården /barnläkare.
På nästa sida har vi sammanställt övergripande kliniska rekommendationer för levande vaccin till barn exponerade in utero utifrån typ av behandling och vaccin. Rekommendationerna överensstämmer med de nya EULAR-rekommendationerna (11), men skiljer sig något från dem som ges i Rikshandboken från 2022 (70). Vid osäkerhet diskutera alltid med barnläkare. Observera också att rekommendationerna gäller friska och fullgångna barn (1, 11).
Tabell: Rekommendation avseende levande vaccin till nyfödda barn exponerade in utero för biologiska läkemedel
Män
Inledning
Avseende nedsatt fertilitet eller teratogenicitet bland barn till män till följd av paternell antiinflammatorisk och/eller antireumatisk behandling finns sparsamt med kontrollerade data. Nedanstående rekommendationer baseras på i litteraturen tillgängliga uppgifter och är långt ifrån heltäckande. Vid de läkemedel där uppgifter saknas har vi valt att avstå från att ge någon rekommendation. Detta gäller bland annat för samtliga bDMARD, förutom TNF-hämmare och rituximab, samt för targeted syntetiska DMARD frånsett JAK-hämmare.
NSAID och glukokortikoider

Konventionella syntetiska DMARD
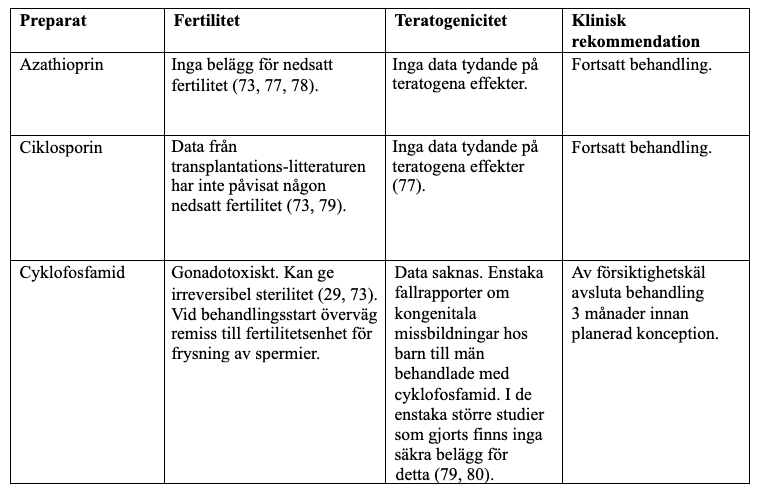
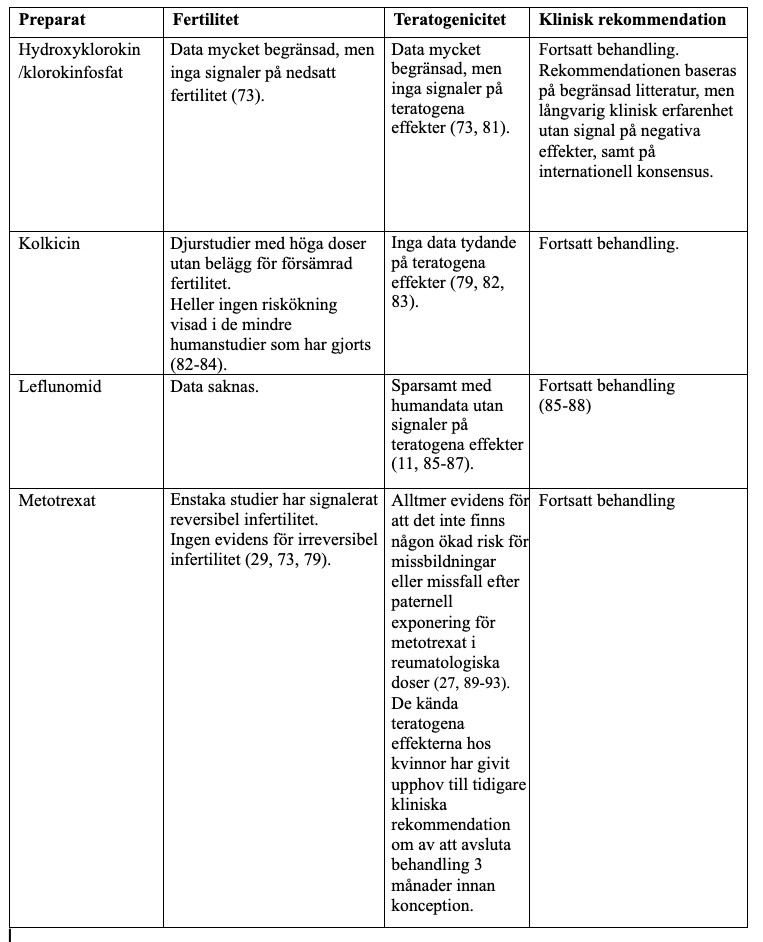
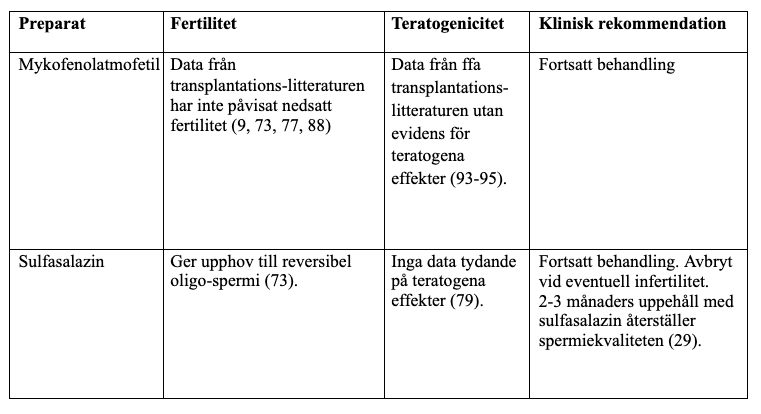
Biologiska och targeted syntetiska läkemedel
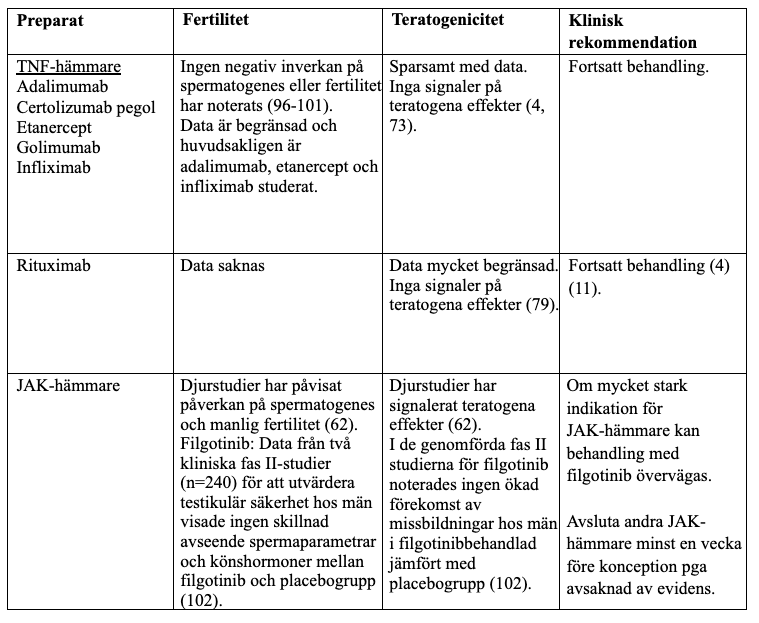
Referenser
Hänvisad litteratur
- Rüegg L, Pluma A, Hamroun S, Cecchi I, Perez-Garcia LF, Anderson PO, et al. EULAR recommendations for use of antirheumatic drugs in reproduction, pregnancy, and lactation: 2024 update. Annals of the rheumatic diseases. 2025;84(6):910-26.
- Russell MD, Dey M, Flint J, Davie P, Allen A, Crossley A, et al. British Society for Rheumatology guideline on prescribing drugs in pregnancy and breastfeeding: immunomodulatory anti-rheumatic drugs and corticosteroids. Rheumatology (Oxford, England). 2023;62(4):e48-e88.
- Dathe K, Frank J, Padberg S, Hultzsch S, Beck E, Schaefer C. Fetal adverse effects following NSAID or metamizole exposure in the 2nd and 3rd trimester: an evaluation of the German Embryotox cohort. BMC Pregnancy Childbirth. 2022;22(1):666.
- Sammaritano LR, Bermas BL, Chakravarty EE, Chambers C, Clowse MEB, Lockshin MD, et al. 2020 American College of Rheumatology Guideline for the Management of Reproductive Health in Rheumatic and Musculoskeletal Diseases. Arthritis care & research. 2020;72(4):461-88.
- Palmsten K, Bandoli G, Vazquez-Benitez G, Xi M, Johnson DL, Xu R, et al. Oral corticosteroid use during pregnancy and risk of preterm birth. Rheumatology (Oxford, England). 2020;59(6):1262-71.
- Bookshelf. Drugs and Lactation Database (LactMed®). National Institute of Child Health and Human Development. https://www.ncbi.nlm.nih.gov/books/NBK501922/. NIH. 2006.
- Park-Wyllie L, Mazzotta P, Pastuszak A, Moretti ME, Beique L, Hunnisett L, et al. Birth defects after maternal exposure to corticosteroids: prospective cohort study and meta-analysis of epidemiological studies. Teratology. 2000;62(6):385-92.
- Bandoli G, Palmsten K, Forbess Smith CJ, Chambers CD. A Review of Systemic Corticosteroid Use in Pregnancy and the Risk of Select Pregnancy and Birth Outcomes. Rheumatic diseases clinics of North America. 2017;43(3):489-502.
- Temprano KK, Bandlamudi R, Moore TL. Antirheumatic drugs in pregnancy and lactation. Seminars in arthritis and rheumatism. 2005;35(2):112-21.
- Selinger CP, Rosiou K, Broglio G, Lever G, Chiu CM, Stocker LJ, et al. Antenatal thiopurine exposure in women with IBD is associated with intrahepatic cholestasis of pregnancy. Expert Opin Drug Saf. 2023;22(11):1091-7.
- Pluma A, Hamroun S, Rüegg L, Cecchi I, Kramer M, Perez-Garcia LF, et al. Antirheumatic drugs in reproduction, pregnancy, and lactation: a systematic literature review informing the 2024 update of the EULAR recommendations. Annals of the rheumatic diseases. 2025;84(9):1561-90.
- Gisbert JP. Safety of immunomodulators and biologics for the treatment of inflammatory bowel disease during pregnancy and breast-feeding. Inflamm Bowel Dis. 2010;16(5):881-95.
- Saha S, Wald A. Safety and efficacy of immunomodulators and biologics during pregnancy and lactation for the treatment of inflammatory bowel disease. Expert Opin Drug Saf. 2012;11(6):947-57.
- Chandra A, Midtvedt K, Åsberg A, Eide IA. Immunosuppression and Reproductive Health After Kidney Transplantation. Transplantation. 2019;103(11):e325-e33.
- Moretti ME, Sgro M, Johnson DW, Sauve RS, Woolgar MJ, Taddio A, et al. Cyclosporine excretion into breast milk. Transplantation. 2003;75(12):2144-6.
- Russell MD, Dey M, Flint J, Davie P, Allen A, Crossley A, et al. British Society of Rheumatology guideline working group response to European Medicines Agency safety update on Hydroxychloroquine. Rheumatology (Oxford, England). 2024;63(2):e37-e8.
- Andreoli L, Bertsias GK, Agmon-Levin N, Brown S, Cervera R, Costedoat-Chalumeau N, et al. EULAR recommendations for women’s health and the management of family planning, assisted reproduction, pregnancy and menopause in patients with systemic lupus erythematosus and/or antiphospholipid syndrome. Annals of the rheumatic diseases. 2017;76(3):476-85.
- Huybrechts KF, Bateman BT, Zhu Y, Straub L, Mogun H, Kim SC, et al. Hydroxychloroquine early in pregnancy and risk of birth defects. American journal of obstetrics and gynecology. 2021;224(3):290.e1-.e22.
- Nguyen NV, Svenungsson E, Dominicus A, Altman M, Hellgren K, Simard JF, et al. Hydroxychloroquine in lupus or rheumatoid arthritis pregnancy and risk of major congenital malformations: a population-based cohort study. Rheumatology (Oxford, England). 2024.
- Bérard A, Sheehy O, Zhao JP, Vinet E, Quach C, Bernatsky S. Chloroquine and Hydroxychloroquine Use During Pregnancy and the Risk of Adverse Pregnancy Outcomes Using Real-World Evidence. Front Pharmacol. 2021;12:722511.
- Clowse MEB, Eudy AM, Balevic S, Sanders-Schmidler G, Kosinski A, Fischer-Betz R, et al. Hydroxychloroquine in the pregnancies of women with lupus: a meta-analysis of individual participant data. Lupus science & medicine. 2022;9(1).
- Østensen M, Andreoli L, Brucato A, Cetin I, Chambers C, Clowse ME, et al. State of the art: Reproduction and pregnancy in rheumatic diseases. Autoimmun Rev. 2015;14(5):376-86.
- Indraratna PL, Virk S, Gurram D, Day RO. Use of colchicine in pregnancy: a systematic review and meta-analysis. Rheumatology (Oxford, England). 2018;57(2):382-7.
- Götestam Skorpen C, Hoeltzenbein M, Tincani A, Fischer-Betz R, Elefant E, Chambers C, et al. The EULAR points to consider for use of antirheumatic drugs before pregnancy, and during pregnancy and lactation. Annals of the rheumatic diseases. 2016;75(5):795-810.
- Weber-Schoendorfer C, Beck E, Tissen-Diabaté T, Schaefer C. Leflunomide – A human teratogen? A still not answered question. An evaluation of the German Embryotox pharmacovigilance database. Reprod Toxicol. 2017;71:101-7.
- Bérard A, Zhao JP, Shui I, Colilla S. Leflunomide use during pregnancy and the risk of adverse pregnancy outcomes. Annals of the rheumatic diseases. 2018;77(4):500-9.
- Eck LK, Jensen TB, Mastrogiannis D, Torp-Pedersen A, Askaa B, Nielsen TK, et al. Risk of Adverse Pregnancy Outcome After Paternal Exposure to Methotrexate Within 90 Days Before Pregnancy. Obstetrics and gynecology. 2017;129(4):707-14.
- Läkemedelsverket. Biverkningsnytt; Fetal hemolytisk anemi vid sulfasalazinbehandling under graviditet. Information från Läkemedelsverket 2004;1217(1; 2004: 59-60.).
- Sammaritano LR, Bermas BL, Chakravarty EE, Chambers C, Clowse MEB, Lockshin MD, et al. 2020 American College of Rheumatology Guideline for the Management of Reproductive Health in Rheumatic and Musculoskeletal Diseases. Arthritis & rheumatology (Hoboken, NJ). 2020;72(4):529-56.
- Hebert MF, Zheng S, Hays K, Shen DD, Davis CL, Umans JG, et al. Interpreting tacrolimus concentrations during pregnancy and postpartum. Transplantation. 2013;95(7):908-15.
- Gouraud A, Bernard N, Millaret A, Bruel M, Paret N, Descotes J, et al. Follow-up of tacrolimus breastfed babies. Transplantation. 2012;94(6):e38-40.
- EMA. https://www.ema.europa.eu/en/documents/product-information/lupkynis-epar-product-information_en.pdf.
- Han A, Lee SK, Park JC, Park CW, Han JW, Lee KH. Maternal and fetal safety of intravenous immunoglobulin in women with reproductive failure. Am J Reprod Immunol. 2021;86(6):e13492.
- Achiron A, Kishner I, Dolev M, Stern Y, Dulitzky M, Schiff E, et al. Effect of intravenous immunoglobulin treatment on pregnancy and postpartum-related relapses in multiple sclerosis. J Neurol. 2004;251(9):1133-7.
- EMA. https://ec.europa.eu/health/documents/communityregister/2006/2006032911165/anx_11165_sv.pdf.
- EMA. https://www.ema.europa.eu/en/medicines/human/EPAR/tracleerutm_source=chatgpt.com. 2019.
- BSR. https://academic.oup.com/rheumatology/article/62/4/e48/6783012. 2023.
- Mariette X, Förger F, Abraham B, Flynn AD, Moltó A, Flipo RM, et al. Lack of placental transfer of certolizumab pegol during pregnancy: results from CRIB, a prospective, postmarketing, pharmacokinetic study. Annals of the rheumatic diseases. 2018;77(2):228-33.
- Clowse ME, Förger F, Hwang C, Thorp J, Dolhain RJ, van Tubergen A, et al. Minimal to no transfer of certolizumab pegol into breast milk: results from CRADLE, a prospective, postmarketing, multicentre, pharmacokinetic study. Annals of the rheumatic diseases. 2017;76(11):1890-6.
- EMA. https://www.ema.europa.eu/en/documents/product-information/humira-epar-product information_en.pdf.
- Matro R, Martin CF, Wolf D, Shah SA, Mahadevan U. Exposure Concentrations of Infants Breastfed by Women Receiving Biologic Therapies for Inflammatory Bowel Diseases and Effects of Breastfeeding on Infections and Development. Gastroenterology. 2018;155(3):696-704.
- Kane SV, Acquah LA. Placental transport of immunoglobulins: a clinical review for gastroenterologists who prescribe therapeutic monoclonal antibodies to women during conception and pregnancy. Am J Gastroenterol. 2009;104(1):228-33.
- Kumar M, Ray L, Vemuri S, Simon TA. Pregnancy outcomes following exposure to abatacept during pregnancy. Seminars in arthritis and rheumatism. 2015;45(3):351-6.
- EMA. https://ec.europa.eu/health/documents/communityregister/2022/20220214154608/anx_154608_sv.pdf.
- Petri M, Landy H, Clowse MEB, Gemzoe K, Khamashta M, Kurtinecz M, et al. Belimumab use during pregnancy: a summary of birth defects and pregnancy loss from belimumab clinical trials, a pregnancy registry and postmarketing reports. Annals of the rheumatic diseases. 2023;82(2):217-25.
- EMA. https://www.ema.europa.eu/en/documents/pip-decision/p-0307-2024-ema-decision-16-august-2024-acceptance-modification-agreed-paediatric-investigation-plan-benralizumab-fasenra-emea-001214-pip04-19-m01_en.pdf. 2024.
- EMA. https://www.ema.europa.eu/en/documents/product-information/bimzelx-epar-product-information_en.pdf. 2025.
- Jeong YD, Jo H, Cho H, Jang W, Park J, Lee S, et al. Biologics Use for Psoriasis during Pregnancy and Its Related Adverse Outcomes in Pregnant Women and Newborns: Findings from WHO Pharmacovigilance Study. Int Arch Allergy Immunol. 2025;186(6):579-93.
- EMA. https://ec.europa.eu/health/documents/communityregister/2017/20171110139063/anx_139063_sv.pdf.
- EMA. https://ec.europa.eu/health/documents/communityregister/2019/20190206143686/anx_143686_sv.pdf.
- EMA. https://ec.europa.eu/health/documents/communityregister/2009/2009102365309/anx_65309_sv.pdf.
- EMA. https://www.ema.europa.eu/en/documents/pip-decision/p-0367-2024-ema-decision-25-october-2024-acceptance-modification-agreed-paediatric-investigation-plan-mepolizumab-nucala-emea-000069-pip01-07-m09_en.pdf. 2024.
- EMA. https://www.ema.europa.eu/en/documents/pip-discontinuation/obinutuzumab-notification-discontinuation-paediatric-development-which-covered-agreed-pip-decision_en.pdf. 2022.
- EMA. https://ec.europa.eu/health/documents/communityregister/2023/20230110157990/anx_157990_sv.pdf.
- Schwake C, Steinle J, Thiel S, Timmesfeld N, Haben S, Ayzenberg I, et al. Neonatal B-Cell Levels and Infant Health in Newborns Potentially Exposed to Anti-CD20 Monoclonal Antibodies During Pregnancy or Lactation. Neurol Neuroimmunol Neuroinflamm. 2024;11(4):e200264.
- EMA. https://ec.europa.eu/health/documents/community-register/2022/20220425155352/anx_155352_sv.pdf.
- Meyer A, Miranda S, Drouin J, Weill A, Carbonnel F, Dray-Spira R. Safety of Vedolizumab and Ustekinumab Compared With Anti-TNF in Pregnant Women With Inflammatory Bowel Disease. Clin Gastroenterol Hepatol. 2024.
- Julsgaard M, Wieringa JW, Baunwall SMD, Bibby BM, Driessen GJA, Kievit L, et al. Infant Ustekinumab Clearance, Risk of Infection, and Development After Exposure During Pregnancy. Clin Gastroenterol Hepatol. 2025;23(1):134-43.
- EMA. https://ec.europa.eu/health/documents/community-register/2019/20190823145559/anx_145559_sv.pdf.
- EMA. https://www.ema.europa.eu/en/documents/product-information/tavneos-epar-product-information_en.pdf. 2025.
- EMA. https://ec.europa.eu/health/documents/community-register/2022/20220620156061/anx_156061_sv.pdf.
- EMA. https://ec.europa.eu/health/documents/community-register/2023/20230310157901/anx_157901_sv.pdf.
- Mitrova K, Julsgaard M, Augustijns P, Cerna K, Mahadevan U, Duricova D. Tofacitinib in Pregnancy: Assessing Pregnancy and Infant Outcomes, Cord Blood, and Breast Milk Concentrations. Clin Gastroenterol Hepatol. 2024.
- EMA. https://www.ema.europa.eu/en/documents/product-information/xeljanz-epar-product-information_en.pdf.
- Mahadevan U, Levy G, Gensler L, Ali M, Lacerda AP, Wegrzyn L, et al. Pregnancy Outcomes in Patients Treated with Upadacitinib: Analysis of Data from Clinical Trials and Postmarketing Reports. Drug Saf. 2024;47(10):1039-49.
- EMA. https://ec.europa.eu/health/documents/community-register/2023/20230310157921/anx_157921_sv.pdf.
- Schell TL, Fass L, Hitchcock ME, Farraye FA, Hayney MS, Saha S, et al. Safety of Rotavirus Vaccination in Infants That Were Exposed to Biologics In Utero: A Systematic Review. Inflamm Bowel Dis. 2024.
- Ernest-Suarez K, Murguía-Favela LE, Constantinescu C, Fitzpatrick T, Top KA, Hu J, et al. Live Rotavirus Vaccination Appears Low-risk in Infants Born to Mothers With Inflammatory Bowel Disease on Biologics. Clin Gastroenterol Hepatol. 2024.
- Fitzpatrick T, Alsager K, Sadarangani M, Pham-Huy A, Murguía-Favela L, Morris SK, et al. Immunological effects and safety of live rotavirus vaccination after antenatal exposure to immunomodulatory biologic agents: a prospective cohort study from the Canadian Immunization Research Network. Lancet Child Adolesc Health. 2023;7(9):648-56.
- Rikshandboken. https://www.rikshandboken-bhv.se/globalassets/rhb/media/dokument/vaccination/nationell-vagledning-levande-vaccin-immunhammande.pdf.
- Sands K, Jansen R, Zaslau S, Greenwald D. Review article: the safety of therapeutic drugs in male inflammatory bowel disease patients wishing to conceive. Aliment Pharmacol Ther. 2015;41(9):821-34.
- Larsen MD, Friedman S, Magnussen B, Nørgård BM. Birth Outcome of Children Fathered by Men Treated with Systemic Corticosteroids during the Conception Period – A Cohort Study based on Nationwide Data. Basic Clin Pharmacol Toxicol. 2018;122(1):133-8.
- Bermas BL. Paternal safety of anti-rheumatic medications. Best Pract Res Clin Obstet Gynaecol. 2020;64:77-84.
- Joyce CL, Nuzzo NA, Wilson L, Jr., Zaneveld LJ. Evidence for a role of cyclooxygenase (prostaglandin synthetase) and prostaglandins in the sperm acrosome reaction and fertilization. J Androl. 1987;8(2):74-82.
- Martini AC, Molina RI, Tissera AD, Ruiz RD, Fiol de Cuneo M. Analysis of semen from patients chronically treated with low or moderate doses of aspirin-like drugs. Fertility and sterility. 2003;80(1):221-2.
- Banihani SA. Effect of aspirin on semen quality: A review. Andrologia. 2020;52(1):e13487.
- Armenti VT, Constantinescu S, Moritz MJ, Davison JM. Pregnancy after transplantation. Transplant Rev (Orlando). 2008;22(4):223-40.
- Perez-Garcia LF, Dolhain R, Vorstenbosch S, Bramer W, van Puijenbroek E, Hazes JMW, et al. The effect of paternal exposure to immunosuppressive drugs on sexual function, reproductive hormones, fertility, pregnancy and offspring outcomes: a systematic review. Hum Reprod Update. 2020;26(6):961-1001.
- Mouyis M, Flint JD, Giles IP. Safety of anti-rheumatic drugs in men trying to conceive: A systematic review and analysis of published evidence. Seminars in arthritis and rheumatism. 2019;48(5):911-20.
- Green DM, Whitton JA, Stovall M, Mertens AC, Donaldson SS, Ruymann FB, et al. Pregnancy outcome of partners of male survivors of childhood cancer: a report from the Childhood Cancer Survivor Study. J Clin Oncol. 2003;21(4):716-21.
- Rizzi S, Wensink MJ, Lindahl-Jacobsen R, Tian L, Lu Y, Eisenberg ML. Risk of pre-term births and major birth defects resulting from paternal intake of COVID-19 medications prior to conception. BMC Res Notes. 2020;13(1):509.
- Ben-Chetrit E, Berkun Y, Ben-Chetrit E, Ben-Chetrit A. The outcome of pregnancy in the wives of men with familial mediterranean fever treated with colchicine. Seminars in arthritis and rheumatism. 2004;34(2):549-52.
- Haimov-Kochman R, Ben-Chetrit E. The effect of colchicine treatment on sperm production and function: a review. Hum Reprod. 1998;13(2):360-2.
- Both T, van Laar JA, Bonte-Mineur F, van Hagen PM, van Daele PL. [Colchicine has no negative effect on fertility and pregnancy]. Nederlands tijdschrift voor geneeskunde. 2012;156(12):A4196.
- Kieseier BC, Benamor M. Pregnancy outcomes following maternal and paternal exposure to teriflunomide during treatment for relapsing-remitting multiple sclerosis. Neurol Ther. 2014;3(2):133-8.
- De Santis M, Straface G, Cavaliere A, Carducci B, Caruso A. Paternal and maternal exposure to leflunomide: pregnancy and neonatal outcome. Annals of the rheumatic diseases. 2005;64(7):1096-7.
- Andersen JB, Wandall-Holm MF, Magyari M. Pregnancy outcomes following maternal or paternal exposure to teriflunomide in the Danish MS population. Mult Scler Relat Disord. 2022;59:103529.
- De Santis M, Cesari E, Cavaliere A, Ligato MS, Nobili E, Visconti D, et al. Paternal exposure and counselling: experience of a Teratology Information Service. Reprod Toxicol. 2008;26(1):42-6.
- Viktil KK, Engeland A, Furu K. Outcomes after anti-rheumatic drug use before and during pregnancy: a cohort study among 150,000 pregnant women and expectant fathers. Scandinavian journal of rheumatology. 2012;41(3):196-201.
- Weber-Schoendorfer C, Hoeltzenbein M, Wacker E, Meister R, Schaefer C. No evidence for an increased risk of adverse pregnancy outcome after paternal low-dose methotrexate: an observational cohort study. Rheumatology (Oxford, England). 2014;53(4):757-63.
- Winter RW, Larsen MD, Magnussen B, Friedman S, Kammerlander H, Nørgård BM. Birth outcomes after preconception paternal exposure to methotrexate: A nationwide cohort study. Reprod Toxicol. 2017;74:219-23.
- Perez-Garcia LF, Röder E, Krijthe BP, Kranenburg-van Koppen LJ, van Adrichem R, Zirkzee E, et al. Is methotrexate safe for men with an immune-mediated inflammatory disease and an active desire to become a father? Results of a prospective cohort study (iFAME-MTX). Annals of the rheumatic diseases. 2023;82(8):1068-75.
- Zarén P, Turesson C, Giwercman A. Methotrexate use among men-association with fertility and the perinatal health of their children: a Swedish nationwide register study. Fertility and sterility. 2023;120(3 Pt 2):661-9.
- Midtvedt K, Bergan S, Reisæter AV, Vikse BE, Åsberg A. Exposure to Mycophenolate and Fatherhood. Transplantation. 2017;101(7):e214-e7.
- Lopez-Lopez I, Rodelo-Haad C, Agüera ML, Cabello-Jabalquinto R, Esquivias-Motta E, Navarro MD, et al. Administration of mycophenolic acid is not associated with malformations in descendants from kidney transplanted males. PloS one. 2018;13(9):e0202589.
- Villiger PM, Caliezi G, Cottin V, Förger F, Senn A, Østensen M. Effects of TNF antagonists on sperm characteristics in patients with spondyloarthritis. Annals of the rheumatic diseases. 2010;69(10):1842-4.
- Heetun ZS, Byrnes C, Neary P, O’Morain C. Review article: Reproduction in the patient with inflammatory bowel disease. Aliment Pharmacol Ther. 2007;26(4):513-33.
- Mahadevan U, Terdiman JP, Aron J, Jacobsohn S, Turek P. Infliximab and semen quality in men with inflammatory bowel disease. Inflamm Bowel Dis. 2005;11(4):395-9.
- Grosen A, Bungum M, Christensen LA, Cordelli E, Larsen OH, Leter G, et al. Semen Quality and Sperm DNA Integrity in Patients With Severe Active Inflammatory Bowel Disease and Effects of Tumour Necrosis Factor-alpha Inhibitors. J Crohns Colitis. 2019;13(5):564-71.
- Puchner R, Danninger K, Puchner A, Pieringer H. Impact of TNF-blocking agents on male sperm characteristics and pregnancy outcomes in fathers exposed to TNF-blocking agents at time of conception. Clin Exp Rheumatol. 2012;30(5):765-7.
- Micu MC, Ostensen M, Bojincă V, Șerban O, Mihai M, Suța C, et al. Pregnancy Outcomes in Couples with Males Exposed to Longterm Anti-tumor Necrosis Factor-α Inhibitor Therapies: A Prospective Study. The Journal of rheumatology. 2019;46(9):1084-8.
- Reinisch W, Hellstrom W, Dolhain R, Sikka S, Westhovens R, Mehta R, et al. Effects of filgotinib on semen parameters and sex hormones in male patients with inflammatory diseases: results from the phase 2, randomised, double-blind, placebo-controlled MANTA and MANTA-RAy studies. Annals of the rheumatic diseases. 2023;82(8):1049-58.

